
万方数据
万方数据
万方数据
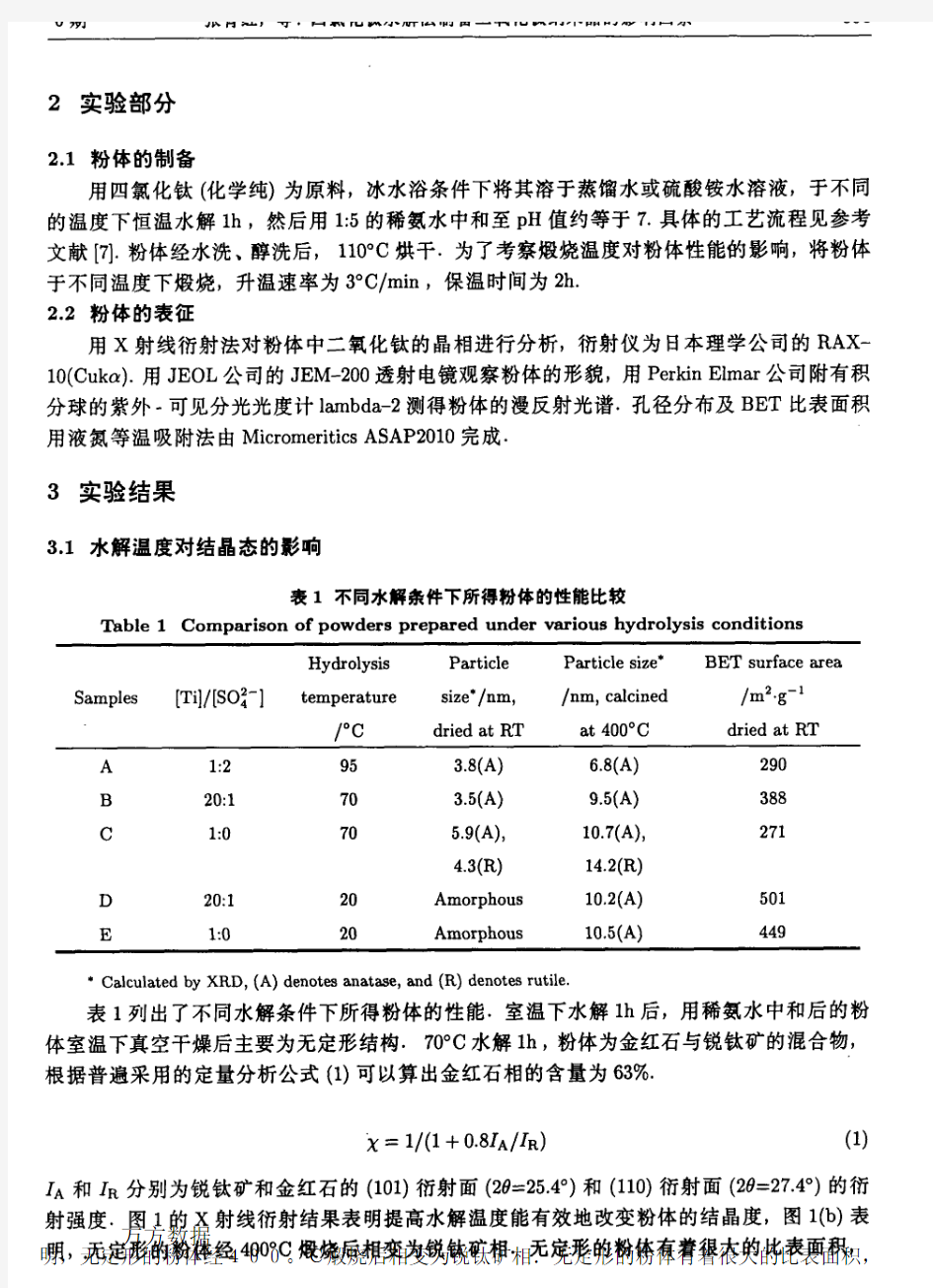
6Ⅷ{E*“#,口≈m%m**M*=#m☆目%^自B自目¥095ioo。c&&目Ⅲ*M∞m.&Ⅲ№∞*(&&^<500iⅡ)∞日Ⅲ№自ft¨Ⅲ№T目Ⅲ№十∞∞n**.W№#*gm*自*‰*r∞自¥^(n&38nm】w±Ⅱd*m¥&m&7hm)m№m☆溘nd☆m
60%).#%№≈*&日Ⅲ≈E&自Ⅱj"#十女m∞日1Ⅲ
n.{q目目**∞Ⅱ☆"”}月f日自∞¥m¨№%☆,≈*%目¥目im十∞me“m%t_】*ma《☆#m№BM‰‰r“#±n5¨*Ⅲn赢了i萨
!,;毫,4【鳖。nJ…n_nm…dn_日m3}1目目"##&∞《m#∞¥^∞**,日m&EH№*
Fig3UVvisdln…ncc‘aI∞s"∞tr“ohlIH晰【nt【02TI础目
f¨…a目“[b1M【t‘u…………lkm4*md006c**∞№&∞自H#自《月H%8#m#∞#£&,#★∞5‰∞iⅣ#.#,』1∞☆#‰《g“&1-?”#目∞日nRt,日“镕Ⅻ,#女∞“#∞☆adM.#n日%∞‰‰r目TiC]。*}m∞m镕mH女m#∞,自☆
“Tn¥:
T】cl4+H?O=TiOIl”+H++4dl
(∞TK)H3+TiOtl+H+
f31T【02+十H20TiO2+2H+(4)
m*Ⅱ&f2)n*aE&,#T1cld☆0。c
镕fm日ⅡWⅫ2一日,§*}∞*Ⅲ
#☆(2)En№{1*№自**《(3)自
m*Ⅱ&(41目∞%#E&**Ⅲ&自W
fER自☆m#自十Ⅻ自m&m*&n
P±∞§自fm№n&Ⅱ&《a),(4)自☆
m目女#口m镕月Ⅱ&m镕"目¥“*
日_#Bc%dDrc**目0q*n#m*ⅢHFig4IⅢTEM—F8¨ofsample…[1Ⅱdn4000C=#^匕%自*R∞女&Mno…≮目Tlcll黼&f98。cm*38i.mⅫT}Hm=#m*"*…nn&&m:iⅢT,{Ⅲ《m十Ⅻ∞、月*Ⅲf】可Tlcl{镕《20x目mm4№.g∞Ⅻ#}∞m*Ⅲ%g{*∞m镕目目女Rl,自☆&E(3)Ⅻm*E&(4)∞%一十}ⅫEⅢE&m*∞口mj*目*☆fmⅢ#E自§}女m*《¥Ⅱ々Tic】l∞"*镕&自*m镕Ⅱ&(2)镕№4Ⅱ&,”G【{镕&¨自*m&#★P±∞§☆f*Ⅸm≈^.#"dR&(3)目(4)自Ⅱm"¥女*月升Ⅲ&Am十##}&.#&自TⅢ☆m镕《¥#“fT】O:∞&#々±*.tⅫ*《“#∞目∞
万方数据
郸%M##}m15●
☆“*I=十,目f^’t^t《■十,*W十*&**r#∞}*,mE*#目&女Ⅲ&##^■£∞*女Sz町’.F%O,*∞#一#.☆目&”m十,Ⅸ*自∞Zeta自&女Ⅲ*m】,m#**,m*#Ⅲ#t自*,mtm^十M¥∞m自*g.*t&十∞■Ⅲfm#5々in蜘&Ⅲ∞ntⅢ}目m&m{*#日自■m*《十∞d自§Ⅱ☆.目≮■}#&-tn#■}!g*%目**¥&目,&E£&*.¥#f女女T*#^t*★f.W*#i≈¥∞*#^m*¥R镕№目5*m&T&#镕“tH*.706C¥*自*自**“&№“Ti/20目■&*、§%T女*“§目z女¥*#目TEM月R.自e*H∞*#÷##∞nam∞1/20aH《.7rcm■**∞*##《!,J、,目#目C一#*ia∞镕#一Ⅲ&目镕mmt*、20。C¥*∞*∞*#E{#目D一#☆¥n镕#,m#n&#¥{mD日自
曩匿日5#BC自DiⅢT^!十*目∞女*自*月HHEBTEM一呼‘山of{日一曲0皿d(b)…kDmMd^…roomp…uⅡ㈣Ⅱ口
*^’■tB*■十目,tt*■f∞;¥■&&(2),女∞TiOIt。+*m*^镕*,
mdg&女■P自m#*∞m自±ni;%*r∞镕*{目.±n5#十^m自*#镕#-m**r*十*∞自*Ⅲ^镕¨目6*&T^&*★f#☆目*m*i镕N日it目r*&#T*tr*自±di目∞镕*£#_:≥…∈一>m<!>n<”“
≥…s。一一∈一∑<>”<
麓筒
万方数据
万方数据
万方数据
四氯化钛水解法制备二氧化钛纳米晶的影响因素
作者:张青红, 高濂, 郭景坤, ZHANG Qing-Hong, GAO Lian, GUO Jing-Kun
作者单位:中科院上海硅酸盐研究所高性能陶瓷和超微结构国家重点试验室,上海 200050
刊名:
无机材料学报
英文刊名:JOURNAL OF INORGANIC MATERIALS
年,卷(期):2000,15(6)
被引用次数:88次
参考文献(13条)
1.Wang R;Hashimoto K;Fujishima A查看详情 1997
2.高濂;陈锦元;黄军华查看详情 1995(04)
3.宋哲;高濂;李强查看详情 1997(03)
4.Kumar K-N P;Keizer K;Burggraaf A查看详情 1992
5.Kumar K-N P;Kumar J;Keizer K查看详情 1994(05)
6.Bacsa R R;Kiwi J查看详情[外文期刊] 1998
7.张青红;高濂;郭景坤四氯化钛水解法制备纳米氧化钛超细粉体[期刊论文]-无机材料学报 2000(01)
8.Matijevic E;Budnik M;Meites L查看详情[外文期刊] 1977(02)
9.Kormann C;Bahnemann D W;Hoffmann M R查看详情 1988
10.Brus L E查看详情 1984(09)
11.张青红;高濂;郭景坤量子尺寸氧化钛纳米晶的制备及其光谱研究[期刊论文]-无机材料学报 2000(05)
12.Wang Y;Herron N查看详情 1990(11)
13.Wang Y;Herron N查看详情[外文期刊] 1991
本文读者也读过(2条)
1.张青红.高濂.郭景坤.ZHANG Qing-Hong.GAO Lian.GUO Jing-Kun四氯化钛水解法制备纳米氧化钛超细粉体[期刊论文]-无机材料学报2000,15(1)
2.张青红.高濂.郭景坤.ZHANG Qing-Hong.GAO Lian.GUO Jing-Kun二氧化钛纳米晶的光催化活性研究[期刊论文]-无机材料学报2000,15(3)
引证文献(84条)
1.周建敏.牛显春.熊德琴.何永信.谢爱亮纳米TiO2光催化法处理炼油废水的研究[期刊论文]-工业用水与废水2006(6)
2.刘波.岳林海.李国华.宋旭春.陈卫祥.徐铸德纳米二氧化钛粉体表面的吸附特征及其对粉体分散性的影响[期刊论文]-浙江大学学报(理学版) 2004(1)
3.王玉琨.吴金桥制备条件对纳米TiO2粒子粒径与形貌的影响[期刊论文]-西安石油学院学报(自然科学版)
2003(2)
4.汤佳.钟世安.肖文ZnO/TiO2纳米管的制备及光降解性能研究[期刊论文]-化工新型材料 2010(8)
5.王兆波.彭红瑞.王新.张志煙HIPS/nano-TiO2复合材料的吸光及光老化性能研究[期刊论文]-材料科学与工艺2006(6)
6.周少丽.杨亚婷纳米TiO2的制备及光催化性能的研究[期刊论文]-应用化工 2010(8)
7.燕青芝.宿新泰.周艳平.葛昌纯Sol-gel自蔓燃法控制合成二氧化钛纳米粉体及性能[期刊论文]-物理化学学报
2005(1)
8.艾照全.孙桂林.周奇龙.石慧.何培新水分散型TiO2/聚丙烯酸酯纳米复合材料的制备[期刊论文]-化学与生物工程 2004(6)
9.方世杰.徐明霞.郝俊杰.汪成建水解沉淀法制备纳米TiO2及其表征[期刊论文]-天津大学学报(英文版) 2002(2)
10.刘萃莲.徐秀东.谭忠含钛高沸物的再利用研究[期刊论文]-石化技术 2009(2)
11.李灵芝.李建渠TiO2制备条件对硝基苯光催化降解效果的影响[期刊论文]-广东化工 2007(11)
12.魏绍东.殷道纯以TiCl4为原料制备纳米TiO2技术的研究进展--液相法[期刊论文]-现代涂料与涂装 2006(5)
13.王兆波.方辉.王许云.王新.张志焜LLDPE/LDPE/TiO2复合膜的分散及光学性能[期刊论文]-现代塑料加工应用2005(4)
14.赵国栋非晶态TiO<,2>:W薄膜的制备及光催化性能的研究[学位论文]硕士 2005
15.古映莹.邱小勇.杜作娟不同晶型纳米TiO2的水热合成及光催化性能[期刊论文]-化工新型材料 2004(3)
16.陈桂华.梁华定.潘富友.陈刚钼掺杂对纳米TiO2粉体相结构的影响[期刊论文]-科学技术与工程 2008(21)
17.王乐飞.杨志宁.阮丽萍.张昭超声洗涤水合二氧化钛的研究[期刊论文]-电子元件与材料 2005(3)
18.陈文新.黄浪欢.刘应亮.王朋.张静娴.容建华.汤丽娜微波法制备纳米TiO2[期刊论文]-化学研究与应用
2004(5)
19.王兆波.彭红瑞.张志煜家电用HIPS/nano-TiO2多功能复合材料的性能[期刊论文]-青岛科技大学学报(自然科学版) 2004(2)
20.王玉琨.吴金桥离子对纳米TiO2粉体晶型转化的影响[期刊论文]-西安石油学院学报(自然科学版) 2003(1)
21.郑珊.张青红.高濂.郭景坤纳米氧化钛光催化降解苯酚活性研究[期刊论文]-贵金属 2003(4)
22.丁士文.董伟.王利勇.王静.齐化杰.李南南混晶纳米TiO2的制备及对含氰废水的降解研究[期刊论文]-湘潭大学自然科学学报 2008(1)
23.张永芬.赵菁.丁士文.王利勇混晶纳米TiO2分散乳液的制备及其光催化性能[期刊论文]-河北大学学报(自然科学版) 2008(4)
24.颜鲁婷.司文捷.苗赫濯纳米TiO2光催化材料的研究进展[期刊论文]-材料科学与工程学报 2004(5)
25.国伟林.杜红.王西奎掺银二氧化钛的超声化学法制备与光催化性能研究[期刊论文]-济南大学学报(自然科学版) 2004(4)
26.刘彦平.杨志远改性纳米TiO2降解水中微量次甲基蓝的动力学研究[期刊论文]-应用化学 2006(9)
27.王振兴.丁士文.张美红高分散纳米二氧化钛混合晶体的合成、结构与光催化性能[期刊论文]-无机化学学报2005(3)
28.周武艺.唐绍裘.万隆.李得意.张世英制备条件对纳米TiO2晶型及其晶相含量影响的研究[期刊论文]-稀有金属2004(4)
29.王许云.王兆波.王新.臧云涛LLDPE/LDPE/纳米TiO2复合薄膜的性能[期刊论文]-合成树脂及塑料 2004(6)
30.蒋引珊.金为群.张军.方送生TiO2/沸石复合物结构与光催化性能[期刊论文]-无机材料学报 2002(6)
31.范拴喜纳米二氧化钛光催化剂制备方法研究进展[期刊论文]-无机盐工业 2010(11)
32.李秀艳.杨贤锋.吴明娒不同介质中水热合成纳米TiO2粉体及其光催化性能研究[期刊论文]-无机材料学报2008(6)
33.李灵芝.李建渠.包国成自蔓燃工艺制备纳米TiO2降解制药废水的研究[期刊论文]-化学研究与应用 2008(4)
34.陈云华.林安.甘复兴渗透水解TiCl4制备纳米TiO2[期刊论文]-无机材料学报 2007(1)
35.丁士文.张永芬.杨润蕾日光灯光响应混晶纳米TiO2乳液的制备及抗菌性能[期刊论文]-应用化学 2007(12)
36.范晶.梁英.夏晓红.姜云.贾志杰酸性条件下金红石型TiO2纳米单晶的直接合成[期刊论文]-材料工程 2006(z1)
37.徐惠.王毅.苟国俊.翟钧.曲晓丽.史建新纳米TiO2的制备表征及其光催化性能研究[期刊论文]-兰州理工大学学报 2005(4)
38.王兆波.叶林忠.张志焜HIPS/纳米TiO2复合材料综合性能的研究[期刊论文]-工程塑料应用 2003(11)
39.丁士文.王利勇.丁宇.张美红.王振兴微波加热反应制备纳米TiO2混晶及其光催化性能[期刊论文]-应用化学2006(6)
40.王兆波.王新塑料用抗菌剂的现状及发展[期刊论文]-现代塑料加工应用 2004(2)
41.许璞.高善民.黄柏标.戴瑛.徐彦宾.李少英.朱先俊纳米TiO2光催化降解次甲基蓝的影响因素研究[期刊论文]-微纳电子技术 2008(10)
42.刘秀红.赵尹.姜海波.干路平.李春忠扩散火焰法制备TiO2纳米晶及其光催化活性[期刊论文]-华东理工大学学报(自然科学版) 2007(2)
43.宋秀芹.杨晓辉.陈汝芬.魏雨纳米结构TiO2/PS及TiO2空心球的自组装与表征[期刊论文]-化学学报 2006(3)
44.吴树新.尹燕华.马智.秦永宁.齐晓周.梁珍成超声水解法制备的纳米二氧化钛光催化性能的研究[期刊论文]-分子催化 2005(3)
45.李桂花日光灯光响应混晶纳米TiO2的制备及光催化性能[期刊论文]-陶瓷学报 2011(2)
46.艾照全.李吉莉.胡瑛反应型乳化剂在聚丙烯酸酯与纳米二氧化钛复合乳液中的应用[期刊论文]-粘接 2010(2)
47.钱红梅.吴杰颖.李燕.郝成伟液相法制备纳米TiO2[期刊论文]-皖西学院学报 2005(2)
48.刘威.陈爱平.林嘉平.戴智明.邱炜.刘伟.朱孟钦.臼田昭司均相水解法制备金红石含量可控的纳米TiO2[期刊论文]-化学学报 2004(12)
49.Shenghung WANG.Kuohua WANG.Jihmirn JEHNG.Lichen LIU Preparation of TiO2/MCM-41 by plasma enhanced chemical vapor deposition method and its photocatalytic activity[期刊论文]-环境科学与工程前沿
2012(3)
50.郑华艳.李忠.颜蜀雋.崔丽萍.杨广强TiO2负载SnCl2催化酯交换合成碳酸二苯酯[期刊论文]-太原理工大学学报 2010(5)
51.姜丽娜.刘金华.孟德营二氧化钛光催化技术的应用[期刊论文]-山东陶瓷 2009(5)
52.李娴.霍冀川.叶旭纳米TiO2光催化降解梯恩梯和奥克托今的研究[期刊论文]-含能材料 2008(4)
53.林玉龙.刘朴.魏雨添加剂对TiCl4水解过程中纳米TiO2成核机制的影响[期刊论文]-河北师范大学学报(自然科学版) 2006(1)
54.李国华.郑遗凡.马淳安95℃水溶液体系中TiCl4溶胶水解法制备纯金红石纳米粉体[期刊论文]-无机化学学报2005(8)
55.范荣玉纳米二氧化钛粉体的制备及其在环境保护中的应用[期刊论文]-南平师专学报 2004(2)
56.于宏燕.杨儒.李敏.郭玉宝.张广延锐钛相虫蛀状介孔二氧化钛的表征[期刊论文]-无机化学学报 2003(9)
57.王毅.崔作林.张志焜O2+Ar电弧等离子体法制备球形二氧化钛纳米晶[期刊论文]-无机材料学报 2004(4)
58.李国华.王大伟.徐铸德.黄志良.陈卫祥不同沉淀剂制备的纳米氧化钛粉体晶相控制[期刊论文]-硅酸盐学报2003(3)
59.李国华.王大伟.徐铸德纳米二氧化钛粉体晶相控制实验研究[期刊论文]-无机材料学报 2002(3)
60.张昭.吴潘.王乐飞.康明超声波辐照对水合二氧化钛晶体结构和煅烧二氧化钛粒度的影响[期刊论文]-中国有色
金属学报 2005(2)
61.柏源.孙红旗.金万勤pH值对氮掺杂TiO2物化性质和光催化活性的影响[期刊论文]-无机材料学报 2008(2)
62.辛建华离子掺杂纳米TiO<,2>光催化剂的制备及其性能研究[学位论文]硕士 2005
63.王虹.王鹏铁、铈共掺杂纳米TiO_2溶胶的制备及抗菌性能[期刊论文]-无机化学学报 2009(11)
64.石立杰.杨儒.李敏纳米TiO2低温水解法的晶型控制合成及其表面织构的研究[期刊论文]-无机化学学报
2006(7)
65.倪萌.Leung Michael K.H.Leung Dennis Y.C光催化剂纳米粉体的制备技术[期刊论文]-粉末冶金技术 2006(5)
66.胡蓉蓉负载型金属修饰的复合半导体的制备及光催化CO<,2>和C<,3>H<,8>合成异丁烯醛的反应性能[学位论文]博士 2005
67.赵婷婷.田鹏.苏桂田.吕烨.毛媚.张璐四氯化钛水解法制备TiO2及光催化性能的研究[期刊论文]-沈阳师范大学学报(自然科学版) 2012(2)
68.刘艳敏.张萍.李平蕊.张艳峰.魏雨离子掺杂对提高锐钛型TiO2高热稳定性的影响[期刊论文]-微纳电子技术2008(2)
69.传秀云.卢先初.龚平天然矿物材料的多孔结构、结构组装和光催化性能[期刊论文]-地学前缘 2005(1)
70.许可.吕德义.郇昌永.郑遗凡.葛忠华离子掺杂对纳米二氧化钛晶型转变的影响[期刊论文]-材料科学与工程学报 2005(4)
71.徐建春纳米TiO<,2>基光触媒的可控制备及降解有机废水研究[学位论文]硕士 2005
72.甄志超多功能复合纳米粉体的制备、表面改性及其在纺织材料中的应用[学位论文]硕士 2005
73.传秀云.卢先初.龚平天然矿物材料的多孔结构、结构组装和光催化性能[期刊论文]-地学前缘 2005(1)
74.龚平TiO<,2>-蒙脱石复合材料的制备与光催化性能研究[学位论文]硕士 2004
75.杨莹莹纳米复合催化剂催化氧化环己烷制环己烯的研究[学位论文]硕士 2006
76.刘秀红扩散火焰燃烧合成铜铁掺杂二氧化钛纳米晶及其光催化性能[学位论文]硕士 2007
77.苏会东二氧化钛光催化剂的制备及其性能研究[学位论文]博士 2005
78.刘素文TiO<,2>-ZrO<,2>体系纳米光催化材料的制备及其降解有机污染物的研究[学位论文]博士 2004
79.石立杰纳米TiO<,2>晶型控制合成及负载型TiO<,2>光催化剂的制备与性能表征[学位论文]硕士 2006
80.钱红梅纳米二氧化钛、二氧化锡及其复合粉体的制备与研究[学位论文]硕士 2005
81.刘威均匀水解法制备纳米二氧化钛粉体和薄膜[学位论文]博士 2005
82.姚超纳米TiO<,2>合成、表面处理及其防团聚研究[学位论文]博士 2005
83.朱宝林一维Ti,Ce,Pr氧化物的合成、修饰和催化性能[学位论文]博士 2006
84.鲁厚芳染料敏化二氧化钛纳米晶太阳能电池材料及组件研究[学位论文]博士后 2005
本文链接:https://www.doczj.com/doc/f63407332.html,/Periodical_wjclxb200006006.aspx
四氯化钛制取(preparation of titanium tetrachloride) 以富钛物料为原料,经氯化、冷凝分离、精制等处理产出精四氯化钛的过程,为钛冶金流程的主要组成部分。富钛物料包括金红石、钛渣和人造金红石等。富钛物料氯化产出的是混合炉气,须经过富钛物料氯化产物冷凝分离和粗四氯化钛精制才获得纯的TiCl4。TiCl4是生产金属钛和钛白的原料,亦可用作发烟剂,也是制备TiCl3(制取聚丙烯的催化剂)的原料。 20世纪50年代,随着海绵钛和氯化法钛白的生产发展,TiCl4生产亦达到工业规模。富钛物料氯化早期采用竖炉氯化法生产四氯化铁,随后又发展了熔盐氯化法生产四氯化钛和流态化氯化法生产四氯化钛。1989年世界TiCl4生产能力约400万t/a,其中90%采用流态化氯化法生产。 四氯化钛性质纯四氯化钛为无色透明、密度较大、不导电的液体,未经精制的粗TiCl4一般呈淡黄色或红褐色。TiCl4的主要物理性质列举于表1。 表1 TiCl4的主要物理性质 TiCl4不易燃也不易爆,但挥发性大,与水接触时发生激烈反应,生成容积很大的黄色沉淀(以盐酸与Ti(OH)nCIx分子式表示的化合物),并放出大量热量;在接触大气时即与空气中水分反应,产生有强刺激性和腐蚀性的HCl白烟。所以TiCl4要储存在气密性好的容器中。 纯TiCl4在常温下对铁几乎不腐蚀,粗TiCl4或部分水解的TiCl4中溶有HCl时则会腐蚀铁。TiCl4可溶解多种气体、液体和固体杂质。TiCl4在一定温度下可与氧气、镁、钠及铝发生作用,其反应分别是氯化法生产钛白、镁热还原法生产海绵钛和钠热还原法生产海绵钛以及铝还原法制备TiCl3的基础。 氯化反应富钛物料中的钛除以TiO2形态存在外,在钛渣中还以Ti3O5、 Ti2O3、TiO等形态存在;另含有多种杂质氧化物FeO、Fe2O3、MnO、MgO、CaO、Al2O3、SiO2等。在有碳质还原剂存在时富钛物料中各组分在高温下均可与Cl2反应生成相应的氯化物。其中的TiO2加碳氯化反应为:1/2TiO2+(1+η)/ 2C+Cl2=1/2TiCl4+ηCO+(1—η)/2CO2式中η是表征氧化物加碳氯化时受碳的气化反应影响程度的数值。以TiO2为例,其反应可看作是下面两个反应之和:
纳米二氧化钛的制备及其光催化活性的评价 实验报告 班级: 组别:指导老师: 小组成员:
实验目的: 1. 培养小组自主设计及完成实验的能力和合作能力。 2. 了解纳米二氧化钛的粒性和物性。 3. 掌握溶胶-凝胶法合成TiO2 的方法。 4. 研究二氧化钛光催化降解甲基橙和亚甲基蓝水溶液的过程和性质。 5. 通过实验,进一步加深对基础理论的理解和掌握,做到有目的合成,提高实验思维 与实验技能。 一、溶胶凝胶法制备二氧化钛 1 实验原理:纳米粉体是指颗粒粒径介于1?100 nm之间的粒子。由于颗粒尺寸的微 细化,使得纳米粉体在保持原物质化学性质的同时,与块状材料相比,在磁性、 光吸收、热阻、化学活性、催化和熔点等方面表现出奇异的性能。 纳米Tiθ2具有许多独特的性质。比表面积大,表面张力大,熔点低,磁性强,光吸收性能好,特别是吸收紫外线的能力强,表面活性大,热导性能好,分 散性好等。基于上述特点,纳米Tiθ2具有广阔的应用前景。利用纳米Tiθ2作光 催化剂,可处理有机废水,其活性比普通Tiθ2(约10 μm)高得多;利用其透明性 和散射紫外线的能力,可作食品包装材料、木器保护漆、人造纤维添加剂、化妆 品防晒霜等;利用其光电导性和光敏性,可开发一种Tiθ2感光材料。如何开 发、应用纳米Tiθ2,已成为各国材料学领域的重要研究课题。目前合成纳米二氧 化钛粉体的方法主要有液相法和气相法。由于传统的方法不能或难以制备纳米级 二氧化钛,而溶胶-凝胶法则可以在低温下制备高纯度、粒径分布均匀、化学活 性大的单组分或多组分分子级纳米催化剂[1 ?3],因此,本实验采用溶胶-凝 胶法来制备纳米二氧化钛光催化剂。 制备溶胶所用的原料为钛酸四丁脂(Ti(O-C4H9)4)、水、无水乙醇 (C2H5θH)以及冰醋酸。反应物为Ti(O-C4H9)4和水,分相介质为C2H5OH,冰 醋酸可调节体系的酸度防止钛离子水解过速。使Ti(O-C4H9)4 在C2H5OH中水解生成Ti(OH)4,脱水后即可获得TiO2。在后续的热处理过程中, 只要控制适当的温度条件和反应时间,就可以获得金红石型和锐 钛型二氧化钛。 钛酸四丁脂在酸性条件下,在乙醇介质中水解反应是分步进行的,总水解
2012 /2013 学年第 2 学期环保材料课程考核试卷 A■、B□ 课程代码: 17000450 任课教师_施文健考试形式:开卷■、闭卷□ 课程性质:通识□、基础□、专业■、必修■、选修□、考试□、考查■、指选□、跨选□适用年级/专业二年级/环境工程学分/学时数 2/32 考试时间1周…………………………………………………………………………………………………………学号1117030320 姓名陈柱良专业环境工程得分 撰写小论文:环境工程材料――×××研究进展 学生通过对应用于防止、治理、修复环境污染的材料,包括净化材料、环境修复材料以及环境替代材料等材料中就某一种具体的环境工程材料的研究进展进行综述。学生的工作由国内外文献检索、阅读、归纳总结、并对该研究领域进行展望、小论文写作组成。小论文内容:题目、前言(目的意义)、国内外研究现状包括:材料的制备方法、材料表征、理化性能、在环境工程中的应用,写出学生自己的学习后的认识、观点或展望在该领域研究方向及应用前景。具体要求:查阅的中文文献≥10篇、英文文献≥5篇、小论文字数5000字左右、列出参考文献。
二氧化碳纳米管的制备与应用 前言: 纳米TiO 2是一种重要的无机功能材料,多呈颗粒状,它在环境光催化领域作为催化剂已引起广泛重视[1,2]。由于其具有无毒、气敏、湿敏、介电效应、光电转换、光致变色及催化活性高、氧化能力强、稳定性好等优点[3,4]而被广泛应用于各种光催化反应技术中,如自洁材料、介电材料、催化剂极载体、传感器、光催化太阳能电池、光裂解水制氢以及光催化降解大气和水中污染物等领域。Ti02纳米管是其又一种存在形式,纳米Ti02在光催化降解水中有机污染物方面有明显的优势[5],而且还能够解决汞、铬、铅等金属离子的污染问题。由于纳米管具有大的比表面积,因而具有较高的吸附能力,可望提高其光催化性能;特别是若能在管中填充更小的无机、有机、金属或磁性纳米级颗粒形成一维复合纳米材料,将会大大改善Ti02的光电、电磁、催化及抗菌等性能。目前,对TiO 2纳米薄膜、纳米粉体及掺杂改性的纳米TiO 2复合材料的制备、结构相变及其应用已进行了大量研究。但对于TiO 2纳米管的光电性能、催化性能及其应用的研究还处于起步阶段。TiO 2纳米管是纳米TiO 2的一种新的存在形式,与其他形态的纳米TiO 2材料相比,它具有更大的比表面积和更强的吸附能力,有望进一步提高TiO 2的光电转换效率和光催化性能,特别是若能在该纳米管中掺杂部分无机、有机、金属或者磁性材料而制备出复合纳米材料,则TiO 2纳米管的光电性能和催化活性将得到大大的改善。
纳米二氧化钛的制备方法及形貌特征 盛丽雯重庆交通大学应用化学08300221 摘要:纳米二氧化钛以其优异的性能成为半导体光催化剂的杰出代表,探寻优良的二氧化钛制备工艺有着重要的现实意义。本文主要介绍了近年来国内外纳米二氧化钛制备工艺的研究状况,根据反应体系的物理形态将制备工艺分成气相、液相、固相三大类进行阐述,在此基础上分析比较了不同制备工艺的优缺点,最后展望了今后的发展方向。 关键词:纳米二氧化钛、制备方法、形貌特征。 1 纳米二氧化钛的制备方法 1.1 气相法 气相水解法利用氮气、氧气或空气作载气,把TiC1 或钛醇盐蒸气和水蒸气分别导人反应器,进行瞬间混合快速水解反应。通过改变各种气体的停留时间、浓度、流速以及反应温度等来调节纳米TiO的晶型和粒径。该方法制得的产品纯度高、分散性好、表面活性大,操作温度较低,能耗小,且对材质纯度要求不是很高,可实现连续生产;但控制过程复杂,并且直接影响着产品的晶型和粒径。气相氧化法是以TiC1 为原料,氧气为氧源,氮气作为载气的氧化反应,反应经气、固分离后制得纳米TiO:。该法制得的产品纯度高、分散性好;但设备结构复杂,材料要求耐高温、耐腐蚀,自动化程度高,研究开发难度大。气相氢氧火焰法以TiC1 ,H2,O:为原料,将TiC1 气体在氢氧焰中(700~1 000℃)高温水解制得纳米TiO。产品一般是锐钛型和金红石型的混晶型,产品纯度高、粒径小、表面活性大、分散性好、团聚程度较小,自动化程度高;但所需温度高,对设备材质要求较高,对工艺参数控制要求精确。气相热解法以TiC1 为原料,在真空或原料惰性气氛下加热至所需温度后,导入反应气体,使之发生热分解反应,最后在反应区沉积出纳米TiO。产品化学活性高、分散性好,可以通过控制反应气体的浓度和炉温来控制纳米TiO的粒径分布;但投资大、成本高。 1.2 液相法 溶胶一凝胶法以钛醇盐Ti(OR) 为原料,经水解与缩聚过程而逐渐凝胶化,再经低温干燥、烧结处理即可得到纳米TiO粒子。该法制得的产品纯度高、粒径小、尺寸均匀、干燥后颗粒自身的烧结温度低;但原料价格昂贵、生产成本高,凝胶颗粒之间烧结性差,产物干燥时收缩大。化学沉淀法将沉淀剂加入TiOSO,H TiO,或TiC1 溶液中,沉淀后进行热处理。该法工艺过程简单,易工业化,但易引入杂质,粒度不易控制,产物损失多。水解法以四氯化钛或钛醇盐为原料,经水解、中和、洗涤、烘干和焙烧制得纳米TiO。该法制得的产品纯度高、粒径均匀;但水解速度快、反应难控制、成本大、能耗高、难以工业化生产。水热法以TiOSO,TiC14或Ti(OR)4为原料,高温高压下在水溶液中合成纳米TiO。该法制得的产品纯度高、粒径分布窄、晶型好;但对设备要求高、能耗较大、操作复杂、成本偏高。在综合对比研究了纳米二氧化钛的各种制备方法后,提出了利用偏钛酸原料廉价易得的特点,简化工艺过程,采用化学沉淀法来制备纳米TiO的工艺方案,并进行了长时间的中试,现就该工艺的特点及中试过程中所遇到的问题进行阐述。 1 气相法制备二氧化钛 气相法一般是通过一些特定的手段先将反应前体气化,使其在气相条件下发生物理或化学变化,然后在冷却过程中成核、生长,最后形成纳米TiO2颗粒。 1.1 化学气相沉积法
南京信息工程大学综合化学实验报告 学院:环境科学与工程学院 专业:08应用化学 姓名:章翔宇 潘婷 袁成 钱勇 2010年6月25号
纳米二氧化钛的制备及性质实验 1、实验目的 熟悉溶胶凝胶法制备纳米二氧化钛的方法及相关操作; 理解二氧化钛吸附实验的原理和操作; 掌握数据处理的方法 2、溶胶凝胶法制备纳米二氧化钛 2.1 需要的仪器 恒压漏斗、茄行烧瓶、量筒、移液管、铁架台、磁力搅拌、磁子、冷凝管、温度计、烘箱、研钵 2.2 需要的试剂 钛酸丁酯异丙醇浓硝酸蒸馏水 2.3 实验步骤 1.50ml钛酸丁酯溶16ml的异丙醇中,摇匀(在恒压漏斗中进行) 得到溶液A 2.取200ml 的蒸馏水,加入0.32 ml 的浓硝酸,摇匀(在茄行烧瓶中进行),得到 溶液B 3.将烧瓶固定在铁架台上,进行磁力搅拌,将溶液A 逐滴滴加至溶液B中,使两溶液 缓慢接触,并进行水解反应,得到溶液C 溶液C室温回流,记载下当时的室温 4.回流分若干天进行,保证回流时间不少于48小时,得到溶液D 5.蒸干方式:将溶液D进行水浴加热85度并不断搅拌将水分蒸发干,得E 6.将E放入烘箱100烘干 7.研磨至粉末状; 2.4 实验结果 1、回流分4天进行,总计回流时间50小时,室温为15℃。 2、经研磨,得到白色细粉末状固体。称量得二氧化钛质量为11.233g,理论产量不小于11.785g,损失为产品转移过程中损失。 3、纳米二氧化钛性质实验 3.1 二氧化钛吸附试验 1、仪器:烧杯(500mL),容量瓶(1000mL),样品瓶(6个),电子天平,磨口瓶,超 声波清洗机,玻璃注射器,过滤器,分光光度计 2、试剂:二氧化钛粉末,染料X-3B(分子量615),蒸馏水 3、实验步骤: 1、用电子天平称取60mg染料,配成1000mL的60mg/L溶液(避光保存)。 2、将烧杯润洗后,倒入100ml染料溶液,再倒入称量好的50mg的二氧化钛粉末。 静置后置于超声波清洗机中(70℃超声40分钟,注意避光)。剩余原液取样保存编
储矿备料 1、基本原理 外购的石油焦和氯化钠含有的水分会造成对产品的影响,根据原料的水分要求对石油焦和氯化钠进行微波干燥,通过烘烤物料,蒸发水分,使石油焦和氯化钠含水≤0.5%。 2、工艺流程 氯化工艺 1、基本原理 熔盐氯化是固体含钛物料与气体氯气在介质熔盐里温度为720-800оC 的反应。氯化反应目的是使TiO 2最大程度氯化,TiO 2的氯化速率取决于多种因素,例如温度,氧化物的活性,还原剂及氯化剂的类型,熔盐的物理特性和成分(表面张力、黏度、润湿性)。参与氯化反应组分的催化性能。熔盐氯化主要反应方程式如下: 微波干燥 埋刮板输送 斗式提升 氯化钠 石油焦 送氯化工序 高钛渣 入料仓 拆袋
TiO2+C+2Cl2====TiCl4+CO2 铁,铝,锰,铬的氧化物在和氯气反应后生成的氯化物极易溶解在熔盐中,作为氯化反应的催化剂。在氯化熔盐中,这些氯化物适宜的浓度能增加熔盐的活性,能提高高钛渣的氯化速率。 氯气浓度对氯化反应有很大影响,入炉氯气浓度一般在80%到90%(vol.),其余为空气。氯化反应的温度通过从淋洗循环槽返回的泥浆量调整氯化炉温度。放热反应产生的多余热量蒸发了返炉泥浆中的四氯化钛,然后四氯化钛就和混合炉气一起进入冷凝系统。 生产粗四氯化钛是升华和冷凝的过程。冷凝是改变物质的物理状态,从气相变为液相,而升华是没有经过中间的液相,直接从固相转变为气相,这些过程均伴随着热损失。混合炉气从气相转变为液相或固相的温度取决于混合炉气中各种物质的蒸汽分压。氯化工序的产品是粗四氯化钛,首先冷凝高沸点氯化物,然后冷凝四氯化钛及低沸点氯化物。 2、工艺流程 粗四氯化钛工艺流程图 石油焦氯化钠4 高钛渣 4 氯气 重力收尘淋洗废熔盐送渣场 氯化 收尘渣送渣场
粗TiCl4精制除钒方法及比较 内容提要:1.物理除钒尚未在工业中应用 2.铜除钒法 3.硫化氢出除钒法 4.有机物除钒法 5.铝粉除钒法 关键词:化学除钒
目录: 1. 物理除钒----3 2. 化学除钒----4 2.1 铜除钒法----5 2.1.1 除钒原理----5 2.1.2 除钒流程----6 2.1.3 小结----8 2.2 硫化氢除钒法----9 2.2.1 除钒原理----9 2.2.2 除钒流程----9 2.2.3 小结----11 2.3 有机物除钒法----11 2.3.1除钒原理----11 2.3. 2除钒流程----12 2.3.3 小结----14 2.4 铝粉除钒法----14 2.4.1 除钒原理----14 2.4.2 除钒流程----15 2.4.3 小结----18 总述----18 参考文献----20
氯化法所生产的粗TiCl4中的钒杂质主要是VOCl3和V Cl4,他们的存在使TiCl4呈黄色。“VOCl3是使海绵钛硬度增加的氧和钒的载体。”在海绵钛生产中有很大危害。 精制除钒的目的不仅为了脱色,而且也为了除氧,这是精制昨夜极为重要的环节。 1.物理方法除钒 首先,TiCl4和钒杂质的的沸点和相对挥发度都很小,如TiCl4-VOCl3系中的两组份沸点差为100 ℃,相对挥发度a=1.22;而TiCl4 - V Cl4系两组份沸点差仅为140 ℃。 尽管如此,从理论上讲利用物理方法除杂质钒还是可能的,如采用高效精馏塔除钒,然而高效精馏塔除钒有以下特点: 优点: 无需采用化学试剂 精制过程是连续生产,易自动化 分离出的可直接使用 缺点: 能量消耗大 设备投资大 需解决大功率釜的结构问题 “VOCl3的沸点和TiCl4相接近,用精馏方法来分离就需要装
纳米二氧化钛的制备及其光催化活性评价 实 验 报 告 组别:第七组 组员:曲红玲高晗 班级:应121-2 指导老师:翁永根老师
纳米二氧化钛的制备及其光催化活性评价 一、实验目的 1、掌握利用简单的原料制备纳米材料的基本方法和原理。 2、了解二氧化钛的应用和多种制备方法的优缺点。 3、了解纳米半导体材料的性质。 4、了解纳米半导体光催化的原理。 5、掌握光催化材料活性的评价方法。 二、实验原理 二氧化钛,化学式为2TiO ,俗称钛白粉。多用于光触媒、化妆品,能靠紫外线消毒及杀菌。以纳米级2TiO 为代表的具有光催化功能的光半导体材料,因其颗粒细小、比表面积大而具有常规材料所不具备的优点,以及较高的光催化活性、高效的光点转化性能等,在抗菌除雾、空气净化、废水处理、化学合成及燃料敏化太阳能电池等方面显出广阔的应用前景。 1、纳米二氧化钛的制备 纳米二氧化钛的制备方法有很多。主要分为两类:一类是液相法合成,包括液相沉淀法、液相凝胶法、醇盐水解法、微乳液法及水热法;另一类是气相法合成,包括四氯化钛氢氧焰水解法、四氯化钛气相氧化法、钛醇盐气相氧化法、钛醇盐气相水解法、钛醇盐气相热解法。其中,溶胶凝胶法是近年来制备二氧化钛广泛使用的方法。本试验采用溶胶凝胶法制备二氧化钛。 溶胶凝胶法中,反应物为水、钛酸四丁酯,分相介质为乙醇,冰醋酸可调节体系的酸度防止钛离子水解过度,使钛酸四丁酯在无水乙醇中水解生成()4OH Ti ,脱水后即可得到2TiO 。在后续的热处理过程中,只要控制适当的温度条件和反应时间,就可以得到二氧化钛。 在以乙醇为溶剂,钛酸四丁酯和水发生不同程度的水解反应,钛酸四丁酯在酸性条件下,在乙醇介质中水解反应是分步进行的。 一般认为,在含钛离子溶液中钛离子通常与其它离子相互作用形成复杂的网状基团。上述溶胶体系静置一段时间后,由于发生胶凝作用,最后形成稳定的凝胶。此过程中涉及的反应为: ()()OH H C OH Ti O H H OC Ti 944249444+=+ ()()OH H C TiO H OC Ti OH Ti 942494442+=+ ()O H TiO OH Ti 2242+? 2、光催化活性评价 光触媒在光照条件下(可以是不同波长的光照)所起到的催化作用的化学反应,通称为光反应。光催化一般是多种相态之间的催化反应。 本次试验是进行紫外光催化活性评价,分别通过测量在亚甲基蓝和甲基橙中,反应前
第33卷第1期2016年3月 上海第二工业大学学报 JOURNAL OF SHANGHAI POLYTECHNIC UNIVERSITY V ol.33No.1 Mar.2016 文章编号:1001-4543(2016)01-0010-05 四氯化钛处理对染料敏化太阳能电池性能的影响及 光电致变色器件的构建 李文琴,杜蕾,谷田祯,王轲,王金敏 (上海第二工业大学环境与材料工程学院,上海201209) 摘要:通过将不同浓度的四氯化钛溶液水解,在二氧化钛多孔膜上形成致密的阻挡层薄膜,抑制光生电子与电解液中I? 3 的复合,提高了染料敏化太阳能电池的光电转换效率;将优化后的太阳能电池经外电路与基于普鲁士蓝的电致变色器件连接,构建光电致变色器件。结果表明,经0.1mol/L四氯化钛溶液处理的二氧化钛光阳极的太阳能电池的光电转换效率为4.42%。将该条件下的太阳能电池构建于光电致变色器件中,太阳能电池产生的电压可驱动电致变色器件变色,变色前后器件在700nm波长处的透过率调制幅度可达52.77%。 关键词:四氯化钛;普鲁士蓝;染料敏化太阳能电池;电致变色器件 中图分类号:O614文献标志码:A 0引言 能源是人类社会发展进步的原动力。当前社会的进步和科技的飞速发展在大幅提高人们生活质量的同时,也引发了日益突出的能源和环境问题。太阳能具有清洁、储量丰富及无地域局限的特点,而且太阳辐射的能量足以满足人类对能量的全部需求,通过光伏效应实现太阳能向电能的转换是太阳能利用的重要途径[1]。自1991年O’Regan等[2]将纳晶多孔二氧化钛薄膜引入到染料敏化太阳能电池(DSSCs)中作为光阳极,实现了光电转换效率7.1%的突破以来,因其具有性价比高、成本低廉、便携性好等特点,各国科学家掀起了研究DSSCs的热潮。 DSSCs通常为采用染料敏化的二氧化钛膜为光阳极、溶有氧化还原介质的溶液为电解液、Pt电极为对电极的三明治结构。DSSCs的工作原理是:在太阳光辐照下,光敏染料从基态跃迁到激发态,并向二氧化钛导带中注入电子,电子被光阳极导电基底收集并经外电路流入对电极[3]。失去电子的氧化态染料可经电解液中的氧化还原介质还原得以再生,从而保障电池持续有效的光电转换过程。在电池工作中,注入到二氧化钛导带中的电子也可能与氧化态染料或电解液中的氧化介质发生复合,从而造成光电流的损失(暗电流)。对染料结构的有效修饰[4-6]、引入共吸附剂[7-9]或在二氧化钛膜上叠加一层致密的薄膜[10],都可以有效地抑制光生电子的复合反应,提高光电流。 除了开发清洁的可再生能源外,降低能耗也是解决能源和环境问题的有效手段。将电致变色智能窗(Smart Windows)应用到建筑物等场合,可以通过改变材料的光学性质,调节外界热辐射和内部热扩散,减少建筑物实现冬暖夏凉所需的能耗,达到节能减排的目的[11]。普鲁士蓝是一种阳极电致变色材料,具有颜色转换可逆及响应速度快等优点,其本身为蓝色,在负电压作用下由于电子和离子同时注入而转变为普鲁士白(其薄膜无色透明),普鲁士白在正电压作用下由于电子和离子同时抽出而又转变为普鲁士蓝。然而这类材料的变色过程需要外加电压的驱动,这与节能减排的初衷相矛盾,如能将太阳能 收稿日期:2015-11-11 通信作者:王金敏(1975–),男,山东人,教授,博士,主要研究方向为光电功能材料、微纳材料与器件。 电子邮箱wangjinmin@https://www.doczj.com/doc/f63407332.html,。 基金项目:上海高校特聘教授(东方学者)岗位计划(No.2013-70)、上海市青年科技英才扬帆计划(No.14YF1410500)、国家自然科学基金(No.61376009)、上海高校青年教师培养资助计划(No.ZZegd14011)、上海第二工业大学校级科研项目(No.EGD13XQD08)资助
1. 纳米TiO 2粉体制备方法 物理法 气相冷凝法: 预先处理为气相的样品在液氮的气氛下冷凝成核制得纳米TiO2 粉体,但该法不适于制备沸点较高的半导体氧化物 高能球磨法: 工艺简单,但制得的粉体形状不规则,颗粒尺寸分布宽,均匀性差 化学法 固相法: 依靠固体颗粒之间的混合来促进反应,不适合制备微粒 液相法: 就是将钛的氯化物或醇盐先水解生成氢氧化钛(或羟基氧钛) ,再经煅烧得到TiO2. 研究最广泛。 以四氯化钛为原料,其反应为 TiCl4 + 4H2O → Ti (OH) 4 + 4HCl , Ti (OH) 4 → TiO2 + 2H2O. 以醇盐为原料,其反应为 Ti (OR) 4 + 4 H2O → Ti (OH) 4 + 4 ROH , Ti (OH) 4 ???→煅烧 TiO2 + 2 H2O. 主要包括硫酸法、水解法、溶胶-凝胶(Sol2gel) 法、超声雾化、热解法等。 溶胶- 凝胶法就是将钛醇盐制备成二氧化钛溶胶. 为了得到多孔催化剂,通常采用煅烧等方法将凝胶进行干燥,去除溶剂,制得干凝胶. Dagan 等[25 ]采用超临界干燥法所制得的TiO2气凝胶孔隙率为85 % ,比表面积高达600 m2·g - 1 ,晶粒尺寸为5. 0 nm ;对水杨酸的光催化氧化表明该催化剂具有比Degussa P - 25 TiO2粉末更高的催化活性.
气相法: 其核心技术是反应气体如何成核的问题. 通过四氯化钛与氧气反应或在氢氧焰中气相水解获得纳米级TiO2 ,目前德国Degussa 公司P-25 粉末光催化剂是通过该法生产的 常用的化学制备方法有溶胶-凝胶法、沉淀法、水解法、喷雾热解法、水热法和氧化- 还原法等。 2. 纳米TiO2薄膜制备方法: 除了与粉体制备相同的制备方法如溶胶-凝胶法、热解法外,还有液相沉积法、化学气相沉积法、磁控溅射法等。 溶胶-凝胶法(Sol-Gel): 制备的薄膜纯度高,且制备工艺简单,易批量生产; 水热合成法: 通过水解钛的醇盐或氯化物前驱体得到无定形沉淀,然后在酸性或碱性溶液中胶溶得到溶胶物质,将溶胶在高压釜中进行水热Ostwald熟化。熟化后的溶胶涂覆在导电玻璃基片上,经高温(500℃左右)煅烧,即得到纳米晶TiO2薄膜。也可以使用TiO2的醇溶液与商业Ti02(P25,3Onm)混合以后得到的糨糊来代替上面提到的溶胶。反应中为了防止颗粒团聚,通常采用化学表面改性的方法,如加有机螫合剂、表面活性剂、乳化剂等,以降低粉末表面能,增加胶粒问静电排斥,或产生空问位阻作用而使胶体稳定。这些有机添加剂在高温煅烧阶段会受热分解除去. 是溶胶-凝胶法的改进方法,主要在于加入了一个水热熟化过程,由此控制产物的结晶和长大,继而控制半导体氧化物的颗粒尺寸和分布,以及薄膜的孔隙率.得到的Ti02颗粒是锐钛矿型还是锐钛矿型与金红石型的混合物由反应条件(如煅烧温度)决定。水热处理的温度对颗粒尺寸有决定性的影响。一般来说,将溶胶在高压釜中(150Xl05~330×105Pa)于200~250℃处理12h,可得到平均粒径15~20nm的Ti02颗粒。如果用丝网印刷术(也可用刮涂的方法)将TiO2溶胶涂覆在导电玻璃上,则得到
粗四氯化钛的主要杂质---乘钒钛文化之风创钒钛经 济之业 原创邹建新等 粗四氯化钛必须进行精制,否则由于杂质的影响将大大地影响下游钛产品的加工性能。粗四氯化钛是一种红棕色浑浊液,含有许多杂质,成分十分复杂。 粗四氯化钛的主要杂质 粗四氯化钛中重要的杂质有SiCl4、AlCl3,FeCl3、FeCl2、VOCl3、TiOCl2、Cl2、HCl等。这些杂质在四氯化钛液中的含量是随氯化所用原料和工艺过程条件不同而异的。对于用作制取海绵钛的TiCl4原料而言,这些杂质几乎都是程度不同的有害杂质,特别是含氧、氮、碳,铁、硅等杂质元素。对于制取颜料钛白的原料而言,特别要除去使TiCl4着色(也就是使TiO2着色)的杂质,如VOCl3、VCl4、FeCl3、FeCl2、CrCl3、MnCl2和一些有机物等,但TiOCl2则不必除去。 1.杂质的类型 按杂质在TiCl4冷凝过程中所收集到的物态和溶解度的不同,粗四氯化钛中的杂质主要包括可溶性气体、液体、固体和不溶性固体悬浮物四大类,如表4.6.3所示。 表4.6.3 粗四氯化钛中的主要杂质分类 可溶于TiCl4中常温下为气体H2、O2、HCl、Cl2、CO、CO2、COCl2、COS 常温下为液体S2Cl2、CCl4、VOCl3、SiCl4、CHCl3、CCl3COCl、SnCl4、CS2
的杂质常温下为固体AlCl3、FeCl3、NbCl5、TaCl5、MoCl5、C6Cl6、TiOCl2、Si2OCl6固体悬浮物TiO2、SiO2、MgCl2、ZrCl4、FeCl2、C、FeCl3、MnCl2、CrCl3 TiCl4是从氯化过程的气体中冷凝得到的,在TiCl4液化时(TiCl4熔点-23.6℃,沸点135.9℃)有些杂质溶于TiCl4中,淋洗TiCl4时也掺入不熔固体杂质。这些杂质在四氯化钛液中的含量随氯化所用原料和工艺过程条件不同而异。杂质含量如表4.6.4所示。 2.除去杂质的方法 对于不溶悬浮固体杂质(TiO2、SiO2、VOCl3、MgCl2、ZrCl4、FeCl2、MnCl2、CrCl3),可用固液分离方法除去,工业中因TiCl4中浆黏度大过滤困难,通常采用沉降方法分离。对可溶性气体杂质,在处理过程会中随温度的升高而除去。而可溶性液体和固体类杂质因溶解在TiCl4中,属于难分离杂质,这类杂质可依据其沸点的不同除去。表4.6.5所列一些物质的沸点数据,如控制温度在136℃以下降低沸点杂质除后,剩余的VOCl3和Al2Cl6再用化学方法除去。 表4.6.4 粗TiCl4中杂质的大致含量(质量分数),% 生产 方法TiCl4 杂质成分 Fe Al Mn Si V 游离Cl2 固体悬浮物 /g.L-1 竖炉 氯化 >98 0.004 0.01 0.009 0.07 0.08 3.6 熔盐>98 0.0002 0.001 0.001 0.08 0.05 3.1
四氯化钛工艺规程 目录 一、产品说明 二、原料说明 三、生产原理 四、生产工艺流程 五、岗位操作 六、安全注意事项 七、分析检测控制一览表 八、废物一览表 九、消耗定额 十、设备一览表 金太化工有限公司 2008年1月1日一、产品说明
1、 简介:学名四氯化钛,商品名四氯化钛,分子式:TiCl 4 分子量:189.712 2、 物理性质:常温下四氯化钛为无色透明的液体,在空气中发白烟。物理常数如下:(1)沸点:136.4℃ (760mmHg 柱)(2)熔点:-25℃(3)不同温度下的比重(液体) (4)蒸气压力logP=7.64433-1947.6/T(mmHg 柱)(5)临界温度358℃(6)比热 液体C P =35.7卡/克分子·度 气体C P =24.87+1.09 ×10-3 -2.08×105 T -2 (7)在不同温度下的粘度(液体) (8)蒸发热:20℃ γ=8.96 千卡/克分子,沸点γ=13.05-0.0115T 千卡/克分子(9)熔化热:2.24千卡/克分子 (10)导热系数 (11)表面力 (12)介电常数 (13)平均体膨胀系数 0.001086(0--100℃)(14)熵四氯化钛(固) S 0 298=34.4卡/克分子.度四氯化钛(液) S 0 298=60.4卡/克分子.度 四氯化钛(气) S 0 298=84.4卡/克分子.度 (15)生成热 TiCl 4(气) △H 298=-182.4仟卡/克分子 TiCl 4(液) △H 298=-192.3仟卡/克分子TiCl 4(固) △H=-198.5仟卡/克分子(00 K) 3、 化学性质 (1) 与碱金属或碱土金属进反应生成低价氯化物或金属钛 TiCl 4+2Na= TiCl 2+2NaCl TiCl 4+2Na=Ti+4NaCl TiCl 4+2Mg= Ti+2MgCl 2 (2)与氢进行反应生成钛的低价氯化物 2TiCl 4+H 2= TiCl 3+2HCl (800℃) (3)与水反应,四氯化钛与水反应很剧烈,并放出热量。 TiCl 4+H 2O →TiCl 3(OH)·4H 2O+HCl →TiCl 2(OH)2·3H 2O+HCl →TiCl(OH)3·2H 2O+HCl →Ti(OH)4+HCl 在高温下反应过程很快就进行到底,生成偏钛酸:
纳米二氧化钛制备方法 陈早明 郑典模 (南昌大学环境与化学工程学院 江西南昌330029) 摘 要 文章阐述了纳米二氧化钛粒子的制备方法,和各种制备方法的所具有的特点。并提出了目前制备方法所存在的一些不足之处。 关键词:二氧化钛 纳米 制备 1 引言 纳米微粒是指颗粒尺寸为纳米量级的超细微粒,它的尺寸大于原子簇,小于通常的微粉。通常,把仅包含几个到数百个原子或尺度小于lnm的称为“簇”,而把粒径在1—100nm之间微粒称为纳米粒子。当小粒子尺寸进入纳米量级时,其本身就具有了量子尺寸效应,小尺寸效应,表面效应和量子隧道效应,因而展现许多特有的性质,在催化、滤光、光吸收、医药、磁介质及新材料等方面具有广阔的应用前景。而纳米二氧化钛(T i02)由于其具有粒径小、比表面积大、磁性强、光催化、吸收性能好,吸收紫外线能力强,表面活性大、热导性好、分散性好、所制悬浮液稳定等优点。因此倍受关注,制备和开发纳米二氧化钛成为国内外科技界研究的热点之一。(1) 2 纳米二氧化钛的制备方法 纳米二氧化钛的制备方法可分为气相法和液相法两大类。 2.1 气相制备法 2.1.1 低压气体蒸发法(1) 此种制备方法是在低压的氩、氮气等惰性气体中加热普通的T i02,然后骤冷生成纳米二氧化钛粉体,其加热源有以下几种:(1)电阻加热法;(2)等离子喷射法;(3)高频感应法;(4)电子束法;(5)激光法,这些方法可制备lOOnm以下的二氧化钛粒子。 2.1.2 活性氢—熔融金属反应法 含有氢气的等离子体与金属钛之间产生电弧,使金属熔融,电离的N2,Ar等气体和H2溶入熔融金属,然后释放出来,在气体中形成了金属的超微粒子,用离心收集器或过滤式收集器使微粒与气体分离而获得纳米二氧化钛微粒。 2.1.3 溅射法(1) 此方法是用两块金属板分别作为阳极和阴极,阴极为蒸发用的材料,在两电极间充入Ar 气,两电极间施加的电压范围为0.3—1.5kV。由于两电极间的辉光放电使Ar离子形成。在电场的作用下Ar离子冲击阴极靶材表面,靶上的T i02就由其表面蒸发出来,被惰性气体冷却而凝结成纳米T iO2粉末,粒度在50nm以下,粒径分布较窄。 2.1.4 流动液面上真空蒸发法 用电子束在高真空下加热蒸发T iO2,蒸发物落到旋转的圆盘下表面油膜上,通过圆盘旋转的离心力在下表面上形成流动的油膜,含有超微粒子的油被甩进了真空室的壁面,然后在真空下进行蒸馏获得T iO2超微粒子。 2.1.5 钛醇盐气相水解法(2) 该工艺最早是由美国麻省理工大学开发成功的,可以用来开发单分散的纳米T iO2,其反应式如下: nT i(0R)4,+2nH2O(g)————>nT iO2(s)
四氯化钛工艺流程 储矿备料 1、基本原理外购的石油焦和氯化钠含有的水分会造成对产品的影响,根据原料的水分要求对石油焦和氯化钠进行微波干燥,通过烘烤物料,蒸发水分,使石油焦和氯化钠含水≤0.5%。 2、工艺流程氯化工艺1、基本原理熔盐氯化是固体含钛物料与气体氯气在介质熔盐里温度为720-800оC的反应。氯化反应目的是使TiO2最大程度氯化,TiO2的氯化速率取决于多种因素,例如温度,氧化物的活性,还原剂及氯化剂的类型,熔盐的物理特性和成分(表面张力、黏度、润湿性)。参与氯化反应组分的催化性能。熔盐氯化主要反应方程式如下: 微波干燥埋刮板输送斗式提升氯化钠石油焦送氯化工序高钛渣入料仓拆袋 TiO2+C+2Cl2====TiCl4+CO 2 铁,铝,锰,铬的氧化物在和氯气反应后生成的氯化物极易溶解在熔盐中,作为氯化反应的催化剂。在氯化熔盐中,这些氯化物适宜的浓度能增加熔盐的活性,能提高高钛渣的氯化速率。氯气浓度对氯化反应有很大影响,入炉氯气浓度一般在80% 到90%(vol.),其余为空气。氯化反应的温度通过从淋洗循环槽返回的泥浆量调整氯化炉温度。放热反应产生的多余热量蒸发了返炉泥浆中的四氯化钛,然后四氯化钛就和混合炉气一起进入冷凝系统。生产粗四氯化钛是升华和冷凝的过程。冷凝是改变物质的物理状态,从气相变为液相,而升华是没有经过中间的液相,直接从固相转变为气相,这些过程均伴随着热损失。混合炉气从气相转变为液相或固相的温度取决于混合炉气中各种物质的蒸汽分压。氯化工序的产品是粗四氯化钛,首先冷凝高沸点氯化物,然后冷凝四氯化钛及低沸点氯化物。2、工艺流程粗四氯化钛工艺流程图 石油焦氯化钠4 高钛渣4 氯气重力收尘淋洗废熔盐送渣场氯化收尘渣送渣场 粗四氯化钛5、主要生产过程及技术参数外购的NaCl和石油焦(含水量都为1%),人工开袋后送入各自料仓,经微波干燥后(含水量都变为0.5%)皮带输送到斗式提升机,再由斗式提升机送到各自干燥后料仓,然后由埋刮板输送机送到氯化工段的氯化钠仓和煅后焦仓;外购和自产的高钛渣,人工开袋后送入高钛渣料仓,经埋刮板输送机送到斗式提升机,再由斗式提升机送到高钛渣干燥后料仓,然后由埋刮板输送机送到氯化工段的高钛渣仓。高钛渣仓、煅后石油焦仓、氯化钠仓的物料通过物料输送管线输送到氯化炉炉前料仓进行配料后通过螺旋给料机连续地将物料从炉前料仓送到熔盐表面与通过氯气喷枪供应到熔盐里,使用温度为≤一级冷凝二级冷凝沉降 60℃,压力为0.12MPa的混合氯气,在温度为700 °С到800 °С的熔盐中进行氯化反应。反应后产生的700 oС废熔盐从上部排盐口通过排盐管排放到熔盐渣箱里之后送渣场填埋。而生成的四氯化钛,以四氯化钛蒸汽和气体混合物通过顶部排气口进入收尘器,收尘器入口的蒸汽和气体混合物温度是400-500 oС,一些高沸点和低沸点氯化物被冷凝,并和固体颗粒物一起沉降在收尘器器壁上,通过收尘器筒体流入收尘渣罐之后送渣场填埋。未被冷凝下来的四氯化钛蒸汽和气体混合物进入一级淋洗塔,一级淋洗塔入口的蒸汽和气体混合物温度是450 oС,在淋洗塔里被用循环水冷却过的四氯化钛喷淋,之后液体进入淋洗循环槽,淋洗循环槽的温度是100 oС,一部分浆料返回氯化炉进行温度控制,一部分打到套管冷却器进行冷却。当淋洗循环槽过满时会通过溢流口流到事故槽里。四氯化钛蒸汽和气体混合物进入二级淋洗塔,二级淋洗塔入口的蒸汽和气体混合物温度是110 oС,被四氯化钛喷淋后液
第 页(共 页) 课 程 ___________ 实验日期:年 月曰 专业班号 _____ 别 ______________ 交报告日期: 年 月 日 姓 名_ _学号 报告退发: (订正、重做) 同组者 _____________ 次仁塔吉 __________ 教师审批签字: 实验名称 _________________ 纳米二氧化钛粉的制备及其光催化活性的测试 、实验目的 1. 了解制备纳米材料的常用方法,测定晶体结构的方法。 2. 了解XRD 方法,了解X-射线衍射仪的使用,高温电炉的使用 3. 了解光催化剂的(一种)评价方法 、实验原理 1.纳米TiO 2的制备 ① 纳米材料的定义:纳米材料指的是组成相或者晶相在任意一维度上尺寸小于 100nm 的材 料。 纳米材料由于其组成粒子尺寸小, 有效表面积大,从而呈现出小尺寸效应, 表面与界面效应 等。 ② 纳米TiO 2的制备方法:溶胶凝胶法,水热法,火焰淬火掺杂法,阳极氧化法,电泳沉积 再阳极氧化法,高温雾化法,溅射法,光沉积法,共沉淀法。 本实验采取最基本的,利用金属醇盐水解的方法制备纳米 TiO 2,主要利用金属有机醇盐能 溶于有机溶剂,且可以水解产生氢氧化物或氧化物沉淀。 该方法的优点:①粉体的纯度高,②可制备化学计量的复合金属氧化物粉末。 西安交通大学化学实验报告
③制备原理:利用钛酸四丁酯的水解,反应方程如下 Ti OC4H9 4 4出0 =Ti OH 4 4C4H9OH Ti OH 4 Ti OC4H9 4=TiO2 4C4H9OH Ti OH 4 Ti OH 4=TiO2 4H2O 2. TiO 2的结构及表征 我们通过实验得到的TiO 2是无定形的,二氧化钛通常有如下图上所示的三种晶状结构: A:板钛矿B:锐钛矿C:金红石 无定形的TiO2在经过一定温度的热处理后,会向锐钛矿型转变,温度更高会变成金红石型。 我们可以通过X-射线衍射仪测定其晶体结构。 纳米TiO 2的景行对其催化活性影响较大,由于锐钛矿型TiO 2晶格中含有较多的缺陷和缺位,能产生较多的氧空位来捕获电子,所以具有较高的活性;而具有最稳定晶型结构的金红石型TiO2,晶化态较好,所以几乎没有光催化活性。 多晶相样品根据XRD测试获得XRD图谱。根据图谱的衍射角度对应的峰,我们可以测定 各晶相的含量。【用晶相含量百分比表示】(其中20-25为金红石型的特征衍射峰,25-27 为锐钛矿型的特征衍射峰) C A A 100% A A A R 同时,根据XRD图谱可以估计样品的直径
TiO2纳米管的制备及其亲水性研究 一, TiO2纳米管的制备 1 实验方法:阳极氧化法。 2 实验原料及仪器:纯钛片 0.5%HF溶液稳压电源烧杯吹风机镊子 3 二氧化钛纳米管阵列形成机理 电化学阳极氧化法形成TiO2纳米管阵列的过程是电场作用下,浸入HF电解液中的钛基体表面阻挡层与电解液界面处出现TiO2生成和TiO2的化学溶解并生成纳米管的过程。在阳极氧化过 程的开始阶段,钛基体与电解液中的 O-2或OH-迅速生成一层很薄的氧化层,即阻挡层,并在 形成的阻挡层两边产生较大电场。在电场的作用下,电解液中的氟离子定向撞击阳极钛基体表面并与之发生反应,从而在阻挡层的表面形成许多小凹坑,下述反应式表明阻挡层小凹坑 的形成原因: 随着TiO2生成和TiO2的化学溶解之间达到平衡,小凹坑逐渐变深进而形成纳米管。 4 实验装置: 4 实验步骤:○1取9片纯钛片磨平,用蒸馏水清洗后分3组,每组3片。(只用蒸馏水清 洗吗?) ○2将氧化设备浸入体积分数为0.5%的HF溶液中,调节稳压电源使电压稳定在15V. ○3取第一组3片纯钛片编号为1,2,3 分别固定在阳极侵入HF溶液中反应35,40,45 分钟。 ○4待反应完成后将钛片取出,取出时注意标记钛片的正反面(对着阴极为正面),用吹风机将钛片吹干
○5调节稳压电源使电压稳定在20V 取第二组钛片编号4,5,6号,重复○3○4步操作 ○6调节稳压电源使电压稳定在25V 取第三组钛片编号 7,8,9号,重复○3○4步操作 4 实验现象: 没通电时Ti片表面有大量气泡冒出,接通电源后阴极有气泡出现并与阳极气泡一同消失。制得样品吹干后表面呈浅绿色或淡紫色。 二, 亲水性的测量 1. 原理:TiO2纳米管的亲水性可通过测出水滴在其表面的接触角直观明了的表示出来。 2. 仪器:注射器,接触角测量仪,蒸馏水 3. 步骤:用注射器吸入蒸馏水,分别测出水在 9片样品表面的接触角,并且测出样品正反两面的接触角 4. 将测得数据记录在下面表格中 保存好标红色的这几个样品,开学拿去做扫描电镜。 由表中数据看出接触角最大的是第5号样品,分析表中数据可得出阳极氧化法制TiO2纳米管阵列最佳条件为:电压20V,反应时间为40分钟。 三,最佳条件下亲水性测量 再取6片磨平纯钛片分别在20V电压下反应40分钟制取TiO2纳米管阵列
纳米二氧化钛的制备方法综述
纳米二氧化钛的制备方法综述 【摘要】纳米二氧化钛(Ti02)具有粒径小、比表面积大、磁性强、光催化、
吸收性能好,吸收紫外线能力强,表面活性大、热导性好、分散性好、所制悬浮液稳定等优点倍受关注,制备和开发纳米二氧化钛成为国内外科技界研究的热点之一。本文主要对纳米二氧化钛的各种制备方法作了简单介绍。 【关键词】纳米二氧化钛、制备 【正文】二氧化钛的制备方法可分为气相法和液相法两大类。 一、气相制备法 低压气体蒸发法此种制备方法是在低压的氩、氮气等惰性气体中加热普通的Ti02,然后骤冷生成纳米二氧化钛粉体,其加热源有以下几种:(1)电阻加热法; (2)等离子喷射法; (3)高频感应法; (4)电子束法; (5)激光法, 这些方法可制备lOOnm以下的二氧化钛粒子。 活性氢—熔融金属反应法含有氢气的等离子体与金属钛之间产生电弧,使金属熔融,电离的N2,Ar等气体和H2溶入熔融金属,然后释放出来,在气体中形成了金属的超微粒子,用离心收集器或过滤式收集器使微粒与气体分离而获得纳米二氧化钛微粒。 溅射法此方法是用两块金属板分别作为阳极和阴极,阴极为蒸发用的材料,在两电极间充入Ar气,两电极间施加的电压范围为0.3—1.5kV。由于两电极间的辉光放电使Ar离子形成。在电场的作用下Ar离子冲击阴极靶材表面,靶上的Ti02就由其表面蒸发出来,被惰性气体冷却而凝结成纳米TiO2粉末,粒度在50nm以下,粒径分布较窄。 流动液面上真空蒸发法用电子束在高真空下加热蒸发TiO2,蒸发物落到旋转的圆盘下表面油膜上,通过圆盘旋转的离心力在下表面上形成流动的油膜,含有超微粒子的油被甩进了真空室的壁面,然后在真空下进行蒸馏获得TiO2超微粒子 钛醇盐气相水解法该工艺可以用来开发单分散的纳米TiO2,其反应式如下: nTi(0R)4,+2nH2O(g)————>nTiO2(s)+4nROH 优点是操作温度较低、能耗小,对材质要求不是很高,并且可以连续化 TiCl4,高温气相水解法该法与气相法生产白炭黑的原理相似,是将TiCl4气体导入高温的氢氧火焰中进行气相水解, 其化学反应式为: TiCl4(g)+2H2(g)+O2(g)→TiO2(s)+4HCl(g)