
GaussView高级技巧(二):纯手工搭建富勒烯C20
星期三, 2008-11-19 05:31 —teechodemenos
软件名称:
GaussView
本文展示了如何利用GaussView 纯手工搭建富勒烯C20分子。
前面我们已介绍了GaussView构建分子模型的一些高级技巧。本文将进一步展示一个应用实例:利用GaussView纯手工搭建富勒烯C20分子。本文所使用的版本是GaussView 3。
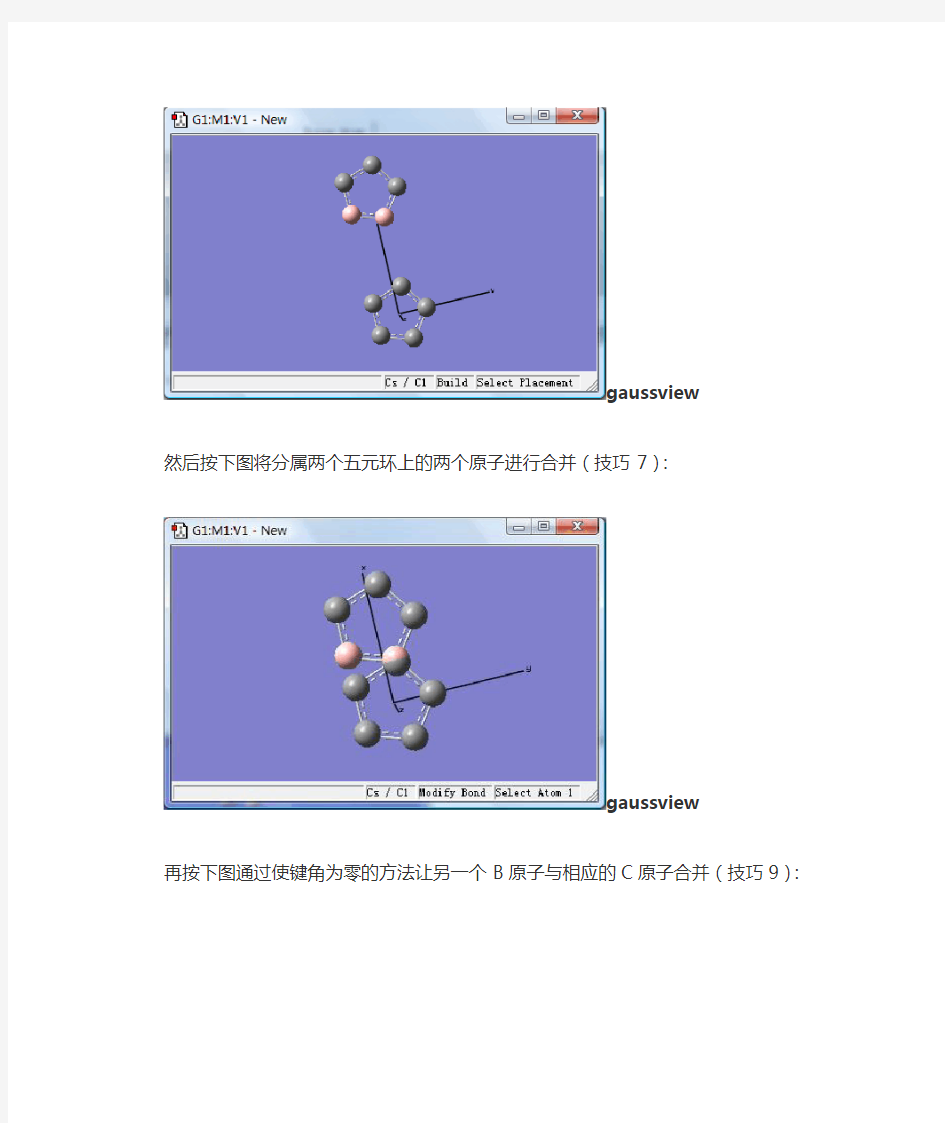
我们首先构造一个具有D5h对称性的五元环,方法见前文(系列1)中第二个例子(构造二茂铁)。然后我们点一下复制工具,然后在同窗口中粘贴(注意选择第二种粘贴方式:“Append Molecule”)。然后在复制出来的新五元环的两个C原子上用B原子取代掉(着色技巧,技巧7),如下图所示。
gaussview
然后按下图将分属两个五元环上的两个原子进行合并(技巧7):
gaussview
再按下图通过使键角为零的方法让另一个B原子与相应的C原子合并(技巧9):
GaussView
删去粉红色的B原子和残键,就得到共边相连的两个五元环。再点击一下粘贴按钮(仍然是选择第二种粘贴方式:“Append Molecule”),按照上述同样的方法将第三个五元环合并到第一个五元环的一个边上。按照类似方法,将第一个五元环的五条边上全部都连上五元环,并在中心添加一个虚原子(后面用得到,技巧10)。利用点群工具将该结构对称化为D5h的对称性(技巧5),如下图所示:
GaussView
接下来我们要将外围的五元环一同翻上来,使得邻边重合。因此,有5对原子在翻起后要合并。为此,我们预先用B原子对将要被合并掉的原子先行着色,同时还要断开相应的B-C键(否则无法进行后面的翻转操作)如下图所示:
GaussView
这时的点群对称性是C5h,但这个对称性限制却阻止我们接下来的翻转操作,因此必须去掉镜面对称性。于是我们需要按下图添加一个虚原子(技巧10),并将体系对称化为C5点群:
GaussView 这时,利用二面角工具依次点击如下图的四个原子:
GaussView 调整二面角使得翻起的五个五元环的邻边重合,如下图所示:
GaussView
然后删去粉红色的B原子和残键,并将结构对称化为C5v点群,如下图所示:
GaussView
接下来用Ctrl+V新建一个窗口,用粘贴工具粘贴出一个五元环,显示坐标轴,在环中心添加一个虚原子,并使连上一个C-X键。然后将这个结构粘贴到原先的窗口中,如下图所示:
GaussView
合并上方的两个虚原子,使得新五元环居于半笼状结构的正上方,如下图所示:
GaussView
利用二面角工具旋转上方的五元环,使得上下两个五元环成交错式(见系列1
中的乙烷和二茂铁的例子)。删去虚原子,利用点群工具将整个结构对称化为
D5d点群。调整下图中的 C-C键长:
GaussView
最后,将整个结构对称化为Ih点群(可适当加大容差值)。此时,可以使用键长工具设定任何一个C-C键长(如1.45?),则由于对称性,其余所有C-C键长都具有相同长度。这样,由我们纯手工打造的C20最终结构如下图所示:
GaussView
富勒烯 制备 目前较为成熟的富勒烯的制备方法主要有电弧法、热蒸发法、燃烧法和化学气相沉积法等。 电弧法 一般将电弧室抽成高真空, 然后通入惰性气体如氦气。电弧室中安置有制备富勒烯的阴极和阳极, 电极阴极材料通常为光谱级石墨棒,阳极材料一般为石墨棒, 通常在阳极电极中添加铁,镍,铜或碳化钨等作为催化剂。当两根高纯石墨电极靠近进行电弧放电时, 炭棒气化形成等离子体,在惰性气氛下碳分子经多次碰撞、合并、闭合而形成稳定的C60及高碳富勒烯分子, 它们存在于大量颗粒状烟灰中, 沉积在反应器内壁上, 收集烟灰提取。电弧法非常耗电,成本高,是实验室中制备空心富勒烯和金属富勒烯常用的方法。 燃烧法 将苯、甲苯在氧气作用下不完全燃烧的碳黑中有C60或C70,通过调整压强、气体比例等可以控制C60与C70的比例,该法设备要求低,产率可达到%-9%,是工业中生产富勒烯的主要方法。 化学气相沉积(CVD) 主要用于制备碳纳米管,合适实验条件可制备出富勒烯。反应过程:有机气体和N2压入石英管,用激光、电阻炉或等离子体加热,气体分子裂解后在催化剂表面生长成富勒烯或碳纳米管。催化剂一般为Fe、Co、Ni、Cu颗粒。CVD设备简单,原料成本低,产率高;并且反应过程易于控制,可大规模生产。 提纯
通常是以C60为主,C70为辅的混合物,还有碳纳米管、无定形碳和碳纳米颗粒。决定富勒烯的价格和其实际应用的关键就是富勒烯的纯化。实验室常用的富勒烯提纯步骤是:从富含C60和C70的烟尘中先用甲苯索氏提取,然后纸漏斗过滤。蒸发溶剂后,剩下的部分(溶于甲苯的物质)用甲苯再溶解,再用氧化铝和活性碳混合的柱色谱粗提纯,第一个流出组分是紫色的C60溶液,第二个是红褐色的C70,此时粗分得到的C60或C70纯度不高,还需要用高效液相色谱(纯度高,设备昂贵,分离量小)来精分。Nagata发明了一项富勒烯的公斤级纯化技术。该方法通过添加二氮杂二环到C60, C70等同系物的1、2、3-三甲基苯溶液中。DBU只会和C70以及更高级的同系物反应,并通过过滤分离反应产物,而富勒烯C60与DBU不反应,因此最后得到C60的纯净物;其它的胺化合物,如DABCO,不具备这种选择性。 C60可以与环糊精以 1:2的比例形成配合物,而C70则不行,一种分离富勒烯的方法就是基于这个原理,通过S-S桥固定环糊精到金颗粒胶体,这种水溶性的金/环糊精的复合物[Au/CD]很稳定,与不水溶的烟灰在水中回流几天可以选择性地提取C60,而C70组分可以通过简单的过滤得到。将C60从[Au/CD] 复合物中分离是通过向环糊精水溶液加入对环糊精内腔具有高亲和力的金刚烷醇使得C60与[Au/CD] 复合物分离而实现C60的提纯,分离后通过向[Au/CD/ADA]的复合物中添加乙醇,再蒸馏,实现试剂的循环利用。50毫克[Au/CD]可以提取5毫克富勒烯C60。后两种方法都只停留在实验室阶段,并不常用。 Coustel重结晶法 Coustel等利用C60和C70在甲苯溶液中溶解度的不同,通过简单的重结晶法得到纯度为95-99%的C60 。本方法第一次重结晶得到C60的纯度约为95%,通过二次重结晶得到的C60 ,纯度达到98%-99%。 Prakash法由于C70等高富勒烯对AlCl3的亲和力大于C60 ,据此,Prakash将C60与C70的混合物溶入CS2中,加入适量AlCl3 ,由于C70等高富勒烯与AlCl3形成络合物,因而从溶液中析出, C60仍留在溶液
富勒烯的发现、特性、结构极其应用 化学与材料科学学院化学专业0501班吴铭 摘要:长期以来,人们只知碳的同素异形体有三种:金刚石,石墨和无定形碳。自1985年发现了巴基球,1991年1992年又相继发现了巴基管(碳纳米管)和巴基葱,碳有了第四种同素异形体富勒烯,于是人们便开始了对其结构与特性的研究,并广泛应用。本文综述了富勒烯的发现、特性、结构极其应用。 关键词:富勒烯结构特性应用 目前为止,碳的同素异形体已被发现四种:金刚石,石墨,不定形碳和富勒烯。其中,人们对前三种应该早就熟知了,而对于最后一种恐怕大多人知知甚少。巴基球,巴基管和巴基丛统称富勒烯。以下则介绍富勒烯的发现特性,结构极其应用。 一.发现 (一) 巴基球的发现 英国萨塞克斯大学的波谱学家克罗托(h.w.kvoto)在研究星际空间暗云中含碳的尘埃时,发现此尘埃中有氰基聚分子,克罗托很想研究该分子形成的机制,但没有相应的设备.1984年克罗托赴美参加陂得萨斯州奥斯汀举行的学术会议,并到莱斯大学参观,现该校化学系系主任科生(R.F.cuv.jv)教授介绍,认识了研究原子簇化学的斯莫利教授,观看了斯莫利和他的研究生用他们设计的激光超团簇发生器,在氦气中用激光使碳化硅变成蒸汽的实验,克罗托对这台仪器非常感兴趣,这正是所渴求的仪器。三位科学家优异合作并安排在1985年8月到9月间进行合作研究。是时,他们用功率激光轰击石墨,使石墨中的碳原子汽化,用氮气流把气态碳原子送入真空室。迅速冷却后形成碳原子簇,再用质谱仪检测。他们解析质谱图后发现,该实验产生了含不同碳原子数的原子簇。其中相当于60个碳原子,质量数落在720处的信号最强,其次是相当于70个碳原子,质量数为840处的信号最强。说明C60是相对稳定的原子簇分子。(图1) (二) 巴基管和巴基丛的发现 1991年日本NFC公司的电镜专家饭岛博士,在氮气直流电弧放电后的阴极棒上发现了管状的结构的碳原子簇,直径约几纳米,成为碳纳米管(Cerbonnanofubes),又称巴基管(Buckytabes)。碳纳米管也是典型的富勒烯,可以有单层和多层之分,多层管则由几个或几十个单层管回轴套叠而成.想另管距为0。34nm与石墨层检举0。335nm相近.饭岛发现,如果巴基管全由方边形碳环组成,该管是不封闭的,可以向两端伸长;如果在管子两端有五边形,会将巴基管末端封闭。(图4) 1992年瑞士联邦大学的D.vgarte年人用高强度电子来对碳棒长时间照射,发现了多层相套的巴基球,结构像洋葱(Buckyonlons)。巴基葱的层面可达70多层。(图5) 二.结构及特性 (一)结构
富勒烯(C60)研究与应用现状
富勒烯(C60)研究与应用现状 大连工业大学 摘要:富勒烯发现至今只有短短20年时间,由于其独特的结构和物理、化学性质,吸引了众多科学家的目光,因此在这20 年中,使得C60化学得到了很大的发展.文章综述了富勒烯的几种合成方法,并阐述了目前常用的应用现状,最后对其未来的发展作了展望。 关键词富勒烯;合成方法;应用 引言 富勒烯的发现始于1985 年Kroto 等【1】在高真空环境下激光溅射石墨的研究。利用这种方法只能产生数以千计的富勒烯分子,根本无法进行富勒烯详细的性质表征研究, 当然更谈不上应用。1990 年,Krastchmer 等【2】发明了低压氦气环境下石墨电极电弧放电法合成富勒烯,能够得到克量级的C60 产物。由于富勒烯特殊的结构和性能,在材料、化学、超导与半导体物理、生物等学科和激光防护、催化剂、燃料、润滑剂、合成、化妆品、量子计算机等工程领域具有重要的研究价值和应用前景。1991 年富勒烯被美国《科学》杂志评为年度分子,富勒烯被列为21 世纪的新材料。此后,科学家经过不断的探索和研究,发明了更多生产富勒烯的方法,例如连续石墨电极放电法、激光配合高温石墨棒蒸发法【3】、引入铁磁性金属催化剂法【4、5】、高温等离子体石墨蒸发法【6、7】,苯高温火焰燃烧法【8-10】等。而且富勒烯在日常生活中的应用越来越广泛, 因而富勒烯产品在未来社会具有很好的发展前景。 2.富勒烯的合成方法 2.1水下放电法 水下放电法【11】将电弧室中的介质由惰性气体换为去离子水, 采用直流电弧放电, 以碳纯度为99%、直径6mm的碳棒做阳极, 直径为12mm的碳棒做阴极, 放入2. 5L 的去离子水中至其底部3mm的位置, 在电压为16 ~17V、电流为30A的条件下拉直流电弧, 产物可在水表面收集。 水下放电法不需要传统电弧法的抽气泵和高度密封的水冷真空室等系统, 免除了复杂昂贵的费用, 可进一步降低反应温度, 能耗更小, 并且产物在水表面收集而不是在整个有较多粉尘的反应室。与传统电弧法相比, 此法产率及质量均较高。此法可制备出球形洋葱富勒烯、像富勒烯似的碳纳米粒子、类似碳纳米管和富勒烯粉末。 总之, 电弧法是目前应用最广泛、有可能进一步扩大生产规模的制备方法, 其C60产率可达10% ~13% , 为其物理、化学的研究奠定了基础。电弧法制备碳纳米管产率约为30% ~70% , 在电弧放电的过程中能达到4 000K的高温, 这样的温度下碳纳米管最大程度地石墨化, 所以制备的管缺陷少, 比较能反映碳纳米管的真正性能。但由于电弧放电通常十分剧烈, 难以控制进程和产物, 合成的沉积物中存在有碳纳米颗粒、无定形炭或石墨碎片等杂质, 而且碳管和杂质融合在一起, 很难分离。 2.2CVD法 CVD是制备富勒烯的另一种典型方法。催化热分解反应过程一般是将有机气体(通常为C2 H2 )混以一定比例的氮气作为压制气体, 通入事先除去氧的石英管中, 在一定的温度下, 在催化剂表面裂解形成碳源, 碳源通过催化剂扩散,在催化剂后表面长出碳纳米管, 同时推着小的催化剂颗粒前移。直到催化剂颗粒全部
专业课程实践论文题目:富勒烯及其衍生物的制 备和生物医学效应任课教师:罗志勇 姓名:刘远见 学号:20096918 学院:化学化工学院 专业班级:2009级材料化学1班
富勒烯及其衍生物的制备和生物医学效 应 刘远见liuyuanjian [重庆大学化工学院2009级材料化学1班重庆中国 400044] [摘要]:富勒烯和其衍生物作为一种新型含碳纳米材料,由于其独特的结构和物理化学性质,在生物、医学、超导、光学及催化等多领域有着极为广阔的应用前景。在生物和医学领域,富勒烯及其衍生物具有抗氧化活性和细胞保护作用、抗菌活性、抗病毒作用、载带药物和肿瘤治疗等活性。在总结国内外相关研究基础上,论文重点综述了几种典型富勒烯及衍生物的制备和生物效应。 [关键字]:富勒烯;纳米材料;生物效应;细胞保护; [Abstract]:Due to their unique structure and physical and chemical properties,fullerene and its denvatives have a widerange of potential appacations in biomedical field.They have many advantages in cell protection and antioxidant properties,antibacterial activity,antiviral activity,drug delivery and anti-tumor activities.In this paper,biomedical effects of fullerenes have been highlighted,and the synthesis of fullerene its derivative have been reviewed as well. [Key words]:fullerene;Nano-materials;Biological effects;Cytoprotective 纳米科学、信息科学和生命科学并列成为2l世纪的三大支柱科学领域。纳米颗粒(nanoparticles,Nas)和超细颗粒物(ultrafine particles,UFPs),一般是指尺寸至少有一维在l~100 nm间的粒子。纳米尺度是处在原子簇和宏观物体交界的过渡区域,处于这个区域的材料具有一些独特性质,如小尺寸效应、表面、界面效应和量子尺寸效应等。空气中纳米颗粒虽然浓度很低,但具有很高的颗粒物数目。将宏观物体细分成纳米颗粒后,它的光学、热学、电学、磁学、力学以及化学性质和大体积固体相比将会显著不同。纳米材料的小尺寸、化学成分、表面结构、溶解性、外形和聚集情况决定着它们特殊的物理化学性质,这些性质使得纳米材料在将来有着广泛的用途。(1) Kroto等(1985)于1985年发现了巴基球,并提出了球型中空分子的模型,将之命名为富勒烯(C60)。Kratschrner等(1990)首先用石墨电弧放电法实现了富勒烯的宏量制备,此后在世界范围内掀起了研究富勒烯的热潮。涉及的学科包括物理、化学、生物、天文和材料科学等。一个分子能如此迅速地打开通向科学新领域的大门,这是非常罕见的。由于富勒烯分子的巨大科学意义,被美国‘科学’杂志评为1991年的“明星分子”。
GaussView教程【1】——界面介绍 Gview是一个专门设计于高斯配套使用的软件,其主要用途有两个:构建高斯的输入文件;以图的形式显示高斯计算的结果。除了可以自己构建输入文件外,Gview还可读入Chem3D,HyperChem和晶体数据等诸多格式的文件。从而使其可以于诸多图形软件连用,大大拓宽了使用范围。 开启GaussView会看到一大一小两个窗口,后面灰色背景的窗口为选择窗口,在里面选择要输入的分子或基团;前面紫色的窗口为绘图窗口,使用鼠标绘制想要绘制的图形。 菜单栏 ?【File】主要功能是建立,打开,保存和打印当前的文件 ?【Edit】完成对分子的剪贴、拷贝、删除、抓图等 ?【View】与显示分子相关的都在这个菜单下,如显示氢原子、键、元素符号、坐标等 ?【Calculate】直接向Gaussian提交计算 ?【Results】接收并显示Gaussian计算后的结果 ?【Windows】控制窗体,如关闭、恢复等 ?【Help】帮助 快速工具栏 【左面第一个】选择元素与价键,单击打开会看到一个元素周期表,通过它可以选择需要绘制的元素以及价态。 【左面第二个】环工具,作用与上一个差不多,只是这里提供的都是环状化合物残基; 【左面第三个】提供常用的R基团模板,其中包括乙基、丙基、异丙基、异丁基等 【左面第四个】氨基酸残基,使用它可以迅速绘制氨基酸 【左面第五个】用户自定义基团,您可以将常用的基团存放到此处 这条快速编辑栏中从左到右依次是【键调整】|【键角调整】|【二面角调整】|【查询已有结构】|【增加化学键】|【删除化学键】|【翻转原子】|【单个选择】|【框选】|【去除选择】|【全选】 这里面的所有选项都可以通过在绘图窗口点击右键得到。
富勒烯的性质,性能以及研究现状 2009210309 化院0906 陈青英 摘要:本文总结了近十几年的文献资料, 对[C60 ]富勒烯的化学修饰及其功能材料性能研究进行综述. 关键词:富勒烯, 化学修饰, 功能材料, 性能 Abstract:Three kinds of [60 ]fullerene-coumarin compounds were synthesized by esterification with the coumarin derivatives and characterized by 1H NMR, 13 C NMR, FT-IR and MS. Their fluorescence intensity drastically reduced owing to the competition of excitation light and the fluorescence re-absorption of the coumarin to fullereneRetro-cycloaddition reaction is one of the most important reactions of fullerene derivatives.Many kinds of organofullerenes are not stable under reductive,oxidative or thermal conditions,where the functional addends are removed from the fullerene sphere and lead to the formation of pristine fullerenes.Such addition-retro-addition reaction has shown promising application in the protection/deprotection strategy for the purification and functionalization of fullerenes.. Keywords:Fullerene,Coumarin,Fluorescence,fullerene derivatives; retro-cycloaddition reactions; C-H-X hydrogen bonding 石墨和金刚石是大家所熟悉的.碳元素的两种同素异形体。二十世纪八十年代中期,科学家又发现了碳的第三种同素异形体C60富勒烯。这是二十世纪九十年代,物理学和化学学科领域中最重要的发现之一,C60化学是目前有机化学领域的前沿,它是是Kro to 等在1985 年发现的碳的第3 种同素异形体, 当时采用激光蒸发石墨法制备, 只能得到微克量级,直到1990 年Krabt schmer2Hu t tman 等采用石墨棒电孤蒸发法获得克量级的C60产品, 从而有力地促进了全碳分子的研究. C60分子是由12 个五边形环与20 个六边形环稠合所构成的笼状32 面体, 其形状很象一个足球, 五边形环为单键(键长约01145 nm ) , 2 个六边形环的公共棱边则为双键(键长约01138 nm ) , 共有12 根双键, 因而C60分子具有缺电子芳香烃的一些性质. 它能发生环加成反应, 亲核、亲电加成, 自由基加成, 包合反应, 聚合反应, 光化学反应, 氧化还原反应等. 迄今对它的研究已涉及无机化学、有机化学、物理化学、分析化学、材料科学、高分子科学、生命科学等众多学科及应用领域. 1富勒烯的化学修饰 C60的化学修饰主要集中在它的化学活性、反应和机理研究以及设计、合成功能性化物, 包括C60的二次衍生物上. 根据修饰方法不同, 可分为: 经典有机化学反应, 金属有机化学反应和电化学合成. 1.1富勒烯的有机化学反应 C60具有典型的缺电子芳香烃的性质, 容易与供电子的亲核基团反应. 多数情况下, 亲核试剂是进攻C60分子的6, 6 环共用边双键, 有时也会发生重排而得到插入5, 6 环共用边键的衍生物
富勒烯及其衍生物的发展及研究 ——文献综述 摘要:富勒烯是无机化学研究中十分重要的一个领域。近年来,对富勒烯的结构、衍生物、在各方面的应用等都有了新的突破,而本文则是以文献综述的形式,通过阅读文献对近五年来有关富勒烯及其衍生物的发展及研究进行总结描述。 关键词:富勒烯物理性质化学性质应用 前言:1985年,人类在相继发现了石墨、金刚石之后,Kroto等发现了富勒烯,即C60,更以其独特的物理、化学性质引起了科学界普遍的关注。C60是含有众多双键具有独特笼型结构的三维芳香化合物.它的60个位于顶点上的碳原子组成了球形32面体,其中有12个面是五边形,20个面是六边形[1].这种结构类似于日常生活中所见到的足球,因此也被称作“足球烯”。这种特殊的结构使它具有特殊的超导、强磁性、耐高压、抗化学腐蚀等优异的性质.在超导材料、光电导材料、化妆品、纳米粒子材料、生物医学等领域应用前景广阔。内嵌式富勒烯的研究更是近来有关富勒烯研究的热门课题。 1.富勒烯的性质 1.1物理性质 C60是非极性分子,外观呈深黄固体,随厚度不同颜色可呈棕色到黑色.密度为1.678g/cm,不导电,但具有良好的非线性光学性质、光电导性,是很好的光电导材料,熔点>553K,易升华,易溶于含有大∏键的芳香性溶剂中,磁流中性,但是其五元环有很强的顺磁性,而六元环具有较为缓和的介磁性;分子中的60个碳原子是完全等价的.由于球面的弯曲效应、五元环的存在,使得碳原子的杂化方式介于sp2和sp3杂化之间,从立体构型来看,C60具有点群对称性,分子价电子数高达240个。[2] 1.2化学性质 1.2.1亲核反应—与金属的反应 C60与金属的反应主要分为两类一种是金属被置于C60碳笼的内部; 另一种是金属位于C60碳笼的外部。 (1)C 60碳笼内配合物生成反应: C60碳笼为封 闭的中空的多面体结构, 其内腔直径为7. 1 A,内部可嵌入原子、离子 或小分子形成新的团簇分子 , C 60+ A C60 ( A)。其主要包含物种 类为金属、惰性气体及部分极性分子(如LiF),其中金属包含物研究 最为广泛。Sm alley等人现已发现如 K、Na、Ba、Sr、Ho、Th等碱金 属、碱土金属、绝大多数稀有金属均可与C60形成C60(A)。 (2)C60碳笼外键合反应: 能与 C60键合的金属有: V、Fe、Co、Ni、Rh、Cu、La、Yb、Ag 等[3]。 1.2.2加成反应 由于C60的不饱和性,C60可以与胺类、磷化物等发生加成反应,在格氏试剂作用下还可以与CH3I反应,生成烷基化物。
GaussView高级技巧(一): 十个基本高级技巧 摘要 本文主要介绍了利用GaussView 分子模型的十个高级技巧,其中大多数技巧是鲜为人知的。这些技巧的组合能够使GaussView发挥巨大威力,可以快速方便地构造出复杂的分子结构。最后,以构造乙烷的重叠式构象和二茂铁结构为例进一步说明了这些高级技巧的具体应用。 本文主要介绍利用GaussView构建分子模型的高级技巧,希望对大家有所帮助。本文所使用的版本是GaussView 3。 1. 三个变形工具 上图的三个变形工具可以实现平移和旋转分子的某一部分以及断键成键和选择键型等功能,我们不妨将这些工具依次称为“键长”、“键角”和“二面角”工具。根据需要必须适当选择某些原子的移动方式,有“平移全组”(“T ranslate group”,默认),“平移原子”(“Translate atom”)和“固定”(“F ixed ”)三种,如下图所示。 2. 添加虚原子定义参考原子或参考旋转轴
在很多场合,我们可以利用添加虚原子X来定义参考原子或参考旋转轴,然后利用前述的三个变形工具对分子进行我们想要的操作。一旦操作完成,我们再删除掉原先添加的虚原子。我们可以用删除工具直接删除(见下图): 但由于虚原子体积很小,有时会被其他原子覆盖,这时无法用删除工具直接删除。更通用的删除方法是:点击“原子列表”按钮(也可以选择菜单Edit > Atom List...),见下图。 在弹出的“Atom List Editor”窗口中选中要删除的原子,然后选择菜单Edit > Delete Atoms > Selected。 3. 利用加氢工具获得最佳成键位置 利用上图的加氢工具可以对某个原子添加一个氢原子。但这个氢原子的成键取向有时并非我们想要的。解决办法是:既然我们第一个加氢的取向不理想,那么我们就再添加一个,就这样连续不断地加氢,直到所加的氢原子的位置符合我们需要位置。然后利用删除工具将前面添加的氢原子全部删除即可。 加氢工具的另一个目的就是为后面添加其他基团做准备。用下面介绍的基团工具点击氢原子将氢原子取代掉后即可达到在一定的成键方向添加某个基团的目的。 4. 基团取代工具 如上图所示,基团取代工具有:元素基团、环状基团、R基团、生物基团和自定义基团。元素基团可以添加或取代各种杂化状态的原子基团,其余各种基团工具则提供许多常用基团的模板,在此基础上我们可以构建相当复杂的分子。我们可以点击当前基团(“Current Fragment”)面板中的“Hot”位置来选择取代位置,如下图所示。
碳纳米管和富勒烯的光电特性和应用 一、碳纳米管的结构性能及应用 (一)碳纳米管的结构 碳纳米管是指由类似石墨的六边形网格组成的管状物,可以看作是石墨片层绕中心轴按一定的螺旋角卷曲而成。管子一般由单层或多层组成,相应的纳米碳管就称为单壁纳米碳管(SWNT)和多壁纳米碳管(MWNT)。碳纳米管具有典型的层状中空结构特征,构成碳纳米管的层片之间存在一定的夹角碳纳米管的管身是准圆 管结构,并且大多数由五边形截面所组成。管 身由六边形碳环微结构单元组成, 端帽部分 由含五边形的碳环组成的多边形结构,或者称 为多边锥形多壁结构。是一种具有特殊结构 (径向尺寸为纳米量级,轴向尺寸为微米量 级、管子两端基本上都封口)的一维量子材料。 固定的距离,约为0.34nm,直径一般为2~20nm。长度可达数微米,因此有较大的长径比。资料表明:碳纳米管的晶体结构为 密排六,c=0.6852nm,c/a=2.786 ,与石墨相 比,a值稍小而c值稍大,预示着同一层碳管 内原子间有更强的键合力,碳纳米管有极高 的同轴向强度。多壁碳纳米管存在三种类型 的结构,分别称为单臂纳米管、锯齿形纳米 管和手性形纳米管。 由于其独特的结构,碳纳米管的研究具 有重大的理论意义和潜在的应用价值,如:其独特的结构是理想的一维模型材料;巨大的长径比使其有望用作坚韧的碳纤维,其强度为钢的100倍,重量则只有钢的1/6;同时它还有望用作为分子导线,纳米半导体材料,催化剂载体,分子吸收剂和近场发射材料等。 (二)碳纳米管的主要性质及应用 (1)碳纳米管的性质如下:
1. 碳纳米管上碳原子的P电子形成大范围的离域π键,由于共轭效应显著,碳纳米管具有一些特殊的电学性质。 碳纳米管具有良好的导电性能,由于碳纳米管的结构与石墨的片层结构相同,所以具有很好的电学性能。理论预测其导电性能取决于其管径和管壁的螺旋角。当CNTs的管径大于6nm时,导电性能下降;当管径小于6nm时,CNTs可以被看成具有良好导电性能的一维量子导线。有报道说Huang通过计算认为直径为0.7nm的碳纳米管具有超导性,尽管其超导转变温度只有1.5×10-4K,但是预示着碳纳米管在超导领域的应用前景。 常用矢量Ch表示碳纳米管上原子排列的方向,其中Ch=na1+ma2,记为(n,m)。a1和a2分别表示两个基矢。(n,m)与碳纳米管的 导电性能密切相关。对于一个给定(n,m)的纳米 管,如果有2n+m=3q(q为整数),则这个方向上 表现出金属性,是良好的导体,否则表现为半导 体。对于n=m的方向,碳纳米管表现出良好的导 电性,电导率通常可达铜的1万倍。 2. 碳纳米管具有很高的杨氏模量和抗拉强度,杨氏模量估计可高达5T Pa;同时碳纳米管还具有极高的韧性,十分柔软.碳纳米管的导电性与本身的直径和螺旋度有关,随着这些参数的变化可表现出导体或半导体性质。碳纳米管管壁在生长过程中有时会出现五边形和七边形缺陷,使其局部区域呈现异质结特性。不同拓扑结构的碳纳米管连接在一起会出现非线性结效应,有近乎理想的整流效应.在室温条件下,碳纳米管能够吸收较窄频谱的光波,能以新的频谱发射光波,还能发射与原来频谱完全相同的光波。 (2)碳纳米管还有以下的应用: 1. 纳米电子学方面 作为典型的一维量子输运材料,用金属性单层碳纳米管制成的三极管在低温下表现出典型的库仑阻塞和量子电导效应。碳纳米管既可作为最细的导线被用在纳米电子学器件中,也可以被制成新一代的量子器件。碳纳米管还可用作扫描隧道显微镜或原子力显微镜的探针。碳纳米管还为合成其它一维纳米材料的控制生长供了一种模板或框架,碳纳米管在高温下非常稳定,利用碳纳米管的限制反应可制备其它材料的一维纳米结构。这一方法用于制备多种金属碳化物一维纳米晶
富勒烯(C60)研究与应用现状 化工与材料学院
富勒烯(C60)研究与应用现状 (辽宁省大连市甘井子区轻工苑1号大连工业大学化工与材料学院 116034) 摘要:富勒烯发现至今只有短短20年时间,由于其独特的结构和物理、化学性质,吸引了众多科学家的目光,因此在这20 年中,使得C60化学得到了很大的发展.文章综述了富勒烯的几种合成方法,并阐述了目前常用的应用现状,最后对其未来的发展作了展望。 关键词富勒烯;合成方法;应用 引言 富勒烯的发现始于1985 年Kroto 等【1】在高真空环境下激光溅射石墨的研究。利用这种方法只能产生数以千计的富勒烯分子,根本无法进行富勒烯详细的性质表征研究, 当然更谈不上应用。1990 年,Krastchmer 等【2】发明了低压氦气环境下石墨电极电弧放电法合成富勒烯,能够得到克量级的C60 产物。由于富勒烯特殊的结构和性能,在材料、化学、超导与半导体物理、生物等学科和激光防护、催化剂、燃料、润滑剂、合成、化妆品、量子计算机等工程领域具有重要的研究价值和应用前景。1991 年富勒烯被美国《科学》杂志评为年度分子,富勒烯被列为21 世纪的新材料。此后,科学家经过不断的探索和研究,发明了更多生产富勒烯的方法,例如连续石墨电极放电法、激光配合高温石墨棒蒸发法【3】、引入铁磁性金属催化剂法【4、5】、高温等离子体石墨蒸发法【6、7】,苯高温火焰燃烧法【8-10】等。而且富勒烯在日常生活中的应用越来越广泛, 因而富勒烯产品在未来社会具有很好的发展前景。 2.富勒烯的合成方法 2.1水下放电法 水下放电法【11】将电弧室中的介质由惰性气体换为去离子水, 采用直流电弧放电, 以碳纯度为99%、直径6mm的碳棒做阳极, 直径为12mm的碳棒做阴极, 放入2. 5L 的去离子水中至其底部3mm的位置, 在电压为16 ~17V、电流为30A的条件下拉直流电弧, 产物可在水表面收集。 水下放电法不需要传统电弧法的抽气泵和高度密封的水冷真空室等系统, 免除了复杂昂贵的费用, 可进一步降低反应温度, 能耗更小, 并且产物在水表面收集而不是在整个有较多粉尘的反应室。与传统电弧法相比, 此法产率及质量均较高。此法可制备出球形洋葱富勒烯、像富勒烯似的碳纳米粒子、类似碳纳米管和富勒烯粉末。 总之, 电弧法是目前应用最广泛、有可能进一步扩大生产规模的制备方法, 其C60产率可达10% ~13% , 为其物理、化学的研究奠定了基础。电弧法制备碳纳米管产率约为30% ~70% , 在电弧放电的过程中能达到4 000K的高温, 这样的温度下碳纳米管最大程度地石墨化, 所以制备的管缺陷少, 比较能反映碳纳米管的真正性能。但由于电弧放电通常十分剧烈, 难以控制进程和产物, 合成的沉积物中存在有碳纳米颗粒、无定形炭或石墨碎片等杂质, 而且碳管和杂质融合在一起, 很难分离。 2.2CVD法 CVD是制备富勒烯的另一种典型方法。催化热分解反应过程一般是将有机气体(通常为C2 H2 )混以一定比例的氮气作为压制气体, 通入事先除去氧的石英管中, 在一定的温度下, 在催化剂表面裂解形成碳源, 碳源通过催化剂扩散,在催
简述富勒烯C60的结构及应用 结构: C60的分子结构为球形32面体,它是由60个碳原子以20个六元环和12个五元环连接而成的具有30个碳碳双键(C=C)的足球状空心对称分子,所以,富勒烯也被称为足球烯。球体直径约为710pm,即由12个五边形和20个六边形组成。其中五边形彼此不相联接只与六边形相邻。与石墨相似,每个碳原子以sp2杂化轨道和相邻三个碳原子相连,剩余的p 轨道在C60分子的外围和内腔形成π键 应用: 一.用于增强金属: 在增强金属材料方面,C60的作用将比焦炭中的碳更好,这是因为C60比碳的颗粒更小、活性更高,C60与金属作用产生的碳化物分散体的颗粒大小是0.7nm,而碳与金属作用产生的碳化物分散体的颗粒大小为2μm~5μm,在增强金属的作用上有较大差别。 二.用作新型催化剂 C60具有烯烃的电子结构,可以与过渡金属(如铂系金属和镍)形成一系列络合物。例如C60与铂、锇可以结合成{[(C2H5)3P]2Pt}C60和C60OsO4·(四特丁基吡啶)等配位化合物,它们有可能成为高效的催化剂。 三.用于气体的贮存: 利用C60独特的分子结构,可以将C60用作比金属及其合金更为有效和新型的吸氢材料。每一个C60分子中存在着30个碳碳双键,因此,把C60分子中的双键打开便能吸收氢气。与金属或其合金的贮氢材料相比,用C60贮存氢气具有价格较低的优点,而且C60比金属及其合金要轻,因此,相同质量的材料,C60所贮存的氢气比金属或其合金要多。C60不但可以贮存氢气,还可以用来贮存氧气。与高压钢瓶贮氧相比,高压钢瓶的压力为3.9×106Pa,属于高压贮氧法,而C60贮氧的压力只有2.3×105 Pa,属于低压贮氧法。利用C60在低压下大量贮存氧气对于医疗部门、军事部门乃至商业部门都会有很多用途。 四.用于制造光学材料: 由于C60分子中存在的三维高度非定域电子共轭结构使得它具有良好的光学及非线性光
姓名:秦晨学号:201130451119 富勒烯材料 前言: 富勒烯(Fullerene) 是一种碳的同素异形体。任何由碳一种元素组成,以球状,椭圆状,或管状结构存在的物质,都可以被叫做富勒烯。富勒烯与石墨结构类似,但石墨的结构中只有六元环,而富勒烯中可能存在五元环。1985年Robert Curl等人制备出了C60。1989年,德国科学家Huffman和Kraetschmer的实验证实了C60的笼型结构,从此物理学家所发现的富勒烯被科学界推向一个崭新的研究阶段。富勒烯的结构和建筑师Fuller的代表作相似,所以称为富勒烯。 1985年英国化学家哈罗德·沃特尔·克罗托博士和美国科学家理查德·斯莫利在莱斯大学制备出了第一种富勒烯,即富勒烯分子,因为这个分子与建筑学家巴克明斯特·富勒的建筑作品很相似,为了表达对他的敬意,将其命名为巴克明斯特·富勒烯。饭岛澄男早在1980年之前就在透射电子显微镜下观察到这样洋葱状的结构。自然界也是存在富勒烯分子的,2010年科学家们通过史匹哲太空望远镜发现在外太空中也存在富勒烯。“也许外太空的富勒烯为地球提供了生命的种子”。 在富勒烯的发现之前,碳的同素异形体的只有石墨、钻石、无定形碳(如炭黑和炭),它的发现极大地拓展了碳的同素异形体的数目。巴基球和巴基管独特的化学和物理性质以及在技术方面潜在的应用,引起了科学家们强烈的兴趣,尤其是在材料科学、电子学和纳米技术方面。 命名 很像足球的球型富勒烯也叫做足球烯,或音译为巴基球,中国大陆通译为富勒烯,台湾称之为球碳,香港译为布克碳;偶尔也称其为芙等;管状的叫做碳纳 为例,第一种是标准的写法,米管或巴基管。富勒烯的中文写法有三种,以C 60 即[60]富勒烯;第二种为碳60,60也不用下标,这是中文专用的写法;第三种为
第40卷增刊12000年12月 大连理工大学学报 JOurnal Of Dalian University Of TechnOlOgy VOl .40 S 1Dec .2000 文章编号:1000-8608(2000D S 1-S 0041-05 收稿日期:2000-07-31 基金项目:国家自然科学基金资助项目(29506041D ;辽宁省科学基金资助项目(95031D 作者简介:邱介山(1964-D 男 教授 博士生导师;E -mail :jgiu @chem .dlut .edu .cn . 煤基富勒烯的制备研究 邱介山 周 颖 王琳娜 杨兆国 韩红梅 (大连理工大学材料化工系 辽宁大连 116012D 摘要:以14种国产煤为原料 用电弧等离子体蒸发法制备富勒烯.富勒烯产品的表征采用质 谱~紫外光谱~红外光谱及高压液相色谱技术.考察了煤样的基础性质对富勒烯产率的影响.结果表明 由实验所用煤种均可制得富勒烯;原料煤本身的化学结构和组成影响富勒烯的产率和分布;由某些煤得到的富勒烯中 C 70的含量较之以石墨电极为原料时的含量要高得多. 关键词:煤;电弧等离子体/富勒烯中图分类号:T;221.23;T;536文献标识码:A 15年前以C 60分子为代表的富勒烯新材料的 发现[1] 开创了化学和材料研究的新领域 它从一开始就在世界范围内成为众多科学家关注的研究热点.已有的研究工作表明 富勒烯在物理~化学~材料~生命科学等众多领域均有巨大的应用潜力.C 60富勒烯的发现者Kroto 等人因此被授予1996年度的诺贝尔化学奖.随着对C 60性质和应用研究的不断深入与发展 寻找廉价原料 扩大制备富勒烯的原料来源 已成为广大研究者的共识.以储量丰富的煤炭为原料制备富勒烯 由于其低廉的价格~独特的化学结构而得到许多研究者的关注[2~6]. 本文以14种国产煤为原料 用电弧等离子体蒸发法制备富勒烯 着重研究了煤的灰分~挥发分及固定碳含量等基础性质对富勒烯产率的影响. 1 实验部分 实验所用煤种包括4种无烟煤(阳泉~北京~晋城和汝萁沟D 8种烟煤(贫煤~瘦煤~1/3焦煤~肥煤~气煤和长焰煤D 以及2种褐煤(扎赉诺尔和宝日希勒煤D.煤样经预处理后得到直径为12mm 的煤基炭棒.成型所用粘结剂为鞍山钢铁公司的中温沥青.原料煤的预处理工艺流程参见文献[7].制备富勒烯所用的电弧等离子体蒸发实验装置参见文献[8].在电弧蒸发焦棒过程中所使用的缓冲 气体是高纯氦气. 为考察煤中灰分对富勒烯形成的影响 对一部分煤样进行了碱法脱灰处理[9] 具体步骤如下:原煤粉碎至粒度小于150pm 在NaO 的溶液中(碱煤质量比为0.4D 于55 下浸泡24h 在100 下烘干后放入温度为340 的马弗炉中进行碱煤反应90min 煤样冷却后用去离子水洗涤至中性 然后再用10%的盐酸溶液浸泡90min 最后用去离子水洗涤至中性并烘干备用.煤样脱灰前后的工业分析数据示于表1. 富勒烯的制备是在如下条件[8]下进行的:氦气压力0.018~0.020M a 直流电流1=80~100A .目标产物富勒烯存在于所制得的烟灰中 这些烟灰沉积在电弧反应器的内壁上.烟灰经甲苯索氏抽提即获得黑色的晶体状富勒烯混合物.富勒烯的表征采用质谱(MS D ~紫外可见吸收光谱(UV -Vis D ~红外光谱(FT -IR D 和高压液相色谱( LC D 进行. 2 实验结果与讨论 MS ~UV -Vis 和FT -IR 等技术是对富勒烯进行定性研究的可靠分析手段.用MS ~UV -Vis 和FT -IR 技术对电弧等离子体蒸发煤基炭棒所得烟灰经索氏抽提后得到的富勒烯进行了研究 结果见图1~3.
富勒烯 富勒烯(Fullerene) 是一种碳的同素异形体.任何由碳一种元素组成, 以球状, 椭圆状, 或管状结构存在的物质, 都可以被叫做富勒烯. 富勒烯与石墨结构类似, 但石墨的结构中只有六元环, 而富勒烯中可能存在五元环. C60是于1985年由Rich ard Buckminster Fuller发现的第一个富勒烯, 又被称为足球烯. 这是因为C60的表面结构与足球完全一致. 富勒烯这个名称也由Fuller 而来, 而我们一般用Buckm inster fullerene 指足球烯. 性质 密度和溶解性 C60的密度为cm。 C60不溶于水,在正己烷、苯、二硫化碳、四氯化碳等非极性溶剂中有一定的溶解性。 导电性 碳原子本具有导电性,而C60分子的导电性优于铜,重量只有铜的六分之一,一个巴克球分子相当于一纳米,可谓极微小,它的导电性来自奇特的分子结构并非靠其他原子,可见不久的将来人类世界将诞生非金属电缆、非金属电路板...等富勒烯产品。 结构
克罗托受建筑学家理查德·巴克明斯特·富勒(RichardBuckminsterFuller,18 95年7月12日~1983年7月1日)设计的美国万国博览馆球形圆顶薄壳建筑的启发,认为C60可能具有类似球体的结构,因此将其命名为buckminster fullerene(巴克明斯特·富勒烯,简称富勒烯)。 富勒烯是一系列纯碳组成的原子簇的总称。它们是由非平面的五元环、六元环等构成的封闭式空心球形或椭球形结构的共轭烯。现已分离得到其中的几种,如C60和C70等。在若干可能的富勒烯结构中C60,C240,C540和直径比为1:2:3。C60的分子结构的确为球形32面体,它是由60个碳原子以20个六元环和12个五元环连接而成的具有30个碳碳双键(C=C)的足球状空心对称分子,所以,富勒烯也被称为足球烯。球体直径约为710pm,即由12个五边形和20个六边形组成。其中五边形彼此不相联接只与六边形相邻。与石墨相似,每个碳原子以sp2杂化轨道和相邻三个碳原子相连,剩余的p轨道在C60分子的外围和内腔形成π键。 (补充:C60双键数的计算方法 由于每个孤立的碳原子周围有三个键(一个双键,两个单键)。而每个键却又是两个碳原子所共有,因此棱数=60×3×(1/2)=90 由于单键数+双键数=总棱边数单键数=2×双键数(即单键数为双键数的2倍)设单键数为a个,双键数为b个,则 a+b=90 a=2b 所以b=30) 其他
富勒烯的研究进展
摘要:富勒烯发现至今只有短短 20 年时间,由于其独特的结构和物理、化学 性质,吸引了众多科学家的目光,因此在这 20 年中,使得 C60 化学得到了很大的 发展.文章综述了富勒烯的几种合成方法,并阐述了目前常用的应用现状,最后 对其未来的发展作了展望。 关键词: 无机富勒烯 碳纳米管 结构富勒烯 C90 生物富勒烯 硅富勒烯电弧法 芳烃分步 凝聚相 Abstract: the fullerenes found so far only a short span of 20 years, because of its unique structure and physical and chemical properties, attracted the attention of many scientists, so in these 20 years, makes the C60 chemical got great development. The article summarizes the several synthetic methods of fullerenes, and expounds the present situation of the application of commonly used at present, finally made a prospect for its future development. 引言:富勒烯的发现始于 1985 年 Kroto 等【1】在高真空环境下激光溅射石 墨的研究。利用这种方法只能产生数以千计的富勒烯分子,根本无法进行富勒烯 详细的性质表征研究, 当然更谈不上应用。 1990 年,Krastchmer 等【2】发明了低 压氦气环境下石墨电极电弧放电法合成富勒烯,能够得到克量级的 C60 产物。由 于富勒烯特殊的结构和性能,在材料、化学、超导与半导体物理、生物等学科和 激光防护、催化剂、燃料、润滑剂、合成、化妆品、量子计算机等工程领域具有 重要的研究价值和应用前景。1991 年富勒烯被美国《科学》杂志评为年度分子, 富勒烯被列为 21 世纪的新材料。此后,科学家经过不断的探索和研究,发明了更 多生产富勒烯的方法,例如连续石墨电极放电法、激光配合高温石墨棒蒸发法
【3】
、 引入铁磁性金属催化剂法【4、5】 、高温等离子体石墨蒸发法【6、7】,苯高温火
焰燃烧法【8-10】等。 而且富勒烯在日常生活中的应用越来越广泛, 因而富勒烯产品 在未来社会具有很好的发展前景。
1.富勒烯的结构
因为 C60 是富勒烯家庭
[11]
中相对最容易得到、最容易提纯和最廉价的各类,因此
C60 及其衍生物是被研究和应用最多的富勒烯。 通过质谱分析、X 射线分析后证明,C60 的分子结构为球形 32 面体[12],它是 由 60 个碳原子通过 20 个六元环和 12 个五元环连接而成的具有 30 个碳碳双键的 足球状空心对称分子[13],所以,富勒烯也被称为足球烯。C60 是高度的 Ih 对称, 高度的离域大π 共轭,但不是超芳香体系,它的核磁共振碳谱只有一条谱线,但 是它的双键是有两种,它有 30 个六元环与六元环交界的键,叫[6,6]键,60 个