
第一章 气体的pVT 关系
1-1物质的体膨胀系数V α与等温压缩系数T κ的定义如下:
1
1T
T p V p V
V T V V ???? ????-=??? ????=
κα 试导出理想气体的V α、T κ与压力、温度的关系?
解:对于理想气体,pV=nRT
111 )/(11-=?=?=???
????=??? ????=
T T V
V p nR V T p nRT V T V V p p V α 1211 )/(11-=?=?=???? ????-=???? ????-
=p p V
V p
nRT V p p nRT V p
V V T T T κ 1-2 气柜内有121.6kPa 、27℃的氯乙烯(C 2H 3Cl )气体300m 3
,若以每小时90kg 的流量输往使
用车间,试问贮存的气体能用多少小时?
解:设氯乙烯为理想气体,气柜内氯乙烯的物质的量为
mol RT pV n 623.1461815
.300314.8300106.1213=???==
每小时90kg 的流量折合p 摩尔数为 13
3153.144145
.621090109032-?=?=?=h mol M v Cl H C
n/v=(14618.623÷1441.153)=10.144小时
1-3 0℃、101.325kPa 的条件常称为气体的标准状况。试求甲烷在标准状况下的密度。
解:33
714.015
.273314.8101610132544
4--?=???=?=?=m kg M RT p M V n CH CH CH ρ 1-4 一抽成真空的球形容器,质量为25.0000g 。充以4℃水之后,总质量为125.0000g 。若改用充以25℃、13.33kPa 的某碳氢化合物气体,则总质量为25.0163g 。试估算该气体的摩尔质量。
解:先求容器的容积33)(0000.10010000.100000.250000.1252cm cm V l O H ==-=ρ
n=m/M=pV/RT
mol g pV RTm M ?=?-??==-31.3010
13330)0000
.250163.25(15.298314.84
1-5 两个体积均为V 的玻璃球泡之间用细管连接,泡内密封着标准状况条件下的空气。若将其
中一个球加热到100℃,另一个球则维持0℃,忽略连接管中气体体积,试求该容器内空气的压力。
解:方法一:在题目所给出的条件下,气体的量不变。并且设玻璃泡的体积不随温度而变化,则始态为 )/(2,2,1i i i i RT V p n n n =+=
终态(f )时 ???
?
??+=???? ??+=
+=f f f
f f f
f f f f T T T T R V
p T V T V R p n n n ,2,1,1,2,2,1,2,1
kPa
T T T T T p T T T T VR n p f f f f i i f
f f f f 00.117)
15.27315.373(15.27315.27315.373325.1012 2,2,1,2,1,2,1,2,1=+???=?
??? ??+=???? ??+=
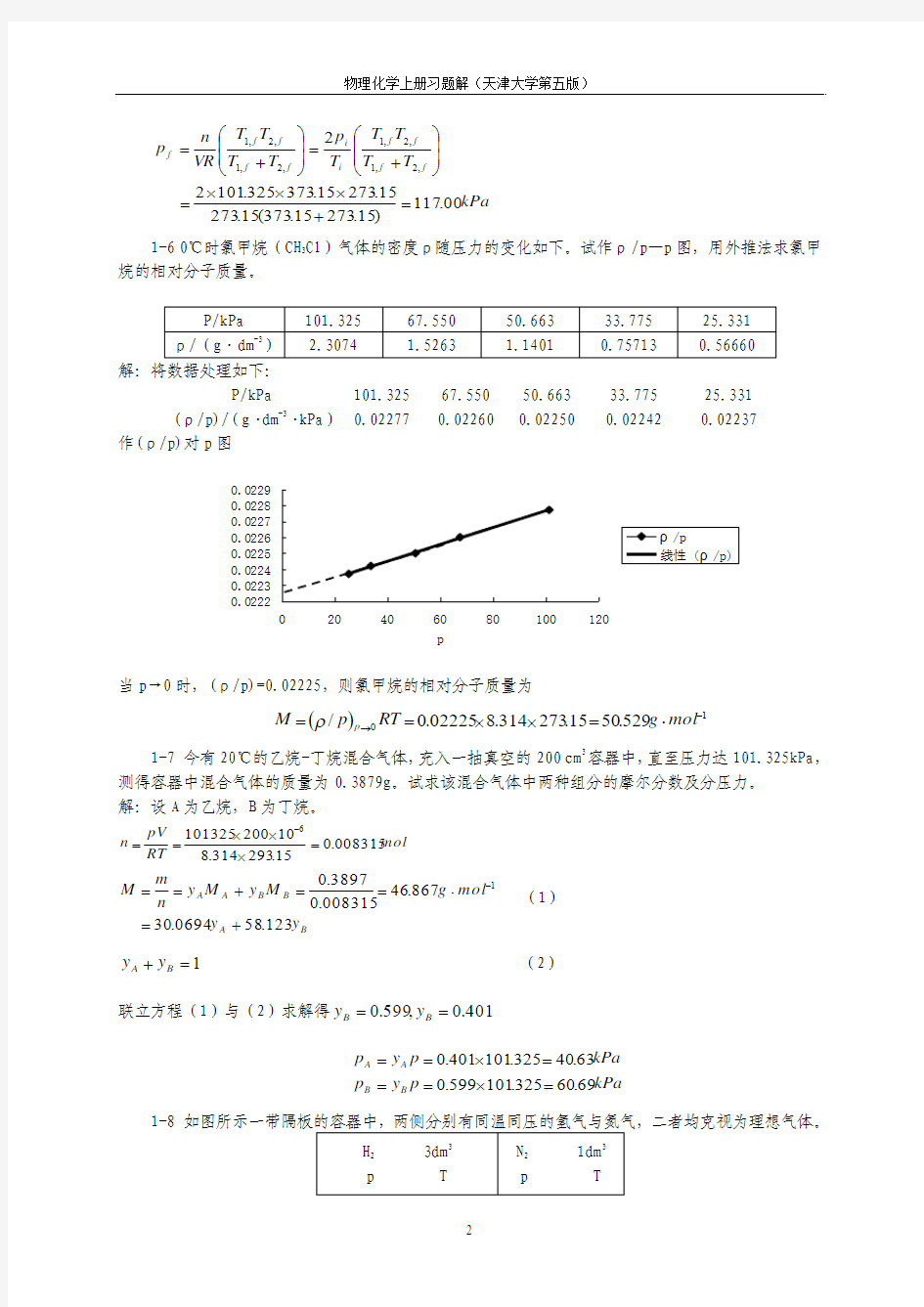
1-6 0℃时氯甲烷(CH 3Cl )气体的密度ρ随压力的变化如下。试作ρ/p —p 图,用外推法求氯甲烷的相对分子质量。
解:将数据处理如下:
P/kPa 101.325
67.550 50.663 33.775
25.331 (ρ/p)/(g 〃dm -3
〃kPa ) 0.02277
0.02260 0.02250
0.02242
0.02237
作(ρ/p)对p 图
当p →0时,(ρ/p)=0.02225,则氯甲烷的相对分子质量为
()10529.5015.273314.802225.0/-→?=??==mol g RT p M p ρ
1-7 今有20℃的乙烷-丁烷混合气体,充入一抽真空的200 cm 3
容器中,直至压力达101.325kPa ,测得容器中混合气体的质量为0.3879g 。试求该混合气体中两种组分的摩尔分数及分压力。 解:设A 为乙烷,B 为丁烷。
mol RT pV n 008315.015
.293314.8102001013256
=???==
- B A B B A A y y mol g M y M y n m M 123.580694.30 867.46008315.03897
.01+=?==+==
- (1) 1=+B A y y (2)
联立方程(1)与(2)求解得401.0,599.0==B
B y y
kPa
p y p kPa p y p B B A A 69.60325.101599.063.40325.101401.0=?===?==
1-8 如图所示一带隔板的容器中,两侧分别有同温同压的氢气与氮气,二者均克视为理想气体。
(1)保持容器内温度恒定时抽去隔板,且隔板本身的体积可忽略不计,试求两种气体混合后的压力。
(2)隔板抽去前后,H 2及N 2的摩尔体积是否相同?
(3)隔板抽去后,混合气体中H 2及N 2的分压力之比以及它们的分体积各为若干? 解:(1)抽隔板前两侧压力均为p ,温度均为T 。
p dm
RT n p dm RT n p N N H H ====3
3132222 (1) 得:2
23N H n n = 而抽去隔板后,体积为4dm 3
,温度为,所以压力为
3331444)3(2222dm
RT n dm RT n dm RT n n V nRT p N N N N ==+==
(2) 比较式(1)、(2),可见抽去隔板后两种气体混合后的压力仍为p 。 (2)抽隔板前,H 2的摩尔体积为p RT V H m /2,=,N 2的摩尔体积p RT V N m /2,=
抽去隔板后
2
2
222222223n 3 /)3(/H ,,N N N N N N m N H m H n p
RT n p
RT n p RT n n p nRT V n V n V =+=+==+= 总
所以有 p RT V H m /2,=,p RT V N m /2,= 可见,隔板抽去前后,H 2及N 2的摩尔体积相同。 (3)4
1 ,433322
222
==+=
N N N N H y n n n y p p y p p p y p N N H H 4
1
;432222===
= 所以有 1:34
1:43:2
2
==p p p p N H
3
3144
1
3443
22
22dm V y V dm V y V N N H H =?===?== 1-9 氯乙烯、氯化氢及乙烯构成的混合气体中,各组分的摩尔分数分别为0.89、0.09和0.02。于恒定压力101.325kPa 条件下,用水吸收掉其中的氯化氢,所得混合气体中增加了分压力为2.670 kPa 的水蒸气。试求洗涤后的混合气体中C 2H 3Cl 及C 2H 4的分压力。
解:洗涤后的总压为101.325kPa ,所以有 kPa p p H C Cl H C 655.98670.2325.1014232=-=+ (1) 02.0/89.0///423242324232===H C Cl H C H C Cl H C H C Cl H C n n y y p p (2)
联立式(1)与式(2)求解得
kPa p kPa p H C Cl H C 168.2 ;49.964232==
1-10 室温下一高压釜内有常压的空气。为进行实验时确保安全,采用同样温度的纯氮进行臵换,步骤如下向釜内通氮直到4倍于空气的压力,尔后将釜内混合气体排出直至恢复常压。这种步骤共重复三次。求釜内最后排气至年恢复常压时其中气体含氧的摩尔分数。设空气中氧、氮摩尔分数之比为1∶4。
解: 高压釜内有常压的空气的压力为p 常,氧的分压为
常p p O 2.02=
每次通氮直到4倍于空气的压力,即总压为
p=4p 常,
第一次臵换后釜内氧气的摩尔分数及分压为
常
常常
常p y p p p p p
p y O O O O ?=?===
=
=
05.005
.04
2
.042.01,1,1,2222 第二次臵换后釜内氧气的摩尔分数及分压为
常常常
常p y p p p p p
p y O O O O ?=
?==
=
=
4
05
.0405.0405.02,2,1,2,2222
所以第三次臵换后釜内氧气的摩尔分数
%313.000313.016
05
.04)4/05.0(2,3,22===
=
=
常
常
p p p
p y O O 1-11 25℃时饱和了水蒸汽的乙炔气体(即该混合气体中水蒸汽分压力为同温度下水的饱和蒸气压)总压力为138.7kPa ,于恒定总压下泠却到10℃,使部分水蒸气凝结成水。试求每摩尔干乙炔气在该泠却过程中凝结出水的物质的量。已知25℃及10℃时水的饱和蒸气压分别为 3.17kPa 和1.23kPa 。
解:p y p B B =,故有)/(///B B A B A B A B p p p n n y y p p -=== 所以,每摩尔干乙炔气含有水蒸气的物质的量为 进口处:)(02339.017
.37.13817.3222222mol p p n n H C O H H C O H =-=?
???
??=????
??进进 出口处:)(008947.0123
7.1381232
222
22mol p p n n H C O H H C O H =-=?
???
??=????
??出出 每摩尔干乙炔气在该泠却过程中凝结出的水的物质的量为 0.02339-0.008974=0.01444(mol )
1-12 有某温度下的2dm 3湿空气,其压力为101.325kPa ,相对湿度为60%。设空气中O 2和N 2
的体积分数分别为0.21和0.79,求水蒸气、O 2和N 2的分体积。已知该温度下水的饱和蒸气压为20.55kPa (相对湿度即该温度下水蒸气分压与水的饱和蒸气压之比)。
解:水蒸气分压=水的饱和蒸气压×0.60=20.55kPa ×0.60=12.33 kPa O 2分压=(101.325-12.33 )×0.21=18.69kPa N 2分压=(101.325-12.33 )×0.79=70.31kPa 33688.02325
.10169
.1822
2dm V p p V y V O O O =?=
=
=
33878.12325
.10131
.70222dm V p
p V y V N N N =?=
=
=
32434.02325
.10133
.12222dm V p
p V y V O
H O H O H =?=
=
=
1-13 一密闭刚性容器中充满了空气,并有少量的水,当容器于300K 条件下达到平衡时,器内压力为101.325kPa 。若把该容器移至373.15K 的沸水中,试求容器中达到新的平衡时应有的压力。设容器中始终有水存在,且可忽略水的体积变化。300K 时水的饱和蒸气压为3.567kPa 。
解:300K 时容器中空气的分压为 k P a k P a k P a p 758.97567.3325.101=-='空 373.15K 时容器中空气的分压为
)(534.121758.9730015
.37330015.373kPa p p =?='=空空
373.15K 时容器中水的分压为 =O H p 2101.325kPa
所以373.15K 时容器内的总压为
p=空p +=O H p 2121.534+101.325=222.859(kPa )
1-14 CO 2气体在40℃时的摩尔体积为0.381dm 3〃mol -1。设CO 2为范德华气体,试求其压力,并与实验值5066.3kPa 作比较。
解:查表附录七得CO 2气体的范德华常数为
a=0.3640Pa 〃m 6〃mol -2;b=0.4267×10-4m 3〃mol -1
5187.7kPa
5187675250756176952362507561100.338332603.5291
)10381.0(3640
.0104267.010381.015.313314.8)(3
-2
3432==-=-?=
?-
?-??=--=---Pa V a b V RT p m m 相对误差E=5187.7-5066.3/5066.3=2.4%
1-15今有0℃、40530kPa 的氮气体,分别用理想气体状态方程及范德华方程计算其摩尔体积。其实验值为70.3cm 3〃mol -1。
解:用理想气体状态方程计算如下: 1
313031.56000056031.0 40530000
15.273314.8/--?=?=÷?==mol cm mol m p RT V m
将范德华方程整理成
0/)/()/(23=-++-p ab V p a V p RT b V m m m (a)
查附录七,得a=1.408×10-1Pa 〃m 6〃mol -2,b=0.3913×10-4m 3〃mol -1
这些数据代入式(a ),可整理得
10
0.1)}/({100.3 )}/({109516.0)}/({13
1392
134133
=?-??+??-?------mol m V mol m V mol m V m m m 解此三次方程得 V m =73.1 cm 3〃mol -1
1-16 函数1/(1-x )在-1<x <1区间内可用下述幂级数表示:
1/(1-x )=1+x+x 2+x 3+…
先将范德华方程整理成
2/11m
m m V a V b V RT p -???? ??-=
再用述幂级数展开式来求证范德华气体的第二、第三维里系数分别为
B (T )=b-a (RT ) C=(T )=b 2
解:1/(1-b/ V m )=1+ b/ V m +(b/ V m )2+… 将上式取前三项代入范德华方程得
3222221m m m m m m m V RTb V a RTb V RT V a V b V b V RT p +-+=-???? ?
?++=
而维里方程(1.4.4)也可以整理成 32m
m m V RTC V RTB V RT p ++=
根据左边压力相等,右边对应项也相等,得 B (T )=b – a/(RT ) C (T )=b 2
*1-17 试由波义尔温度T B 的定义式,试证范德华气体的T B 可表示为
T B =a/(bR )
式中a 、b 为范德华常数。
解:先将范德华方程整理成22
)(V
an nb V nRT p --=
将上式两边同乘以V 得 V
an nb V nRTV pV 2
)(-
-= 求导数
22222222)( )()( )()(nb V RT bn V an V an nb V nRTV nRT nb V V an nb V nRTV p p pV T
T --=+---=???? ?
?--??=???? ????
当p →0时0]/)([=??T p pV ,于是有 0)
(2
222=--nb V RT
bn V an 2
2)(bRV a nb V T -=
当p →0时V →∞,(V-nb )2≈V 2,所以有 T B = a/(bR )
1-18 把25℃的氧气充入40dm 3的氧气钢瓶中,压力达202.7×102kPa 。试用普遍化压缩因子图求解钢瓶中氧气的质量。
解:氧气的临界参数为 T C =154.58K p C =5043kPa
氧气的相对温度和相对压力
929.158.154/15.298/===C r T T T 019.45043/107.202/2=?==C r p p p
由压缩因子图查出:Z=0.95
mol mol ZRT pV n 3.34415
.298314.895.01040107.2023
2=?????==-
钢瓶中氧气的质量 kg kg nM m O O 02.1110999.313.34432
2=??==- 1-19
1-20
1-21 在300k 时40dm 3钢瓶中贮存乙烯的压力为146.9×102kPa 。欲从中提用300K 、101.325kPa 的乙烯气体12m 3,试用压缩因子图求解钢瓶中剩余乙烯气体的压力。
解:乙烯的临界参数为 T C =282.34K p C =5039kPa 乙烯的相对温度和相对压力
063.134.282/15.300/===C r T T T
915.254039/109.146/2=?==C r p p p
由压缩因子图查出:Z=0.45
)(3.52315
.300314.845.010*******.1463
32mol mol ZRT pV n =??????==-
因为提出后的气体为低压,所提用气体的物质的量,可按理想气体状态方程计算如下:
mol mol RT pV n 2.48715
.300314.812
101325=??==
提 剩余气体的物质的量
n 1=n-n 提=523.3mol-487.2mol=36.1mol 剩余气体的压力
kPa Z Pa Z V RT n Z p 13
1
111225210
4015.300314.81.36=???==- 剩余气体的对比压力
11144.05039/2252/Z Z p p p c r ===
上式说明剩余气体的对比压力与压缩因子成直线关系。另一方面,T r =1.063。要同时满足这两个
条件,只有在压缩因子图上作出144.0Z p r =的直线,并使该直线与T r =1.063的等温线相交,此交点相当于剩余气体的对比状态。此交点处的压缩因子为
Z 1=0.88
所以,剩余气体的压力
kPa kPa kPa Z p 198688.022********=?==
第二章 热力学第一定律
2-1 1mol 理想气体于恒定压力下升温1℃,试求过程中气体与环境交换的功W 。 解:J
T nR nRT nRT pV pV V V p W am b 314.8)(121212-=?-=+-=+-=--= 2-2 1mol 水蒸气(H 2O ,g )在100℃,101.325 kPa 下全部凝结成液态水。求过程的功。 解: )(g l am b V V p W --=≈kJ RT p nRT p V p g am b 102.315.3733145.8)/(=?=== 2-3 在25℃及恒定压力下,电解1mol 水(H 2O ,l ),求过程的体积功。
)(2
1
)()(222g O g H l O H +=
解:1mol 水(H 2O ,l )完全电解为1mol H 2(g )和0.50 mol O 2(g ),即气体混合物的总的物质的量为1.50 mol ,则有
)()(2l O H g am b V V p W --=≈)/(p nRT p V p g am b -=-
kJ nRT 718.315.2983145.850.1-=??-=-= 2-4 系统由相同的始态经过不同途径达到相同的末态。若途径a 的Q a =2.078kJ ,W a = -4.157kJ ;而途径b 的Q b = -0.692kJ 。求W b 。
解:因两条途径的始末态相同,故有△U a =△U b ,则 b b a a W Q W Q +=+ 所以有,kJ Q W Q W b a a b 387.1692.0157.4078.2-=+-=-+=
2-5 始态为25℃,200kPa 的5 mol 某理想气体,经a ,b 两不同途径到达相同的末态。途径a 先经绝热膨胀到 – 28.57℃,100kPa ,步骤的功W a = - 5.57kJ ;在恒容加热到压力200 kPa 的末态,步骤的热Q a = 25.42kJ 。途径b 为恒压加热过程。求途径b 的W b 及Q b 。
解:过程为:
2
0,42.25200,57.510200510057.285200255V kPa C t mol
V kPa C mol V kPa C mol a a
a a W kJ Q Q kJ W ?????→
?-?????→?=''=''='-='
33111062.0)10200(15.2983145
.85/m p nRT V =?÷??== 33222102.0)10100()15.27357.28(3145.85/m p nRT V =?÷+-??== kJ J V V p W am b b 0.88000)062.0102.0(10200)(312-=-=-??-=--= kJ W W W a a a 57.5057.5-=+-=''+'=
kJ Q Q Q a a
a 42.2542.250=+=''+'= 因两条途径的始末态相同,故有△U a =△U
b ,则 b b a a W Q W Q +=+ kJ W W Q Q b a a b 85.270.857.542.25=+-=-+=
2-6 4mol 某理想气体,温度升高20℃,求△H -△U 的值。 解:
665.16J
208.3144 )20()( 2020,,20,20,=??=-+==-=-=?-??
?
?
?++++T K T nR nRdT dT C C n dT
nC dT nC U H K T T
K
T T
m V m p K
T T
m V K
T T m p
2-7 已知水在25℃的密度ρ=997.04 kg 〃m -3
。求1 mol 水(H 2O ,l )在25℃下: (1)压力从100 kPa 增加到200kPa 时的△H ; (2)压力从100 kPa 增加到1 MPa 时的△H 。
假设水的密度不随压力改变,在此压力范围内水的摩尔热力学能近似认为与压力无关。 解:)(pV U H ?+?=?
因假设水的密度不随压力改变,即V 恒定,又因在此压力范围内水的摩尔热力学能近似认为与压力无关,故0=?U ,上式变成为
)()(12122p p M p p V p V H O
H -=
-=?=?ρ
(1)J p p M H O
H 8.110)100200(04.9971018)(33
122=?-??=-=
?-ρ
(2)J p p M H O
H 2.1610)1001000(04
.9971018)(33
122=?-??=-=
?-ρ
*
2-8 某理想气体, 1.5V m C R =。今有该气体5 mol 在恒容下温度升高50℃,求过程的W ,Q ,△H 和△U 。
解:恒容:W=0;
kJ
J K nC T K T nC dT nC U m V m V K T T
m V 118.33118503145.823
550 )
50(,,50,==???=?=-+==??
+
kJ
J K
R C n T K T nC dT nC H m V m p K
T T
m p 196.55196503145.82
5
5 50)()50(,,50,==???=?+==-+==??
+
根据热力学第一定律,:W=0,故有Q=△U=3.118kJ
2-9 某理想气体, 2.5V m C R =。今有该气体5 mol 在恒压下温度降低50℃,求过程的W ,Q ,△H 和△U 。 解:
kJ
J K nC T K T nC dT nC U m V m V K T T
m V 196.55196503145.825
5)50( )
50(,,50,-=-=???-=-?=--==??
-
kJ
J K nC T K T nC dT nC H m p m p K
T T
m p 275.77275503145.82
7
5)50( )
50(,,50,-=-=???-=-?=--==??
-
kJ
kJ kJ Q U W kJ
H Q 079.2)725.7(196.5275.7=---=-?=-=?=
2-10 2mol 某理想气体,R C m P 2
7,=。由始态100 kPa ,50 dm 3
,先恒容加热使压力升高至200
kPa ,再恒压泠却使体积缩小至25 dm 3
。求整个过程的W ,Q ,△H 和△U 。 解:整个过程示意如下:
3
33
203
125200250200250100221dm kPa T mol
dm kPa T mol dm kPa T mol W W ?→???→?=
K nR V p T 70.3003145.821050101003
3111=????==- K nR V p T 4.6013145.8210501020033222=????==-
K nR V p T 70.3003145
.821025102003
3333=????==-
kJ J V V p W 00.5500010)5025(10200)(331322==?-??-=-?-=- kJ W kJ W W 00.5W W ;00.5 ;02121=+=== 0H 0,U ;70.300 31=?=?∴==K T T
-5.00kJ
-W Q 0,U ===? 2-11 4 mol 某理想气体,R C m P 2
5,=。由始态100 kPa ,100 dm 3
,先恒压加热使体积升增大到150
dm 3
,再恒容加热使压力增大到150kPa 。求过程的W ,Q ,△H 和△U 。 解:过程为
3
30
3
23
115015041501004100100421dm kPa T mol
dm kPa T mol dm kPa T mol W W ??→
??→?= K nR V p T 70.3003145.84101001010033111=????==-; K nR V p T 02.4513145.8410150101003
3222=????==-
K nR V p T 53.6763145
.8410150101503
3333=????==-
kJ J V V p W 00.5500010)100150(10100)(331311-=-=?-??-=-?-=- kJ W kJ W W 00.5W W ;00.5 ;02112-=+=-== )(2
3
)(13,,3
1
3
1
T T R n dT R C n dT nC U T T m p T T m V -??
=-==??? kJ J 75.1818749)70.30053.676(314.8234==-???=
)(2513,3
1T T R n dT nC H T T m P -??
==??kJ J 25.3131248)70.30053.676(314.82
5
4==-???=
kJ kJ kJ W U Q 23.75)00.5(75.18=--=-?=
2-12 已知CO 2(g )的
C p ,m ={26.75+42.258×10-3(T/K )-14.25×10-6(T/K )2} J 〃mol -1〃K -1 求:(1)300K 至800K 间CO 2(g )的m p C ,;
(2)1kg 常压下的CO 2(g )从300K 恒压加热至800K 的Q 。
解: (1):
?=?2
1
,T T m p m dT C H
1
-12615.80015.3003mol 22.7kJ )/(})/(1025.14)/(10258.4275.26{?=??-?+=---?
mol J K T d K T K T K
K
11113,4.45500/)107.22(/----??=???=??=K mol J K mol J T H C m m p
(2):△H=n △H m =(1×103)÷44.01×22.7 kJ =516 kJ
2-13 已知20 ℃液态乙醇(C 2H 5OH ,l )的体膨胀系数131012.1--?=K V α,等温压缩系数191011.1--?=Pa T κ,密度ρ=0.7893 g 〃cm -3
,摩尔定压热容11,30.114--??=K mol J C m P 。求20℃,液态乙醇的m V C ,。
解:1mol 乙醇的质量M 为46.0684g ,则 ρ/M V m =
=46.0684g 〃mol -1
÷(0.7893 g 〃cm -3
)=58.37cm 3
〃mol -1
=58.37×10-6m 3
〃mol -1
由公式(2.4.14)可得:
1
1111119213136112
,,963.94337.1930.1141011.1)1012.1(1037.5815.29330.114 /--------------??=??-??=?÷?????-??=-=K m ol J K m ol J K m ol J Pa K m ol m K K m ol J TV C C T
V m m p m V κα 2-14 容积为27m 3的绝热容器中有一小加热器件,器壁上有一小孔与100 kPa 的大气相通,以维持容器内空气的压力恒定。今利用加热器件使容器内的空气由0℃加热至20℃,问需供给容器内的空气多少热量。已知空气的11,4.20--??=K mol J C m V 。 假设空气为理想气体,加热过程中容器内空气的温度均匀。
解:假设空气为理想气体 RT
pV n =
kJ
J J T T R pV R C T d R
pV C dT RT pV C dT nC H Q Q m
V T T m
p T T m p T T m p p 59.6658915
.27315.293ln 8.314271000008.314)(20.40 ln
)(ln 1
2
,,,,2
1
2
12
1
==??
+=+====?==?
?
?
2-15 容积为0.1m 3的恒容密闭容器中有一绝热隔板,其两侧分别为0℃,4 mol 的Ar (g )及
150℃,2mol 的Cu (s )。现将隔板撤掉,整个系统达到热平衡,求末态温度t 及过程的△H 。 已知:Ar (g )和Cu (s )的摩尔定压热容C p ,m 分别为20.78611--??K mol J 及24.43511--??K mol J ,且假设均不随温度而变。
解:用符号A 代表Ar (g ),B 代表Cu (s );因Cu 是固体物质,C p ,m ≈C v ,m ;而 Ar (g ):1111,472.12)314.8786.20(----??=??-=K mol J K mol J C m V 过程恒容、绝热,W=0,Q V =△U=0。显然有 {}{}0)()(n(B)C )()(n(A)C )
()(12m V,12m V,=-+-=?+?=?B T T B A T T A B U A U U
得
K
K B C B n A C A n B T B C B n A T A C A n T m V m V m V m V 38.34724.435
212.4724423.15
24.4352273.1512.4724 )
()()()()
()()()()()(,,1,1,2=?+???+??=
++=
所以,t=347.38-273.15=74.23℃
{}{})()(n(B)C )()(n(A)C )
()(12m p,12m p,B T T B A T T A B H A H H -+-=?+?=?
kJ
J J J J J H 47.2246937036172 )15.42338.347(435.242)15.27338.347(786.204==-=-??+-??=? 2-16水煤气发生炉出口的水煤气温度是1100℃,其中CO (g )及H 2(g )的体积分数各为0.50。
若每小时有300kg 水煤气有1100℃泠却到100℃,并用所回收的热来加热水,使水温有25℃升高到75℃。试求每小时生产热水的质量。
CO (g )和H 2(g )的摩尔定压热容Cp ,m 与温度的函数关系查本书附录,水(H 2O ,l )的比定压热容c p =4.18411--??K g J 。
解:已知 5.0y ,01.28M ,016.222
H CO ====CO H y M 水煤气的平均摩尔质量
013.15)01.28016.2(5.022=+?=+=CO CO H H M y M y M
300kg 水煤气的物质的量 mol mol n 19983013
.15103003
=?=
由附录八查得:273K —3800K 的温度范围内
2316213112,103265.010347.488.26)(T K mol J T K mol J K mol J H C m p --------???-???+??= 231621311,10172.1106831.7537.26)(T K mol J T K mol J K mol J CO C m p --------???-???+??=
设水煤气是理想气体混合物,其摩尔热容为
2
3162131
1,)(,10)172.13265.0(5.0 10)6831.7347.4(5.0 )537.2688.26(0.5)(T K m ol J T K m ol J K m ol J B C y C B
m p B mix m p --------???+?-???+?+??+?==∑ 故有
2
31
6
21311)(,1074925.0 1001505.67085.26T
K mol
J T K mol J K mol J C mix m p --------???-???+??=
得 dT C H Q K
K
mix m p m m p ?
=?=15.37315.1373)(,,
{}
dT
T K mol J T K mol J K mol
J Q K
K
p 231621315.37315.13731
1
1074925.0100151.6 7085.26--------???-???+??=?
= 26.7085×(373.15-1373.15)1
-?mol J
+2
1×6.0151×(373.152
-1373.152
)×10-3
1
-?mol J
-3
1×0.74925×(373.153
-1373.153
)×10-6
1
-?mol J
= -26708.51-?mol J -5252.081-?mol J +633.661
-?mol J
=313271
-?mol J =31.3271
-?mol kJ 19983×31.327=626007kJ
kg kg g kg C Q m kg p p 35,1099.2387.29922992387)
2575(184.410626007t ?===-??=??-=
水
2-17 单原子理想气体A 与双原子理想气体B 的混合物共5mol ,摩尔分数y B =0.4,始态温度T 1=400 K ,压力p 1=200 kPa 。今该混合气体绝热反抗恒外压p=100 kPa 膨胀到平衡态。求末态温度T 2及过程的W ,△U ,△H 。
解:先求双原子理想气体B 的物质的量:n (B )=y B ×n=0.4×5 mol=2mol ;则 单原子理想气体A 的物质的量:n (A )=(5-2)mol =3mol
单原子理想气体A 的R C m V 23,=,双原子理想气体B 的R C m V 25,=
过程绝热,Q=0,则 △U=W
)())(()())(()(1212,12,V V p T T B C B n T T A C A n am b m V m V --=-+-
1
2112121211212125.055)/()(5)(5.4)(25
2)(233T T T p p n nT T T T T p nRT p nRT p T T R T T R amb amb amb ?+-=?+-=-?+-????
? ??--=-?+-?
于是有 14.5T 2=12T 1=12×400K
得 T 2=331.03K
33222213761.010000003.331314.85//--=÷??===m m p nRT p nRT V abm 3311108314.0200000
400314.85/--=÷??==m m p nRT V kJ J V V p W U am b 447.5)08314.013761.0(10100)(312-=-??-=--==? kJ
J J J J V p V p U pV U H 314.8831428675447 )08314.010********.010(100-5447J )
()(331122-=-=--=??-??+=-+?=?+?=? 2-18 在一带活塞的绝热容器中有一绝热隔板,隔板的两侧分别为2mol ,0℃的单原子理想气体A 及5mol ,100℃的双原子理想气体B ,两气体的压力均为100 kPa 。活塞外的压力维持 100kPa 不变。
今将容器内的绝热隔板撤去,使两种气体混合达到平衡态。求末态温度T 及过程的W ,△U 。
解:单原子理想气体A 的R C m p 25,=,双原子理想气体B 的R C m p 27,=
因活塞外的压力维持 100kPa 不变,过程绝热恒压,Q=Q p =△H=0,于是有
)15.373(5.17)15.273(50)15.373(2
7
5)15.273(2520)15.373)(()()15.273)(()(,,=-?+-?=-?+-?=-+-K T K T K T R K T R K T B C B n K T A C A n m p m p
于是有 22.5T=7895.875K 得 T=350.93K W -369.3J 2309.4-1940.1J )15.37393.350(2
3145
.855)15.27393.350(23145.832 )
15.373)(()()15.273)(()(,,===-???+-???
=-+-=?J J K T B C B n K T A C A n U m V m V 2-19在一带活塞的绝热容器中有一固定绝热隔板,隔板活塞一侧为2mol ,0℃的单原子理想气体A ,压力与恒定的环境压力相等;隔板的另一侧为6mol ,100℃的双原子理想气体B ,其体积恒定。
今将绝热隔板的绝热层去掉使之变成导热隔板,求系统达平衡时的T 及过程的W ,△U 。
解:过程绝热,Q=0,△U=W ,又因导热隔板是固定的,双原子理想气体B 体积始终恒定,所以双原子理想气体B 不作膨胀功,仅将热量传给单原子理想气体A ,使A 气体得热膨胀作体积功,因此,W=W A ,故有
△U=W=W A
得
{}
K
T K T K T p K R p RT p K T R K T R V V p K T B C B n K T A C A n amb amb amb A A amb m V m V 15.27322)15.373(15)15.273(3/15.2732()/2( )15.373(25
6)15.273(232)()15.373)(()()15.273)(()(1,2,,,?+-=-?+-??--=-?+-?
--=-+-
得 20×T=6963K 故 T=348.15K
332,205789.010000015.3483145.82/--=÷??==m m p nRT V abm A 331,104542.010000015.2733145
.82/--=÷??==m m p nRT V abm A J J V V p W U A A am b 1247)04542.005789.0(10100)(3,1,2-=-??-=--==?
2-20 已知水(H 2O ,l )在100℃的饱和蒸气压p s
=101.325 kPa ,在此温度、压力下水的摩尔蒸发焓1668.40-?=?mol kJ H m vap 。求在100℃,101.325 kPa 下使1kg 水蒸气全部凝结成液体水时的Q ,W ,△U 及△H 。设水蒸气适用理想气体状态方程。
解:过程为 kPa C g O kgH 325.101,100),(10
2kPa C l O kgH 325.101,100),(102 mol n 524.5501.18/1000==
H kJ kJ H n Q Q m vap p ?=-=-?=?-?==2258)668.40(524.55)( kJ J RT n pV V V p W g g g l amb 35.172)15.373314.818
1000()(=??==≈--=
kJ W Q U 65.2085)35.1722258(-≈+-=+=?
2-17今有温度分别为80℃、40℃及10℃的三种不同的固体物质A 、B 及C 。若在与环境绝热条件下,等质量的A 和B 接触,热平衡后的温度为57℃;等质量的A 与C 接触,热平衡后的温度为36℃。若将等质量的B 、C 接触,达平衡后系统的温度应为多少?
解:设A 、B 、C 的热容各为c A 、c B 、c C ,于是有
mc A (57-80)+m c B (57-40)=0 (1) mc A (36-80)+ mc C (36-10)=0 (2) mc B (t-40)+m c C (t-10)=0 (3) 得:c A (57-80)= - c B (57-40) (4)
c A (36-80)= - c C (36-10) (5) c B (t-40)+ c C (t-10)=0 (6) 由式(4)除以式(5),解得 c B =0.7995c C 将上式代入式(6)得
0.7995c C (t-40)+ c C (t-10)=0 (7) 方程(7)的两边同除以c C ,得
0.7995×(t-40)+ (t-10)=0 (8) 解方程(8),得 t=23.33℃
结果表明,若将等质量的B 、C 接触,达平衡后系统的温度应为23.33℃。
2-21 求1mol N 2(g )在300K 恒温下从2 dm 3 可逆膨胀到40 dm 3
时的体积功W r 。 (1)假设N 2(g )为理想气体;
(2)假设N 2(g )为范德华气体,其范德华常数见附录。 解:(1)假设N 2(g )为理想气体,则恒温可逆膨胀功为
)/ln(12V V nRT W r -== -1×8.3145×300×ln (40÷2)J = - 7472J =7.472 kJ
(2)查附录七,得其范德华常数为
2613108.140mol m Pa a ???=---;1361013.39---??=mol m b
-7.452kJ
-7452J 102110401108.1401- 1013.3911021013.3911040300ln 8.314-1 11V -nRT ln 33326
3-6
3-12
212222
1
21
==??? ??
?-???????
? ?
???-???-???=???? ??-+???? ??--=???? ??---=-=-----?
?J J V V an nb V nb dV V an nb V RT pdV W V V V V r
2-22 某双原子理想气体1mol 从始态350K ,200 kPa 经过如下四个不同过程达到各自的平衡态,求各过程的功W 。
(1)恒温可逆膨胀到50 kPa ;
(2)恒温反抗50 kPa 恒外压不可逆膨胀; (3)绝热可逆膨胀到50kPA ;
(4)绝热反抗50 kPa 恒外压不可逆膨胀。 解:(1)恒温可逆膨胀到50 kPa :
()kJ J J p p nRT W r 034.4403410201050ln 3503145.81/ln 3
312-=-=????
? ?
?????==
(2)恒温反抗50 kPa 恒外压不可逆膨胀:
{}{}{}kJ
J J p p nRT p nRT p V V p W amb amb amb 183.22183 200/50(13503145.81)/(p -1-nRT )/()/()(1amb 112-=-=-??-==--=--= (3)绝热可逆膨胀到50kPa: K K T p p T R R C R m
p 53.235350102001050)
2/7/(331/122,=??
??
? ????=????
? ??=
绝热,Q=0,
kJ J J T T C n dT nC U W T T m V m V 379.22379)35053.235(2
8.3145
51 )
(12,,2
1-=-=-???
=-??==?=?
(4)绝热反抗50 kPa 恒外压不可逆膨胀 绝热,Q=0, U W ?= {})
()2/5()/()/()
()(1211212,12T T R n p nRT p nRT p T T nC V V p amb amb m V abm -?=---=--
上式两边消去nR 并代入有关数据得
K T K T 3505.25.235025.022?-=?+-
3.5T 2=2.75×350K 故 T 2=275K kJ J J T T C n dT nC U W T T m V m V 559.11559)350275(2
8.3145
51 )
(12,,2
1-=-=-???
=-??==?=?
2-23 5 mol 双原子理想气体1mol 从始态300K ,200 kPa ,先恒温可逆膨胀到压力为50kPa ,再绝热可逆压缩末态压力200 kPa 。求末态温度T 及整个过程的Q ,W ,△U 及△H 。
解:整个过程如下
mol
p kPa T mol
p kPa K mol
kPa K 5200550300520030021=????→?=????→?绝热可逆压缩恒温可逆膨胀
K K T p p T R R C R m
p 80.445400105010200)
2/7/(3
3
1/12,=????
? ?
???=??
??
? ??=
恒温可逆膨胀过程:
()kJ J J p p nRT W r 29.171728910201050ln 3003145.85/ln 3
312-=-=????
? ?
?????== 因是理想气体,恒温,△U 恒温=△H 恒温=0 绝热可逆压缩:Q=0,故 kJ
J J T T R T T nC U W m V 15.1515153)30080.445(314.82
5
5 )(2
5
5)(11,==?-???=-?
=-=?=绝绝
kJ
J J T T R T T nC H m p 21.2121214)30080.445(314.82
7
5 )(2
7
5)(11,==?-???=-?
=-=?绝
故整个过程:
W=W r +W 绝= (-17.29+15.15)kJ=2.14 kJ △U=△U r +△U 绝=(0+15.15)=15.15kJ △H=△H r +△H 绝=(0+21.21)=21.21kJ
2-24 求证在理想气体p —V 图上任一点处,绝热可逆线的斜率的绝对值大于恒温可逆线的斜率的绝对值。
解:理想气体绝热可逆方程为:=γpV 常数=K (1)
理想气体恒温可逆方程为:=pV 常数=C (2)
对方程(1)及方程(2)求导,得
)/()/(V p V p Q γ-=?? (3) )/()/(V p V p T -=?? (4)
因m V m p C C ,,/=γ>1,故在理想气体p —V 图上任一点处,绝热可逆线的斜率的绝对值)/(V p γ-大于恒温可逆线的斜率的绝对值)/(V p -。
2-25一水平放臵的绝热圆筒中装有无磨檫的绝热理想活塞,左、右两侧分别为50dm 3
的单原子
理想气体A 和50dm 3
的双原子理想气体B 。两气体均为0℃、100kPa 。A 气体内部有一体积及热容均可忽略的电热丝.现在经通电无限缓慢加热左侧气体A ,推动活塞压缩右侧气体B 使压力最终到达200kPa 。求:(1)气体B 的最终温度;(2)气体B 得到的功;(3)气体A 的最终温度;(4)气体A 从电热丝得到的热。
解:(1)右侧气体B 进行可逆绝热过程
K K p p T R R C R
m p 97.3321010010
20015.273T 2
/733
1212,=???
?
?????=?
??
? ???=
(2) 因绝热,Q B =0, )()(12,1
1
112,T T C RT V p T T nC U W m V m V B -=
-=?= kJ J J 738.22738)15.27397.332(2
314.8515.273314.810501010033==?-???????=-
(3)气体A 的末态温度:
33
3
31221122
11
1226.48.3015
.2731020097.3325010100dm dm T p T V p p RT RT V p p nRT V B =?????==== V A =(2×50-30.48)dm 3=69.52dm 3
K K V p T V p R RT V p V p R n V p T A A A A B 58.759501010015.27352.6910200)/(3
3111211122=?????==== (4)气体A 从电热丝得到的热: B A n mol RT V p n ==????==-2017.215
.273314.81050101003
3111
kJ
kJ kJ kJ kJ W T T nC W U Q B
B m V 094.16738.2356.13 738.210)15.27358.759(314.82
3
2017.2 )(31,=+=+?-???=+-=-?=-
2-26 在带活塞的绝热容器中有4.25 mol 的某固态物质A 及5 mol 某单原子理想气体B ,物质A 的11,454.24--??=K mol J C m p 。始态温度T 1=400 K ,压力p 1=200 。
今以气体B 为系统,求经可逆膨胀到p 2=100 kPa 时,系统的T 2及过程的Q ,W ,△U 及△H 。(注意:以p 2=50kPa 解题,得不到和答案一样的结果,可能是p 2=100 kPa 。估计是打印错误所致)
解:今以气体B 为系统:
K K T p p T R R C R m
p 14.3034001020010100)
2/5/(3
3
1/122,=????
? ????=??
??
? ??=
kJ J J J
dT Q Q K
K
A 07.1010067)}40014.303(454.2425.4{}454.2425.4{14.303400≈=-??-=?-=-=?
kJ J J R U 04.66040)}40014.303(23
0.5{-≈-=-??=?
kJ J J R H 07.1010067)}40014.303(2
5
0.5{-≈-=-??=?
kJ Q U W 11.16-=-?=
2-28 已知100kPa 下冰的熔点为0℃,此时冰的比熔化焓13.333-?=?g J h fus 。水的均比定压热容11184.4--??=K g J c p 。求绝热容器内向1kg 50℃的水中投入0.1 kg 0℃的冰后,系统末态的温度。计算时不考虑容器的热容。
解:变化过程示意如下 ( 0.1kg ,0℃冰)( 0.1kg ,0℃,水)
( 0.1kg ,t ,水)
( 1kg ,50℃,水)( 1kg ,t ,水)
过程恒压绝热:0=?=H Q p ,即021=?+?=?H H H K
1433015.564602.4T 0)15.323(184.41000 )15.273(184.41003.333100111111==-????+-????+???------K T K g J K T K g J g K g J g
311.363K T =, 故 t=38.21℃
2-29 已知100kPa 下冰的熔点为0℃,此时冰的比熔化焓13.333-?=?g J h fus 。水和冰的均比定压热容p c 分别为11184.4--??K g J 及11000.2--??K g J 。今在绝热容器内向1kg 50℃的水中投入0.8 kg 温度-20℃的冰。求:(1)末态的温度;(2)末态水和冰的质量。
解:过程恒压绝热:0=?=H Q p ,即021=?+?=?H H H
261.27K
T 7531.2T
1352059.6-914287.68-26664032000 0)15.323(184.41000 )
15.273(184.480033.333800)15.25315.273(0.280011111111==+=-????+-????+???+-????--------K T K g J K T K g J g K g J g K K K g J g
这个结果显然不合理,只有高温水放出的热量使部分冰熔化为水,而维持在 0℃,所以末态的温度
为 0℃。
(2)设0℃冰量为 m ,则0℃水量为(500 – m )g ,其状态示意如下
K
l O H g K
s O mH l O gH m K l O H g K s O H g p Q 15.273 ),( ,100015.273 ),( ),()800(15.323 ),( ,100015.253 ),(,800222022-??→
?= 800 g ×2. J ·g -1·K -1×(273.15 K –253.15K )+(800-m )g ×333.3 J ·g -1 + 1000g ×4.184 J ·g -1·K -1×(273.15K – 323.15K )=0 333.3 m = 89440 g
m=268g =0.268 kg =冰量
水量= {1000+(800-268)}g = 1532 g =1.532 kg 2-30 蒸气锅炉中连续不断地注入20℃的水,将其加热并蒸发成180℃,饱和蒸气压为1.003Mpa 的水蒸气。求每生产1kg 饱和水蒸气所需的热。
已知:水(H 2O ,l )在100℃的摩尔相变焓1668.40)15.373(-?=?mol kJ K H m vap ,水的平均摩尔定压热容为12,32.75),(-?=mol J l O H C m p ,水蒸气(H 2O ,g )的摩尔定压热容与温度的关系见附录。 解:据题意画出下列方框图:
△H 1 =J J t t C m m p l O H 76.334)20100(32.7518
1000
)(12,)(2=-??=-
kJ
kJ K dT K T K T dT nC H K
K T T g O H p 54.154}/)/102.002- /1049.1416.29(181000{226-15.45315.3733)(,2212=??+=????- 所以每生产1kg 饱和蒸气所需的热
Q p =△H=△H 1+△vap H kg (373.15K )+△H 2= =(334.76+2257+154.54)kJ =2.746×103kJ
2-31 100kPa 下,冰(H 2O ,s )的熔点为0℃,在此条件下冰的摩尔熔化焓1012.6-?=?mol kJ H m fus 。已知在-10℃~0℃范围内过泠水(H 2O ,l )和冰的摩尔定压热容分别为C p ,m (H 2O ,
l )=76.2811--??K mol J 和C p ,m (H 2O ,s )=37.2011--??K mol J 。求在常压下及 – 10℃下过泠水结冰的摩尔凝固焓。 解:
C s O H C l O H m
H 020210),(10),(-??→?-?
△H 1,m △H 3,m
C s O H C l O H m
H
02020 ),(0 ),(,2??→??
1,2012.6-?-=?-=?mol kJ H H m fus m
1
112,,22,215.26315.273,,2215.27315.263,,3,2,1621.55621 )102.3760121028.76( )15.27315.263(),( )
15.26315.273(),( ),(),( 1
---?-=?-=??--?=-?+?+-?=+?+=?+?+?=??
?
mol kJ mol J mol J K K s O H C H K K l O H C dT
s O H C H dT l O H C H H H H m p m m p K
K
m p m K K m p m m m m
2-32 已知水(H 2O ,l )在100℃的摩尔蒸发焓1668.40-?=?mol kJ H m vap ,水和水蒸气在25~100℃的平均摩尔定压热容分别为75.75),(2,=l O H C m p 11--??K mol J 和76.33),(2,=g O H C m p 11--??K mol J 。求在25℃时水的摩尔蒸发焓。
解:C g O H C
l O H m
H 020225 ),(25 ),(??→??
△H 1,m △H 3,m
C g O H C
l O H m
vap H
0202010 ),(010 ),(??→??
1
112,2,215.29815.373,,2215.37315.298,,3,13821.443817 )7576.33406687575.75( )15.37315.298(),( )
15.29815.373(),( ),(),( 1
---?-=?-=??-+?=-?+?+-?=+?+=?+?+?=??
?
m ol kJ m ol J m ol J K K g O H C H K K l O H C dT
s O H C H dT l O H C H H H H m p m vap m p K
K
m p m K
K m p m
m vap m m
2-33 25℃下,密闭恒容的容器中有10g 固体萘C 10H 8(s )在过量的O 2(g )中完全燃烧成CO 2
(g )和H 2O (l )。过程放热401.727 kJ 。求
(1))(4)(10)(12)(222810l O H g CO g O s H C +=+的反应进度;
(2)C 10H 8(s )的θm C U ?; (3)C 10H 8(s )的θ
m C H ?。
解:(1)反应进度:mmol mol n n n 019.78078019.0173
.12810
1//===
?=?=?=νξ
(2)C 10H 8(s )的θm C U ?:M 萘=128.173
每摩尔萘的恒容恒温燃烧热为
1
15149 )727.401(10
173
.128)15.298()15.298(--?-=?-?=
?=?m ol kJ m ol kJ K U K U m r m c θ
第一章气体的PVT性质 选择题 1. 理想气体模型的基本特征是 (A) 分子不断地作无规则运动、它们均匀分布在整个容器中 (B) 各种分子间的作用相等,各种分子的体积大小相等 (C) 所有分子都可看作一个质点, 并且它们具有相等的能量 (D) 分子间无作用力, 分子本身无体积 答案:D 2. 关于物质临界状态的下列描述中, 不正确的是 (A) 在临界状态, 液体和蒸气的密度相同, 液体与气体无区别 (B) 每种气体物质都有一组特定的临界参数 C)在以p、V为坐标的等温线上, 临界点对应的压力就是临界压力 (D) 临界温度越低的物质, 其气体越易液化 答案:D 3. 对于实际气体, 下面的陈述中正确的是 (A) 不是任何实际气体都能在一定条件下液化 (B) 处于相同对比状态的各种气体,不一定有相同的压缩因子 (C) 对于实际气体, 范德华方程应用最广, 并不是因为它比其它状态方程更精确 (D) 临界温度越高的实际气体越不易液化 答案:C 4. 理想气体状态方程pV=nRT表明了气体的p、V、T、n、这几个参数之间的定量关系,与气体种类无关。该方程实际上包括了三个气体定律,这三个气体定律是 (A) 波义尔定律、盖-吕萨克定律和分压定律 (B) 波义尔定律、阿伏加德罗定律和分体积定律 (C) 阿伏加德罗定律、盖-吕萨克定律和波义尔定律 (D) 分压定律、分体积定律和波义尔定律 答案:C 问答题 1. 什么在真实气体的恒温PV-P曲线中当温度足够低时会出现PV值先随P 的增加而降低,然后随P的增加而上升,即图中T1线,当温度足够高时,PV值总随P的增加而增加,即图中T2线?
第一章 气体的pVT 关系 1-1物质的体膨胀系数V α与等温压缩系数T κ的定义如下: 1 1T T p V p V V T V V ???? ????-=??? ????= κα 试导出理想气体的V α、T κ与压力、温度的关系 解:对于理想气体,pV=nRT 111 )/(11-=?=?=??? ????=??? ????= T T V V p nR V T p nRT V T V V p p V α 1211 )/(11-=?=?=???? ????-=???? ????- =p p V V p nRT V p p nRT V p V V T T T κ 1-2 气柜内有、27℃的氯乙烯(C 2H 3Cl )气体300m 3 ,若以每小时90kg 的流量输往使用车间,试问贮存的气体能用多少小时 解:设氯乙烯为理想气体,气柜内氯乙烯的物质的量为 mol RT pV n 623.1461815 .300314.8300 106.1213=???== 每小时90kg 的流量折合p 摩尔数为 13 3153.144145 .621090109032-?=?=?=h mol M v Cl H C n/v=(÷)=小时 1-3 0℃、的条件常称为气体的标准状况。试求甲烷在标准状况下的密度。 解:33 714.015 .273314.81016101325444 --?=???=?=?=m kg M RT p M V n CH CH CH ρ 1-4 一抽成真空的球形容器,质量为。充以4℃水之后,总质量为。若改用充以25℃、的某碳氢化合物气体,则总质量为。试估算该气体的摩尔质量。 解:先求容器的容积33)(0000.10010000.100000.250000.1252cm cm V l O H ==-=ρ n=m/M=pV/RT mol g pV RTm M ?=?-??== -31.3010 13330) 0000.250163.25(15.298314.84 1-5 两个体积均为V 的玻璃球泡之间用细管连接,泡内密封着标准状况条件下的空气。若将其
四川大学期末考试试题 (2010—2011学年第一学期) 课程代码:(Ⅰ)—1 课程名称:物理化学任课教师:李泽荣、何玉萼适用专业:化学、应化、材化专业印数:200份班级:学号:姓名:成绩 注:1、试题字迹务必清晰,书写工整。本卷3页,本页为第1页 2、题间不留空,一般应题卷分开教务处试题编号: 3、务必用16K纸打印
注:1、试题字迹务必清晰,书写工整。本卷3页,本页为第2页 2、题间不留空,一般应题卷分开教务处试题编号: 3、务必用16K纸打印 2200 2400 2300 t/℃ a
注:1、试题字迹务必清晰,书写工整。本卷3页,本页为第3页 2、题间不留空,一般应题卷分开教务处试题编号: 3、务必用16K纸打印 2010级物理化学(Ⅰ)-1期末考试题B卷答案
一、选择题(12分,每题2分) 1、B 2、A 3、B 4、C 5、C 6、D 二、填空题(20分,每空2分) 1、> ;> ;> ;= 2、 3、 ; 4、1 ;2 5、y A >0,B x >x A ;纯A ;纯B 6、- 三、(16分) 解:33.3kJ R P vap m Q Q H n H ==?=?= 4分 kJ 2.32.383324.81)(=??==≈?=nRT pV V p W g R 2分 kJ 1.302.33.33=-=+=?W Q U 2分 1-3vap K J 9.862 .383103.33?=?=?==?b m R T H T Q S 体 2分 -186.9J K R Q Q S T T ?==-=-?环环 2分 0R R G H T S Q Q ?=?-?=-= 2分 kJ 2.3-=-=-?=?-?=?R R W Q U S T U F 2分 四、(12分) 解: ∵ A A B B P x P x P ** +=总 ∴ 13 78.844 A B P P **+= 6分 1182.722 A B P P **+= 联立求解得 kPa P A 5.90=* 6分 kPa P B 9.74=* 五、(20分) 解:1.(7分) 2.
三、计算 1、测得300C时某蔗糖水溶液的渗透压为252KPa。求 (1)该溶液中蔗糖的质量摩尔浓度; (2)该溶液的凝固点降低值; (3)在大气压力下,该溶液的沸点升高值已知Kf =1.86K mol–1Kg–1 , Kb =0.513K mol–1Kg–1 ,△vapH0m=40662J mol–1 2、有理想气体反应2H2(g)+O2(g)=H2O(g),在2000K时,已知K0=1.55×107
1、计算H2 和O2分压各为1.00×10 4 Pa, 水蒸气分压为1.00×105 Pa的混合气体中,进行上述反应的△rGm,并判断反应自发进 行的方向。 2、当H2和O2分压仍然分别为1.00×10 4 Pa 时。欲使反应不能正向自发进行,水蒸气分 压最少需多大? △rGm=-1.6﹡105Jmol–1;正向自发;P (H2O)=1.24﹡107Pa。 装 订 线
在真空的容器中放入固态的NH4HS,于250C 下分解为NH3(g)与H2S(g), 平衡时容器内的压力为66.6kPa 。 (1)当放入NH4HS时容器中已有39.99kPa 的 H2S(g),求平衡时容器内的压力;(2)容器中已有6.666kPa的NH3(g),问需加多大压力的H2S(g),才能形成NH4HS 固体。 1)77.7kPa 2)P(H2S)大于166kPa。
4、已知250C时φ0(Fe3+/ Fe) =-0.036V,φ0(Fe3+/ Fe2+) =-0.770V 求250C时电极Fe2+|Fe的标准电极电势φ0(Fe2+/ Fe)。 答案: φ0(Fe2+/ Fe)= -0.439V 5、0.01mol dm-3醋酸水溶液在250C时的摩尔电导率为1.62×10-3S m2 mol–1,无限稀释时的摩尔电导率为39.07×10-3S m2 mol–1 计算(1)醋酸水溶液在250C,0.01mol dm-3
第二章 热力学第一定律 思考题.:1. 一封闭系统,当始终态确定后:(a )当经历一个绝热过程,则功为定值;(b )若经历一个等容过程,则Q 有定值:(c )若经历一个等温过程,则热力学能有定值:(d )若经历一个多方过程,则热和功的和有定值。 解释:始终态确定时,则状态函数的变化值可以确定,非状态函数则不是确定的。但是热力学能U 和焓没有绝对值,只有相对值,比较的主要是变化量。 2. 从同一始态A 出发,经历三种不同途径到达不同的终态: (1)经等温可逆过程从A→B;(2)经绝热可逆过程从A→C;(3)经绝热不可逆过程从A→D。 试问: (a )若使终态的体积相同,D 点应位于BC 虚线的什么位置,为什么? (b )若使终态的压力相同,D 点应位于BC 虚线的什么位置,为什么,参见图 12p p (a) (b) 图 2.16 解释: 从同一始态出发经一绝热可逆膨胀过程和一经绝热不可逆膨胀过程,当到达相同的 终态体积V 2或相同的终态压力p 2时,绝热可逆过程比绝热不可逆过程作功大,又因为W (绝热)=C V (T 2-T 1),所以T 2(绝热不可逆)大于T 2(绝热可逆),在V 2相同时,p=nRT/V,则p 2(绝热不可逆)大于 p 2(绝热可逆)。在终态p 2相同时,V =nRT/p ,V 2(绝热不可逆)大于 V 2(绝热可逆)。 不可逆过程与等温可逆过程相比较:由于等温可逆过程温度不变,绝热膨胀温度下降,所以T 2(等温可逆)大于T 2(绝热不可逆);在V 2相同时, p 2(等温可逆)大于 p 2(绝热不可逆)。在p 2相同时,V 2(等温可逆)大于 V 2(绝热不可逆)。 综上所述,从同一始态出发经三种不同过程, 当V 2相同时,D 点在B 、C 之间,p 2(等温可逆)>p 2(绝热不可逆)> p 2(绝热可逆)当p 2相同时,D 点在B 、C 之间,V 2(等温可逆)> V 2(绝热不可逆)>V 2(绝热可逆)。 总结可知:主要切入点在温度T 上,绝热不可逆做功最小。
大学生物化学考试题库 附有答案 Pleasure Group Office【T985AB-B866SYT-B182C-BS682T-STT18】
蛋白质的二级结构内含子酶的活性部位氧化磷酸化基因组核酸的变性高能化合物反转录新陈代谢酶原的激活pI Tm 米氏常数Glycolysis β-氧化、蛋白质的四级结构增色效应米氏常数 PCR 1、蛋白质在一个较宽的生理pH范围内具有缓冲能力,是因为() A、它们是相对分子量很大的分子 B、它们含有许多具有不同pKa值的功能基团 C、它们含有许多肽键,而肽键对于体内的H+和OH-是不敏感的 D、它们含有许多氢键 2、下述氨基酸中,()与茚三酮作用呈黄色斑点 A、组氨酸 B、苏氨酸 C、脯氨酸 D、精氨酸 3、在生理pH条件下,下述三肽在水中的溶解度最大的是() A、Asp-Ser-His B、Ala-Asn-Phe C、Ala-Ile-Phe D、Ala-Ser-His 4、下列关于双螺旋DNA的结构与性质的有关叙述,除()外都是正确的 A、A/T = G/C B、AT含量为35%的DNA解链温度高于AT含量为65%的DNA C、当DNA复性时,紫外吸收值增高 D、温度升高是导致DNA变性的因素之一 5、酶能加快化学反应速度是由于下述哪种原因所致() A、增高活化能 B、降低活化能 C、降低反应物能量水平 D、降低反应的自由能 6、E. coli DNA复制涉及除()之外的哪些蛋白质 A、DNA聚合酶 B、RNA聚合酶 C、DNA解链蛋白 D、DNA旋转酶
7、下述DNA分子中,除()外都具有双链结构 A、E. coli DNA B、质粒DNA C、噬菌体X174 DNA D、线粒体DNA 8、在采用链终止法测定DNA顺序时,为了获得以腺苷酸残基为末端的一组大小不同的片段,应该采用哪种双脱氧类似物() A、5’-ddATP B、5’-ddCTP C、5’-ddGTP D、5’-ddTTP 9、催化单底物反应的酶的米氏常数(Km)是()无答案 A、底物和酶之间的反应的平衡常数 B、给出最大反应速度的底物浓度 C、给出最大半反应速度的底物浓度 C、大致与酶催化反应的速度成比例 10、在下列转录抑制剂中,能对真核生物和原核生物的转录都有作用的是() A、放线菌素D B、利福平 C、利链菌素 D、a-鹅膏蕈碱 11、下列氨基酸中,在水中溶解度最低的是() A、组氨酸 B、赖氨酸 C、亮氨酸 D、苏氨酸 12、X174噬菌体基因组的大小不足以编码它的九种不同的蛋白质,但它实际 编码了这些蛋白质。这是下述哪种原因所致() A、密码子的简并性 B、密码子重叠 C、基因重叠 D、密码子的摆动性 13、下述RNA在细胞内的含量最高的是() A、tRNA B、rRNA C、mRNA D、hnRNA 14、用于肌肉收缩的能量主要以哪种形式贮存在组织中() A、磷酸肌酸 B、磷酸精氨酸 C、ATP D、磷酸烯醇式丙酮酸 15、在DNA复制与DNA修复中共同出现的酶是() A、DNA连接酶 B、RNA聚合酶 C、DNA内切酶 D、RNA外切酶
物理化学期末考试试题(1)
《物理化学》上册期末试卷本卷共 8 页第1页 《物理化学》上册期末试卷本卷共 8 页第2页 化学专业《物理化学》上册期末考试试卷(1)(时间120分钟) 一、单 项选择题(每小题2分,共30分) 1、对于内能是体系状态的单值函数概念,错误理解是( ) A 体系处于一定的状态,具有一定的内能 B 对应于某一状态,内能只能有一数值不能有两个以上的数值 C 状态发生变化,内能也一定跟着变化 D 对应于一个内能值,可以有多个状态 2、在一个绝热刚瓶中,发生一个放热的分子数增加的化学反应,那么( ) A Q > 0,W > 0,?U > 0 B Q = 0,W = 0,?U < 0 C Q = 0,W = 0,?U = 0 D Q < 0,W > 0,?U < 0 3、一种实际气体,其状态方程为PVm=RT+αP (α<0),该气体经节流膨胀后,温度将( ) A 、升高 B 、下降 C 、不变 D 、不能确定 4、在隔离体系中发生一个自发过程,则ΔG 应为( ) A. ΔG < 0 B. ΔG > 0 C. ΔG =0 D. 不能确定 5、理想气体在绝热条件下,在恒外压下被压缩到终态,则体系与环境的熵变( ) A 、ΔS 体>0 ΔS 环>0 B 、ΔS 体<0 ΔS 环<0 C 、ΔS 体>0 ΔS 环<0 D 、ΔS 体>0 ΔS 环=0 6、下面哪组热力学性质的配分函数表达式与体系中粒子的可别与否 无关( ) (A ). S 、G 、F 、C V (B) U 、H 、P 、C V (C) G 、F 、H 、U (D) S 、U 、H 、G 7、在N 个独立可别粒子组成体系中,最可几分布的微观状态数t m 与配分函数q 之间的关系为 ( ) (A) t m = 1/N ! ·q N (B) t m = 1/N ! ·q N ·e U /kT (C) t m = q N ·e U /kT (D) t m = N ! q N ·e U /kT 8、挥发性溶质溶于溶剂形成的稀溶液,溶液的沸点会( ) A 、降低 B 、升高 C 、不变 D 、可能升高或降低 9、盐碱地的农作物长势不良,甚至枯萎,其主要原因是( ) A 、天气太热 B 、很少下雨 C 、水分倒流 D 、肥料不足 10、在恒温密封容器中有A 、B 两杯稀盐水溶液,盐的浓度分别为c A 和c B (c A > c B ),放置足够长的时间后( ) (A) A 杯盐的浓度降低,B 杯盐的浓度增加 ; (B) A 杯液体量减少,B 杯液体量增加 ; (C) A 杯盐的浓度增加,B 杯盐的浓度降低 ; (D) A 、B 两杯中盐的浓度会同时增大 。 11、298K 、101.325kPa 下,将50ml 与100ml 浓度均为1mol·dm -3 萘的苯溶液混合,混合液的化学势μ为:( ) (A) μ = μ1 + μ2 ; (B) μ = μ1 + 2μ2 ; (C) μ = μ1 = μ2 ; (D) μ = ?μ1 + ?μ2 。 12、硫酸与水可组成三种化合物:H 2SO 4·H 2O (s )、H 2SO 4·2H 2O (s )、H 2SO 4·4H 2O (s ),在P θ 下,能与硫酸水溶液共存的化合物最多有几种( ) A 、1种 B 、2种 C 、3种 D 、4种 13、A 与B 可以构成2种稳定化合物与1种不稳定化合物,那么A 与B 的体系 可以形成几种低共熔混合物( ) A 、5种 B 、4种 C 、3种 D 、2种 14、对反应CO(g)+H 2O(g)=H 2(g)+CO 2(g) ( ) (A) K p $=1 (B) K p $=K c (C) K p $>K c (D) K p $ <K c 15、 一定温度下,一定量的 PCl 5(g)在某种条件下的解离度为α,改变下列条件, 何者可使α增大?( ) 题号 一 二 三 四 五 六 七 八 得 分 得分 得分 评卷人 复核人 学院: 年级/班级: 姓名: 学号: 装 订 线 内 不 要 答 题
物理化学试卷(A ) 41. 5 分 (6698) 有一吹肥皂泡装置,下端连有一个一端通大气的 U 型水柱压力计,当肥皂泡的直径是 5×10-3 m 时,压力计水柱高度差为 2×10-3 m ,试计算该肥皂液在直径为 1×10-4 m 的毛细管中的升高值。设皂液对毛细管壁完全润湿,且密度与水相同。 41. 5 分 (6698) [答] p s = 2×2γ /R ' = ρgh γ = 0.01225 N ·m -1 (3分) h = 2γ cos θ /ρgR 2= 0.05 m (2分) 135. 5 分 (7035) 在298.15 K 时,苯蒸气在石墨上吸附服从Langmuir 吸附等温式。当苯蒸气压力为760 Pa 时,石墨表面覆盖率θ=0.5,求苯蒸气在石墨表面上的吸附系数a 。 135. 5 分 (7035) [答] 1ap ap θ= + 将θ=0.5 p =760 Pa 代入解得a =0.001 315 Pa -1 (5分) 7. 10 分 (4813) 298 K 时, 以Pt 为阳极, Fe 为阴极, 电解浓度为1 mol ·kg -1的NaCl 水溶液(活度系数为 0.66)。 设电极表面有H 2(g)不断逸出时的电流密度为0.1A ·cm -2, Pt 上逸出Cl 2(g)的超电势可近似看作零。 若Tafel 公式为 η =a+blg(j /1A ·cm -2), 且Tafel 常数 a=0.73 V, b=0.11V , φ ? (Cl 2/Cl -)=1.36 V ,请计算实际的分解电压。 7. 10 分 (4813) [答] E 理论 =φ +-φ -=[φ ? (Cl 2/Cl -)-RT F ln α (Cl -)]-[(φ? (H +/H 2)+RT F ln α (H +)) =1.36 - 0.01 - 8314298 96500 .?ln10-7 =1.76 V (3分) η阴= a + b lg j =0.73+0.11× lg0.1 =0.62 V (2分) η阳=0 (2分) E 分解 =E 理论+η阴+η阳=2.38 V (3分) 213. 10 分 (4710) 有电池Hg(l)|Hg 22+(a 1)||Hg 22+(a 1),Hg 2+(a 2)|Pt 。 (1) 写出电池反应式; (2) 计算电池的标准电动势。已知2+2Hg |Hg(l)和Hg 2+ |Hg(l)的标准电极电势分别为0.798 V 和0.854 V 。 (3) 求电池反应的平衡常数。 213. 10 分 (4710) (1) Hg(l)+Hg 2+(a 2)→Hg 22+(a 1) (3分) (2) E ? = E ? (Hg 2+|Hg 22+) –E ? (Hg 22+|Hg) E ? (Hg 2+|Hg 22+) = 2E ? (Hg 2+|Hg) –E ? (Hg 22+|Hg)=(2×0.854 – 0.798) V= 0.910 V
第二章热力学第一定律 1.热力学第一定律ΔU=Q+W 只适用于 (A) 单纯状态变化 (B) 相变化 (C) 化学变化 (D) 封闭物系的任何变化 答案:D 2.关于热和功, 下面的说法中, 不正确的是 (A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上 (B) 只有在封闭系统发生的过程中, 功和热才有明确的意义 (C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量 (D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消 答案:B 3.关于焓的性质, 下列说法中正确的是 (A) 焓是系统内含的热能, 所以常称它为热焓 (B) 焓是能量, 它遵守热力学第一定律 (C) 系统的焓值等于内能加体积功 (D) 焓的增量只与系统的始末态有关 答案:D。因焓是状态函数。 4.涉及焓的下列说法中正确的是 (A) 单质的焓值均等于零 (B) 在等温过程中焓变为零 (C) 在绝热可逆过程中焓变为零 (D) 化学反应中系统的焓变不一定大于内能变化 答案:D。因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0 则ΔH<ΔU。 5.下列哪个封闭体系的内能和焓仅是温度的函数 (A) 理想溶液 (B) 稀溶液 (C) 所有气体 (D) 理想气体 答案:D 6.与物质的生成热有关的下列表述中不正确的是 (A) 标准状态下单质的生成热都规定为零 (B) 化合物的生成热一定不为零 (C) 很多物质的生成热都不能用实验直接测量 (D) 通常所使用的物质的标准生成热数据实际上都是相对值 答案:A。按规定,标准态下最稳定单质的生成热为零。 7.dU=CvdT 及dUm=Cv,mdT 适用的条件完整地说应当是 (A) 等容过程 (B)无化学反应和相变的等容过程 (C) 组成不变的均相系统的等容过程 (D) 无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能 只与温度有关的非等容过程 答案:D 8.下列过程中, 系统内能变化不为零的是 (A) 不可逆循环过程 (B) 可逆循环过程 (C) 两种理想气体的混合过程 (D) 纯液体的真空蒸发过程 答案:D。因液体分子与气体分子之间的相互作用力是不同的故内能不同。另外,向真 空蒸发是不做功的,W=0,故由热力学第一定律ΔU=Q+W 得ΔU=Q,蒸发过程需吸热Q>0,
第一章 气体pVT 性质 1-1物质的体膨胀系数V α与等温压缩系数T κ的定义如下: 1 1T T p V p V V T V V ???? ????-=??? ????= κα 试导出理想气体的V α、T κ与压力、温度的关系? 解:对于理想气体,pV=nRT 111 )/(11-=?=?=??? ????=??? ????= T T V V p nR V T p nRT V T V V p p V α 1211 )/(11-=?=?=???? ????-=???? ????- =p p V V p nRT V p p nRT V p V V T T T κ 1-2 气柜内有121.6kPa 、27℃的氯乙烯(C 2H 3Cl )气体300m 3,若以每小时90kg 的流量输往使用车间,试问贮存的气体能用多少小时? 解:设氯乙烯为理想气体,气柜内氯乙烯的物质的量为 mol RT pV n 623.1461815 .300314.8300 106.1213=???== 每小时90kg 的流量折合p 摩尔数为 13 3153.144145 .621090109032-?=?=?=h mol M v Cl H C n/v=(14618.623÷1441.153)=10.144小时 1-3 0℃、101.325kPa 的条件常称为气体的标准状况。试求甲烷在标准状况下的密度。 解:33 714.015 .273314.81016101325444 --?=???=?=?=m kg M RT p M V n CH CH CH ρ 1-4 一抽成真空的球形容器,质量为25.0000g 。充以4℃水之后,总质量为125.0000g 。若改用充以25℃、13.33kPa 的某碳氢化合物气体,则总质量为25.0163g 。试估算该气体的摩尔质量。 解:先求容器的容积33) (0000.1001 0000.100000.250000.1252 cm cm V l O H ==-=ρ
《物理化学》练习题 一、填空题 1. 理想气体经过节流膨胀后,焓____(升高,降低,不变)。 2. ()0T dH dV =,说明焓只能是温度的函数,与_____无关。 3. 1molH 2(g )的燃烧焓等于1mol_______的生成焓。 4. 物理量Q 、T 、V 、W ,其中属于状态函数的是 ;与过程有关的量是 ;状态函数中属于广度量 的是 ;属于强度量的是 。 5. 焦耳汤姆逊系数J-T μ= ,J-T 0μ>表示节流膨胀后温度 节流膨胀前温度。 6. V Q U =?的应用条件是 。 7. 热力学第二定律可表达为:“功可全部变为热,但热不能全部变为功而 。 8. 用ΔG ≤0判断过程的方向和限度的条件是_________。 9. 热力学第三定律的表述为 。 10. 写出热力学基本方程d G = 。 11. 卡诺热机在T 1=600K 的高温热源和T 2=300K 的低温热源间工作,其热机效率η=___。 12. 高温热源温度T 1=600K ,低温热源温度T 2=300K 。今有120KJ 的热直接从高温热源传给低温热源,此 过程ΔS =________。 13. 1mol 理想气体由298K ,100kpa 作等温可逆膨胀,若过程ΔG =-2983J ,则终态压力为 。 14. 25°C 时,0.5molA 与0.5molB 形成理想液态混合物,则混合过程的ΔS= 。 15. 一定量的理想气体经历某种过程变化到终态,若变化过程中 pV γ不变,则状态函数(ΔS 、ΔH 、ΔU 、ΔG 、ΔA )中, 不变。 16. 在一定的温度及压力下,溶液中任一组分在任意浓度范围均遵守拉乌尔定律的溶液称为___________。 17. 25°C 时,10g 某溶质溶于1dm 3溶剂中,测出该溶液的渗透压Π=0.4000kpa ,该溶质的相对分子质量 为________ 18. 氧气和乙炔气溶于水中的享利系数分别是717.2010Pa kg mol -???和 811.3310Pa kg mol -???,由享利定律系数可知,在相同条件下, 在水中的溶解度大 于 在水中的溶解度。 19. 28.15℃时,摩尔分数0.287x =丙酮 的氯仿-丙酮溶液的蒸气压为29.40kPa ,饱和蒸气中氯仿的摩尔分数为0.287x =氯仿。已知纯氯仿在该温度时的蒸气压为29.57kPa 。以同温度下纯氯仿为标准态, 氯仿在该溶液中的活度因子为 ;活度为 。 20. 混合理想气体中组分B 的化学势B μ与温度T 及组分B 的分压p B 的关系是B μ= ,其标准态选为 。 21. 吉布斯-杜亥姆方程的表达式为 。 22. 液体饱和蒸气压的定义是 。 23. 苯的标准沸点是80.1℃,则在80.1℃时苯的饱和蒸气压是为 Pa 。 24. 纯物质两相平衡的条件是 。
第十章界面现象 10-1 请回答下列问题: (1) 常见的亚稳定状态有哪些?为什么产生亚稳态?如何防止亚稳态的产生? (2) 在一个封闭的钟罩内,有大小不等的两个球形液滴,问长时间放置后,会出现什么现象? (3) 下雨时,液滴落在水面上形成一个大气泡,试说明气泡的形状和理由? (4) 物理吸附与化学吸附最本质的区别是什么? (5) 在一定温度、压力下,为什么物理吸附都是放热过程? 答:(1) 常见的亚稳态有:过饱和蒸汽、过热液体、过冷液体、过饱和溶液。产生这些状态的原因就是新相难以生成,要想防止这些亚稳状态的产生,只需向体系中预先加入新相的种子。 (2) 一断时间后,大液滴会越来越大,小液滴会越来越小,最终大液滴将小液滴“吃掉”,根据开尔文公式,对于半径大于零的小液滴而言,半径愈小,相对应的饱和蒸汽压愈大,反之亦然,所以当大液滴蒸发达到饱和时,小液滴仍未达到饱和,继续蒸发,所以液滴会愈来愈小,而蒸汽会在大液滴上凝结,最终出现“大的愈大,小的愈小”的情况。 (3) 气泡为半球形,因为雨滴在降落的过程中,可以看作是恒温恒压过程,为了达到稳定状态而存在,小气泡就会使表面吉布斯函数处于最低,而此时只有通过减小表面积达到,球形的表面积最小,所以最终呈现为球形。 (4) 最本质区别是分子之间的作用力不同。物理吸附是固体表面分子与气体分子间的作用力为范德华力,而化学吸附是固体表面分子与气体分子的作用力为化学键。 (5) 由于物理吸附过程是自发进行的,所以ΔG<0,而ΔS<0,由ΔG=ΔH-TΔS,得 ΔH<0,即反应为放热反应。
10-2 在293.15K 及101.325kPa 下,把半径为1×10-3m 的汞滴分散成半径为1×10-9m 的汞滴,试求此过程系统表面吉布斯函数变(ΔG )为多少?已知293.15K 时汞的表面张力为0.4865 N ·m -1。 解: 3143r π=N×3243r π N =3 132 r r ΔG =2 1 A A dA γ?= (A 2-A 1)=4·( N 2 2 r -21 r )=4 ·(3 12 r r -21r ) =4× ×(339 (110)110 --??-10-6) =5.9062 J 10-3 计算时373.15K 时,下列情况下弯曲液面承受的附加压力。已知时水的表面张力为58.91×10-3 N ·m -1 (1) 水中存在的半径为0.1μm 的小气泡;kPa (2) 空气中存在的半径为0.1μm 的小液滴; (3) 空气中存在的半径为0.1μm 的小气泡; 解:(1) Δp =2r γ=36 258.91100.110--???=1.178×103 kPa (2) Δp =2r γ =36 258.91100.110--???=1.178×103 kPa (3) Δp =4r γ=36 458.91100.110--???=2.356×103 kPa 10-4 在293.15K 时,将直径为0.1nm 的玻璃毛细管插入乙醇中。问需要在管内加多大的压力才能防止液面上升?若不加压力,平衡后毛细管内液面的高度为多少?已知该温度下乙醇的表面张力为22.3×10-3 N ·m -1,密度为789.4 kg ·m -3,重力加速度为9.8 m ·s -2。设乙醇能很好地润湿玻璃。
物理化学 试卷一 一、选择题 ( 共15题 30分 ) 1. 下列诸过程可应用公式 dU = (Cp- nR)dT进行计算的是: ( C ) (A) 实际气体等压可逆冷却 (B) 恒容搅拌某液体以升高温度 (C) 理想气体绝热可逆膨胀 (D) 量热弹中的燃烧过程 2. 理想气体经可逆与不可逆两种绝热过程: ( B ) (A) 可以从同一始态出发达到同一终态因为绝热可逆ΔS = 0 (B) 从同一始态出发,不可能达到同一终态绝热不可逆S > 0 (C) 不能断定 (A)、(B) 中哪一种正确所以状态函数 S 不同 (D) 可以达到同一终态,视绝热膨胀还是绝热压缩而定故终态不能相同 3. 理想气体等温过程的ΔF。 ( C ) (A)>ΔG (B) <ΔG (C) =ΔG (D) 不能确定 4. 下列函数中为强度性质的是: ( C ) (A) S (B) (G/p)T (C) (U/V)T 容量性质除以容量性质为强度性质 (D) CV 5. 273 K,10p下,液态水和固态水(即冰)的化学势分别为μ(l) 和μ(s),两者的关系为:( C ) (A) μ(l) >μ(s) (B) μ(l) = μ(s) (C) μ(l) < μ(s) (D) 不能确定
6. 在恒温抽空的玻璃罩中封入两杯液面相同的糖水 (A) 和纯水 (B)。经历若干
时间后,两杯液面的高度将是(μ(纯水)>μ(糖水中水) ,水从(B) 杯向(A) 杯转移 ) ( A ) (A) A 杯高于 B 杯 (B) A 杯等于 B 杯 (C) A 杯低于 B 杯 (D) 视温度而定 7. 在通常情况下,对于二组分物系能平衡共存的最多相为: ( D ) (A) 1 (B) 2 (C) 3 (D) 4 * Φ=C+2-f=2+2-0=4 8. 硫酸与水可形成H2SO4·H2O(s)、H2SO4·2H2O(s)、H2SO4·4H2O(s)三种水合物,问在 101325 Pa 的压力下,能与硫酸水溶液及冰平衡共存的硫酸水合物最多可有多少种? ( C ) (A) 3 种 (B) 2 种 (C) 1 种 (D) 不可能有硫酸水合物与之平衡共存。 * S = 5 , R = 3 , R' = 0,C= 5 - 3 = 2 f*= 2 -Φ+ 1 = 0, 最大的Φ= 3 , 除去硫酸水溶液与冰还可有一种硫酸水含物与之共存。 9. 已知 A 和 B 可构成固溶体,在 A 中,若加入 B 可使 A 的熔点提高,则B 在此固溶体中的含量必 _______ B 在液相中的含量。 ( A ) (A) 大于 (B) 小于 (C) 等于 (D)不能确定 10. 已知反应 2NH3= N2+ 3H2在等温条件下,标准平衡常数为 0.25,那么,在此条件下,氨的合成反应 (1/2) N2+(3/2) H2= NH3 的标准平衡常数为: ( C ) (A) 4 (B) 0.5 (C) 2 K (D) 1 * $p(2) = [K $p(1)]= (0.25)= 2 11. 若 298 K 时,反应 N2O4(g) = 2NO2(g) 的 K $p= 0.1132,则: (1) 当 p (N2O4) = p (NO2) = 1 kPa 时,反应将 _____( B )_____; (2) 当 p (N2O4) = 10 kPa,p (NO2) = 1 kPa 时,反应将 ____( A )____ 。
气体pVT 性质 1. 1-1物质的体膨胀系数V α与等温压缩系数T κ的定义如下: 试导出理想气体的V α、T κ与压力、温度的关系? 解:对于理想气体,pV=nRT 1-2 气柜内有121.6kPa 、27℃的氯乙烯(C 2H 3Cl )气体300m 3,若以每 小时90kg 的流量输往使用车间,试问贮存的气体能用多少小时? 解:设氯乙烯为理想气体,气柜内氯乙烯的物质的量为 每小时90kg 的流量折合p 摩尔数为 133153.144145 .621090109032-?=?=?=h mol M v Cl H C n/v=(14618.623÷1441.153)=10.144小时 1-3 0℃、101.325kPa 的条件常称为气体的标准状况。试求甲烷在标准状况下的密度。 解:33714.015 .273314.81016101325444--?=???=?=?=m kg M RT p M V n CH CH CH ρ 1-4 一抽成真空的球形容器,质量为25.0000g 。充以4℃水之后,总质量为125.0000g 。若改用充以25℃、13.33kPa 的某碳氢化合物气体,则总质量为25.0163g 。试估算该气体的摩尔质量。 解:先求容器的容积33)(0000.1001 0000.100000.250000.1252cm cm V l O H ==-=ρ n=m/M=pV/RT 1-5 两个体积均为V 的玻璃球泡之间用细管连接,泡内密封着标准状况条件下的空气。若将其中一个球加热到100℃,另一个球则维持0℃,忽略连接管中气体体积,试求该容器内空气的压力。
解:方法一:在题目所给出的条件下,气体的量不变。并且设玻璃泡的体积不随温度而变化,则始态为 )/(2,2,1i i i i RT V p n n n =+= 终态(f )时 ??? ? ??+=???? ??+=+=f f f f f f f f f f T T T T R V p T V T V R p n n n ,2,1,1,2,2,1,2,1 1-6 0℃时氯甲烷(CH 3Cl )气体的密度ρ随压力的变化如下。试作ρ/p —p 图,用外推法求氯甲烷的相对分子质量。 解:将数据处理如下: P/kPa 101.325 67.550 50.663 33.775 25.331 (ρ/p)/ (g ·dm -3·kPa ) 0.02277 0.02260 0.02250 0.02242 0.02237 作(ρ/p)对p 图 当p →0时,(ρ/p)=0.02225,则氯甲烷的相对分子质量为 1-7 今有20℃的乙烷-丁烷混合气体,充入一抽真空的200 cm 3容器中,直至压力达101.325kPa ,测得容器中混合气体的质量为0.3879g 。试求该混合气体中两种组分的摩尔分数及分压力。 解:设A 为乙烷,B 为丁烷。 B A B B A A y y mol g M y M y n m M 123.580694.30 867.46008315 .03897.01+=?==+==- (1) 1=+B A y y (2) 联立方程(1)与(2)求解得401.0,599.0==B B y y
一 化学热力学基础 1-1 判断题 1、可逆的化学反应就是可逆过程。(×) 2、Q 和W 不是体系的性质,与过程有关,所以Q+W 也由过程决定。(×) 3、焓的定义式H=U+pV 是在定压条件下推导出来的,所以只有定压过程才有焓变。(×) 4、焓的增加量ΔH 等于该过程中体系从环境吸收的热量。(×) 5、一个绝热过程Q=0,但体系的ΔT 不一定为零。(√) 6、对于一个定量的理想气体,温度一定,热力学能和焓也随之确定。(√) 7、某理想气体从始态经定温和定容两个过程达终态,这两个过程Q 、W 、ΔU 及ΔH 是相等的。(×) 8、任何物质的熵值是不可能为负值或零的。(×) 9、功可以全部转化为热,但热不能全部转化为功。(×) 10、不可逆过程的熵变是不可求的。(×) 11、任意过程中的热效应与温度相除,可以得到该过程的熵变。(×) 12、在孤立体系中,一自发过程由A B,但体系永远回不到原来状态。(√) 13、绝热过程Q=0,而T Q dS δ= ,所以dS=0。(×) 14、可以用一过程的熵变与热温商的大小关系判断其自发性。(√)
15、绝热过程Q=0,而ΔH=Q ,因此ΔH=0。(×) 16、按克劳修斯不等式,热是不可能从低温热源传给高温热源的。(×) 17、在一绝热体系中,水向真空蒸发为水蒸气(以水和水蒸气为体系),该过程W>0,ΔU>0。(×) 18、体系经过一不可逆循环过程,其体S ?>0。(×) 19、对于气态物质,C p -C V =nR 。(×) 20、在一绝热体系中有一隔板,两边分别是空气和真空,抽去隔板,空气向真空膨胀,此时Q=0,所以ΔS=0。(×) 21、高温物体所含的热量比低温物体的多,因此热从高温物体自动流向低温物体。(×) 22、处于两相平衡的1molH 2O (l )和1molH 2O (g ),由于两相物质的温度和压力相等,因此在相变过程中ΔU=0,ΔH=0。(×) 23、在标准压力下加热某物质,温度由T 1上升到T 2,则该物质吸收的 热量为?=21 T T p dT C Q ,在此条件下应存在ΔH=Q 的关系。 (√) 24、带有绝热活塞(无摩擦、无质量)的一个绝热气缸装有理想气体,内壁有电炉丝,将电阻丝通电后,气体慢慢膨胀。因为是一个恒压过程Q p =ΔH ,又因为是绝热体系Q p =0,所以ΔH=0。(×) 25、体系从状态I 变化到状态Ⅱ,若ΔT=0,则Q=0,无热量交换。(×) 26、公式Vdp SdT dG +-=只适用于可逆过程。 ( × ) 27、某一体系达到平衡时,熵最大,自由能最小。
大学《物理化学》下学期试题及答案2009-2010学年物理化学(下)复习讲义 【电化学纲要】 一、重要概念 阳极、阴极,正极、负极,原电池,电解池,电导,比电导,(无限稀释时)摩尔电导 率,迁移数,可逆电池,电池的电动势,电池反应的写法,分解电压,标准电极电位、电极 的类型、析出电位,电极极化,过电位,电极反应的次序二、重要定律与公式 1.电解质部分 (1)法拉第定律: (2)电导,电导率,摩尔电导率,摩尔电导率与浓度关系:稀的强电解质(3)离子独立定律:无限稀释溶液,电解质(4)电导应用: i. 计算弱电解质的解离度和解离常数 ii. 计算难溶盐的溶解度 (5)平均活度及活度系数:电解质 (6)德拜-许克尔公式: 2. 原电池 (1)热力学 G= -zFE S= -(,G/, T)
= zF (, E/, T) pp H = G + T S = -zFE +zFT (, E/, T) p Q = T S =zFT (, E/, T) irp (2)能斯特方程 G =zFE= -RTlnK rm (3)电极电势,电池的电动势 E = E- E,电池的写法, + -三、关键的计算题类型 1.电解质溶液部分 由摩尔电导率计算解离率和解离平衡常数相关的题型。 2.给出电池,写出电极反应及计算电池反应热力学基本函数。这一类型相对容易。 3.给出反应,设计电池并计算电池反应热力学基本函数。 4.给出二个反应的基本量或若干个电极的电极电池,求相关反应的电动势或热力学量。这类题比较综合。 【化学动力学纲要】 一、主要概念 反应速率,依时计量学反应,(非依时计量学反应,)消耗速率,生成速率,基元反应,非基元反应,质量作用定律,级数,总级数,(基元反应的)反应分子数,速率方程,半衰
一章气体的pVT关系 1.1 物质的体膨胀系数与等温压缩率的定义如下 试推出理想气体的,与压力、温度的关系。 解:根据理想气体方程 1.2 气柜内贮有121.6 kPa,27℃的氯乙烯(C2H3Cl)气体300 m3,若以每小时90 kg的流量输往使用车间,试问贮存的气体能用多少小时? 解:假设气柜内所贮存的气体可全部送往使用车间。 1.3 0℃,101.325kPa的条件常称为气体的标准状况,试求甲烷在标准状况下的密度? 解:将甲烷(M w=16g/mol)看成理想气体: PV=nRT , PV =mRT/ M w 甲烷在标准状况下的密度为=m/V= PM w/RT =101.32516/8.314273.15(kg/m3) =0.714 kg/m3 1.4 一抽成真空的球形容器,质量为25.0000g充以4℃水之后,总质量为125.0000g。若改充以25℃,13.33 kPa的某碳氢化合物气体,则总质量为 25.0163g。试估算该气体的摩尔质量。水的密度1g·cm3计算。 解:球形容器的体积为V=(125-25)g/1 g.cm-3=100 cm3 将某碳氢化合物看成理想气体:PV=nRT , PV =mRT/ M w M w= mRT/ PV=(25.0163-25.0000)8.314300.15/(1333010010-6) M w =30.51(g/mol)
1.5 两个容积均为V 的玻璃球泡之间用细管连结,泡内密封着标准状态下的空气。若将其中的一个球加热到 100℃,另一个球则维持 0℃,忽略连接细管中气体体积,试求该容器内空气的压力。 解:由题给条件知,(1)系统物质总量恒定;(2)两球中压力维持相同。 标准状态: 因此, 1.6 0℃时氯甲烷(CH 3Cl )气体的密度ρ随压力的变化如下。试作p p -ρ 图,用外推法求氯甲烷的相对 分子质量。