
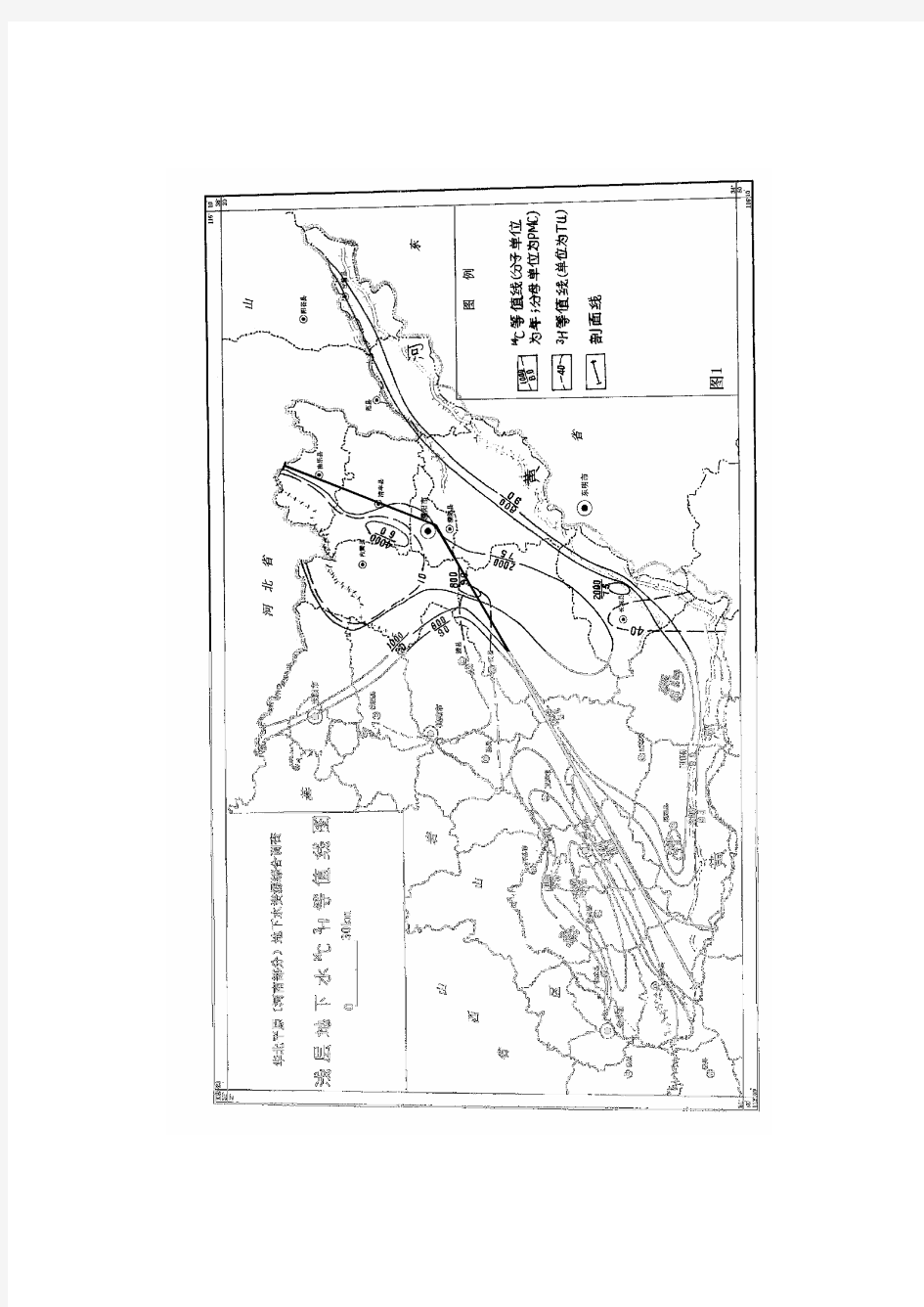
14C同位素技术在豫北平原地下水资源调查评价方面的应用
赵云章 仝长水 吴继臣 苗晋祥
(河南省地质调查院 郑州 450007)
摘 要: 地下水中14C的年代与pmc (与大气中现代碳的百分含量之比)值的大小反映了地下水的补给、迳流、排泄的状况与循环条件。豫北平原地下水中的14C的年代与pmc值反映出:引黄灌区主干渠、山前冲洪积扇、近黄河地带为地下水强补给与径流带,地下水14C年龄较小,地下水循环交替的快;在交接洼地、微咸水区、地下水位下降漏斗区,地下水流滞缓,地下水14C年龄较大,地下水循环交替的慢。其它资料也验证了此规律。
关键词:14C同位素 地下水 应用
1 引言
华北平原(河南部分)地下水调查评价是中国地质调查局下达的任务,为了完成该项任务,查清地下水的补迳排条件,在该项目设计中部署了同位素分析样50件。
工作区地处黄河冲积平原的上游,西北部为山前倾斜平原,工作区地下水主要赋存于第四系多层交叠的各种砂及粉土的孔隙中,是一个形状复杂的含水地质体。在平面上可以分为山前倾斜平原含水层系统与黄河冲积平原含水层系统;在垂向上可划分为浅层含水层系统与深层含水层系统。从水文地质和同位素资料来看,各含水层系统之间有着密切的联系。
样品采集严格按规程进行,对不符合要求的样品已进行了补样,分析单位为地质矿产部环境地质开放研究实验室,采样按不同水文地质、不同层位、地表水分别布置了样品,基本控制了全区。
2 14C同位素技术在豫北平原地下水资源调查评价方面的应用
2.1 利用14C资料圈定地下水补给区与强径流带、判断地下水循环交替的快慢
工作区14C、3H的资料整理分析成果见图1、图2。从图上可知,浅层地下水从补给源向下游、从山前到平原、从黄河向北14C年龄逐渐变大,pmc值逐渐变小。这种现象反映了地下水的循环条件,同位素等值线与地下水等水位线非常吻合。第一、在人民胜利渠、武嘉灌渠从上游到下游出现低年龄段水,pmc值为100,属现代碳,地下水等水位线图呈外凸形,此区地下水力坡度大,为地下水补给与强迳流带,水循环交替快;第二、在山前冲洪积扇、近黄河地带地下水年龄较低,pmc值为80至90,水力坡度大,水循环交替快;第三、在交
赵云章(1957—),男,汉族,河南省获嘉人,教授级高级工程师。1982年毕业于长春地质学院水工系,地质工程硕士,长期从事水工环工作。
接洼地、背河洼地的局部地段,山前的地下水从西北向东南流动,沿黄河地带的地下水由西南向东北流动,两个方向上的地下水在此交汇,地下水14C年龄较大,pmc值小于75,地下水迳流滞缓,水循环交替慢,该区为咸水分布区;第四、在地下水水位下降漏斗的中心地带, 地下水14C年龄较大,pmc值小于60,反映水循环交替较快,有部分深层水越流混合到浅层水漏斗中。证明浅层地下水补给量远低于现状开采量,致使地下水位持续下降。第五、根据以上证据,14C年龄<1000年,pmc值为大于80的区域为地下水强补给带与强径流带;14C年龄>2000年,pmc值小于75的区域为咸水区和地下水位下降漏斗区;在内黄、清丰与南乐地下水位下降漏斗区3H<10TU,也佐证了此种现象。第六、根据以上五条内容,利用14C资料可以判断地下水污染情况、划分地下水资源评价分区、判断各含水层之间的水力联系。
2.2 利用14C年龄划分浅层和深层含水层系统
同位素14C年龄与地下水体的取样深度的关系见图2。
(1) 地下水14C年龄随着地层埋深(取样深度)增大而增大;pmc值则逐渐变小。
(2) 根据本次资料,豫北平原地下水埋深<150m,14C年龄小于3000年,pmc值大于75;而大于150m的地下水,年龄大于5000年,地层为Q1/Q2界面。从而说明150m左右为一明显的分界面。本次以此界面划分为浅层含水层系统与深层含水层系统。
(3) 地层250m以深的地下水14C年龄均大于10000年。
2.3 14C年龄反映了水化学类型的类别
14C年龄与水化学类型关系见图Ⅲ—19分布于山前与近黄地带的地下水的上游区、地下水强径流带、滑县西南的C?M型水14C年龄较小,pmc值较大;而下游的N?M型水14C年龄较大,pmc值较小。
在新乡市东部H型地下水切开了非H型水,在此地带地下水14C年龄较小,pmc值100,属现代碳;在交接洼地、延津北、内黄周围砂地区非H型水地下水14C年龄较大,pmc值较小,3H小于10TU。
在咸水区,浅层地下水(<150m)的14C年龄>1000年,反映该区地下水中混合有部分的“年龄大的水”。也就是说,咸水区的形成是一个长期的盐分积累的过程,地下水年龄比较大;
14C年龄与水化学类型的关系也间接地证明了地下水的补迳排特征。
3 结论
3.1 14C同位素数值的初始值不受纬度、地域的控制,在应用该资料时,干扰因素较少,使用较简单,易于应用。
3.2 地下水中14C的大小是以其沉淀物中14C的含量计算的。如沉淀物中混有地层的土
颗粒,14C值偏大,在使用时,应考虑地质情况及取样的情况进行校正。
3.3在应用14C同位素技术时,应结合地下水位、水化学资料以及其它测试结果进行综合分析。
3.4 14C同位素技术可用于判断地下水的补迳排条件、判断地下水的污染分析、判断各种类型的地下水的水力联系、地下水资源评价的分区等。在以后的应用中,还会发现更多的用处。
镭 镭,英文名radium,是一种具有很强的放射性的元素,在化学元素周期表中位于第7周期,第IIA族,原子序数88,元素符号Ra。纯的金属镭是几乎无色的,但是暴露在空气中会与氮气反应产生黑色的氮化镭(Ra3N2)。镭的所有同位素都具有强烈的放射性,其中最稳定的同位素为镭-226,半衰期约为1600年,会衰变成氡-222。当镭衰变时,会产生电离辐射,使得荧光物质发光。是居里夫人发现的新元素,镭的发现对科学贡献伟大。 镭元素符号Ra,原子序数88,原子量226.03。外围电子排布7s,密度6.0g/cm,熔点700℃,沸点<1140℃,位于第七周期第ⅡA族。银白色有光泽的软金属。第一电离能509.37kJ/mol,电负性0.9。化学性质活泼,在空气中不稳定,易跟空气中氮气和氧气化合。跟水反应生成氢氧化镭(Ra(OH)2)并放出氢气。溶于稀酸。化学性质跟钡十分相似。镭的氯化物、溴化物、氢氧化物易溶于水,硫酸盐、碳酸盐微溶于水。已知镭有多种同位素,镭-226半衰期最长,为1622年。镭有很强的放射性,衰变时放出α和γ两种射线,并放出大量热(每克镭每小时放热586.18焦耳),裂变生成氢和氮。在镭射线照射下,水、氨、氯化氢能分解,氧气能转变成红氧。硫化锌、硫化钙等碱土金属硫化物,在镭射线的照射激发下能发出浅绿色柔和的磷光。镭射线能破坏动物体,杀死细胞、细菌。利用镭的放射性可治疗癌症,在硫化锌,硫化钙中混入10ppm的镭盐,可制成发光涂料、发光塑料。镭盐跟铍粉的混合制剂,可作中子放射源,用于探测石油资源和岩石的组成。镭在自然界中以化合态存在,主要存在于多种矿物、土壤、矿泉水和海底淤泥中。镭在自然界中分布特别稀少,仅占地壳原子总数的一百亿亿分之八。1898年12月,玛丽〃居里和皮埃尔〃居里从沥青铀矿提取铀后的矿渣中分离出氯化镭,1907年测出镭元素的新的原子量,1910 年又用电解氯化镭的方法制得了金属镭(白色金属)它的英文名称来源于拉丁文radius,含义是“射线”。镭在地壳中的含量为1×10-9%,至今已发现质量数为206~230的同位素中,除镭223、镭224、镭226、镭228是天然放射性同位素外,其余都是用人工方法合成的。镭存在于所有的铀矿中,每2.8吨铀矿中含1克镭。 镭是荧蓝色/银白色金属,是最活泼的碱土金属。镭在空气中可迅速与氮气和氧气生成氮化镭(Ra2N3)和氧化镭(RaO),与水反应剧烈,生成氢氧化镭和氢气。镭的最外电子层有两个电子,氧化态为+2,只形成+2价化合物。镭盐和相应的钡盐属同晶形化合物,化学性
元素序号:5 元素符号:B 元素名称:硼 元素原子量:10.81 元素类型:非金属 发现人:戴维、盖吕萨克、泰纳发现年代:1808年 发现过程: 1808年,英国的戴维和法国的盖吕萨克、泰纳,用钾还原硼酸而制得硼。 元素描述: 它是最外层少于4个电子的仅有的非金属元素。其单质有无定形和结晶形两种。前者呈棕黑色到黑色的粉末。后者呈乌黑色到银灰色,并有金属光泽。硬度与金刚石相近。无定形的硼密度2.3克/厘米3,(25-27℃);晶形的硼密度2.31克/厘米3,熔点2300℃,沸点2550℃,化合价3。在室温下无定形硼在空气中缓慢氧化,在800℃左右能自燃。硼与盐酸或氢氟酸,即使长期煮沸,也不起作用。它能被热浓硝酸和重铬酸钠与硫酸的混合物缓慢侵蚀和氧化。过氧化氢和过硫酸铵也能缓慢氧化结晶硼。上述试剂与无定形硼作用激烈。与碱金属碳酸盐和氢氧化物混合物共熔时,所有各种形态的硼都被完全氧化。氯、溴、氟与硼作用而形成相应的卤化硼。约在600℃硼与硫激烈反应形成一种硫化硼的混合物。硼在氮或氨气中加热到1000℃以上则形成氮化硼,温度在1800-2000℃是硼和氢仍不发生反应,硼和硅在2000℃以上反应生成硼化硅。在高温时硼能与许多金属和金属氧化物反应,生成金属硼化物。 元素来源: 制备方法有:硼的氧化物用活泼金属热还原;用氢还原硼的卤化物;用碳热还硼砂;电解熔融硼酸盐或其他含硼化合物;热分解硼的氢化合物上述方法所得初产品均应真空除气或控制卤化,才可制得高纯度的硼。 元素用途: 由于硼在高温时特别活泼,因此被用来作冶金除气剂、锻铁的热处理、增加合金钢高温强固性,硼还用于原子反应堆和高温技术中。棒状和条状硼钢在原子反应堆中广泛用作控制棒。由于硼具有低密度、高强度和高熔点的性质,可用来制作导弹的火箭中所用的某些结构材料。硼的化合物在农业、医药、玻璃工业等方面用途很广。 元素辅助资料:
环境同位素在地下水中的研究进展及应用 王永森 河海大学水资源环境学院,南京(210098) E-mail :wangyongsen@https://www.doczj.com/doc/965416470.html, 摘 要:本文介绍了环境同位素在地下水研究的一些研究和应用以及发展动态,阐述了其在地下水中应用的一些问题和前景。地下水来源于大气降水,同位素分馏效应导致了不同水体具有不同的同位素含量,大气降水中的同位素组成影响着地下水的同位素比值,环境同位素可以有效进行地下水年龄的测定,估计地下水的补给源、以及定量估计不同水源对地下水的补给量。 关键词:环境同位素;地下水;地下水示踪;同位素测年 1. 引言 大气过程改变了水的稳定同位素的组成,在特定的环境下,补给水就会产生一个特征性的同位素信息,根据这个信号可以示踪地下水的起源,放射性同位素的衰减提供了地下水滞留时间的测量,特别是1951-1962年期间的一系列核试验提供了放射性同位素的输入信号,同时根据同位素的差异指示地下水的来源、补给过程、地球化学演化、及地下水水质以及污染过程。科学家已经逐渐认识导他们在生物化学循环和土壤水大气过程研究的重要性。 2. 环境同位素的概念、原理 自然界中,环境同位素又分为稳定同位素和放射性同位素,由于同为素间地物理化学性质不同,引起同位素地变化,又称为同位素分馏。用稳定同位素研究地下水,主要利用的同位素之间的微小差异,一般我们同位素比值或δ值来表示,δ值定义为一种物质相对于标准参照物的同位素比率,如下式 1R R δ=?样品标准 × 103 (‰) (1) R 表示重同位素相对于轻同位素的比值,一个正的δ值表示样品的同位素比值高于标准样品的,负值表示样品的同位素比率低于标准样品。 放射性同位测地下水年龄是根据放射性同位素的衰变速率来测量的,不同于稳定同位素,氚浓度用绝对浓度氚单位(TU )表示,不需要参照标准, 14C 含量通常用样品的放射比度表示,即每克碳的放射性活度(Bq/gC)。实际中常使用相对浓度单位(A)表示,即现代碳百分含量(pmc 或%mod)。放射性同位素,诸如36Cl ,129I,39Ar 以及铀系列都可以用来测地下水年龄。下式是测龄原理: A t = A 0e ?λt A 0为母核的初始放射性活度,A t 为经过t 时间后的放射性,λ为衰变常数,时间可以表示为T = (1/λ)ln(A/A 0),通常放射性同位素的的不稳定性用半衰期来表示,T 1/2 = (?1/λ)ln(1/2) 则,1/21/2ln 20.693T T λ= =,14C 半衰期为5730年,氚的半衰期为12.43年,他们都可以测量地下水年龄,有时两个结合起来会更能解释地下水的动态。 稳定同位素可以用来测年的校正像13C ,放射性同位素也产生分馏,为了维持测年的普遍性,14C 的放射性必须用-25‰δ13C 归一化。才具有可比性。
科学研究中,还自己创造和改进了许多新仪器,例如压电水晶秤、居里天平、居里静电计等。1895年7月25日比埃尔·居里与玛丽·居里结婚。 玛丽·斯克罗多夫斯基·居里(Marie Curie)1867年11月7日生于沙皇俄国统治下的华沙,父亲是中学教员。16岁她以金质奖章毕业于华沙中学,因家庭无力供她继续读书,而不得不去担任家庭教师达六年之久。后来靠自己的一点积蓄和姐姐的帮助,于1891年去巴黎求学。在巴黎大学,她在极为艰苦的条件下勤奋地学习,经过四年,获得了物理和数学两个硕士学位。 居里夫妇结婚后次年,即1896年,贝克勒尔发现了铀盐的放射性现象,引起这对青年夫妇的极大兴趣,居里夫人决心研究这一不寻常现象的实质。她先检验了当时已知的所有化学元素,发现了钍和钍的化合物也具有放射性。她进一步检验了各种复杂的矿物的放射性,意外地发现沥青铀矿的放射性比纯粹的氧化铀强四倍多。她断定,铀矿石除了铀之外,显然还含有一种放射性更强的元素。 ? 居里以他作为物理学家的经验,立即意识到这一研究成果的重要性,放下自己正在从事的晶体研究,和居里夫人一起投入到寻找新元素的工作中。不久之后,他们就确定,在铀矿石里不是含有一种,而是含有两种未被发现的元素。1898年7月,他们先把其中一种元素命名为钋,以纪念居里夫人的祖国波兰。没过多久, 1898年12月,他们又把另一种元素命名为镭。为了得到纯净的钋和镭,他们进行了艰苦的劳动。在一个破棚子里,日以继夜地工作了四年。自己用铁棍搅拌锅里沸腾的沥青铀矿渣,眼睛和喉咙忍受着锅里冒出的烟气的刺激,经过一次又一次的提炼,才从几吨沥青铀矿渣中得到十分之一克的镭。由于发现放射性,居里夫妇和贝克勒尔共同获得了1903年诺贝尔物理学奖。 元素描述 密度6.0克/立方厘米(20℃)。熔点700℃,沸点约1140℃。银白色有光泽的软金属。在空气中不稳定,易与空气中氮和氧化合。与水作用放出氢气,生成氢氧化镭Ra(OH)2。溶于稀酸。化学性质与钡十分相似;所有镭盐与相应的钡盐是同晶型的。镭能生成仅微溶于水的硫酸盐、碳酸盐、铬酸盐、碘酸盐;镭的氯化物、溴化物、氢氧化物溶于水。已知镭有13种同位素,226Ra半衰期最长,为1622年。
同位素科普常识 同位素比值R、δ值及同位素标准 同位素比值R为某一元素的重同位素丰度与轻同位素丰度之比,例如 D/H、13C/12C、34S/32S等,由于轻元素在自然界中轻同位素的相对丰度很高,而重同位素的相对丰度都很低,R值就很低且很冗长繁琐不便于比较,故在实际工作中采用了样品的δ值来表示样品的同位素成分。样品(sq)的同位素比值R sq与一标准物质(st)的同位素比值(R st)比较,比较结果称为样品的δ值,其定义为: δ(‰)=( R sq / R st - 1)×1000 即样品的同位素比值相对于标准物质同位素比值的千分差。 对同位素标准物质的要求是:(a)组成均一性质稳定;(b)数量较多,以便长期使用;(c)化学制备和同位素测量的手续简便;(d)大致为天然同位素比值变化范围的中值,以便用于绝大多数样品的测定;(e)可以做为世界范围的零点。 目前国际通用的同位素标准如下: (1)氢同位素:分析结果均以标准平均大洋水(Standard Mean Ocean Water,即SMOW)为标准报导,D/H SMOW =(155.76 ± 0.10)× 10-6(2)碳同位素:标准物质为美国南卡罗来纳州白垩纪皮狄组层位中的拟箭石化石(Peedee Belemnite,即PDB),其13C/12C =(11237.2 ± 9 0)× 10-6
(3)氧同位素:大部分氧同位素分析结果均以SMOW标准报导,18O/16O (2005.2 ± 0.43)×10-6,17O/16O SMOW=(373 ± 15)×10-6;而在SMOW= 碳酸盐样品氧同位素分析中则经常采用PDB标准,其18O/16O = 2067.1×10-6,它与SMOW标准之间存在转换关系。 (4)硫同位素:标准物质选用Canyon Diablo铁陨石中的陨硫铁(Troi lite),简称CDT。 34S/32S ± 93 CDT = 0.0450045 (5)氮同位素:选空气中氮气为标准。 15N/14N = (3.676.5 ± 8.1)×10-6 (6)硅同位素:选用美国国家标准局的石英砂NBS-28做为标准。(7)硼同位素:采用SRM951硼酸做为标准,NBS推荐的 11B/10B比值为4.04362±0.00137。
室外水体蒸发氢氧同位素日变化特征 为研究室外水体蒸发氢氧同位素变化特征,连续12个小时采集四川大学听荷池的水样,获得了水体蒸发氢氧稳定同位素与温度的关系。实验结果表明,水体蒸发实验中,温度越高,蒸发速度越快,在同样的蒸发时间内水体重同位素富集程度越大;室外水体自由蒸发实验中得出的蒸发线方程斜率较大地偏离了当地降水线,表明实验期间水体蒸发分馏作用较明显。该研究为进一步揭示水体蒸发分馏规律提供了可靠的实验依据。 标签:水体蒸发;氢氧同位素;日变化;实验研究 1 实验区概况 取样点位于成都市武侯区四川大学听荷池,北纬30°38’3.64〃,东经104°05’12.38〃,海拔大约为490m,池面积为1.2hm2,降水是听荷池水量的主要来源。成都市属于中亚热带湿润季风气候区,常年最多风向是静风,冬湿冷、春早、无霜期较长,四季分明,热量丰富,年平均气温16°C,最高气温38.6°C,最低气温-5.9°C,无霜期为287d,初霜期出现的时候大约为11月底,终霜期一般在2月,冬季的平均气温大概为5°C,平均气温比同纬度的长江中下游地区高1~2°C。冬春雨少,夏秋多雨,雨量充沛,多年平均降雨量约为900~1300mm,多集中在7~9月份。光、热、水基本同季,气候资源的组合合理,很有利于生物繁衍。风速小,风速为1~1.5m/s,晴天少,日照率在24~32%之间,年平均日照时数为1042~1412小时。 2 样品收集与分析 2.1 样品收集 2016年12月4日,在听荷池采集水样,气象数据为当时现场测量记录。 取样品之前,需要把塑料瓶放入7N的HNO3浸泡一整天,然后用超纯水清洗多次,接着放入烘箱将塑料瓶的水烘干,为了保证取样工具的洁净与干燥,以免污染样品。采取样品时,尽量将水样装满瓶子,这是因为考虑到液态水分子之间存在着范德华力,它会使水分子的运动速度远远小于气态情形,这样可以降低蒸发时的分馏作用。 取样采集:2016年12月4日,8:00至20:00,每个小时分别在听荷池东南西北角采集水样,每次取样的地点以及取样的深度基本上都没有变化。每次将取好的水样装入50ml的塑料瓶中,现场记录日期和温度等,用封口膜将瓶口封住,以免造成分馏。最后把装好的样品带回实验室进行分析。 2.2 样品处理及分析
镭是一种具有很强的放射性的元素,在化学元素周期表中位于第7周期,第IIA 族,原子序 数88,元素符号Ra。能不断放出大量的热量。 镭元素符号ra,原子序数88,原子量226.03。外围电子排布7s,密度6.0g/cm,熔点700℃,沸点<1140℃,位于第七周期第ⅡA族。银白色有光泽的软金属。第一电离能509.37kJ/mol,电负性0.9。化学性质活泼,在空气中不稳定,易跟空气中氮气和氧气化合。跟水反应生成氢氧化镭(Ra(OH)2)并放出氢气。溶于稀酸。化学性质跟钡十分相似。镭的氯化物、溴化物、氢氧化物易溶于水,硫酸盐、碳酸盐微溶于水。已知镭有13种同位素,镭-226半衰期最长,为1622年。镭有很强的放射性,衰变时放出α和γ两种射线,并放出大量热(每克镭每小时放热586.18焦尔),裂变生成氡和氦,氡也有放射性。在镭射线照射下,水、氨、氯化氢能分解,氧气能转变成臭氧。硫化锌、硫化钙等碱土金属硫化物,在镭射线的照射激发下能发出浅绿色柔和的磷光。镭射线能破坏动物体,杀死细胞、细菌。利用镭的放射性可治疗癌症,在硫化锌,硫化钙中混入10ppm的镭盐,可制成发光涂料、发光塑料。镭盐跟铍粉的混合制剂,可作中子放射源,用于探测石油资源和岩石的组成。镭在自然界中以化合态存在,主要存在于多种矿物、土壤、矿泉水和海底淤泥中。镭在自然界中分布特别稀少,仅占地壳原子总数的一百亿亿分之八。1898年法国科学家居里夫妇从沥青铀矿中发现镭,居里夫人于1910年从沥青铀矿中制得纯净金属镭。镭的希腊原文是射线。用汞阴极和钯-铱阳极电解氯化镭溶液可得到镭汞剂,然后在氢气中进行热分解制得。
玛丽·居里发现了一种化学元素镭,化学 发现「镭」元素的玛丽居里 符号Ra,原子序数88,原子量226.0254,属周期系ⅡA族,为碱土金属的成员和天然放射性元素。1898年12月,玛丽·居里和皮埃尔·居里从沥青铀矿提取铀后的矿渣中分离出氯化镭,1907年测出镭元素的新的原子量,1910年又用电解氯化镭的方法制得了金属镭(白色金属)它的英文名称来源于拉丁文radius,含义是“射线”。镭在地壳中的含量为1×10-9%,至今已发现质量数为206~230的同位素中,除镭223、镭224、镭226、镭228是天然放射性同位素外,其余都是用人工方法合成的。镭存在于所有的铀矿中,每2.8吨铀矿中含1克镭 百炼成钢:比喻经过长时间的多次的锻炼,变的坚强 发愤图强:发愤,决心努力图,谋求下定决心,努力谋求富国 坚持不懈:懈,松懈坚持到底,一点也不松懈 迎难而上:迎着困难向前进 . 集思广益:集中群众的智慧,广泛吸收有益的意见 群策群力:策,计策主意指发挥集体作用,大家一起想办法、贡献力量
(19)中华人民共和国国家知识产权局 (12)实用新型专利 (10)授权公告号 (45)授权公告日 (21)申请号 201920236323.9 (22)申请日 2019.02.25 (73)专利权人 淄博鑫兴辉新材料科技有限公司 地址 255000 山东省淄博市张店区人民西 路7号同济商务楼402室 (72)发明人 张辉 牛娜 张莹涵 牛丽智 张森法 (51)Int.Cl. C01B 35/10(2006.01) (54)实用新型名称一种生产硼10酸和硼11酸同位素的制备系统(57)摘要本实用新型公开了一种生产硼10酸和硼11酸同位素的制备系统,包括加热搅拌釜、静态混合器和蒸发罐,所述加热搅拌釜上连通有进气管和第一进水管,所述加热搅拌釜通过管道依次连通有离心机、静态混合器、过滤器和蒸发罐,所述离心机上连通有第二进水管。本实用新型的制备系统主要由加热搅拌釜、静态混合器、蒸发罐、离心机、第二进水管和过滤器组成,制备硼10酸和硼11酸的时候,通过加热搅拌釜对碳酸钙与水的固液混合物加热,通过离心机对固液混合物进行分离,在通过静态混合器对硼酸水溶液进行稀释混合,再通过滤器将硼酸水过滤之后,通入到蒸发罐中对硼酸水溶液进行蒸发结晶,操作方便, 提高了生产效率。权利要求书1页 说明书2页 附图2页CN 209583649 U 2019.11.05 C N 209583649 U
权 利 要 求 书1/1页CN 209583649 U 1.一种生产硼10酸和硼11酸同位素的制备系统,包括加热搅拌釜(1)、静态混合器(2)和蒸发罐(3),其特征在于:所述加热搅拌釜(1)上连通有进气管(4)和第一进水管(5),所述加热搅拌釜(1)通过管道(9)依次连通有离心机(6)、静态混合器(2)、过滤器(8)和蒸发罐(3),所述离心机(6)上连通有第二进水管(7)。 2.根据权利要求1所述的一种生产硼10酸和硼11酸同位素的制备系统,其特征在于:所述管道(9)上安装有阀门(10)。 3.根据权利要求1所述的一种生产硼10酸和硼11酸同位素的制备系统,其特征在于:所述进气管(4)上安装有流量计(11)和计时器(12)。 4.根据权利要求1所述的一种生产硼10酸和硼11酸同位素的制备系统,其特征在于:所述加热搅拌釜(1)上安装有泄压阀(13)。 5.根据权利要求1所述的一种生产硼10酸和硼11酸同位素的制备系统,其特征在于:所述静态混合器(2)上安装有散热片(14)。 6.根据权利要求5所述的一种生产硼10酸和硼11酸同位素的制备系统,其特征在于:所述散热片(14)上安装有温度计(15)。 2
本文由国际原子能机构TC 项目“河海大学院士基金项目”资助。责任编辑:宫月萱。第一作者:陈建生,男,1955年生,教授,博士,博士生导师,主要从事同位素水文学,渗流理论与探测技术研究;E -mail :j schen @hhu .edu .cn 。 巴丹吉林沙漠湖泊及其下游地下水同位素分析 陈建生1) 凡哲超1) 汪集 2) 顾慰祖1) 赵 霞 1) (1)河海大学,江苏南京,210098;2)中国科学院地质与地球物理研究所,北京,100029) 摘 要 本文通过环境同位素水化学等分析方法研究了祁连山北侧、龙首山、巴丹吉林沙漠、古日乃、拐子湖和额济纳盆地的 泉水和井水的来源,揭示了巴丹吉林沙漠等下游地区的地下水来自于祁连山降水的补给,平均补给高程为3300m ,祁连山顶部存在大片裸露的灰岩地层,雪水融化后沿着喀斯特地层或山前大断裂补给到深部,穿过龙首山直接补给到巴丹吉林沙漠及其下游地区,在沙漠湖泊中发现的钙华与钙质胶结证明地下水经过了石灰岩地层,承压水通过越流补给到浅部含水层,通过蒸发量计算得到的地下水补给量接近6×108m 3/a ,承压水中地下水的年龄为20~30a 。关键词 巴丹吉林沙漠 钙质胶结 环境同位素 承压地下水 湖泊 Isotope Methods for Studying the Replenishment of the Lakes and Downstream Groundwater in the Badain Jaran Desert CHEN Jiansheng 1) FAN Zhechao 1) WANG Jiyang 2) GU Weizu 1) ZHAO Xia 1) (1)Hehai Un iversity ,Nanjing ,Jiangsu ,210098;2Institu te of Geol ogy and Geophysics ,CAS ,Beijing ,100029) A bstract I n this paper ,the sources of spring wa ter and well water on the no rthern side of the Qilian M ountain and in Lo ngshou M ountain ,Badain Jaran Desert ,Gurinai ,G uaizi Lake and Ejina Basin are studied by the methods of environmental iso topes and w ater chemistry .T he g roundwater in dow nstream areas such as Badain Jaran Deser t is found to be recharged by the precipitation of the Qi -lian M ountain ,with the average recharge elevation being 3300m .Lots of naked limestone lay ers ex ist at the top of the Qilian M oun -tain .The melted snow water of the Qilian M ountain infiltrates into the deep lay er ,passes through the karst strata o r large faults in f ro nt of the mountain ,and directly recharges Badain Jaran Desert and its downstream areas via the Long shou M ountain .T he calcare -ous cement and travertine found in the lakes of the desert prove that the groundw ater passes through the limestone layer .Confined w ater recharges the shallow aquifer by means of leakage .T he calculation of the evapora tio n amount show s that the groundw ater recharge volume is six hundred million cubic meters per year ,and the age of the confined g roundwater is 20~30y ears .Key words Badain Jaran Desert calcareous cement and traver tine environmental isotope co nfined groundw ater lake 通过稳定同位素、水化学、水文地质等方法进行的额济纳盆地与古日乃草原地下水的补给源调查研究已经取得了初步的成果:调查研究中发现额济纳盆地的地下水与巴丹吉林沙漠的地下水同出一源,是由巴丹吉林沙漠补给到古日乃和额济纳盆地的,而且与黑河水不存在相关关系。研究发现,额济纳盆地与古日乃草原存在多含水层结构,额济纳盆地承压水的水头高出潜水位约60m ,承压水通过越流补给潜水。在国际原子能机构的支持下,研究中对巴丹吉林沙漠及其周边地区的承压地下水中的同位 素δD 、δ18O 、3 H 、CFC (氟里昂)、温度、电导、水化学进行了测试,并做了钻孔中人工同位素测定地下水 流速、流向等试验。通过试验与分析初步确定了承压地下水的来源、补给量和补给通道等,为进一步的深入研究奠定了基础。此次工作通过水-岩相互作用和CFC 证据,确认额济纳盆地地下水的补给年龄只有30a 左右,是完全可以开发利用的。 1 祁连山、巴丹吉林沙漠、拐子湖、古 日乃水文地质概况 祁连山主要是由前寒武纪变质岩系、早古生代这两个时期的各种变质岩系构成。前寒武纪期间,祁连山曾作为原始古地台的一部分与华北台块联成一个整体。震旦纪初开始下沉,形成NWW —SEE 2003年12月 24卷6期:497-504 地 球 学 报AC TA GEOSCIEN TICA SINICA Dec .2003 24(6):497-504
杞麓湖水质参数及水体稳定同位素特征研究湖泊对区域气候调节及地区社会经济发展发挥着至关重要的作用。杞麓湖作为通海县的“母亲湖”,近年来在自然与人类活动的双重影响下,生态环境面临着诸多威胁。 基于此,本文首先利用2016年11月至2017年10月时段内对杞麓湖水质参数水温(Temp)、溶解氧(DO)、叶绿素a(Chl-a)、p H及总磷(TP)、总氮(TN)的逐月监测,对湖泊生态环境状况和水质月际变化作进一步探讨。同时,结合已有气象数据,利用杞麓湖流域各水体稳定氢氧同位素组成特征对湖泊水动力、水汽来源及季节变化进行研究,探讨各水质参数对湖水同位素的影响,通过对各水体稳定氢氧同位素的组成及季节变化特征分析,深入讨论分析流域水循环过程,进一步分析探讨杞麓湖水更换过程及周期。 本文主要的研究结论如下:(1)杞麓湖对流域气候环境有着显著的调节作用,维持流域气温较为恒定,同时减少极端天气对区域气候带来的影响。湖水在不同深度热量分布较为均衡。 水温受风力作用及湖泊动力影响较大。同时,温度是影响湖泊水循环、水生生物活动强度的控制因素。 (2)杞麓湖受流域人类活动的强烈影响,外源输入的影响成为引起湖泊水体理化性质(溶解氧、叶绿素a浓度、p H)的主要因素。营养盐的输入引起的藻类活动的增强,以及污染物的排放与分解,使不同湖区水体酸碱度出现较明显的差异。 有机污染物的分解同时消耗了水体中的溶解氧,因而在湖滨处及入湖河流较为集中的西南部出现较低的溶解氧浓度及p H值,这一现象在雨季尤为明显。不
同湖区营养盐的差异引起藻类空间分布的不同,在工农业排放较集中的东部、西南部湖区,水体叶绿素a浓度远高于其他湖区。 夏季水温及光照的增强、外源输入的增加、以及生物活性的加强,加重了不同湖区水体理化性质的空间差异性。进而引起湖泊底质释放增加、水生物种结构单一化、水体自净能力下降等诸多环境问题。 (3)杞麓湖富营养化程度较高,监测时期内处于中度—重度富营养化状态,水体氮磷浓度全年处于较高水平。磷是湖泊藻类生长繁殖的限制因子。 湖泊总磷浓度季节波动较大,夏季相较冬季总磷浓度增加了近40%,总氮季 节变化相对较小,夏季高于冬季。湖滨化工业排放使湖泊氮磷含量(特别是总磷)大幅上升,农业排放对水体总氮影响较大,对总磷影响则相对较小。 流域河水、地下水营养盐浓度也很高,当地的水资源及水安全问题较为突出。 (4)湖水同位素组成随深度变化不明显,蒸发和河水补给的作用决定了湖泊水同位素的空间分布特征。 水温对表层湖水同位素分馏有一定的影响,对其空间分布的作用也存在,但整体影响不大。其他水质参数与湖泊水同位素组成之间没有必然的联系,在空间分布变化上也没有明显的规律。 (5)杞麓湖无论是全年还是各季节湖水蒸发线方程的斜率、截距相较全球大气水线有着明显的偏离,湖水受到了长时期蒸发分馏作用的影响。杞麓湖流域内河水、地下水的同位素组成相对湖水偏负,蒸发水线的偏离程度也小于湖水,地下水受到的非平衡分馏作用更弱一些。 海洋水汽是当地降水主要来源,入湖河流补给是湖泊水主要补给方式。(6)根据雨季前后湖水同位素组成的差异,利用降水数据我们模拟得出湖水换水周期
镭的资料 一种具有很强的放射性的元素并能不断放出大量的热。镭能生成仅微溶于水的硫酸盐、碳酸盐、铬酸盐、碘酸盐;镭的氯化物、溴化物、氢氧化物溶于水。已知镭有13种同位素,226Ra半衰期最长,为1622年。镭能放射出α和γ两种射线,并生成放射性气体氡。镭放出的射线能破坏、杀死细胞和细菌。因此,常用来治疗癌症等。此外,镭盐与铍粉的混合制剂,可作中子放射源,用来探测石油资源、岩石组成等。是原子弹的材料之一。 发现人:居里夫妇 元素结构 晶体结构: 晶胞为体心立方晶胞,每个晶胞含有3个金属原子。 一种化学元素。化学符号Ra ,原子序数88 ,原子量226.0254,属周期系ⅡA族,为碱土金属的成员和天然放射性元素。1898年M.居里和P.居里从沥青铀矿提取铀后的矿渣中分离出溴化镭,1910年又用电解氯化镭的方法制得了金属镭,它的英文名称来源于拉丁文radius,含义是“射线”。镭是荧蓝色/银白色金属,是最活泼的碱土金属。镭在空气中可迅速与氮气和氧气生成氮化物和氧化物,与水反应剧烈,生成氢氧化镭和氢气。镭的最外电子层有两个电子,氧化态为+2,只形成+2价化合物。镭盐和相应的钡盐属同晶形化合物,化学性质很相似。氯化镭、溴化镭、硝酸镭都易溶于水,硫酸镭、碳酸镭、铬酸镭难溶于水。镭有剧毒,它能取代人体内的钙并在骨骼中浓集,急性中毒时,会造成骨髓的损伤和造血组织的严重破坏,慢性中毒可引起骨瘤和白血病。镭是生产铀时的副产物,用硫酸从铀矿石中浸出铀时,镭即成硫酸盐存在于矿渣中,然后转变为氯化镭,用钡盐为载体,进行分级结晶,可得纯的镭盐。金属镭则由电解氯化镭制得。镭及其衰变产物发射γ射线,能破坏人体内的恶性组织,因此镭针可治癌症。 发现人 玛丽·居里(Marie Curie)和皮埃尔·居里(Pierre Curie)发现年代:1898年12月26日上午8时 皮埃尔·居里(Pierre Curie),或译彼埃尔·居里、比埃尔·居里。 1859年5月15日生于法国巴黎一个医生家庭。他的儿童和少年时期,性格上好个人沉思,不易改变思路,沉默寡言,反应缓慢,不适应普通学校的灌注式知识训练,不能跟班学习,人们都说他心灵迟钝,所以从小没有进过小学和中学。父亲常带他到乡间采集动、植、矿物标本,培养了他对自然的浓厚兴趣,学到了如何观察事物和如何解释它们的初步方法。居里14岁时,父母为他请了一位数理教师,他的数理进步极快,16岁便考得理学士学位,进入巴黎大学后两年,又取得物理学硕士学位。1880年,他21岁时,和他哥哥雅克·居里一起研究晶体的特性,发现了晶体的压电效应。1891年,他研究物质的磁性与温度的关系,建立了居里定律:顺磁质的磁化系数与绝对温度成反比。他在进行科学研究中,还自己创造和改进了许多新仪器,例如压电水晶秤、居里天平、居里静电计等。1895年7月25日皮埃尔·居里与玛丽·居里结婚。
水化学及同位素特征在矿井水源判别中的应用 摘要:毛坪铅锌矿未采矿体均处当地最低侵蚀基准面洛泽河以下,为研究矿区 洛泽河水与矿坑充水之间的相互关系,进一步查清矿坑充水来源,对矿区地表河 水以及矿坑不同出水点采取水样,进行环境同位素测试和水质全分析。分析结果 表明:矿区浅层水和深层承压水在不同深度获得大气降水补给的速度有快有慢, 相差悬殊;河水对矿床充水不强,矿坑水主要补给源为不同标高补给区的非定水 头补给。研究成果为进一步判定矿坑充水水源、分析矿山水文地质条件以及矿山 防治水设计提供了科学的依据。 关键词:矿山防治水;水源判别;水化学特征;氢氧同位素 1 矿区水文地质概况 毛坪铅锌矿为已采矿山,主要矿体位于当地最低侵蚀基准面洛泽河之下[1-3]。区内龙潭河、铜厂沟溪、锈水沟溪等其它河、沟均为洛泽河支流[4]。洛泽河总体 上控制了区内的地下水流动系统。域内地下水接受降水补给后,依地势向洛泽河 汇聚,然后从南往北迳流,部分地下水在沟谷等地形切割强烈地带形成下降泉排泄,补给河水[5,6];部分地下水仍以地下迳流形式运动,于矿区北部遇峨嵋山 组玄武岩隔水层,地下水径流受阻,沿东西向顺层裂隙溢出成泉,排泄地下水。 区内构造发育,地下水对构造裂隙长期溶蚀拓宽,岩溶裂隙水含水层具有一 定库容空间,大气降水对岩溶裂隙地下水补给在时间上把年内或年际不连续的降 水调整为连续的地下迳流,维持泉群长期排泄[7,8];在空间上将较弱的区域裂 隙水汇聚成脉状迳流,最后,汇集于排泄区以泉水形式溢出排泄地下水,本区为 泉排型岩溶地下水系统[9]。 图1 矿区地下水矿化度等值线 2 水化学水源判别 2.1水质全分析特征 本次研究工作水质全分析采样在矿坑、泉水、河水等重要水体采集水样20件。矿床地下水水化学成份及矿化度值自北部、北东部二迭系栖霞茅口组岩溶裂隙水 含水层、石炭系威宁丰宁统岩溶裂隙水含水层、泥盆系宰格组岩溶裂隙水含水层 逐渐升高(见图1),表明矿床地下水接受二迭系栖霞茅口组岩溶裂隙水含水层 地下水补给,经矿床运移至洛泽河即F1弱透水断层一带,地下水迳流滞缓,溶 滤作用增强,水中盐分及矿化度值明显增高,特别是SO42-离子增加明显,同时 说明矿床地下水受洛泽河水淡化不明显,河水对矿床充水不强的特征。 3水体环境同位素水源判别 3.1水体环境同位素特征 本次研究工作环境同位素水样采集雨水1件、泉水4件、河水3件、矿坑水 7件,钻孔涌水5件。 以昆明市雨水线为研究标准。矿区雨水、河水、泉水和坑下水δD与δ18O关 系见图2。 图2 毛坪矿雨水、泉水、河水、坑下水δD与δ18O关系 本地区构造活动剧烈,岩溶裂隙发育,雨季矿床深部承压水涌水孔水头上涨 明显,氚进入水中仅按衰变规律变化,衰变公式如下:
基本字义 ◎镭是一种放射性元素,具有很强的放射性,并能不断放出大量的热:镭疗(利用镭引的γ射线或a射线进行治疗)。镭,是一种化学元素。它能放射出人们看不见的射线,不用借助外力,就能自然的发光并发热,含
皮埃尔·居里和玛丽·居里)发现的一种
M3+ - M4+ 4400 M4+ - M5+ 5700 M5+ - M6+ 7300 M6+ - M7+ 8600 M7+ - M8+ 9900 M8+ - M9+ 13500 M9+ - M10+ 15100 晶胞参数: a = 514.8 pm b = 514.8 pm c = 514.8 pm α = 90° β = 90° γ = 90° 元素结构 晶体结构: 晶胞为体心立方晶胞,每个晶胞含有3个金属原子。 一种化学元素。化学符号 Ra ,原子序数 88 ,原子量226.0254,属周期系ⅡA族,为碱土金属的成员和天然放射性元素。1898年M.居里和P.居里从沥青铀矿提取铀后的矿渣中分离出溴化镭,1910年又用电解氯化镭的方法制得了金属镭,它的英文名称来源于拉丁文radius,含义是“射线”。镭是荧蓝色/银白色金属,是最活泼的碱土金属。镭在空气中可迅速与氮气和氧气生成氮化物和氧化物,与水反应剧烈,生成氢氧化镭和氢气。镭的最外电子层有两个电子,氧化态为+2,只形成+2价化合物。镭盐和相应的钡盐属同晶形化合物,化学性质很相似。氯化镭、溴化镭、硝酸镭都易溶于水,硫酸镭、碳酸镭、铬酸镭难溶于水。镭有剧毒,它能取代人体内的钙并在骨骼中浓集,急性中毒时,会造成骨髓的损伤和造血组织的严重破坏,慢性中毒可引起骨瘤和白血病。镭是生产铀时的副产物,用硫酸从铀矿石中浸出铀时,镭即成硫酸盐存在于矿渣中,然后转变为氯化镭,用钡盐为载体,进行分级结晶,可得纯的镭盐。金属镭则由电解氯化镭制得。镭及其衰变产物发射γ射线,能破坏人体内的恶性组织,因此镭针可治癌症。 发现人
硼同位素分离方法 1.同位素概况 1.1稳定同位素 在元素周期表中,原子序数相同,原子质量不同,化学性质基本相同,半衰期大于1015年的元素的同位素,称为稳定同位素。 1913年J.J.汤姆孙和F.W.阿斯顿用磁分析器发现天然氖是由质量数为20和22的两种同位素所组成,第一次发现了稳定同位素。 1919年阿斯顿制成质谱仪,并在71种元素中发现了202种核素,绝大多数是稳定的;后来利用光谱等方法发现了氧、氮等元素的稳定同位素。 地球上已发现的稳定同位素共274种,原子序数在84以上的元素的同位素都是放射性同位素。常用的有34种,已实现规模生产的稳定同位素及化合物有235U、重水、6Li、10B。它们是重要的核工业材料或作示踪原子。 元素的同位素组成常用同位素丰度表示,同位素丰度是指一种元素的同位素混合物中,某特定同位素的原子数与该元素的总原子数之比。 1.2同位素分析方法 同位素分析通常是指样品中被研究元素的同位素比例的测定。它是同位素分离、同位素应用和研究中不可缺少的组成部分。 质谱法它是稳定同位素分析中最通用、最精确的方法。它是先使样品中的分子或原子电离,形成各同位素的相似离子,然后在电场、磁场的作用下,使不同质量与电荷之比的离子流分开进行检测。若用照相底板摄像检测,则称质谱仪。将离子流收集在法拉第杯电极上,并用静电计测量电流,以能使仪器自动连续地接收不同荷质比的离子,这样的仪器称为质谱计。这两种仪器不仅能用于气体,也可用于固体的研究。质谱计能用于几乎所有元素的稳定同位素分析。 核磁共振法它是稳定同位素分析的另一重要方法。由于构成有机体主要元素的稳定同位素氘、碳13、氮 15、氧17和硫33等的核自旋量子数均不为零,在外磁场的作用下,这些原子核都会象陀螺一样进动,若此时在磁场垂直方向加上一个射频电场,当其频率与这些原子核进动频率相同时,即出现共振吸收现象,核自旋取向改变,产生从低能级到高能级的跃迁;当再回到低能级时就放出一定的能量,使核磁共振能谱上出现峰值,此峰的位置是表征原子核种类的。磁场强度恒定时,根椐共振时的射频电场频率,可以检出有机体样品中不同基团上的同位素,根据峰高,还可测定含量,但由于其测定灵敏度较低,一般不作定量分析用。
1000 /)()(000?=标准标准样品-R R R δ8.3 矿区地下水环境同位素分析 在水中天然存在很多种环境同位素,比如2H 、18O 、34S 、13C 、14C 等。地下水和地表水在其演化运动过程中,除了形成其一般的物理、化学踪迹外,还形成了大量微观的同位素踪迹。用同位素方法研究地下水的优越性在于它的化学性质比较稳定,不易被岩土吸附,不易生成沉淀的化合物;它的检测灵敏度非常高,很小的剂量就可获得满意的效果。用环境同位素的示踪方法来研究地下水的运动规律,能快速和有效的取得其它方法难以得到或者根本无法得到的重要水文地质信息,由于环境同位素作为天然示踪剂“标记”着天然水和地下水的形成过程,因此研究它们在各水体中的分布规律就有可能直接获得地下水形成和运动过程的信息。其途径就是通过环境同位素的分析,比较地下水体和地表水体中环境同位素的差异和变化规律来揭示地下水的起源、形成条件、补给机制以及各水体之间的水动力关系。该方法还是解决地下水各种补给来源水的混合比例、各类水体间水力联系等实际问题的有效工具。 8.3.1同位素标准及应用方法原理 在稳定同位素研究中,把某一元素两种同位素的丰度比用R 值来表示, 如D/H 、18O/16O ,在分析时只测定它的丰度比值而不测量单项同位素的绝对含量,通常用δ值表示,δ值定义如下: 其意义是样品中一元素的两种同位素丰度相对于某一对应标准丰度的千分偏差。使用国际标准SMOW(为平均大洋水)为标准。SMOW 定义δ2H 和δ18O 值均为零作为其标准。 氢氧元素共有5个稳定同位素(1H 、2H 、16O 、 17O 、18O ),但通常用于稳定同位素研究的是2H 和18O 。一般在水分子中氢氧的不同稳定同位素以不同方式组合,可形成9种不同形式的水分子,如H 216O 、HD 16O 、D 216O 、H 218O 、HD 18O 、D 218O 、H 217O 、HD 17O 、D 217O ,这些同位素水分子,由于质量不同,因而具有
题目:同位素示踪在植物光合作用研究中应用 学院:XXXXXXX学院 专业班级:XXXXXX班 姓名:XXX 引言: 同位素示踪法是利用放射性核素或稀有稳定核素作为示踪剂对研究对象进行标记的微量分析方法,Hevesy创立了示踪实验并于1923年首先用天然放射性212Pb研究铅盐在豆科植物内的分布和转移。继后Jolit和Curie于1934年发现了人工放射性,以及其后生产方法的建立(加速器、反应堆等),为放射性同位素示踪法的更快的发展和广泛应用提供了基本的条件和有力的保障。 中文名称:同位素示踪 英文名称:isotopic tagging;isotopic tracing 定义:化合物的同位素标记物与其非标记物具有相同 的生物化学性质,且同位素能够很灵敏地被检测,因而 追踪同位素标记物在所研究对象中的移动、分布、转变 或代谢等,是生物科学研究的有力手段。 正文: 同位素示踪所利用的放射性核素(或稳定性核素)及它们的化合物,与自然界存在的相应普通元素及其化合物之间的化学性质和生物学性质是相同的,只是具有不同的核物理性
质。因此,就可以用同位素作为一种标记,制成含有同位素的标记化合物(如标记食物,药物和代谢物质等)代替相应的非标记化合物。利用放射性同位素不断地放出特征射线的核物理性质,就可以用核探测器随时追踪它在体内或体外的位置、数量及其转变等,稳定性同位素虽然不释放射线,但可以利用它与普通相应同位素的质量之差,通过质谱仪,气相层析仪,核磁共振等质量分析仪器来测定。放射性同位素和稳定性同位素都可作为示踪剂(tracer),但是,稳定性同位素作为示踪剂其灵敏度较低,可获得的种类少,价格较昂贵,其应用范围受到限制;而用放射性同位素作为示踪剂不仅灵敏度,测量方法简便易行,能准确地定量,准确地定位及符合所研究对象的生理条件等特点: 1.灵敏度高 放射性示踪法可测到10-14-10-18克水平,即可以从1015个非放射性原子中检出一个放射性原子。它比目前较敏感的重量分析天平要敏感108-107倍,而迄今最准确的化学分析法很难测定到10-12克水平。 2.方法简便 放射性测定不受其它非放射性物质的干扰,可以省略许多复杂的物质分离步骤,体内示踪时,可以利用某些放射性同位素释放出穿透力强的r射线,在体外测量而获得结果,这就大大简化了实验过程,做到非破坏性分析,随着液