
上海市华师大一附中2010届高三上学期期中试题卷
一、选择题(本题共10分,每小题2分,只有一个正确选项)
1. 《中华人民共和国食品安全法》于今年6月1日起实施。下列做法不影响食品安全的是
A. 在食品加工中科学使用食品添加剂
B. 用聚氯乙烯塑料袋包装食品
C. 用二氧化硫漂白银耳
D. 用福尔马林作食品防腐剂 2.下列表述正确的是
A. 16O 与18O 互为同位素,H 216O 与H 218O 互为同素异形体
B. S 2-的结构示意图
C. NH 4+、H 2O 、NH 2—、—OH 都有相同的电子数
D. CH 4O 、C 2H 6O 、C 3H 8O 互为同系物
3. 氢是新型清洁能源,但难储运。研究发现,合金可用来储藏氢气。镧(La 13957
) 和镍(Ni 59
28)
的一种合金就是储氢材料。下列关于
La 13957
和Ni 59
28说法正确的是
A. 镧元素的质量数为139
B. Ni 59
28的中子数为28
C.
La 13957
和
13257
La 是同一种原子 D. Ni 59
28读作镍-59
4. 以下有机物命名错误的是
A. 1,1,2,2—四溴乙烷
B. 2—甲基—3—丙醇
C. 2—甲基—1,3—丁二烯
D. α—氨基—β—苯基丙酸
5. 现代大爆炸理论认为:天然元素源于氢、氦等发生的原子核融合反应。这与100多年前,普鲁特运用思辨性推测作出“氢是所有元素之母”的预言恰好“一致”。下列说法正确的是 A. 科学研究中若能以思辨性推测为核心,就能加快科学的进程
B. 普鲁特“既然氢最轻,它就是其他一切元素之母”的推理是符合逻辑的
C. “一致”是巧合,普鲁特的预言没有科学事实和理论支撑,它只是一种猜测
D. “现代大爆炸理论”是解释宇宙诞生的唯一正确的理论
二、选择题(本题共36分,每小题3分,只有一个正确选项) 6. 在单质的晶体中一定不存在的微粒是
A. 原子
B. 分子
C. 阴离子
D. 阳离子
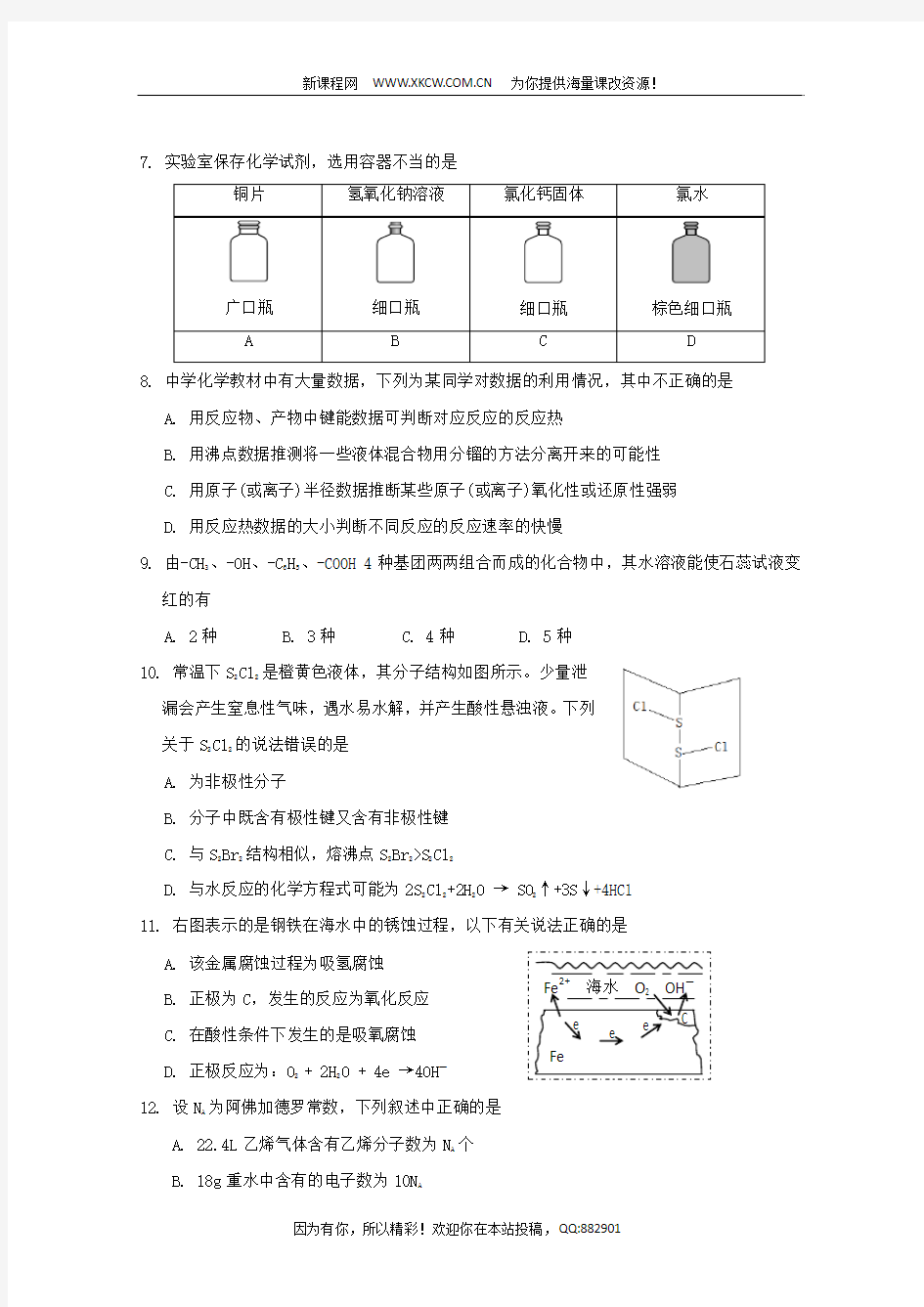
7. 实验室保存化学试剂,选用容器不当的是
8. 中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是
A. 用反应物、产物中键能数据可判断对应反应的反应热
B. 用沸点数据推测将一些液体混合物用分镏的方法分离开来的可能性
C. 用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性强弱
D. 用反应热数据的大小判断不同反应的反应速率的快慢
9. 由-CH 3、-OH 、-C 6H 5、-COOH 4种基团两两组合而成的化合物中,其水溶液能使石蕊试液变红的有
A. 2种
B. 3种
C. 4种
D. 5种 10. 常温下S 2Cl 2是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。下列关于S 2Cl 2的说法错误的是 A. 为非极性分子
B. 分子中既含有极性键又含有非极性键
C. 与S 2Br 2结构相似,熔沸点S 2Br 2>S 2Cl 2
D. 与水反应的化学方程式可能为2S 2Cl 2+2H 2O → SO 2↑+3S ↓+4HCl 11. 右图表示的是钢铁在海水中的锈蚀过程,以下有关说法正确的是
A. 该金属腐蚀过程为吸氢腐蚀
B. 正极为C ,发生的反应为氧化反应
C. 在酸性条件下发生的是吸氧腐蚀
D. 正极反应为:O 2 + 2H 2O + 4e →4OH —
12. 设N A 为阿佛加德罗常数,下列叙述中正确的是
A. 22.4L 乙烯气体含有乙烯分子数为N A 个
B. 18g 重水中含有的电子数为10N A
C. 1L 2mol/L 的硝酸镁溶液中含有的镁离子数为2N A
D. 1 mol NO 2气体降温后颜色变浅,其所含的原子数仍为3N A
13. 木质素是制浆造纸工业的一种副产物,它的一种单体结构简式如下图所示。关于该物质,下列说法错误的是
A. 该物质的分子式是C 10H 12O 3,它属于芳香烃
B. 每摩尔该物质最多能消耗4 mol H 2
C. 遇FeCl 3溶液呈紫色
D. 每摩尔该物质最多能消耗含2 mol Br 2的溴水
14. 下列实验过程中产生的现象与对应图形相符合的是
A. 盐酸中加
B. SO 2气体通
C. pH=1的醋酸和盐酸
D. 氨气通入
NaAlO 2溶液 入溴水中 分别加水稀释 醋酸溶液中
15. 在下列溶液中,各组离子一定能够大量共存的是 A. 使酚酞试液变红的溶液: Na +、Cl -、SO 42-、Fe 3+ B. c (H +)=10-12 mol·L -1的溶液:K +、Ba 2+、Cl --、Br - C. 使紫色石蕊试液变红的溶液:Fe 2+、Mg 2+、NO 3-、Cl - D. 碳酸氢钠溶液:K +
、SO 42-
、Cl -
、H +
16. 下列叙述中正确的是
A. 分子晶体溶解于水时,都只需克服分子间作用力
B. 离子晶体中一定含有金属阳离子
C. 金属晶体容易导电,是因为其中含有自由电子
D. 原子晶体中只存在非极性共价键
17. 某密闭容器中充入等物质的量的气体A 和B ,一定温度下发生反应是:
A(g)+x B(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、
反应速率随时间变化的如下图所示。下列说法中正确是
A. 8min 前正反应速率大于逆反应速率
B. 20min 时A 的反应速率为0.05m ol/(L·min)
C. 反应方程式中的x =1,正反应为吸热反应
D. 30min 时降低温度,40min 时升高温度
三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题不给分) 18. 下列反应的离子方程式书写正确的是
A. 向碳酸氢铵溶液中加入足量氢氧化钠溶液:NH 4++OH -→NH 3·H 2O
B. 氢氧化钠溶液中通入少量二氧化硫:SO 2 +2OH - → SO 32- + H 2O
C. 碳酸钙溶解于醋酸中:CaCO 3 +2H + → Ca 2++CO 2↑+H 2O
D. 碳酸氢钙溶液中加入足量的石灰水:Ca 2+
+ HCO 3-
+OH -
→ CaCO 3 ↓+H 2O
19. 下列分离或提纯物质的方法错误的是
20. 在密闭容器中,反应xA(g)+yB(g)
zC(g),达到平衡后测得A 气体的浓度为0.5
mol/L 。保持温度不变,将密闭容器的容积增加一倍,当达到新的平衡时,测得A 的浓度
为0.3 mol/L ,则下列叙述中正确的是 A. 平衡向正反应方向运动 B. x+y>z
C. 物质C 的体积分数减小
D. 物质B 的转化率增大
21. 右图是198K 时N 2与H 2反应过程中使用催化剂和不使用催化剂条件下能量变化的曲线图。下列叙述正确的是 A. 反应物总能量小于生成物总能量,反应为吸热反应
B. a 曲线是加入催化剂时的能量变化曲线
C. 使用催化剂可以影响该化学反应的反应热大小
D. 一定条件下在密闭容器中含有1mol 氮气与3mol 氢气,充分反应后放出热量92kJ 22. 下列叙述正确的是
A. 氨水和NH 4Cl 的混合液中,若c (Cl -) = c (NH 4+) 则c (OH -)一定等于c (H +)
B. 在0.1mol / L
NH 4C1溶液中,c (OH -
)= c (NH 3·H 2O) + c (H +
)
C. 某温度下0.1mol / L 的NaHB 溶液中,c (Na +) = 0.1mol / L ≥c (B 2-)
D. 0.1mol / L CH 3COONa 溶液中,c (Na +)>c (CH 3COO -)>c (H +)>c (OH -) 四、(本题共24分)
23. 【实验】向少量的Mg(OH)2悬浊液中,加入适量的饱和氯化铵溶液,固体完全溶解。 为解释这一实验现象,同学们开展热烈讨论: (1)大家一致认为氢氧化镁固体溶于水:Mg(OH)2(固)
Mg(OH)2(aq)
由于氢氧化镁是电解质,因此会发生电离①___________________(用方程式表示) (2)甲同学认为:由于NH 4Cl 溶液显酸性,H +与OH -反应生成水,导致了①平衡右移,沉淀溶
解。请用相关方程式表示NH 4Cl 溶液显酸性的原因_________________;
乙同学解释:由于NH 4Cl 电离出的NH 4+与Mg(OH)2电离出的OH -
结合,生成了弱的电解质NH 3·H 2O ,导致了①平衡右移,Mg(OH)2沉淀溶解。
(3)为了验证哪位同学的解释合理 ①丙同学通过查阅数据(见右图),选用下列试剂中的一种进行确定,他选用的试剂是___________(填写编号)。 a. NH 4NO 3 b. CH 3COONH 4
c. Na 2CO 3
d. NH 3·H 2O
并说明丙同学选择这一试剂的理由____________________________________。
②丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理________(填“甲”或“乙”);完成NH 4Cl 饱和溶液使Mg(OH)2悬浊溶解的离子方程式_____________________________。
24. 已知A 、B 、C 、D 是四种短周期非金属元素,它们的原子序数依次增大,A 元素的原子形成的阳离子就是一个质子,B 原子的最外层上s 电子数等于p 电子数,C 、D 在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体。 试回答:
(1)写出C 的原子结构示意图_______,D 原子的电子排布式_______。
有同学将B
原子最外层电子排布的轨道表示式写成:
,你认为_______(填
“正确”或“不正确”),若不正确,请写出正确的轨道表示式__________(若正确,此空不答)。
(2)A 、B 两种元素组成的化合物很多,其中只含有一种类型共价键的化合物名称为_______。BD 2是_______分子(填“极性”或“非极性”)。
(3)这四种元素可组成多种原子个数比的化合物,其中属于离子晶体的化合物的化学式有_______(任意写三种)。
(4)A 单质和C 单质在一定条件下反应生成化合物E ,E 分子的空间结构为_______,电子式为_______。
25. 合成氨工业对国民经济和社会发展具有重要的意义,合成氨气所需的氢气可以由水煤气分离得到。涉及反应信息如下: 反应①:C(s)+H 2O(g)
H 2(g) + CO(g) 平衡常数K 1
反应②:平衡常数 2222[H ][C O ]K [C O ][H O ]
?=?
(1)写出K 1的表达式 ;反应②的化学方程式为 。 (2)在恒容时,对反应①,不能判断该反应达到化学平衡状态的是 (填编号)。
a. 容器中压强不变
b. 混合气体中CO 浓度不变
c. υ(H 2)正=υ(H 2O)逆
d. c (H 2O) = c (CO)
(3)将一定量的H 2O(g)和CO(g)分别通入到体积为1L 的密闭容器中,在不同条件下进行反应,
2s
2p ↑ ↓ ↑
↑
得到以下三组数据: (I )实验1中,用CO 2表示反应开始到平衡的平均反应速率为 ;
(II )在实验3,当a =0.5、b =1时,要使c 、d 数据与实验2相同,且t <3,可以采取的措施为 (填编号)
a. 其它条件不变,温度T<900℃
b. 其它条件不变,温度T>900℃
c. 充入一定量氖气
d. 使用高效催化剂
(III )对于反应②,当升高温度时K 2 (填“增大”、“减小”或“不变”)。
五、(本题共24分)
26. M 是由两种阳离子、一种阴离子组成的化合物。某学习小组的同学对该化合物进行了研究。
(1)取M 的样品配成溶液,溶液呈棕黄色。将溶液分成三份,做了下列3组实验,分别检出A 、B 、C 三种离子。请完成下表中的空格: (2)取9.640 g M 配成溶液,加入足量的NaOH 溶液,得到红褐色沉淀,将沉淀过滤、洗涤、灼烧,冷却后称量。经过4次灼烧、称量得到的红棕色固体的质量数据如下表。
① 灼烧和称量时需用右图所示的仪器,它们的名称分别是: Ⅰ____________、Ⅱ____________。
1.610
Ⅱ
②此红棕色固体为_____(填化学式),其准确质量为____g。
③另取9.640 g M配成溶液,加入足量的BaCl
2
溶液,得到白色沉淀,将沉淀过滤、洗涤,干燥,称得其质量为9.320 g。由此小组同学推算出M的化学式为__________。
(3)将步骤(2)灼烧所得红棕色固体与铝粉按一定比例均匀混合,所得混合物叫做________剂。该混合物在一定条件下可以发生剧烈的化学反应并放出大量热,写出该反应的化学方程式:______________,工业上利用该类反应来______(写一用途)。
27. 元素周期表是指导我们系统学习化学的重要工具。
(1)元素周期表中每种元素的具体信息如右图例示:
从中可以获得氟元素的有关信息有(至少写出两点)_____________。
(2)元素周期表中,相邻近的元素在结构和性质上有许多相似之处。
①如,第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H
2O外,还有H
2
O
2
;碳
元素的氢化物除CH
4外,还有C
2
H
6
等;与之相似的氮元素的氢化物除NH
3
外,还有_____(填化
学式),其沸点比液氨_____ (填“高”或“低”),稳定性比氨_____( 填“好”或“差”),该氢化物与足量盐酸反应的化学方程式为_____________。
②氮原子间也可形成链状结构,假设氮原子间只以N—N键形式连接,并形成氢化物,则该系
列氢化物的通式为___________________。
(3)元素周期表中,相邻近的元素在结构和性质上
也有递变之处。右图中每条折线表示周期表ⅣA~
ⅦA中的某一族元素氢化物的沸点变化(每个小黑
点代表一种氢化物):
①其中a点代表的是__________(填化学式),该元素
在元素周期表中的位置是。
②非金属气态氢化物的沸点与_____________有关,
它们之间的关系为_______________________。
(4)下列关于元素周期表性质的说法中正确的是_________(填写编号)
a. ⅠA族元素的金属性比ⅡA族元素的金属性强
b. ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
c. 同周期非金属氧化物对应的水化物的酸性从左到右依次增强
d. 第三周期元素的离子半径从左到右逐渐减小
六、(本题共20分)
a
28. 丙烯是石油化工的重要原料,一定条件下可发生下列转化:
已知:
RC N RC O O H H 2O /H
+
(1)A 的结构简式为 。
(2)写出反应类型:反应① ;反应④ 。
(3)D 与足量乙醇反应生成E 的化学方程式为 。
(4)CH 3C B r
COOH CH 3
与足量NaOH 乙醇溶液反应的化学方程式为 。
(5)B 有多种同分异构体,写出其中既能发生银镜反应,又能发生酯化反应的2种同分异构体的结构简式: 、 。 29. 常温下,向25 mL 0.1 mol/L MOH 溶液中逐滴加入0.2 mol/L HA 溶液,曲线如图所示(体积变化忽略不计)。回答下列问题:
(1)由图确定MOH 为_____碱(填“强”或“弱”),理由是_______________________________。 (2)MOH 与HA 恰好完全反应时,溶液呈_____性(填
“酸”、“碱”或“中”),理由是(用离子方程式表示)_______;此时,混合溶液中由水电离出的c (H +
)___ 0.2 mol/L HA 溶液中由水电离出的c (H +
)(填“>”“<”或“=”)。 (3)分别写出B 、C 两点,混合溶液中各离子浓度的大小关系
B 点______________;
C 点_____________;
(4)D 点时,溶液中c (A -)+c (HA)________2 c (M +)(填“>”“<”或“=”);若此时测得混合溶液的pH = 3,则 c (HA) + c (H +) = __________mol/L 。
七、(本题共16分)
30. 在硫酸钠和碳酸镁的混合物中加入40 mL 某浓度盐酸,固体完全溶解,在标准状况下收集到0.448 L 二氧化碳。向反应后的溶液中加入含有0.025 mol 氢氧化钡的溶液,得到5.82g
pH
沉淀,此时溶液的pH=12,体积为200mL 。试求: (1)原混合物中MgCO 3的物质的量 (2)原混合物中硫酸钠的质量 (3)盐酸的物质的量浓度
31. 在实验室中,氮氧化物废气(主要成分NO 2和NO )可以用NaOH 溶液来吸收,以除去这些废气,其主要反应为:2NO 2 +2 NaOH →NaNO 2 + NaNO 3 + H 2O
NO + NO 2 + 2NaOH → 2NaNO 2 + H 2O
(1)NO 和NO 2的混合气体的组成可表示为NO x ,该混合气体通入NaOH 溶液被完全吸收时,x 的值可以为____________(填编号)。
a .1.1
b .1.2
c .1.5
d .1.8
(2)若用纯碱溶液处理氮氧化物废气,反应与上述类似,同时放出CO 2。 ①请写出纯碱溶液吸收NO 2的化学方程式。
。 ②现有标准状况下a 升NO 2
(其中N 2O 4体积分数为20%)和b 升NO 的混合气恰好被200mL Na 2CO 3溶液完全吸收,则a 、b 应满足的关系为:___________________;该Na 2CO 3溶液的物质的量浓度为 mol/L (用含a 、b 的代数式表示)。
③若在标准状况下,2.016 L 氮氧化物的混合气和0.896LO 2与1mol/LNa 2CO 3溶液50mL 恰好反应生成NaNO 3,则混和气体中N 2O 4与NO 2的体积比为______________(写出③的计算过程)。
参考答案及评分标准
23. (8分)(1)Mg(OH)2(固) Mg 2++2OH -
(1分),
(2)NH 4+ + H 2O
NH 3·H 2O + H +(2分)
(3)①b (1分)CH 3COONH 4溶液呈中性,滴入Mg(OH)2 悬浊液,若Mg(OH)2溶解,则说明乙同学解释正确,若Mg(OH)2不溶,则甲同学解释正确。(1分) ②乙(1分);Mg(OH)2+2NH 4+→Mg 2++2NH 3·H 2O (2分) 24.(9分)(1)
; 1s 22s 22p 4;正确(每空1分,共3分)
(2)甲烷;非极性;(每空1分,共2分)
(3)NH 4HCO 3、(NH 4)2CO 3、CH 3COONH 4(2分,合理即可,少写一个扣1分)
(4)三角锥形;H :N :H H
(每空1分,共2分)
25.(7分)(1)K 1 =
22[H ][C O ][H O ]
(1分) CO +H 2O H 2+CO 2 (1分)
(2)d (1分) (3)0.16mol/(L·min)(2分);d (1分);减小(1分) 26. (12分)(1)NH 4+
、血红、盐酸(每空1分,共3分) (2)①坩埚、电子天平;②Fe 2O 3,1.600(每空1分,共4分)
③(NH 4)Fe(SO 4)2·12H 2O (2分)
(3)铝热剂,2Al + Fe 2O 3 → 2Fe + Al 2O 3(条件:引燃),冶炼某些难熔金属(3分) 27.(12分)(1)元素符号、元素名称、质子数或原子序数、核电核数、相对原子质量、外层
电子排布(最外层电子数)(2分,合理即可,每答错一点扣一分,扣完为止) (2)①N 2H 4,高,差,N 2H 4+2HCl N 2H 6Cl 2 ;② N n H n+2(每空1分,共5分)
(3)①SiH 4,第三周期第IVA 族;②分子间作用力(或范德华力),除HF 、H 2O 、NH 3外,分子间作用力越强,气态氢化物的沸点越高(“除……外”不写,不得分)(每空1分,共4分)(4)c (1分)
CH 3
Br CH 3
CH
28. (10分)(1) (2分)
(2)加成反应、取代反应(共2分) (3)(2分)
(4)(2分)
(5)(2分)
29. (10分)(1)强;A 点时0. 1mol/L MOH 溶液的pH=13,说明它为强碱(共2分) (2)碱(1分);A —
+ H 2O
HA + OH —
(2分);>(1分)
(3)c (M +) = c (A -)> c (H +) = c (OH -) ;c (A -)>c (M +)> c (H +)> c (OH -) (共2分) (4)= ;0.05(由电荷守恒和物料守恒求得)(共2分) 七、(本题共16分)
30. (6分) (1)n(MgCO 3)=0.02mol (2分) (2)m(Na 2SO 4)=2.84g (2分) (3) 1.2 mol/L (2分)
31. (10分)(1)c 、d (2分)
(2)①2NO 2 + Na 2CO 3 → NaNO 2 + NaNO 3 + CO 2(2分) ②b
a ≥
6
5(或1.2a ≥b 、6a ≥5b )(2分),
1.2a +b m o l /L 8.
96(2分)③1:5 (2分)
+2N aO H
C H 2=C
C O O Na C H 3
+NaB r+2H 2O
醇
△
H 3
+2H 2O
C O O C O O C H 3
C
+ 2C 2H 5O C H 3
C O O H
C O O H C H 3C
C 2H 5C 2H 5
C H 3
C H O
O H C H 3
C
C H 3C H O
O H C H 2C H
2015届高三上学期期中考试语文试题 一、古代诗文阅读(29分) (一)默写常见的名句名篇(8分) 1、补写出下列名篇名句中的空缺部分。(8分) (1)民生各有所乐兮, (2),池鱼思故渊 (3)地崩山摧壮士死, (4)艰难苦恨繁霜鬓, (5),相逢何必曾相识 (6)沧海月明珠有泪, (7)人生如梦, (8)想当年,,气吞万里如虎。 (二)文言文阅读(15分) 阅读下面的文言文,完成2一5题。 马文升,字负图,貌瑰奇多力。登景泰二年进士,授御史。历按山西、湖广,风裁甚著。成化初,召为南京大理卿。满四之乱,录功进左副都御史,振巩昌、临洮饥民,抚安流移。绩甚著。是时败寇黑水口,又败之汤羊岭,勒石纪之而还。进右都御史,总督漕运。淮、徐、和饥,移江南粮十万石、盐价银五万两振之。孝宗即位,召拜左都御史。弘治元年上言十五事,悉议行。帝耕藉田,教坊以杂戏进。文升正色曰:“新天子当使知稼穑艰难,此何为者?”即斥去。明年,为兵部尚书,督团营如故。承平既久,兵政废弛,西北部落时伺塞下。文升严核诸将校,黜贪懦者三十余人。奸人大怨,夜持弓矢伺其门,或作谤书射入东长安门内。为兵部十三年,尽心戎务,于屯田、马政、边备、守御,数条上便宜。国家事当言者,即非职守,亦言无不尽。尝以太子年及四龄,当早谕教。请择醇谨老成知书史者,保抱扶持,凡言语动止悉导之以正。山东久旱,浙江及南畿水灾,文升请命所司振恤,练士卒以备不虞。帝皆深纳之。在班列中最为耆硕,帝亦推心任之,诸大臣莫敢望也。吏部尚书屠滽罢,倪岳代滽,岳卒,以文升代。南京、凤阳大风雨坏屋拔木,文升请帝减膳撤乐,修德省愆,御经筵,绝游宴,停不急务,止额外织造,振饥民,捕盗贼。已,又上吏部职掌十事。帝悉褒纳。正德时,朝政已移于中官,文升老,连疏求去,许之。家居,非事未尝入州城。语及时事,辄颦蹙不答。五年卒,年八十五。文升有文武才,长于应变,朝端大议往往待之决。功在边镇,外国皆闻其名。尤重气节,厉廉隅,直道而行。卒后逾年,大盗至钧州,以文升家在,舍之去。(节选自《明史·马文升传》) 2.对下列句子中加点的词解释,不正确的一项是()(3分) A.登景泰二年进士登:升职。 B.录功进左副都御史录:记载。 C.振巩昌、临洮饥民振:救济。 D.勒石纪之而还勒:铭刻 3.以下各组句子中,全都表明马文升劝谏皇上修身爱民内容的一组是()(3分) ①新天子当使知稼艰难②即非职守,亦言无不尽
WORD格式 2019年上海中考化学试卷及答案 六.选择题 27.氦是太阳中含量较多的元素,其元素符号为 A.H B.He C.N D.Cl 28.厨房中的物质放入足量的水中,充分搅拌,不能形成溶液的是 A.食用油 B.白醋 C. 白糖 D. 食盐 29属于有机物的是 一、C60 B.CO C.H2CO3 D. C2H6O 30.互为同素异形体的一组物质是 A.氢气与液氢 B.水银与银 C.干冰与冰 D. 氧气与臭氧 31.Cr2O3可以作某些化学反应的催化剂,其中Cr元素的化合价为 A.+2 B.+3 C.+5 D.+6 32.pH是水质监测的重要指标之一,下列水样酸性最强的是 A.pH=1.3的工业废水 B.pH=4.5的雨水 C.pH=7.0的蒸馏水 D.pH=7.3的矿泉水 33.在充满氧气的机器瓶中燃烧,产生明亮的蓝紫色火焰的物质是 C.木炭A.硫粉 B.铁丝 D.红磷 34.物质的俗名与化学式相对应正确的是 3 A.天然气:CO B.烧碱:Na2CO C.熟石灰:Ca(OH) 2D.烧碱:KOH 35.镁在二氧化碳中燃烧的化学方程式为 2Mg+CO2====C+2MgO。该反应 属于 A.化合反应 B.分解反应 C.置换反应 D. 复分解反应
36.用稀硫酸除铁锈的原理是 37.自来水厂对天然水进行人工净化的过程中,通常不会采用 A.电解 B.吸附 C.过滤 D.消毒 专业资料整理
WORD格式 38.右图为市售盐酸标签的部分内容,其 中36.0%~38.0%表示该盐酸中 A.氯元素含量 度 B.溶质溶解 C.溶质质量分数 D.溶质式量 39.物质不需要通过化学变化就能体现的性质是 A.可燃性 B.挥发性 C.不稳定性 D.还原性 40.加热胆矾的实验过程中,相关实验操作正确的是 41.在空气中放置较长时 间的锌片,表面会形成一 层薄膜,其中含有 2CO3。若该物质通过化合反 Zn(2OH) 应生成。反应物除了A.一种 B. Zn外,还有 两种 C. 1.N2 2.O2 三种 3.CO2 D. 4.H 四种 2O中的 42下图是某化学反应的示意图( 应可能为 O与o分别代表不同元素原子),该反 A.氢气的燃烧C.甲烷的燃烧 B. D. 水的电解 一氧化碳的燃烧 43.X可以发生如下反应:1.X+酸====盐+水;2.X+非金属氧化物====== 盐+水。X可能是 A.氧化铜 B.盐酸 C.氢氧化钠 D.碳酸钠 44.室温时,对100mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液 A. D.溶质质量相同
2011年全国普通高等学校招生统一考试 上海 化学试卷 (满分150分,答题时间120分钟) 相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Si-28 S-32 Cu-64 I-127 一、选择题(本大题共10分,每小题2分,只有一个正确选项) 1、 下列离子在稳定人体血液的pH 中起作用的是( ) A .Na + B .HCO 3- C .Fe 2+ D .Cl - 2、 从光合作用的反应原理6CO 2+6H 2O ???→叶绿素 光 C 6H 12O 6+6O 2可知碳是农作物生长的必需元素之一。关 二、选择题(本大题共36分,每小题3分,只有一个正确选项) 6、 浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是( ) A .酸性 B .脱水性 C .强氧化性 D .吸水性 7、 下列溶液中通入SO 2一定不会产生沉淀的是( ) A .Ba(OH)2 B .Ba(NO 3)2 C .Na 2S D .BaCl 2 8、 高炉炼铁过程中既被氧化又被还原的元素是( ) A .铁 B .氮 C .氧 D .碳 9、 氯元素在自然界有35Cl 、37C1两种同位素,在计算式34.969×75.77%+36.966×24.23%=35.453中( ) A .75.775%表示35C1的质量分数 B .24.23%表示35C1的丰度 C .35.453表示氯元素的相对原子质量 D .36.966表示37C1的质量数 10、草酸晶体(H 2C 2O 4?2H 2O )100℃开始失水,101.5℃熔化,150℃左右分解产生H 2O 、CO 和CO 2。用 加热草酸晶体的方法获取某些气体,应该选择已略去加热装置的气体发生装置是( )
上海市高三上学期理综-化学期末考试试卷 姓名:________ 班级:________ 成绩:________ 一、单选题 (共7题;共14分) 1. (2分)糖类、蛋白质都是人类必需的基本营养物质,下列关于他们的说法中正确的是() A . 葡萄糖属于单糖,不能被氧化 B . 淀粉、纤维素互为同分异构体 C . 蛋白质水解的最终产物是多肽 D . 重金属盐能使蛋白质变性 2. (2分) (2019高三上·广东期末) 下列说法正确的是() A . 聚乙烯塑料和天然橡胶均不能使溴水褪色 B . 2-丁烯分子中所有原子有可能在同一平面 C . 丙烯和环己烷的二氯代物的数目相同(不考虑立体异构) D . 将溴乙烷和氢氧化钠的乙醇溶液共热产生的气体通入溴水中,溶液褪色,说明有乙烯生成 3. (2分)在反应中,X元素的原子将电子转移给Y元素的原子,则下列说法正确的是() ①元素X被氧化②元素Y被氧化③元素X发生还原反应④元素Y发生还原反应 A . ①② B . ③④ C . ②③ D . ①④ 4. (2分)(2018·威海模拟) 连二亚硫酸钠(Na2S2O4)俗称保险粉,易被氧气氧化。利用如图装置,在锥形瓶中加入HCOONa、NaOH、CH3OH和水形成的混合液,通入SO2时发生反应生成保险粉和一种常见气体,下列说法错误的是()
A . 制备保险粉的离子方程式为HCOO-+OH-+2SO2=S2O42-+CO2↑+H2O B . NaOH溶液的主要作用是吸收逸出的CO2 C . 多孔玻璃球泡的作用是增大气体与溶液的接触面积,使SO2能被充分吸收 D . 为避免产生的Na2S2O4被O2氧化,使硫酸与亚硫酸钠先反应,产生的SO2排出装置中残留的O2 5. (2分) (2019高一下·桂林期中) 下列各组元素中,原子半径依次增大的是() A . I、Br、F B . Li、K、Na C . O、S、Al D . Li、F、Cl 6. (2分) (2019高一下·浙江期中) 金属-空气电池是以金属为燃料,与空气中的氧气发生氧化还原反应产生电能的一种特殊燃料电池。如图为钠-空气电池的装置示意图,其中电解液为含NaPF6的有机电解液,可传导Na+ .下列说法正确的是() A . 装置中电子转移途径:导线电解液 B . b电极为正极,发生还原反应
2018年上海市中考化学试卷 一、选择题(共20分) 1.(1分)属于纯净物的是() A.泉水B.河水C.雨水D.蒸馏水 2.(1分)氦气的化学式是() A.He B.H2C.Hg D.N2 3.(1分)属于氮肥的是() A.NH4NO3B.KCl C.K2SO4D.Ca(H2PO4)2 4.(1分)属于有机物的是() A.酒精B.碳酸C.金刚石D.二氧化碳 5.(1分)在水中能形成溶液的是() A.泥沙B.蔗糖C.植物油D.粉笔灰 6.(1分)自来水生产中起杀菌消毒作用的是() A.明矾B.氯气C.活性炭D.氯化铁 7.(1分)属于石墨化学性质的是() A.黑色B.质软C.稳定性D.导电性 8.(1分)四种溶液的pH如图所示,其中碱性最强的是() A.A B.B C.C D.D 9.(1分)物质俗称正确的是() A.K2CO3:纯碱B.CaCO3:熟石灰 C.Na2CO3:烧碱D.CuSO4?5H2O:胆矾 10.(1分)能用AgNO3溶液鉴别的一组物质是()A.HCl、KNO3B.HCl、MgCl2C.KNO3、NaNO3D.HCl、H2SO4 11.(1分)分子数相等的任何物质具有相同的() A.质量B.体积C.物质的量D.摩尔质量 12.(1分)水电解的化学方程式书写正确的是()
A .2H 2O 2H 2+O 2 B .H 2 O H 2↑+O 2↑ C .2H 2O 2H 2↑+O 2↑ D .2H 2O ═2H 2↑+O 2↑ 13.(1分)有关实验操作正确的是( ) A .A B .B C .C D .D 14.(1分)向盛有氢氧化钠溶液的烧杯中滴加稀硫酸,对反应前后烧杯中溶液分析错误的是( ) A .颜色改变 B .温度升高 C .碱性减弱 D .质量增加 15.(1分)关于氢气在氧气中燃烧的反应,叙述正确的是( ) A .产生蓝色火焰 B .产物无污染 C .证明水由氢气和氧气组成 D .反应的氢气和氧气的质量比为2:1 16. (1分)如图所示,在分别盛有100g 水的烧杯中放入KNO 3充分溶解,则说法正确的是( )
2019年上海市高考化学试卷 一、选择题 1.(3分)元素Og中文名为(气奥),是一种人工合成的稀有气体元素,下列正确的是() A.核外电子数是118 B.中子数是295 C.质量数是117 D.第六周期0族元素 2.(3分)下列变化中,只涉及物理变化的是() A.次氯酸漂白B.盐酸除锈C.石油分馏D.煤干馏 3.(3分)下列反应只需破坏共价键的是() A.晶体硅熔化B.碘升华C.熔融Al2O3D.NaCl溶于水4.(3分)下列固体质量增加的是() A.Cu加入氯化铁B.Zn加入硫酸 C.H2通入灼热氧化铜D.高温下水蒸气通入Fe 5.(3分)25℃时,0.005mol/L Ba(OH)2中H+浓度是() A.1×10﹣12mol/L B.1×10﹣13mol/L C.5×10﹣12mol/L D.5×10﹣13mol/L 6.(3分)所有原子处于同一平面的是() A.B. C.D.CH2=CH﹣C≡CH 7.(3分)已知有一种烃的结构类似自行车,简称“自行车烃”,如下图所示,下列关于它 的叙述正确的是() A.易溶于水B.可以发生取代反应 C.其密度大于水的密度D.与环己烷为同系物 8.(3分)聚异戊二烯的单体是()
A.B.(CH2)2C=CH﹣CH2 C.(CH3)2C=CH﹣CH2D. 9.(3分)下列说法错误的是() A.含有共价键的化合物是共价化合物 B.含有极性键的分子可能是非极性分子 C.有电子转移的反应是氧化还原反应 D.水溶液中能完全电离的电解质是强电解质 10.(3分)用镁带和稀硫酸反应产生氢气来测定氢气的气体摩尔体积,所用的步骤有①冷却至室温,②调节使水准管和量气管液面持平,③读数。正确的顺序是() A.①②③B.①③②C.③①②D.③②①11.(3分)关于离子化合物NH5(H有正价和负价)下列说法正确的是()A.N为+5价 B.阴阳离子个数比是1:1 C.阴离子为8电子稳定结构 D.阳离子的电子数为11 12.(3分)能证明亚硫酸钠中部分变质所需要的试剂是() A.硝酸钡,稀硫酸B.稀盐酸,氯化钡 C.稀硫酸,氯化钡D.稀硝酸,氯化钡 13.(3分)用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法正确的是() A.可以用酚酞代替指示剂 B.滴定前用待测液润洗锥形瓶 C.若氢氧化钠吸收少量CO2,不影响滴定结果 D.当锥形瓶内溶液由橙色变为红色,且半分钟内不褪色,即达到滴定终点
高三生命科学期中考试试卷 本试卷分为第Ⅰ卷和第Ⅱ卷两部分,满分150分.考试时间120分钟 请将所有答案写在答题纸上,否则不给分 第I 卷(共60分) 一、选择题(每题2分,共60分。每小题只有一个正确选项) 1.下列物质中同时含有磷和氮元素的是 A .丙酮酸 B .核苷酸 C .氨基酸 D .脂肪酸 2、微生物的种类繁多,下列微生物中属于原核生物的是 ①黏菌 ②酵母菌 ③蓝细菌 ④大肠杆菌 ⑤乳酸杆菌 A .①②③ B .②③④ C .③④⑤ D .①④⑤ 3、下列关于生物体内有机物的叙述正确的是 A. 脂质不参与生命活动的调节 B. 蛋白质是生物体主要的能源物质 C. 核酸是生物体储存遗传信息的物质 D. 糖类不参与细胞识别和免疫调节 4.生物体中的某种肽酶可水解肽链末端的肽键,导致 A .蛋白质分解为多肽链 B .多肽链分解为若干短肽 C .多肽链分解为氨基酸 D .氨基酸分解为氨基和碳链化合物 5、下列有关ATP 概念的叙述正确的是 ① ATP 是生物体内主要的贮存能量的物质 ② ATP 的能量主要储存在腺苷和磷酸之间的化学键中 ③ ATP 水解一般指ATP 分子中高能磷酸键的水解 ④ ATP 只能在线粒体中生成 ⑤ ATP 在生物细胞内普遍存在,是能量的“携带者”和“转运者”,有“能量货币”之称 A .①③ B . ③⑤ C .②④ D .④⑤ 6、某种植物细胞在浓度分别为200mmol ∕L 和400mmol ∕L 的M 物质溶液中,细胞吸收M 的速率都是10mmol ∕min ,通入空气后,吸收速率不变。对此现象最合理的解释是 A .细胞吸收M 的方式为自由扩散 B .细胞吸收M 需要载体蛋白的参与 C .细胞吸收M 的方式为主动运输 D .所需能量供应不足 7、以下关于微生物的叙述,正确的是 A.细菌芽胞在合适的条件下可萌发形成新的菌体,它是细菌的有性生殖方式 。 B.质粒是许多微生物细胞内独立于拟核外的能自主复制的DNA 分子。 C.光合细菌和蓝细菌都含有叶绿体,所以都能进行光合作用。 D.细菌核糖体是核酸和蛋白质合成的场所。 8.控制传染源是抑制微生物传染病传播的重要措施,下列做法属于对传染源进行控制的是 A .接种特效疫苗 B .设立隔离病房 C .注射相应抗体 D .室内定期通风 9.有机磷农药可抑制胆碱酯酶(分解乙酰胆碱的酶)的作用,对于以乙酰胆碱为递质的 突触来说,中毒后会发生 A .突触前膜的流动性消失 B .关闭突触后膜的Na+离子通道 班级__________ 考试号_________ 姓名______________ …………………………密○………………………………………封○………………………………………○线…………………………
市2018年中等学校高中阶段招生文化考试 (满分120分,考试时间120分钟) 理化试卷化学部分 相对原子质量(原子量): C—12 O—16 Mg—24 Cl—35.5 K—39 Mn—55 Fe—56 六、单项选择题(共12分) 29.下列属于物理变化的是………………………………………………………………()A.铁器生锈B.燃放烟花 C.洒水降温D.食品变质 30.2018年中国足球队进入“世界杯”,小小足球牵动着人们的心。化学物质中有一种由多个五边形和六边形组成的形似足球的笼状分子,称为“足球烯”(如右图),化学式(分子式)为C60。关于C60的说确的是…………………………………() A.属于单质B.属于混合物 C.碳元素的化合价为+4 D.式量(分子量)为60 足球烯结构模型 31.某元素的原子结构示意图为,有关该元素的说法错误的是 A.原子的核质子数为16 B.原子的核外有3个电子层 C.原子的最外层电子数为6 D.属于金属元素 32.氢气是一种绿色能源,科学家们最新研制出利用太阳能产生激光,再用激光使海水分解得到氢气的新技术,其中海水分解可以用化学方程式表示为:2H2O 2H2↑+O2↑。下列说法不正确的是…………………………………………………………………()A.TiO2在反应中作氧化剂B.水分解不产生污染物 C.TiO2在反应中作催化剂 D.该技术可以将太阳能转化为氢能33.现代人正进入以“室空气污染”为标志的第三个污染时期。以下不属于室空气污染
物的是………………………………………………………………………………()A.烹饪时产生的油烟 B.水果散发出的香味 C.石材释放出的有害放射性气体氡 D.劣质粘合剂释放出的甲醛等有毒物质 34.油画上的白色含铅颜料经过一段时间会变为黑色的硫化铅(PbS),使其恢复白色的方法是蘸涂双氧水(H2O2),发生如下反应:PbS+4H2O2PbSO4+4H2O。其中还原剂是………………………………………………………………………………………()A.PbS B.H2O2C.PbSO4D.H2O 35.下列固体物质通常呈蓝色的是………………………………………………………()A.二氧化锰B.无水硫酸铜 C.胆矾D.生石灰 36.室温下,饱和食盐水露置在空气中一段时间后,有少量固体析出,这是因为…()A.氯化钠溶解度变小B.溶液质量百分比浓度变小 C.溶剂质量减小 D.溶液变成不饱和溶液 37.某金属放入稀硫酸中.不产生气泡,该金属可能是………………………………()A.Mg B.Al C.Zn D.Ag 38.CO中混有少量水蒸气和CO2,要得到纯净、干燥的CO,可将该混合气体依次通过…………………………………………………………() A.灼热的CuO、浓H2SO4 B.浓H2SO4、灼热的CuO C.浓H2SO4、NaOH溶液D.NaOH溶液、浓H2SO4 39.17世纪人们认为水能变成土,1768年科学家拉瓦锡对此进行研究。他将一定量的蒸馏水加入特殊的蒸馏器,反复加热蒸馏101天,发现蒸馏器产生少量沉淀,称得整个蒸馏装置的总质量没变、水的质量也没变、沉淀的质量等于蒸馏器减少的质量。对于这项研究的说法错误的是……………………………………………………………() A.精确称量是科学研究的重要方法 B.水在长时间加热后能转变为土 C.物质变化过程中总质量守恒 D.沉淀物来自于蒸馏器本身 40.等质量的碳、镁、铁分别在足量的氧气中充分燃烧,消耗氧气的质量比是……()
2016年上海市高考化学试卷 一、选择题(本题共10分,每小题2分,每题只有一个正确选项) 1.(2分)轴烯是一类独特的星形环烃。三元轴烯()与苯()A.均为芳香烃B.互为同素异形体 C.互为同系物D.互为同分异构体 2.(2分)下列化工生产过程中,未涉及氧化还原反应的是() A.海带提碘B.氯碱工业C.氨碱法制碱D.海水提溴 3.(2分)硼的最高价含氧酸的化学式不可能是() A.HBO2B.H2BO3C.H3BO3D.H2B4O7 4.(2分)下列各组物质的熔点均与所含化学键的键能有关的是()A.CaO与CO2B.NaCl与HCl C.SiC与SiO2D.Cl2与I2 5.(2分)烷烃的命名正确的是() A.4﹣甲基﹣3﹣丙基戊烷B.3﹣异丙基己烷 C.2﹣甲基﹣3﹣丙基戊烷D.2﹣甲基﹣3﹣乙基己烷 二、选择题(本题共36分,每小题3分,每题只有一个正确选项) 6.(3分)能证明乙酸是弱酸的实验事实是() A.CH3COOH溶液与Zn反应放出H2 B.0.1 mol/L CH3COONa溶液的pH大于7 C.CH3COOH溶液与Na2CO3反应生成CO2 D.0.1 mol/L CH3COOH溶液可使紫色石蕊变红 7.(3分)已知W、X、Y、Z为短周期元素,原子序数依次增大.W、Z同主族,X、Y、Z同周期,其中只有X为金属元素.下列说法一定正确的是()A.原子半径:X>Y>Z>W B.W的含氧酸的酸性比Z的含氧酸的酸性强 C.W的气态氢化物的稳定性小于Y的气态氢化物的稳定性
D.若W与X原子序数差为5,则形成化合物的化学式为X3W2 8.(3分)图1是铜锌原电池示意图.图2中,x轴表示实验时流入正极的电子 的物质的量,y轴表示() A.铜棒的质量B.c(Zn2+)C.c(H+)D.c(SO42﹣) 9.(3分)向新制氯水中加入少量下列物质,能增强溶液漂白能力的是()A.碳酸钙粉末B.稀硫酸 C.氯化钙溶液D.二氧化硫水溶液 10.(3分)一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中和代表不同元素的原子. 关于此反应说法错误的是() A.一定属于吸热反应B.一定属于可逆反应 C.一定属于氧化还原反应D.一定属于分解反应 11.(3分)合成导电高分子化合物PPV的反应为: 下列说法正确的是() A.PPV是聚苯乙炔 B.该反应为缩聚反应 C.PPV与聚苯乙烯的最小结构单元组成相同 D.1 mol 最多可与2 mol H2发生反应 12.(3分)下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是() A.氧化镁中混有氧化铝B.氯化铝溶液中混有氯化铁
上海市高三上学期化学期末考试试卷 姓名:________ 班级:________ 成绩:________ 一、单选题 (共16题;共16分) 1. (1分)下列物质加入水中,能使水的电离程度增大,且所得溶液显酸性的是() A . CH3COOH B . Al2(SO4)3 C . NaOH D . Na2CO3 2. (1分) (2018高一上·攀枝花期末) 盛放氢氧化钠固体的试剂瓶上应贴的危险化学品标志是() A . B . C . D . 3. (1分)下列性质中不是所有金属共有的是() A . 不透明 B . 易与氧气反应
C . 易导热 D . 易导电 4. (1分) (2018高二上·腾冲期中) 如图为某原电池的结构示意图,下列说法中正确的是() A . 原电池工作时阴离子移向铜极 B . 原电池工作时Zn发生氧化反应 C . 原电池工作时阳离子移向锌极 D . 原电池工作时电子通过电解质由Zn流向Cu 5. (1分)设 NA 为阿伏加德罗常数的值,下列有关说法正确的是() A . 标准状况下,6.72 L NO2 与水反应转移的电子数为 0.1NA B . 1 mol Na2O 和 Na2O2 混合物中含有的阴、阳离子总数是 3NA C . 1 mol Cl2 与足量 Fe 反应转移电子数一定为 3NA D . 1 L 0.1 mol/L 的碳酸钠溶液中的阴离子总数等于 0.1NA 6. (1分)下列有关镀锌钢管的叙述正确的是() A . 电镀时,钢管做阳极,锌棒做阴极,锌盐溶液做电解质溶液 B . 钢管镀锌后,镀锌层破损后,钢管不能受到保护 C . 镀锌的目的是为了在钢管表面形成 Fe-Zn 合金,增强钢管的耐腐蚀能力 D . 镀锌层破损后,钢管仍可受到保护 7. (1分)参照反应Br+H2―→HBr+H的能量对反应历程的示意图(图甲)进行判断。下列叙述中错误的是()
学军中学2015届高三上学期期中考试 语文试题 一、文言文阅读(42分) (一)阅读下面的文言文,完成后面题目。 张建封,字本立,邓州南阳人,客隐兖州。少喜文章,能辩论,慷慨尚气,自许以功名显.。李光弼镇河南,盗起苏、常间,残掠乡县。代宗诏中人马日新与 光弼麾下皆讨。建封见中人,请前喻贼,可不须战。因到贼屯开譬祸福,一日降数千人,纵还田里,由是知名。时马燧为三城镇遏使雅知之表为判官擢监察御史燧伐李灵耀军中事多所诹访杨炎将任以要职卢杞不喜出为岳州刺史①。 李希烈既破梁崇义,跋扈不臣,寿州刺史崔昭与相闻,德宗召宰相选代昭者,杞仓卒不暇取它吏,即白用建封。希烈数败王师,张.甚,遂僭即天子位。是时, 四方尚多故,乃缮陴隍,益治兵,四鄙附悦。希烈使票帅悍卒来战,建封皆沮衄之。贼平,进封阶。 是时,宦者主宫市,无诏文验核,但称宫市,则莫敢谁何.,大率与直十不偿 一。又邀阍闼②所奉及脚佣,至有重荷趋肆而徒返者。有农卖一驴薪,宦人以数尺帛易之,又取它费,且驱驴入宫,而农纳薪辞帛,欲亟.去,不许,恚曰:“惟有 死耳!”遂击宦者。有司执之以闻,帝黜宦人,赐农帛十匹,然宫市不废也。谏臣交章列上,皆不纳,故建封请间为帝言之,帝颇顺听。会诏书蠲民逋赋,帝问何如,答曰:“残逋积负,决无可敛,虽蠲除之,百姓尚无所益。” 治徐凡十年,躬于所事,一军大治。善容人过,至健黠亦未尝曲法假之。其言忠义感激,故下皆畏悦。性乐士,贤不肖游其门者礼必均,故其往如归。许孟容、韩愈皆奏署幕府,有文章传于时。 (《新唐书·卷一五八·列传第八十三·张建封传》) 【注】①马燧、李灵耀、杨炎、卢杞均为人名。②阍闼:宫门。 1.对下列句子中加点的词语的解释,不正确的一项是()(3分) A、慷慨尚气,自许以功名显.显:显扬 B、希烈数败王师,张.甚张:张狂 C、但称宫市,则莫敢谁何.何:怎样
2015年普通高等学校招生全国统一考试上海化学试卷 相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Ca-40 一、选择题(本题共10分,每小题2分,每题只有一个正确选项) 1.中国科学技术名词审定委员会已确定第116号元素Lv的名称为 293的叙述错误的是A. 原子序数116B. 中子数177C. 鉝。关于Lv 116 核外电子数116D.相对原子质量293 2.下列物质见光不会分解的是A. HClO B. NH4ClC. HNO3D. AgNO3 3.某晶体中含有极性键,关于该晶体的说法错误的是A.不可能有很 高的熔沸点B. 不可能是单质C. 可能是有机物D. 可能是离子晶体 4.不能作为判断硫、氯两种元素非金属性强弱的依据是 A. 单质氧化性的强弱 B.单质沸点的高低 C. 单质与氢气化合的 难易D. 最高价氧化物对应的水化物酸性的强弱 5.二氧化硫能使溴水褪色,说明二氧化硫具有A.还原性 B. 氧化 性C. 漂白性D. 酸性 二、选择题(本题共36分,每小题3分,每题只有一个正确选项) 6.将Na、Na2O、NaOH、Na2S、Na2SO4分别加热熔化,需要克 服相同类型作用力的物质有A. 2种B. 3种C. 4种D. 5种 7.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试 剂是 A. NaOH B. KMnO4 C. KSCN D. 苯酚
8.已知H2O2在催化剂作用下分解速率加快, 其能量随反应进程的变化如下图所示。下列 说法正确的是 A. 加入催化剂,减小了反应的热效应 B. 加入催化剂,可提高H2O2的平衡转化率 O2 + Q D.反应 C. H2O2分解的热化学方程式:H2O2 → H2O + 1 2 物的总能量高于生成物的总能量 9.已知咖啡酸的结构如右图所示。关于咖啡酸的描述 正确的是A. 分子式为C9H5O4 B. 1mol咖啡酸最多可与5mol氢气发生加成反应 C.与溴水既能发生取代反应,又能发生加成反应 D. 能与Na2CO3溶液反应,但不能与NaHCO3溶液反应 10.卤代烃的制备有多种方法,下列卤代烃不适合由相应的烃经卤代 反应制得的是 A. B. C. D. 11.下列有关物质性质的比较,错误的是 A. 溶解度:小苏打<苏打 B. 密度:溴乙烷>水 C. 硬度:晶体硅<金刚石 D. 碳碳键键长:乙烯>苯 12.与氢硫酸反应有沉淀生成的电解质是A.硫酸铜 B. 氢氧化钠 C. 硫酸亚铁D. 二氧化硫 13.实验室回收废水中苯酚的过程如右图所示。下列分析错误的是A. 操作I中苯作萃取剂B. 苯酚钠在苯中的溶解度比在水中的大C.
北京市昌平一中高三上学期期中考试(数学理) [10月28日] 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共120分.考试时间150分钟. 第Ⅰ卷(选择题共40分) 注意事项: 1.答第Ⅰ卷前,考生务必将自己的班级、姓名、学号填写在相应位置上. 2.每小题选出答案后,把答案填写在机读卡上.如需改动,用橡皮擦干净后,再选填其他答案标号. 一、本大题共8小题,每小题5分,共40分.在每小题列出的四个选项中,选出符合题目要求的一项. 1. 已知集合{} lg 0A x x =>, { }220 B x x x =-<,则A B ?= ( ) A . {}210x x << B .{}110x x << C .{}12x x << D .{}02x x << 2. 已知p :关于x 的不等式2 20x ax a +-≥的解集是R ,q :01<<-a ,则p 是q 的 ( ) A .充分非必要条件 B .必要非充分条件w.w.w.k.s.5.u.c.o.m C .充分必要条件 D .既非充分又非必要条件 3. 函数x x g x x f -=+=122)(log 1)(与在同一直角坐标系下的图象大致是( ) A B C D 4. 从4名男生和3名女生中选出3人,分别从事三项不同的工作,若这3人中至少有1名女生,则选派方案共有( ) A .186种 B .31种 C .270种 D . 216种 5. 等差数列{ n a }中, ,数列022112 73=+-a a a {n b }为等比数列,且 77 b a =,则 8 6b b 的值 为( ) A .2 B .4 C .8 D.16 6. 右图是函数 2 ()f x x ax b =++的部分图象,则函数的零点所在的区间是( ) A . B . C . D . 7.设,a b R ∈,若33是3a 与3b 的等比中项,则b a 22+的最小值是( ) ()ln ()g x x f x '=+11(,)42(1,2)1 (,1)2(2,3)
——教学资料参考参考范本—— 【中考化学】2019- 2020最新上海市中考化学试题(word版含解析) ______年______月______日 ____________________部门
一、选择题:共20分。 1.(1分)(20xx?上海)空气中含量最多的气体是() O2B.N2C.H e D.C O2 A . 考点:空气的成分及各成分的体积分数. 专题:空气与水. 分析:根据空气中各成分的体积分数:按体积计算,大约是:氮气占78%、氧气占21%、稀有气体占 0.94%、二氧化碳占0.03%、其它气体和杂质占0.03%,进行分析判断. 解答:解:空气的成分按体积计算,大约是:氮气占78%、氧气占21%、稀有气体占0.94%、二氧化碳占0.03%、其它气体和杂质占0.03%. A、O2占21%,不是空气中含量最多的气体,故选项错误. B、N2占78%,是空气中含量最多的气体,故选项正确. C、氦气属于稀有气体中的一种,体积分数小于0.94%,不是空气中含量最多的气体,故选项错 误. D、二氧化碳占0.03%,不是空气中含量最多的气体,故选项错误. 故选:B. 点评:本题难度不大,熟记空气的成分及各成分的体积分数(口诀:“氮七八氧二一,零点九四是稀气; 还有两个零点三,二氧化碳和杂气”)是解答此类题的关健. 2.(1分)(20xx?上海)属于氮肥的是() A.K2CO3B.N a2SO4C.N H4HCO3D.C a(H2PO4)2 考点:常见化肥的种类和作用. 专题:常见的盐化学肥料. 分析:含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥. 解答:解:A、K2CO3中含有钾元素,属于钾肥. B、Na2SO4中不含氮元素,不属于氮肥. C、NH4HCO3中含有氮元素,属于氮肥. D、Ca(H2PO4)2中含有磷元素,属于磷肥. 故选:C. 点评:本题主要考查化肥的分类方面的知识,确定化肥中营养元素的种类、化肥的分类方法是正确解答此类题的关键. 3.(1分)(20xx?上海)加碘食盐中的“碘”是指() A.分子B.原子C.元素D.单质 考点:元素的概念. 专题:物质的微观构成与物质的宏观组成. 分析:食品、药品、营养品、矿泉水等物质中的“碘”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
中小学教育资源站 1 上海化学试卷 本试卷分为第I 卷(第1—4页)和第Ⅱ卷(第5—12页)两部分,全卷共12页。满分150分,考试时间120分钟。 第I 卷 (共66分) 考生注意: 1. 答第I 卷前,考生务必在答题卡上用钢笔或圆珠笔清楚填写姓名、准考证号、校 验码,并用铅笔正确涂写准考证号和校验码。 2. 第I 卷(1—22小题),由机器阅卷,答案必须全部涂写在答题纸上,考生应将代表正确答案的小方格用铅笔涂黑。注意试题题号和答题约编号一一对应,不能错位。答案需要更改时,必须将原选项用橡皮擦去,重新选择。答案不能写在试卷上,写在试卷上一律不给分。 3. 第Ⅱ卷第23题和第26题为分叉题,各分为A 、B 两题,考生可任选一题。若两题均做,一律按A 题计分。A 题适合使用二期课改新教材的考生解答,B 题适合使用一期课改教材的考生解答。 相对原子质量: H —1 C —12 N —14 O —16 Na —23 Al —27 S —32 Ca —40 Fe —56 一、 选择题(本题共10分),每小题2分,只有一个正确选项,答案涂写在答题纸 上。 1、下列化学名词正确的是( ) A 、三溴笨酚 B 、烧碱 C 、乙酸乙脂 D 、石 碳酸 2、有关化学用语正确的是( ) A 、乙烯的最简式C 2H 4 B 、乙醇的结构简式 C 2H 6O C 、四氯化碳的电子式Cl :C .. Cl ..Cl :Cl D 、臭氧的分子式O 3 3、据报道,科学家已成功合成了少量N 4,有关N 4的说法正确的是( ) A 、N 4是N 2的同素异形体 B 、N 4是N 2的同分异构体 C 、相同质量的N 4和N 2所含原子个数比为1:2 D 、N 4的摩尔质量是56g 4、下列金属冶炼的反应原理,错误的是( ) A 、2NaCl(熔融) →通电 2Na + Cl 2↑ B 、MgO + H 2 →△ Mg + H 2O C 、Fe 3O 4 + 4CO →高温 3Fe + 4CO 2 D 、2HgO → △ 2Hg + O 2↑ 5、以下命题,违背化学变化规律的是( )
高三上学期期中考试题(材料) 3.20XX年11月1日我国成功发射了“神舟八号”卫 星,右图是火箭点火升空瞬间时的照片,关于这一瞬间的火 箭的速度和加速度的判断,下列说法正确的是() A.火箭的速度很小,但加速度可能较大 B.火箭的速度很大,加速度可能也很大 C.火箭的速度很小,所以加速度也很小 D.火箭的速度很大,但加速度一定很小 10.(20XX年高考天津理综)质点做直线运动的位移x与时间t的关系为x=5t+t2(各物理量均采用国际单位制单位),则该质点() A.第1 s内的位移是5 m B.前2 s内的平均速度是6 m/s C.任意相邻的1 s内位移差都是1 m D.任意1 s内的速度增量都是2 m/s 3.正在沿平直轨道匀加速行驶的长为L的列车,保持加速度不变,通过长度为L的桥.车头驶上桥时的速度为v1,车头经过桥尾时的速度为v2,则列车过完桥时的速度为() A.v1v2 B.v22+v21 C.2v22+v21 D.2v22-v21 8.如图所示,以8 m/s匀速行驶的汽车即将通过路口,绿灯还有2 s将熄灭,此时汽车距离停车线18 m,该车加速时最大加速度大小为2 m/s2,减速时最大加速度大小为5 m/s2.此路段允许行驶的最大速度为12.5 m/s,下列说法中正确的有() A.如果立即做匀加速运动,在绿灯熄灭前汽车可能通 过停车线 B.如果立即做匀加速运动,在绿灯熄灭前通过停车线 汽车一定超速 C.如果立即做匀减速运动,在绿灯熄灭前汽车一定不能通过停车线 D.如果距停车线5 m处减速,汽车能停在停车线处 4.某物体运动的v-t图象如图所示,则下列说法正确的是()
2019学年第二学期徐汇区学习能力诊断卷 高三化学试卷 考试时间:60分钟总分:100分2020.5 考生注意: 1、本考试分设试卷和答题纸。试卷包括两部分,第一部分为选择题,第二部分为综合题。 2、作答必须涂或写在答题纸上,在试卷上作答一律不得分。 相对原子质量:O—16 C—12 Na—23 Cl—35.5 K—39 Mn—55 一、选择题(本题共40分,每小题2分,每题只有一个正确选项) 1.日常生活中,下列试剂或方法不能起到消毒、杀菌作用的是 A.75%酒精B.紫外线照射C.明矾D.84消毒液2.工业上获得大量乙烯的方法是 A.卤代烃消除B.煤高温干馏C.炔烃加成D.石油裂解3.下列分离提纯操作与物质溶解性无关的是 A.蒸馏B.萃取C.纸上层析D.分液 4.实验室保存下列试剂时应使用如图试剂瓶的是 A. 硝酸银固体 B. 烧碱溶液 C. 浓硝酸 D. 浓硫酸 5.能说明CS2是非极性分子的事实是 A.是对称的直线型分子B.CS2沸点高于CO2沸点 C.能在空气中燃烧D.分子中存在碳、硫双键 6.铟(49In)与铷(37Rb)同周期,与铝(13Al)同主族。下列说法正确的是 A.In位于第四周期第ⅢA族B.原子半径:In > Rb C.金属性:In>Al D.碱性:In(OH)3>RbOH 7.Be元素与Al元素性质相似,下列说法错误的是 A.BeCl2溶液呈酸性B.BeO能与NaOH溶液反应 C.Be(OH)2 不溶于弱碱D.蒸干BeCl2溶液可得BeCl2晶体 8.常温下,用下列试剂鉴别浓硫酸与稀硫酸,现象差异不大的是 A.pH试纸B.金属铜C.金属铁D.胆矾晶体9.下列有机物中,既能发生水解又能发生消去反应的是 A.乙醇B.一溴乙烷C.乙酸乙酯D.苯 10.化学家用锌片与铜片并夹以食盐水浸湿的布片叠成如右图所示装置,下列说法正确的是A.该装置将电能转化为化学能B.锌片上有H2生成 C.Cu片被还原D.Zn片被氧化 11.下列变化中,气体被氧化的是 A.C2H2通入酸性KMnO4溶液B.Cl2通入KBr溶液C.H2S通入CuSO4溶液D.NH3通入AlCl3溶液浸有食盐水的布片
最新高考化学精品资料 高三化学试卷 考生注意: 1.本试卷满分150分,考试时间120分钟。 2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答案必须涂或写在答题纸上;做在试卷上一律不评分。 3.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。 相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Ca-40 Fe-56 第I卷(共66分) 一、选择题(本题共10分。每小题2分,每题只有一个正确选项) 1.不属于“雾霾”等灾害性天气治理的措施是 A.外出时使用PM2.5口罩,减少有害物质的吸入 B.改燃煤为燃气,可减少废气中SO2等有害物质的量 C.利用太阳能、潮汐能、风力发电,以获取清洁能源 D.使用“乙醇汽油”,减少汽车尾气中有害气体的排放 2.2-氯丁烷常用于有机合成等,有关2-氯丁烷的叙述正确的是 A.分子式为C4H8Cl2 B.与硝酸银溶液混合产生不溶于稀硝酸的白色沉淀 C.微溶于水,可混溶于乙醇、乙醚、氯仿等多数有机溶剂 D.与氢氧化钠、乙醇在加热条件下的消去反应有机产物只有一种 3.在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列说法正确的是A.34S原子核内中子数为16 B.16O2比18O2沸点更低 C.2H+的酸性比1H+的酸性更强D.13C和15N原子核内的质子数相差2 4.某种解热镇痛药的结构简式为: 当它完全水解时,可能得到的产物有 A.2种B.3种C.4种D.5种 5.“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH 溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。
2018年秋四川省宜宾市四中高三期中考试 英语试题 第I卷(选择题,共100分) 第一部分:听力(共两节,满分30分) 第一节(共5 小题;每小题1.5分,满分7.5分) 听下面5段对话。每段对话后有一个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在试卷的相应位置。听完每段对话后,你都有10秒钟的时间来回答有关小题和阅读下一小题。每段对话仅读一遍。 1.What are the speakers doing? A. Preparing for camping. B. Buying sleeping bags. C. Cleaning up the car. 2.What does the man advise the girl to do now? A. Have lunch. B. Go to the park. C. Watch cartoons. 3.What can we infer about the man? A. He was in poor health. B. He didn’t give up drinking. C. He used to be a beer drinker. 4.What does the man ask the woman to do?
A. Turn off the phone. B. Talk outside the cinema. C. Make an apology to him. 5.What is probably the man? A. A reporter. B. A postman. C. A teacher. 第二节(共15小题;每小题1.5分,满分22.5分) 听下面5 段对话或独白。每段对话或独白后有几个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在试卷的相应位置。听每段对话或独白前,你将有时间阅读各个小题,每小题5秒钟;听完后,各小题将给出5秒钟的作答时间。每段对话或独白读两遍。 听下面一段材料,回答第6至7题。 6.Where did Andrew probably go? A. T o a golf course. B. To a grocery store. C. T o a mall downtown. 7.Why will the man go shopping with his sister? A. He needs some groceries. B. His wife wants him to leave the house. C. He needs a new window. 听下面一段材料,回答第8至10题。 8.Why is the man moving to New York? A. T o enjoy the city life. B. To visit his friends. C. T o find a better job. 9.How old is the man? A. 39 years old. B. 29 years old. C. 19 years old. 10. What does the man plan to do after he retires?