
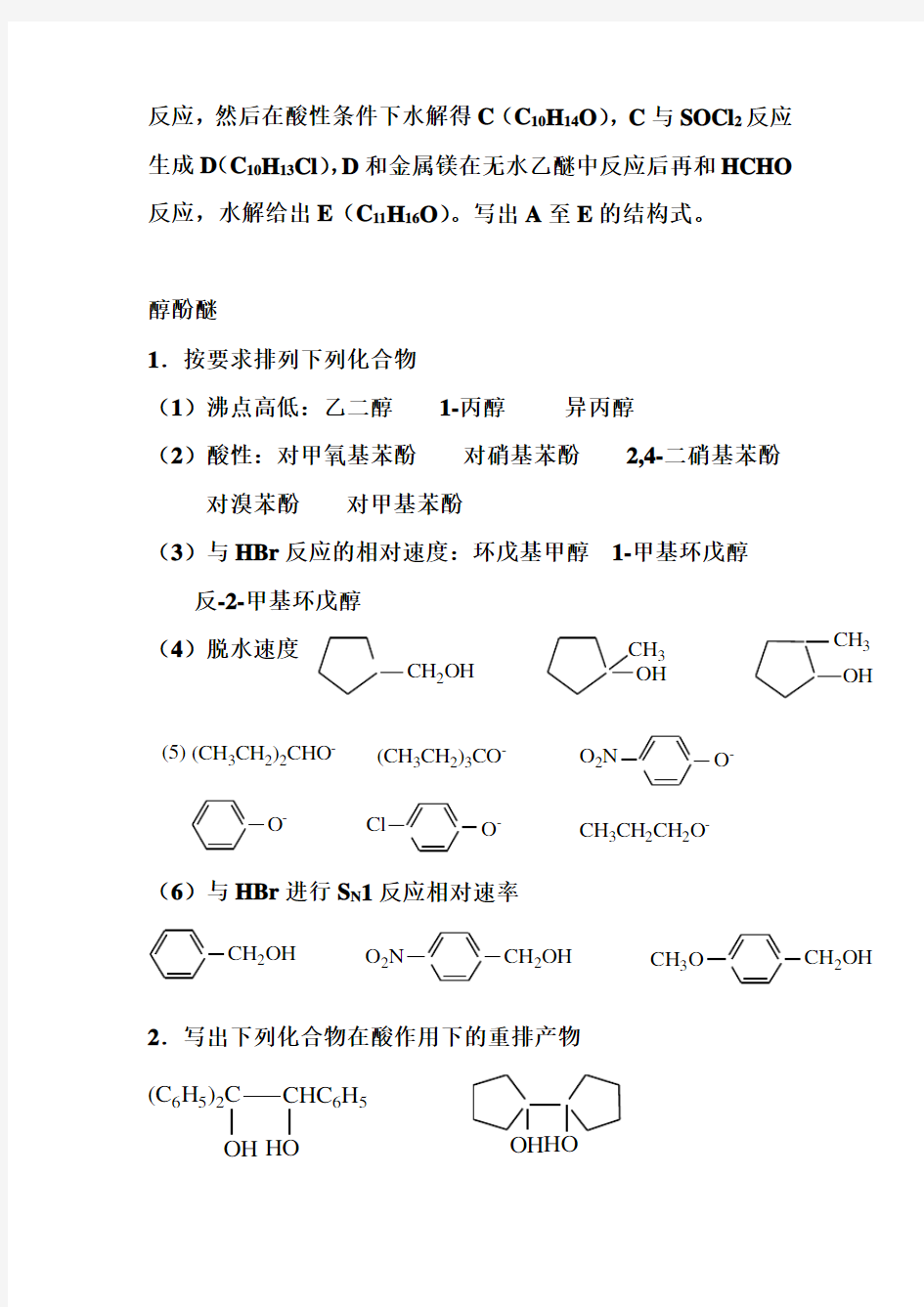
醛酮
1.按羰基活性排列下列化合物
2.按酸性强弱排列下列化合物
3.下列化合物哪些能发生碘仿反应?哪些能和NaHSO 3加成?
4.鉴别
(2)1-苯基乙醇 2-苯基乙醇 1-苯基乙烯醇
(3)丙醛 丙酮 丙醇 异丙醇
5.推断题
化合物A (C 3H 6O )和托伦试剂作用给出B ,A 与C 6H 5CH 2MgCl (1)(C H 3)3C C O C (C H 3)3C H 3C O C H O C H 3C O C H 2C H 3C H 3C H O
C H O (2)C 2H 5C O C H 3
C H 3C O C C l 3C O C 2H 5(1)(2)C H 3N O 2C H 3C H O C H 3C N C H 3C O C H 3O 2N C H 2N O 2C H 3C O C H 2C O C H 3
C 2H 5C O C H 2C O C 2H 5
C 6H 5C O C H 2C O C H 3C 6H 5C O C H 2C O C F 3
C H 3C O C 2H 5C H 3C H 2C H 2C H O
C H 3C H 2O H C H O C 2H 5C O C 2H 5C O C H 3C H 3C H O H C 2H 5(C H 3)3C C H O (1)C H 3C O C 6H 5C H O C 2H 5C O C 2H 5(C H 3)3C O H
C H 3(C H 2)3O H C H 3C H O
反应,然后在酸性条件下水解得C (C 10H 14O ),C 与SOCl 2反应生成D (C 10H 13Cl ),D 和金属镁在无水乙醚中反应后再和HCHO 反应,水解给出E (C 11H 16O )。写出A 至E 的结构式。
醇酚醚
1.按要求排列下列化合物
(1)沸点高低:乙二醇 1-丙醇 异丙醇
(2)酸性:对甲氧基苯酚 对硝基苯酚 2,4-二硝基苯酚 对溴苯酚 对甲基苯酚
(3)与HBr 反应的相对速度:环戊基甲醇 1-甲基环戊醇
反-2-甲基环戊醇
(4)脱水速度
(6)与HBr 进行S N 1反应相对速率
2.写出下列化合物在酸作用下的重排产物
C H 2O
H C H 3O H C H 3O H (5)(C H 3C H 2)2C
H O
-O 2N O -O -O -C l (C H 3C H 2)3C O -C H 3C H 2C H 2O -
O 2N C H 2O H C H 2O H C H 3O C H 2O H O H H O (C
6H 5)2C C H C 6H 5
O H H O
3.写出下列化合物A 、B 的结构式
4.写出酸性条件下
转化为 的反应过程。
5.鉴别
(1)环己烯 叔丁醇 氯化苄 苯 1-戊炔
环己基氯 环己醇
(2)邻甲苯酚 苯甲醇 3-丁烯-1-醇 环己烷 A + H IO 4H O O C (C H 2)4C H O
B + 3H IO
4
2H C O O H + 2C H 2O C H 2O H
第二节 醛 [学习目标定位] 1.能够通过对乙醛的学习,明确醛类的组成、结构和性质。2.学会根据醛基的性质来检验醛类的存在。3.知道甲醛、乙醛在生产生活中的应用。 1.物质 具有的官能团名称是醛基、羰基、羟基、羧基、碳 碳双键。 2.(1)乙醇催化氧化的方程式为 2CH 3CH 2OH +O 2――→催化剂 △2CH 3CHO +2H 2O 。 (2)乙二醇催化氧化的方程式为 (3)上述两个反应有机产物中的官能团是—CHO ,由烃基与醛基相连而构成的化合物称为醛,饱和一元醛的通式为C n H 2n +1CHO 或C n H 2n O 。 探究点一 乙醛的性质 1.乙醛是无色、具有刺激性气味的液体,密度比水小,易挥发,易燃烧,能跟水、乙醇等互溶。 2.按表中要求完成下列实验并填表:
(1)2化学方程式: △AgNO 3+NH 3·H 2O===AgOH↓+NH 4NO 3, AgOH +2NH 3·H 2O===Ag(NH 3)2OH +2H 2O , CH 3CHO +2Ag(NH 3)2OH――→△ CH 3COONH 4+2Ag↓+3NH 3+H 2O 。 △CuSO 4+2NaOH===Cu(OH)2↓+Na 2SO 4, 2Cu(OH)2+CH 3CHO +NaOH――→△CH 3COONa +Cu 2O↓+3H 2O 。 (2)乙醛在一定温度和催化剂存在下,也能被空气中的氧气氧化,方程式为 3.乙醛中的 和烯烃中的性质类似,也能与H 2发生加成反应,方程式 为CH 3CHO +H 2――→催化剂 △CH 3CH 2OH 。 [归纳总结] (1)醛的化学性质与乙醛类似:能发生氧化反应生成羧酸;能与H 2发生加成反应,被还原为醇。 (2)检验醛基的方法:△与银氨溶液反应生成银镜;△与新制的Cu(OH)2悬浊液反应生成红色
最新初三化学化学计算题试题经典 一、中考化学计算题 1.现将100 g溶质质量分数为9.8%的稀硫酸与一定质量的氯化钡溶液恰好完全反应后,过滤得到284.7 g滤液。计算: (1)生成硫酸钡沉淀的质量。 (2)氯化钡溶液中溶质的质量分数。 【答案】(1)生成硫酸钡沉淀的质量为23.3 g。(2)氯化钡溶液中溶质的质量分数为10%。【解析】 试题分析:解:设生成硫酸钡沉淀的质量为x,反应的氯化钡的质量为y。 H2SO4质量为:10 0g×9.8%=9.8 g BaCl2 + H2SO4 = BaSO4↓ + 2HCl 208 98 233 y9.8 g x 233/98 =x/9.8x=23.3 g 208/98 =y/9.8y=20.8 g (2)氯化钡溶液的质量为:284.7 g+23.3 g-100 g=208 g 氯化钡溶液的溶质质量分数为:20.8 g/208 g×100%=10% 考点:根据化学方程式的计算溶质的质量分数 2.氧化亚铜(Cu2O)可用于生产船底防污漆,防止海生物对船舶设备的污损。现将Cu2O 和Cu的固体混合物20g放入烧杯中,加入质量分数为24.5%的稀硫酸50g,恰好完全反应。已知:Cu2O+H2SO4═CuSO4+Cu+H2O.计算: (1)所加稀硫酸中溶质的质量为_____g。 (2)原混合物中Cu2O与Cu的质量比_____(写出计算过程,结果用最简整数比表示)(3)在图中画出向20g Cu2O和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,铜的质量变化曲线_____。
【答案】12.25 9: 1 。 【解析】 【分析】 根据加入的硫酸中溶质的质量和对应的化学方程式求算氧化亚铜的质量,进而求算对应的比值以及画图。 【详解】 (1)所加稀硫酸中溶质的质量为24.5%×50g =12.25g ;故填:12.25 (2)设原混合物中Cu 2O 的质量为x ,生成的铜的质量为y 。 224421449864x 12.Cu O+H SO CuSO +C 2u +H 5O g y ═ 1449864 ==x 12.25g y 解得:x =18 g ;y =8g ; 原混合物中Cu 2O 与Cu 的质量比为18 g :(20 g ﹣18 g )=9:1;故填:9:1 (3)没加入硫酸时,铜的质量为2g ,加入到50g 稀硫酸时铜的质量为2g+8g =10g 。如下图所示; 故填: 【点睛】 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。 3.现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成. (查阅资料)(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气. (2)相对原子质量:Mg ﹣24、Fe ﹣56、Zn ﹣65 (实验步骤及数据)取该混合物粉末8.0g 放入烧杯中,将140.0g 14.0%的稀硫酸分四次加
“妇女节”知识竞赛题库 1、女人往往会变得老样全因是身边出现许多催促女人衰老的东西,下列食品中那个不会催促女人人变老(C) A、白酒 B、烟雾尘埃 C、冰欺凌 D、铝制品 2、女性上火后不应吃哪种食物(C) A、黄瓜 B、绿茶 C、柚子 D、胡萝卜 3、生气会引起哪些疾病(A) A、心肌梗塞 B、脑细胞衰老加速 C、长色斑 D、胃溃疡 4、下列那个行为是正确的(B) A、洗脸可以用毛巾使劲搓 B、用冷水洗脸 C、晚上洗脸后涂抹日用护肤品 D、用冷水洗澡 5、吃阿司匹林后不能喝什么饮料(B) A、咖啡 B、果汁 C、茶 D、牛奶 6、佩戴隐形眼镜每天不能超过几小时(B) A、6小时 B、8小时 C、9小时 D、10小时 7、世界艾滋病防治的国际性标志是: (B) A、黄丝带 B、红丝带 C、绿丝带 8、妇女保健的目的(C )
A 降低孕产妇死亡率 B 促进社会进步 C 维护和促进妇女的健康 D 保证妇女婚姻自由 E 提高妇女自身素质 9、对妇女进行防癌普查的时间为( E ) A 每半年一次 B 每一年一次 C 每三年一次 D 每两年一次 E 每一至两年一次 10、预防子宫脱垂最关键的措施是( B ) A 积极开展计划生育 B 防治慢性气管炎和便秘 C 推行科学接生和做好产褥期保健 D 对老年人适当补充雌激素 E 加强营养、增强体质 11、如果发现乳房肿块应该怎么办(C) A、观察 B、热敷 C、就诊专科医院d自行按摩 12、过度肥胖会增加得乳腺癌的风险吗(B) A、不会B会C、不确定d因人而异? 13、下列哪项可引起乳腺不规律疼痛(D)A、胸罩不合适B、情绪波动C、劳累D、以上几项均是 14、哪些生活不良习性容易引发乳腺疾患(D)A、心情压抑B、缺乏运动C、睡眠不足D、以上均是? 15、保障妇女的合法权益是谁的责任(C)
高中化学选修4--化学平衡习题及答案解析
第三节化学平衡练习题 一、选择题 1.在一个密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) 已知反应过程中某一时刻,SO2、O2、SO3分别是0.2mol/L、0.1mol/L、0.2mol/L,当反应达到平衡时,可能存在的数据是() A.SO2为0.4mol/L,O2为0.2mol/L B.SO2为0.25mol/L C.SO2、SO3(g)均为0.15mol/L D.SO3(g)为0.4mol/L 2.在一定温度下,可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是() A. C生成的速率与C分解的速率相等 B. A、B、C的浓度不再变化 C. 单位时间生成n molA,同时生成3n molB D. A、B、C的分子数之比为1:3:2 3.可逆反应H2(g)+I2(g) 2HI(g)达到平衡时的标志是() A. 混合气体密度恒定不变 B. 混合气体的颜色不再改变 C. H2、I2、HI的浓度相等
D. I2在混合气体中体积分数不变 4.在一定温度下的定容密闭容器中,取一定量的A、B于反应容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g)C(g)+D(g)已达平衡的是() A.混合气体的压强B.混合气体的密度 C.C、D的物质的量的比值D.气体的总物质的量 5.在一真空密闭容器中,通入一定量气体A.在一定条件下,发生如下反应: 2A(g) B(g) + x C(g),反应达平衡时,测得容器内压强增大为P%,若此时A的转化率为a%,下列关系正确的是() A.若x=1,则P>a B.若x=2,则P<a C.若x=3,则P=a D.若x=4,则P≥a 6.密闭容器中,用等物质的量A和B发生如下反应:A(g)+2B(g) 2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C 的物质的量相等,则这时A的转化率为()
计划生育监督技能竞赛题必答题: 1、什么是计划生育技术服务? 答:是指使用手术、药物、工具、仪器、信息及其他技术手段,有目的地向育龄公民提供生育调节及其他有关的生殖保健服务的活动。 2、什么是产前诊断? 答:是指对胎儿进行先天性缺陷和遗传性疾病的诊断。 3、胎儿保健指什么? 答:指为胎儿生长发育进行监护,提供咨询和医学指导。 4、什么是新生儿保健? 答:为新生儿生长发育、哺乳和护理提供的医疗保健服务 5、孕产期保健是指? 答:各级各类医疗保健机构为准备妊娠至产后42天的妇女 及胎婴儿提供全程系列的医疗保健服务。 6、什么是新生儿疾病筛查? 答:是指在新生儿期对严重危害新生儿健康的先天性、遗传性疾病施行专项检查,提供早期诊断和治疗的母婴保健技术。 7、什么是母婴保健指导? 答:是指对孕育健康后代以及严重遗传性疾病和碘缺乏病的发病原因、治疗和预防方法提供医学意见。
8、什么叫“知情选择”? 答::通过宣传教育和良好服务,在育龄夫妻充分了解避孕措施情况、本地提供服务情况及育龄夫妻自身情况等的基础上,自主自愿地选择避孕节育措施。 9、什么是“社会主义新型生育文化”? 答:其主要内容有:晚婚晚育、少生优生、生男生女一样好、女儿也是传后人、男女平等和计划生育丈夫有责。 10、最佳结婚年龄是多少? 答:婚姻法规定结婚年龄男不得早于22 周岁,女不得早于20 周岁。这个法定年龄是结婚的最低年限。现实生活中,一般认为男25-30 岁,女23-28 岁为最佳结婚年龄。11、从事婚前医学检查的医疗保健机构和人员,应由其所在地的哪级卫生行政部门许可? 答:由其所在地的设区的市级人民政府卫生行政部门进行审查,符合条件的,在其《医疗机构执业许可证》上注明。 12、流动人口的计划生育工作应由谁负责管理? 答:流动人口的计划生育工作由其户籍所在地和现居住地的人民政府共同负责管理,以现居住地为主。
高三化学二轮-----------化学反应速率化学平衡 考点内容: 1、了解化学反应速度的概念,反应速度的表示方法,外界条件(浓度、温度、压强、催化剂等)对反应 速度的影响。 2、了解化学反应的可逆性,理解化平学平衡的涵义。掌握化学平衡与反应速度之间的内在联系。 3、理解勒沙特原理的涵义,掌握浓度、温度、压强等条件对化学平衡移动的影响。 4、本章命题以上述知识的综合应用和解决生产生活中的实际问题为主,考查学生运用知识的能力。 考点一:化学反应速率与化学反应速率的影响因素 . 化学反应速率的概念及表示方法:通过计算式:v =Δc /Δt来理解其概念: ①在同一反应中,用不同的物质来表示反应速率时,数值可以相同,也可以是不同的。但这些数值所表示的都是同一个反应速率。因此,表示反应速率时,必须说明用哪种物质作为标准。用不同物质来表示的反应速率时,其比值一定等于化学反应方程式中的化学计量数之比。 ②一般来说,化学反应速率随反应进行而逐渐减慢。因此某一段时间内的化学反应速率,实际是这段时间 内的平均速率,而不是瞬时速率。 ⑵. 影响化学反应速率的因素: I. 决定因素(内因):反应物本身的性质。 Ⅱ. 条件因素(外因)(也是我们研究的对象): ①浓度:其他条件不变时,增大反应物的浓度,可以增大活化分子总数,从而加快化学反应速率。值得 注意的是,固态物质和纯液态物质的浓度可视为常数; ②压强:对于气体而言,压缩气体体积,可以增大浓度,从而使化学反应速率加快。值得注意的是,如果 增大气体压强时,不能改变反应气体的浓度,则不影响化学反应速率。 ③温度:其他条件不变时,升高温度,能提高反应分子的能量,增加活化分子百分数,从而加快化学反应 速率。 ④催化剂:使用催化剂能等同地改变可逆反应的正、逆化学反应速率。 ⑤其他因素。如固体反应物的表面积(颗粒大小)、光、不同溶剂、超声波等。 【例1】可逆反应A(g)+ 4B(g)C(g)+ D(g),在四种不同情况下的反 应速率如下,其中反应进行得最快的是() A. v A==0.15mol/(L·min) B. v B==0.6 mol/(L·min) C. v C==0.4 mol/(L·min) D.v D==0.01 mol/(L·s) [例2]某温度时,在2 L容器中X、Y、Z三种物质的量随时间的变化曲线如图 所示。由图中数据分析,该反应的化学方程式为_________。反应开始至2 min, Z的平均反应速率为。 【例3】反应C(s)+H2O(g) CO(g)+H2(g)在可变容积的密闭容器中进行,下列 的改变,对化学反应速率的影响如何? A、增加碳的量____________________________________________ B、容器的体积缩小一半________________________________________ C、保持体积不变,充入N2,使体系的压强增大一倍_____________________________________ D、保持压强不变充入N2 ________________________________________ 【例4】下列关于催化剂的说法,正确的是() A.催化剂能使不起反应的物质发生反应 B.催化剂在化学反应前后,化学性质和质量都不变 C.催化剂能改变化学反应速率 D.任何化学反应,都需要催化剂 E.电解水时,往水中加少量NaOH,可使电解速率明显加快,所以NaOH是这个反应的催化剂
第二节醛 一、学习目标 1.了解乙醛的物理性质和用途。 2.掌握乙醛的主要化学性质。 3.掌握醛基的检验方法。 4.了解醛的分类和命名。 5.理解饱和一元醛的一般通性和同分异构现象。 二、教学过程 一、乙醛 1.结构 (1)乙醛的分子式为C2H4O,结构式为结构简式为CH3CHO。 (2)饱和一元醛的通式是C n H2n O(n≥1),其官能团是—CHO。 2.物理性质 乙醛是无色的液体,具有刺激性气味。沸点20.8 ℃,易挥发。溶解性是能与水、乙醇、乙醚等互溶。 3.化学性质 乙醛的官能团是醛基(—CHO),醛基较活泼,乙醛的化学性质由醛基决定。 (1)加成反应 写出乙醛与氢气反应的化学方程式: 该反应的机理是:乙醇在一定的条件下被催化氧化成乙醛,实质是脱去两个氢原子,我们称之为氧化反应,而乙醛与氢气加成是乙醇催化氧化的相反的过程,即还原反应。 (2)氧化反应 ①银镜反应: 向硝酸银溶液中逐滴加入少量的氨水,实验现象为产生白色沉淀,滴加氨水至沉淀刚好消失,实验现象为溶液变澄清,有关反应的离子方程式是 Ag++NH3·H2O===AgOH↓+NH4+, AgOH+2NH3·H2O===[Ag(NH3)2]++OH-+2H2O。 再向其中滴入几滴乙醛溶液放在水浴中,实验现象为试管内壁附着一层光亮的银,反应的方程式是: CH3CHO+2[Ag(NH3)2]OH===CH3COONH4+2Ag↓+3NH3+H2O。 据此反应,可应用于检验醛基。产物记忆要点:一水二银三氨,再加一摩羧酸铵。 ②乙醛与氢氧化铜悬浊液反应: 向盛有NaOH溶液的试管中,逐滴滴入CuSO4溶液,得到新制的氢氧化铜,实验中保证碱是过量的,使溶液呈碱性,然后加入几滴乙醛,加热至沸腾,实验现象为产生砖红色沉淀,发生反应的化学方程式为: CH3CHO+2Cu(OH)2 CH3COOH+Cu2O↓+2H2O,
化学计算题经典例题经典 一、中考化学计算题 1.化学兴趣小组取26g石灰石样品(杂质不参加反应,也不溶于水)放在烧杯中,向其中加入90g稀盐酸,恰好完全反应,反应后烧杯中物质的总质量为105g,计算: (1)生成二氧化碳的质量是____。 (2)反应后所得溶液的溶质质量分数是____。 【答案】(1)11克(2) 26.7% 【解析】 试题解析:由质量守恒定律可以知道反应前的各物质的总质量等于反应后各物质的总质量的,所以二氧化碳的质量=26+90-105=11克,反应后的溶质是CaCl2,而溶液的质量等于105克减去石灰石中的不反应的杂质的质量,设:石灰石中CaCO3质量为X,生成的CaCl2质量为Y, CaCO3+ 2HCl==CaCl2 + CO2↑ + H2O 100 111 44 X Y 11克 列比例式:100:X=44::11克解得:X=25克 111:Y=44:11克解得:Y="27.75" 克 反应后所得溶液的溶质质量分数=27.75/105-(26-25)×100%≈26.7% 考点:质量守恒定律及其根据化学方程式的计算溶液的相关计算 2.将25.6 g NaCl和MgCl2固体混合物完全溶于126 g水中配成溶液,再将200 g一定溶质质量分数的NaOH溶液不断加入该溶液中。充分反应后,测得的实验数据如下表。求: (1)上表中m的值为多少。___________ (2)恰好完全反应时,所得溶液中溶质的质量分数。___________ 【答案】8.7 10% 【解析】 【分析】 【详解】 (1)第一次加入40g氢氧化钠溶液质量得到沉淀2.9g,第四次实验加入40g氢氧化钠溶液生成沉淀增加了,说明第一次实验中40g氢氧化钠完全反应只能生成2.9g沉淀,所以第三
2019年三八妇女节知识竞赛试题库及答案 第一、二环节——抢答、必答题库 1、2013年3月8日是第(D)个国际劳动妇女节。 A、100 B、101 C、102 D、103 2、国际家庭日是哪天?(每年的5月15日) 3、偃旗息鼓“偃”的意思是: 答案D A.摘下 B.收起 C.停止 D.放倒 4、被称为酿酒行业的祖师是谁?(D) A、孔子 B、鲁班 C、柳永 D、杜康 5、以下属于我国婚姻法基本原则的有(C、D): A、诚实信用 B、等价有偿 C、男女平等 D、保护妇女、儿童 6、保障妇女的合法权益是谁的责任?(C) A、各级妇联组织 B、各级政府的 C、全社会的共同 D、工会 7、世界消除对妇女暴力日是哪月哪日?(A) A、11月25日 B、10月25日 C、9月25日 D、8月25日 8、什么运动可以使人产生安宁感并减轻应激反应?(A) A、有氧运动 B、剧烈运动 C、散步 D、瑜伽 9、母亲节、父亲节分别是哪一天?(五月的第二个星期天,六月的第三个星期天)中国的情人节是哪一天?中国的敬老节是哪一天?(农历7月初7,农历9月初9重阳节) 10、请说出下列特种电话号码的含义,110、119、120、122。(匪警、火警、急救、交通事故报警) 11、能够降低胆固醇,还能将妇女更年期的潮热反应减少到最低程度的食品是(C)。 A、菠菜 B、牛奶 C、豆腐 D、海带 12、妇女权益保障法是我国第一部以谁为主体、全面保护妇女各项合法权益的基本法?( B ) A、公民 B、妇女 C、妇女儿童 13、下面三项内容,哪一项是国务院制定的新时期妇女发展的总体规划?( C ) A、国民经济和社会发展第十个五年计划 B、国民经济和社会发展第十一个五年规划 C、《中国妇女发展纲要(2001—2010年)》 14、世界上最大的海是哪一个?(A ) A、中国的南海 B、黑海 C、中国的黄海 D、红海 15、世界上是被称为“教育王国”的哪一个国家?(C ) A、中国 B、美国 C、以色列 D、日本 16、妇女权益保障法规定:“制定法律、法规、规章和公共政策,对涉及妇女权益的重大问题,应当听取谁的意见?”( A ) A、妇女联合会 B、基层组织 C、国家健全机制 17、《义勇军进行曲》是哪部电影的主题歌? 答案C A.《塞上风云》 B.《十字街头》 C.《风云儿女》 D.《大路》 18、中华人民共和国年满多少周岁的公民,不分民族、种族、性别等限制都有选举权和被选举权?(C ) A、年满16周岁 B、年满14周岁 C、年满18周岁 19、世界上最早的国歌诞生于哪个国家?答案:C
化学平衡计算题求解技巧 知识体系和复习重点 一、化学平衡常数(浓度平衡常数)及转化率的应用 1、化学平衡常数 (1)化学平衡常数的数学表达式 (2)化学平衡常数表示的意义 平衡常数数值的大小可以反映可逆反应进行的程度大小,K 值越大,反应进行越完全,反应物转化率越高,反之则越低。 2、有关化学平衡的基本计算 (1)物质浓度的变化关系 反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度 其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。 (2)反应的转化率(α):α=(或质量、浓度) 反应物起始的物质的量(或质量、浓度)反应物转化的物质的量×100% (3)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论: 恒温、恒容时: ;恒温、恒压时:n 1/n 2=V 1/V 2 (4)计算模式(“三段式”) 浓度(或物质的量) aA(g)+bB(g) cC(g)+dD(g)
起始 m n O O 转化 ax bx cx dx 平衡 m-ax n-bx cx dx A 的转化率:α(A)=(ax/m )×100% C 的物质的量分数:ω(C)= ×100% 技巧一:三步法 三步是化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。但要注意计算的单位必须保持统一,可用mol 、mol/L ,也可用L 。 例1、X 、Y 、Z 为三种气体,把a mol X 和b mol Y 充入一密闭容器中,发生反应X + 2Y 2Z ,达到平衡时,若它们的物质的量满足:n (X )+ n (Y )= n (Z ),则Y 的转化率为( ) A 、%1005?+b a B 、%1005)(2?+b b a C 、%1005)(2?+b a D 、%1005)(?+a b a 解析:设Y 的转化率为α X + 2Y 2Z 起始(mol ) a b 0 转化(mol ) αb 2 1 αb αb 平衡(mol )- a α b 2 1 -b αb αb 依题意有:-a αb 21+ -b αb = αb ,解得:α= %1005)(2?+b b a 。故应选B 。 技巧二:差量法 差量法用于化学平衡计算时,可以是体积差量、压强差量、物质的量差量等等。
中考化学化学计算题专题经典 一、中考化学计算题 1.现将100 g溶质质量分数为9.8%的稀硫酸与一定质量的氯化钡溶液恰好完全反应后,过滤得到284.7 g滤液。计算: (1)生成硫酸钡沉淀的质量。 (2)氯化钡溶液中溶质的质量分数。 【答案】(1)生成硫酸钡沉淀的质量为23.3 g。(2)氯化钡溶液中溶质的质量分数为10%。【解析】 试题分析:解:设生成硫酸钡沉淀的质量为x,反应的氯化钡的质量为y。 H2SO4质量为:10 0g×9.8%=9.8 g BaCl2 + H2SO4 = BaSO4↓ + 2HCl 208 98 233 y9.8 g x 233/98 =x/9.8x=23.3 g 208/98 =y/9.8y=20.8 g (2)氯化钡溶液的质量为:284.7 g+23.3 g-100 g=208 g 氯化钡溶液的溶质质量分数为:20.8 g/208 g×100%=10% 考点:根据化学方程式的计算溶质的质量分数 2.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,均充分反应,实验数据如下: 第一次第二次第三次第四次第五次第六次 101010101010 加入稀硫酸的质量 (g) 剩余固体的质量(g)9.358.78.057.4 6.75 6.75 (1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同) (2)所用稀硫酸的质量分数为多少? 【答案】(1)32.5%;(2)9.8% 【解析】 质量分数的一种常用的计算方法是分别计算出目的物质的质量和样品的总质量,然后求比值。第(2)问中的化学反应方程式以及计算是关键。 (1)10g样品反应完全后,剩下6.75g为铜的质量,所以锌的质量为
附件二 计生协会知识竞赛试题参考答案 1、计划生育协会的性质 它是在中国共产党领导下,协助政府动员广大群众自愿实行计划生育,促进人口与经济、社会、资源、环境协调发展和可持续发展的全国性非营利群众团体。 2、计划生育协会的宗旨 《中国计划生育协会章程》规定:全心全意为人民服务是计划生育协会的唯一宗旨。 3、中国计划生育协会的主要职能: (1)贯彻实施《人口和计划生育法》及国家相关法律、法规,动员、组织群众依法实行计划生育。 (2)围绕人口、生殖健康和计划生育,加强培训,提高管理服务水平和能力。 (3)组织开展生殖健康、人口和计划生育群众性宣传工作,开展社区家庭计划指导,广泛普及性与生殖健康、计划生育、避孕节育和预防艾滋病等科学知识。
(4)开展“生育关怀行动”,努力为关怀对象排忧解难。 (5)依法参与村(居)民自治,建立和完善基层人口和计生民主管理和民主监督机制,反映会员诉求,维护会员和群众的合法权益,促进基层民主政治建设。 (6)整合募集社会资源,拓展服务领域,开展人口、生殖健康和计生公益活动,配合政府发展生殖健康、计生产业。 (7)加强计生协组织建设,健全完善管理制度和工作制度,促进自身建设。 4、中国计划生育协会成立时间? 1980年5月29日 5、我国什么时候把计划生育确定为一项基本国策? 1982年,我国正式把计划生育确定为我国的一项基本国策,确立了计划生育工作的重要地位。 6、计划生育协会会员小组长的职责是什么? 计划生育协会会员小组长兼有双重身份,既是计生活动组长,又是协会会员小组长,其主要职责是组织会员带动群众,开展"三自活动",起好宣传员、服务员、信息员、联络员、协管员等五员的作用。
化学平衡计算 一、有关概念 1、物质浓度的变化关系 反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度 其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。 2、反应的转化率(α):α=()() 反应物转化的物质的量或质量反应物起始的物质的量或质量、浓度、浓度×100% 3、在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论: 恒温、恒容时:12n n =12P P ;恒温、恒压时:12n n =12 V V 4、混合气体平均分子量的数学表达式 =M1×V1%+M2×V2%+M3×V3%+…式中表示混合气体的平均分子量。 M1,M2,M3分别表示混合气体中各组分的相对分子质量。V1%,V2%,V3%分别表示混合气体中各组分的体积分数。 在相同条件下,气体的体积分数等于气体的物质的量分数(组分气体的物质的量与混合气体总物质的量之比) 5、标三量法化学平衡计算的一般格式,根据题意和恰当的假设列出初始量、变化量、平衡量。这里的量可以是物质的量、物质的量的浓度、体积等。 计算模板: 浓度(或物质的量) a A(g)+b B(g)c C(g) +d D(g) 初始 m n 0 0 变化 ax bx cx dx 平衡 m-ax n-bx cx dx A 的转化率:α(A)=(ax /m )×100% C 的物质的量(或体积)分数:ω(C)= cx m ax n bx cx dx -+-++×100% 二、强化练习 1.在一密闭容器中,用等物质的量的A 和B 发生如下反应:A(g)+2B(g)2C(g),反应达到平衡时,若混合气体中A 和B 的物质的量之和与C 的物质的量相等,则这时A 的转化率为( ) A .40% B .50% C .60% D .70% 【答案】A 【解析】设A 、B 起始物质的量都为1mol ,A 的转化率为x A(g)+2B(g)2C(g) 起始(mol):1 1 0 转化(mol):1×x 2(1×x) 2(1×x) 平衡(mol):1-x 1-2x 2x 平衡时A 和B 的物质的量之和与C 的物质的量相等:(1-x)+(1-2x)=2x ,解得x=0.4。 2.X 、Y 、Z 为三种气体,把a molX 和b molY 充入一密闭容器中,发生反应: X +2Y 2Z ,达到平衡时,若它们的物质的量满足:n (X)+n (Y)=n (Z),则Y 的转化率为( )
第二节 醛 醛类:含“”官能团 1.与氢气加成——加氢还原:碳氧双键的一个价键断开,两端加氢; 反应条件:催化剂、加热 2.氧化反应——加氧氧化 (1)催化氧化: 反应条件:催化剂、加热 (2)银镜反应:(反应条件:水浴加热) 可用银氨溶液来检验醛基; (3)与Cu(OH)2反应(反应条件:加热) 可用Cu(OH)2来检验醛基; 【针对训练三】 1.不洁净玻璃仪器洗涤方法正确的是 ( ) A.做银镜反应后的试管用氨水洗涤 B.做碘升华实验后的烧杯用酒精洗涤 C.盛装苯酚后的试管用盐酸洗涤 D.实验室用KClO 3制取O2后的试管用稀HCl 洗涤 2.已知柠檬醛的结构简式为 ,根据所学知识判断下列说法 不正确的是( ) A .它可使酸性高锰酸钾溶液褪色 B .能发生银镜反应 C .与乙醛互为同系物 D .被催化加氢的最后产物是C 10H 22O 3.今有相对分子质量为58的几种有机物,试写出符合条件的有机物的结构简式 (1)若该有机物为烃,则可能的结构简式为: 、 。 (2)若该有机物是一种饱和一元醛,则其结构简式为: 。 (3)若该有机物1mol 能与足量银氨溶液作用可析出4molAg ,则有机物的结构简式为: 。 (4)若该有机物能与金属钠反应,又能使溴的四氯化碳溶液褪色,则该有机可能是: 。(注羟基连在双键上的有机物极不稳定) R —C —H +2Cu(OH)2 △ O ‖ R —C —O —H +Cu 2O +2H 2O ‖ O R —C —H +2Ag(NH 3)2OH △ O ‖ R —C —ONH 4+2Ag ↓+3NH 3+H 2O ‖ O 催化剂 △ 2R —C —H +O 2 O ‖ 2R —C —O —H ‖ O R —C —H +H 2 O ‖ R —C —O —H ︳ ︳ H H 催化剂 △ —C —H O ‖
初三化学计算题 1.用氯酸钾和二氧化锰的混合物16g,加热制取氧气,待完全反应,冷却后称量,得到11.2g固体物质,计算原混合物中二氧化锰的质量(计算结果保留二位小数)。 2.刘彬同学的姑父从三峡搬迁到我们家乡后,准备兴建一座碳酸钙精粉厂。为检测当地石灰石中碳酸钙的纯度,他在实验室用6g石灰石样品(杂质不参加反应)与19g稀盐酸恰好完全反应,测得残留物为22.8g。求: (1)依椐质量守恒定律,生成二氧化碳g; (2)样品中碳酸钙的质量分数; (3)所用稀盐酸溶液中溶质的质量分数。 3、某工厂的废料中含铁和铜,需回收此废料中的铜.现取铁和铜的混合物样品l0g,向其中加入废弃的稀硫酸50g恰好完全反应,产生0.1gH2。 求:①废料中铜的质量分数。 ②废弃稀硫酸中硫酸的质量分数。 7.取碳酸钠和氯化钠的固体混合物13,6g,与质量为73g的稀盐酸恰好完全反应?产生二氧化碳气体的质量为4.4g,计算: (1)固体混合物中碳酸钠的质量 (2)该稀盐酸中溶质的质量分数 (3)反应所得的溶液中溶质的质量分数(最后结果保留一位小数) 9.(6分) 小华想测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器。 (1)你认为能测出其铜的质量分数的是____________合金; (2)小华取该合金的粉末32.5g,与足量该盐酸充分反应,经测定,产生了0.4g气体请求出该合金中铜的质量分数。 (3)若想测出该盐酸的质量分数,你认为实验时必须提供和测出的数据是_________(选填序号)。 A.参加反应的合金质量B.参加反应的稀盐酸的质量 C.参加反应的稀盐酸的体积和密度D.产生气体的质量 17、(本题要求写出计算过程) 将1.80g不纯的氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,过滤后得到溶质质量分数为20.0%的溶液5.85g。求: (1)样品中氯化铜的质量分数 (2)加入氢氧化钠溶液的质量。 答案: 1.解:设原混合物中KClO3质量为x,依题意可知完全反应后生成氧气的质量为: 16g-11.2g=4.8g(1分) MnO2 由2KClO3=====2KCl+3O2↑(1分) △ 2.44 3.(5分)(1)解:设质量为x的这种稀硫酸可与4.0gCuO恰好完全反应 CuO +H2SO4 =CuSO4 +H2O(2分) 80 98 4.0g 10% x =(1分)
1、在200 o C下的体积为V的容器中,下列吸热反应达到平衡态,通过以下各种措施,反应NH4HS(s)=NH3(g)+H2S(g)再达到平衡态时,NH3的分压跟原来相比,有何变化? A、增加氨气; B、增加硫化氢气体; C、增加固体NH4HS; D、增加温度; E、加入氩气以增加总压; F、把反应容器的体积增加到2 V。 2、PCl5的分解作用为:PCl5(g) ===PCl3(g) +Cl2(g),在523.2 K、101325 Pa下反应到达平衡后,测得平衡混合物的密度为2.695 kg·m–3,试计算该反应在523.2 K下的标准平衡常数。M(PCl5)=208.2 3、在1000 K时,理想气体反应CO(g)+H2O(g)===CO2 (g) + H2(g)的KΦ=1.43。设有一反应系统,各物质的分压分别为p(CO)=0.500 MPa,p(H2O)=0.200 MPa,p(CO2)=0.300 MPa,p(H2)=0.300 MPa。试计算: (1)此反应条件下的Δr G m,并说明反应的方向。 (2)已知在1200 K时KΦ=0.73,试判断反应的方向。 (3)求该反应在1000~1200 K范围内的Δr H mΦ和Δr S mΦ。 4、在机械制造业中,为了消除金属制品中的残余应力和调整其内部组织,常采用有针对性的热处理工艺,以使制品机械性能达到设计要求。CO和CO2的混合气氛用于热处理时,调节CO/CO2既可成为氧化性气氛(脱除钢制品中的过量碳),也可成为还原性气氛(保护制品在处理过程中不被氧化或还原制品表面的氧化膜)。反应式为Fe(s)+CO2(g)=FeO (S)+CO(g)。已知在1673 K,2CO(g)+O2(g)=2CO2(g),△r G mΦ=–278.4 kJ·mol-1;2Fe(s)+O2(g)=2FeO(s),△r G mΦ=–311.4 kJ·mol-1 混合气氛中含有CO、CO2及N2(N2占1.00%,不参与反应) (1)CO/CO2比值为多大时,混合气氛恰好可以防止铁的氧化? (2)此混合气氛中CO和CO2各占多少百分比? (3)混合气氛中CO和CO2的分压比、体积比、物质的量比及质量比是否相同?若相同,写出依据,若不同,请说明相互换算关系。 (4)若往由上述气氛保护下的热处理炉中投入一定的石灰石碎片,如气氛的总压不变(设为101.3 kPa),石灰石加入对气氛的氧化还原性有何影响?已知298.15 K时碳酸钙分解反应的Δr H mΦ=179.2 kJ·mol-1;Δr S mΦ=160.2 J·K-1·mol-1。 5、若用298 K液态水与氧作用不能形成H2O2,但湿的锌片与氧作用却能产生H2O2(耦合反应)。 (1)分析反应H2O(l)+1/2 O2(g)==H2O2(l)不能自发进行的原因; (2)通过计算说明上述反应能不能通过改变温度而实现。 (3)加入锌就能使该过程实现,写出总反应的化学反应方程式。 (4)分析为什么加入锌就能使该过程实现。
化学化学计算题练习全集 一、中考化学计算题 1.BaCl 2是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl 2溶液可立即服用MgSO 4溶液解毒。为测定某BaCl 2溶液的溶质质量分数,现取100克BaCl 2溶液,不断加入MgSO 4溶液,反应过程中溶液总质量与加入MgSO 4溶液的质量关系如图所示,请回答: (1)P 点时溶液中的溶质名称是_________________; (2)反应生成沉淀的最大质量为_________________克; (3)试计算原溶液中BaCl 2溶液的溶质质量分数为_________________。 【答案】MgCl 2 23.3g 20.8% 【解析】 【分析】 【详解】 (1)当硫酸镁溶液的质量加到100g 时,溶液总质量出现拐点,此后随着硫酸镁溶液的增加,溶液总质量增加,不再产生新的变化。故P 点时硫酸镁溶液与氯化钡溶液恰好完全反应生成硫酸钡沉淀和氯化镁。因此P 点时溶液中的溶质名称是氯化镁; (2)由图可知,反应生成沉淀的最大质量为100g+100g-176.7g=23.3g ; (3)设原BaCl 2溶液的溶质质量分数为x 2442 BaCl +MgSO =BaSO +MgCl 208233100g x 23.3g ↓? 208233 =100g x 23.3g ? x=20.8% 答:原BaCl 2溶液的溶质质量分数为20.8%。 2.某校化学兴趣小组用一瓶含有少量氯化钠的硫酸钠回体样品,进行如图所示的实验.
请跟据以上信息计算(结果保留到小数点后两位) (1)反应生成沉淀的质量为g. (2)样品中硫酸钠的质量. (3)求滤液中氯化钠的质量分数. 【答案】(1)11.65 (2)7.1g (3)6.25% 【解析】 试题分析:(1)根据质量守恒定律,反应生成沉淀的质量为10g+87g+54.65g﹣ 140g=11.65g; 故答案为11.65; (2)解:设样品中硫酸钠的质量为x,反应中生成的氯化钠质量为y. Na2SO4+BaCl2=BaSO4↓+2NaCl 142 233 117 x 11.65 g y 142:233=x:11.65g,解得x=7.1g (3)233:117=11.65g:y,解得y=5.85g 滤液中氯化钠的质量=10.00g﹣7.1g+5.85g=8.75g 滤液中氯化钠的质量分数为:×100%=6.25%. 答:(2)样品中硫酸钠的质量为7.1g;(3)滤液中氯化钠的质量分数为6.25%. 考点:根据化学反应方程式的计算. 点评:本题难度较大,主要考查了以化学方程式计算为基础,同时融入溶液等方面的计算题,这样的题目一直是中考的热点,主要培养学生的综合分析能力和计算能力. 3.为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如下图所示。请计算: (1)NaOH的化学式量为_________。 (2)硫酸铜刚好完全反应时,所得溶液的质量为_____g(保留一位小数)。
人口和计划生育基础知识竞赛试题及答案 一、填空题: 、实行计划生育基本国策是全社会____的责任。 2、国家鼓励公民____,提倡一对夫妻_______。 3、夫妻双方在实行计划生育中负有___的责任,其___权益受法律保护。 4、遗弃、残害女婴是___行为。 5、家庭中父母对子女有_________的义务。 6、家庭中,子女对父母应尽____的义务。 7、城镇居民再婚夫妻____也未收养子女,要求生育子女的可以安排生育。 8、虐待、遗弃女婴或者非法送养婴、幼儿的,应当___生育登记,并收回_______。 9、男__周岁、女__周岁以上初婚的为晚婚。 0、国家工作人员和企业事业单位职工实行晚婚的,其婚假为__天;实行晚育的,其产假为__天,并给男方护理假__天 1、育龄夫妻领取《独生子女父母光荣证》,自领证之月至独生子女__周岁止,每月给予不低于__元的独生子女父母奖励费。 2、育龄夫妻系农村居民,只生育一个女孩并领取《独生子女父母光荣证》的,县级人民政府给予不低___元的一次性奖励。 3、人口素质包括_______________。
4、成年人到外地打工需办理________。 5、外出打工应持村委会开具的证明、____和________到乡政府办理《婚育证明》。 6、成年流动人口到达现居住地后应当向__________交验《婚育证明》。 7、流动人口的计划生育工作实行户籍所在地和现居住地的人民政府____、以_____为主的管理制度。 8、各级计划生育技术服务机构是具有____性质、非营利___性的财政拨款事业单位。 9、实行计划生育的育龄妇女在____期间的劳动保护、保健工作和生育待遇等依照国家有关规定执行。 20、育龄夫妻应当依照有关计划生育法律、法规的规定,自觉接受______指导和服务,知情选择避孕节育措施,预防和减少______。 21、公民享有依法生育的权利,也有_______的义务,其生育行为应当______________的规定。 22、计划生育协会的生命力在于__。 23、妇女的“五期”是指:____________。 24、“母亲节”是每年__的第__星期日。 25、公民依法结婚后生育第一个子女的,由夫妻自主选择生育时间,并应当在______或者______的人口和计划生育管理机构登记领取________。
化学平衡练习题 【例1】将3 mol A和1 mol B混合于一体积可变的密闭容器P中,以此时的温度、压强 和体积作为起始条件,发生了如下反应:达到平衡时C的浓度为w mol·L-1。 回答⑴~⑸小题: (1)保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为w mol·L-1的是( ) (A)6 mol A+2 mol B (B)3 mol A+1 mol B十2 mol C, (C)2 mol C+1 mol B+1 mol D (D)1 mol C+2mol D (2)保持原起始温度和体积不变,要使平衡后C的浓度仍为w mol·L-1,应按下列哪种 配比向容器Q中充入有关物质( ) (A)3 mol A+1 mol B (B)4 mol C十2 mol D (C) mol A+ B+1 mol C + mol D (D)以上均不能满足条件, (3)保持原起始温度和体积不变,若仍按3 mol A和1 mol B配比在容器Q中发生反应,则平衡时C的浓度和w rml·L-1的关系是( ) (A)>w (B)< w (C)= w (D)不能确定 (4)将2 mol C和2 mol D按起始温度和压强充入容器Q中,保持温度和体积不变,平衡时C的浓度为V mol·L-1,V与w和叫的关系是( ) (A) V>w (B) V<w (C) V=w (D)无法比较 (5)维持原起始温度和体积不变,按下列哪种配比充入容器Q可使平衡时C的浓度为 V mol·L-1 ( ) (A)1 mol C+ m01 D . (B)3 mol A+2 mol B
(C)3 mol A+1 mol B+1 mol D (D)以上均不能满足条件 解析⑴略:答案为(A) ⑵因容器P的体积可变,且正反应是体积缩小的反应,故相当于加压.而现在容器Q体积不变,条件不同了,不属等效平衡,无法判断.答案为(D). ⑶本题所述条件相当于减压,平衡向逆反应方向移动,C的浓度降低.答案为(B). ⑷温度、体积不变时2mol C和1 mol D反应与3 mol A和1 mol B相当,属等效平衡.再加1 mol D时平衡将向左移动,V