
三、简答题(每小题10分,共50分)。
1、简述以天然气制合成气的工艺流程?
2、什么叫烃类热裂解,烃类热裂解过程中可能发生哪些化学反应?大致可得到哪些产物?
烃类热裂解法是将石油系烃类原料(天然气、炼厂气、轻油、柴油、重油等)经高温作用,使烃类分子发生碳链断裂或脱氢反应,生成分子量较小的烯烃、烷烃和其他分子量不同的轻质和重质烃类。
烃类热裂解过程中可能发生的化学反应及产物
(1)烷烃的裂解反应:
①正构烷烃裂解主要产物是氢、甲烷、乙烯、丙烯
②异构烷烃裂解主要产物是氢、甲烷、乙烯、丙烯、C4烯烃
(2)烯烃的裂解反应:断链反应、脱氢反应、岐化反应、双烯合成反应、芳构化反应主要产物:乙烯、丙烯、丁二烯;环烯烃
(3)环烷烃的裂解反应:断链开环反应、脱氢反应、侧链断裂、开环脱氢
主要产物:单环烷烃生成:乙烯、丁二烯、单环芳烃
多环烷烃生成:C4以上烯烃、单环芳烃
(4)芳烃的裂解反应:烷基芳烃的侧链脱烷基反应或断键反应;环烷基芳烃的脱氢和异构脱氢反应;芳烃缩合反应
主要产物:多环芳烃,结焦
(5)结焦生碳反应:
烯烃经过炔烃中间阶段而生碳;经过芳烃中间阶段而结焦。
3、裂解过程中为什么要加入水蒸汽?它还起到了哪些作用?
由于裂解是在高温下操作的,不宜于抽真空减压的方法降低烃分压,这是因为高温密封困难,一旦空气漏入负压操作的裂解系统,与烃气体形成混合物易爆炸,而且减压操作对以后分离工序的压缩操作也不利,要增加能量消耗。所以采用添加水蒸气作稀释剂,降低烃分压,有利于一次反应,抑制二次反应。
①裂解反应后通过急冷即可实现稀释剂与裂解气的分离,不会增加裂解气的分离负荷和困难。
②水蒸气热容量大,使系统有较大热惯性,当操作供热不平稳时,可以起到稳定温度的作用,保护炉管防止过热。
③抑制裂解原料所含硫对镍铬合金炉管的腐蚀。
④脱除结碳,抑制铁镍催化生碳作用。
4、简述芳烃的主要来源及主要生产过程。
芳烃最初全部来源于煤焦化工业。石油芳烃主要来源于石脑油重整生成油及烃裂解生产乙烯副产的裂解汽油,
主要生产过程:
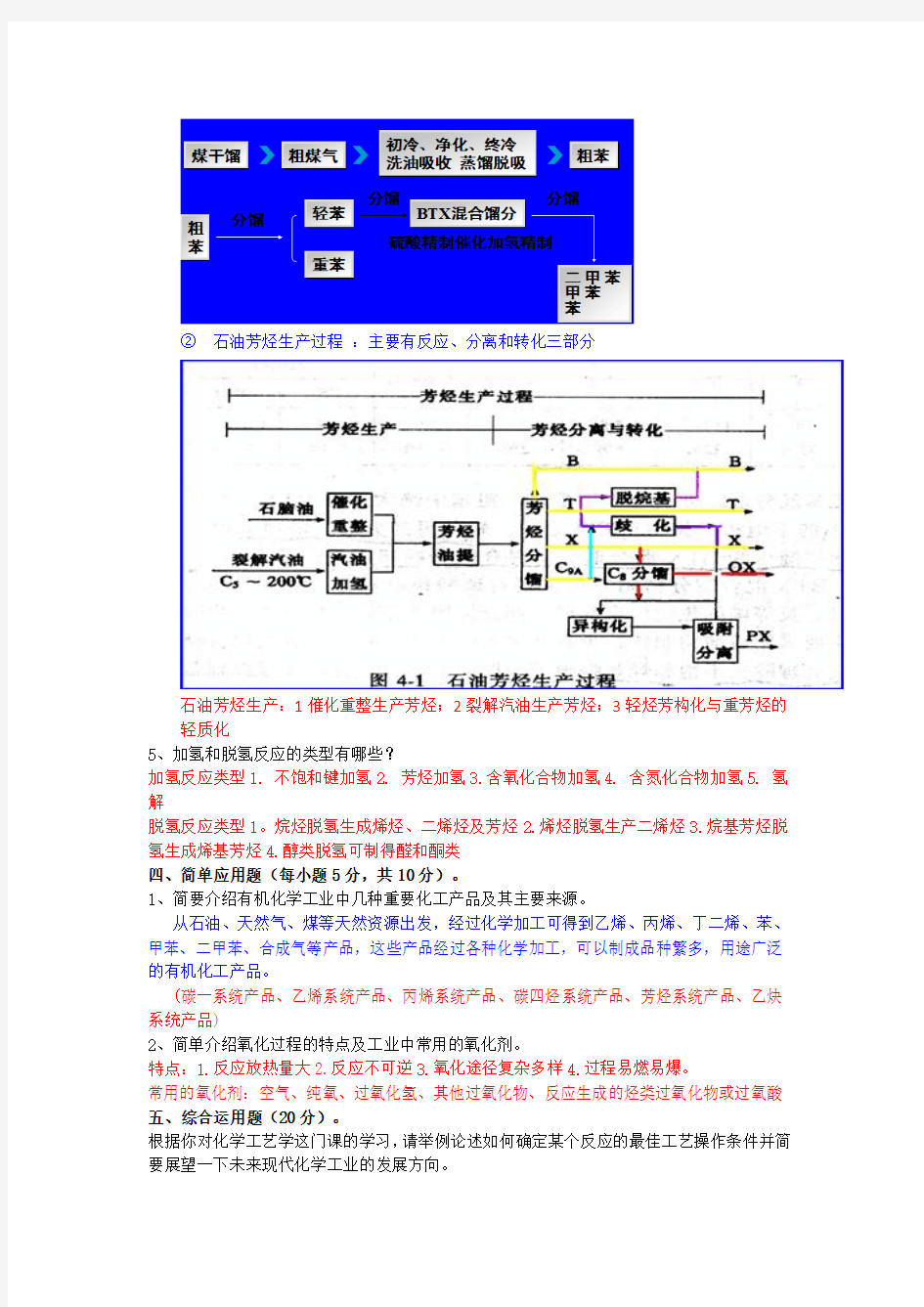
①焦化芳烃生产
②石油芳烃生产过程:主要有反应、分离和转化三部分
石油芳烃生产:1催化重整生产芳烃;2裂解汽油生产芳烃;3轻烃芳构化与重芳烃的轻质化
5、加氢和脱氢反应的类型有哪些?
加氢反应类型1. 不饱和键加氢2. 芳烃加氢3.含氧化合物加氢4. 含氮化合物加氢5. 氢解
脱氢反应类型1。烷烃脱氢生成烯烃、二烯烃及芳烃2.烯烃脱氢生产二烯烃3.烷基芳烃脱氢生成烯基芳烃4.醇类脱氢可制得醛和酮类
四、简单应用题(每小题5分,共10分)。
1、简要介绍有机化学工业中几种重要化工产品及其主要来源。
从石油、天然气、煤等天然资源出发,经过化学加工可得到乙烯、丙烯、丁二烯、苯、甲苯、二甲苯、合成气等产品,这些产品经过各种化学加工,可以制成品种繁多,用途广泛的有机化工产品。
(碳一系统产品、乙烯系统产品、丙烯系统产品、碳四烃系统产品、芳烃系统产品、乙炔系统产品)
2、简单介绍氧化过程的特点及工业中常用的氧化剂。
特点:1.反应放热量大2.反应不可逆3.氧化途径复杂多样4.过程易燃易爆。
常用的氧化剂:空气、纯氧、过氧化氢、其他过氧化物、反应生成的烃类过氧化物或过氧酸五、综合运用题(20分)。
根据你对化学工艺学这门课的学习,请举例论述如何确定某个反应的最佳工艺操作条件并简要展望一下未来现代化学工业的发展方向。
现代化学工业的特点:原料、方法和产品的多样性与复杂性;大型化、综合化、精细化率提高;多学科、生产技术密集型;能量合理利用,节能工艺和方法;资金密集,投资回收速度快,利润高;安全和环境保护
现代化学工业的发展方向:高新技术,缩短开发周期;充分、彻底地利用原;大力发展绿色化工;化工过程要高效、节能和智能化;实施废弃物再生利用工程
《化工工艺学》 一、填空题 1. 空间速度的大小影响甲醇合成反应的选择性和转化率。 2. 由一氧化碳和氢气等气体组成的混合物称为合成气。 3. 芳烃系列化工产品的生产就是以苯、甲苯和 二甲苯为主要原料生产它们的衍生物。 4. 石油烃热裂解的操作条件宜采用高温、短停留时间、低烃分压。 5. 脱除酸性气体的方法有碱洗法和乙醇胺水溶液吸附法。 6. 天然气转化催化剂,其原始活性组分是,需经还原生成才具有活性。 7. 按照对目的产品的不同要求,工业催化重整装置分为生产芳烃为主的化工型,以生产高辛烷值汽油为主的燃料型和包括副产氢气的利用与化工燃料两种产品兼顾的综合型三种。 8. 高含量的烷烃,低含量的烯烃和芳烃是理想的裂解原料。 9. 氨合成工艺包括原料气制备、原料气净化、原料气压缩和合成。
10.原油的常减压蒸馏过程只是物理过程,并不发生化学变化,所以得到的轻质燃料无论是数量和质量都不能满足要求。 11. 变换工段原则流程构成应包括:加入蒸汽和热量回收系统。 12. 传统蒸汽转化法制得的粗原料气应满足:残余甲烷含量小于0.5% 、(H2)2在 2.8~3.1 。 13. 以空气为气化剂与碳反应生成的气体称为空气煤气。 14. 低温甲醇洗涤法脱碳过程中,甲醇富液的再生有闪蒸再生、_ 汽提再生 _、_热再生_三种。 15.石油烃热裂解的操作条件宜采用高温、短停留时间和低烃分压。 16. 有机化工原料来源主要有天然气、石油、煤、农副产品。 18. 乙烯直接氧化过程的主副反应都是强烈的放热反应,且副反应(深度氧化) 防热量是主反应的十几倍。 19. 第二换热网络是指以_ _为介质将变换、精炼和氨合成三个工序联系起来,以更合理充分利用变换和氨合成反应热,达到节能降耗的目的。 20. 天然气转化制气,一段转化炉中猪尾管的作用是
化工工艺学课程设计设计题目:环氧乙烷生产工艺设计
目录 一、设计方案简介 (2) 二、工艺流程草图及说明 (6) 三、物料衡算 (8) 四、计算结果概要 (15) 五、工艺流程说明 (15) 六、工艺流程图 (21) 七、参考文献 (22) 一、设计方案简介 环氧乙烷(沸点10.5℃)是最简单也是最重要的环氧化合物,其用途是制取生产聚酯树脂和聚酯纤维的单体、制备表面活性剂,此外还用于制备乙醇胺类、乙二醇醚类等。 1、反应过程分析:
工业上生产环氧乙烷的方法是乙烯氧化法,在银催化剂上乙烯用空气或纯氧氧化。乙烯在Ag/α-Al2O3催化剂存在下直接氧化制取环氧乙烷的工艺,可用空气氧化也可以用氧气氧化,氧气氧化法虽然安全性不如空气氧化法好,但氧气氧化法选择性较好,乙烯单耗较低,催化剂的生产能力较大,故大规模生产采用氧气氧化法由乙烯环氧化反应的动力学图示可知乙烯完全氧化生成二氧化碳和水,该反应是强放热反应,其反应热效应要比乙烯环氧化反应大 十多倍。 副反应的发生不仅使环氧乙烷的选择性降低,而且对反应热效应也有很大的影响。选择性下降热效应明显增加,故反应过程中选择性的控制十分重要。如选择性下降移热慢,反应温度就会迅速上升,甚至产生飞温。 2、催化剂的选择: 由于选择性在反应过程中的重要性,所以要选择选择性好的催化剂,银催化剂对乙烯环氧化反应较好的选择性,强度、热稳定性、寿命符合要求,所以用银催化剂。催化剂由活性组分银、载体和助催
化剂组成。助催化剂主要有碱金属、碱土金属、稀土金属化合物等。其作用是提高活性、增大稳定性、延长寿命。抑制剂的作用是抑制非目标产物的形成,主要有硒、碲、氯、溴等。载体的主要功能是负载、分散活性组分,提高稳定性。载体的结构(特别是孔结构)对助剂活性的发挥、选择性控制有极大的影响(乙烯氧化制环氧乙烷的特殊性要求载体比表面积低并且以大孔为主)。 3、反应压力: 加压对氧化反应的选择性无显著影响,但可提高反应器的生产能力且有利于环氧乙烷的回收,故采用加压氧化法,但压力高对设备的要求高费用增加催化剂易损坏。故采用操作压力为2Mpa左右。 4、反应温度及空速的影响: 影响转化率和选择性的主要因素是温度。温度过高,反应速度快、转化率高、选择性下降、催化剂活性衰退快、易造成飞温;温度过低,速度慢、生产能力小。所以要控制适宜温度,其与催化剂的选择性有关,一般控制的适宜温度在200-260℃。 另一个因素是空速,与温度相比次因素是次要的,但空速减小,转化率增高,选择性也要降低,而且空速不仅影响转化率和选择性,也影响催化剂得空时收率和单位时间的放热量,故必须全面衡量,现工业上采用的混合起空速一般为7000/h左右,也有更高。以氧气作氧化剂单程转化率控制在12-15%,选择性可达75-80%后更高。 5、原料纯度及配比: 原料其中的杂质可能给反应带来不利影响:使催化剂中毒而活
**学院2011-2012 学年度第2 学期 《化学工艺学》( 本科)期末试卷(A)(时间120分钟) 试卷编号: 院(系) 班姓名学号得分 一、判断题(对的画“√”,错的画“×”)(每小题1分,共10分) 1.对烃类的裂解过程,要求高温,高压,低停留时间() 2.通过CO变换可产生更多氢气和降低CO含量。(√) 3、设备或装置在任何条件下可以达到的最大生产能力,称为设计能力。(×) 4、对于采用循环式流程的过程来说,单程转化率即是全程转化率(×) 5、馏分油的关联指数是表示芳烃的含量。(√) 6、合成气是指二氧化碳和氢气的混合气。(×) 7、关联指数越大,则油品的芳烃含量越高。(√) 8、催化剂的作用是它能与反应物生成不稳定中间化合物,改变了反应途径,活化能得以降低。(√) 9、催化剂能缩短达到化学平衡的时间,故能改变化学平衡。(×) 10、羰基铑催化剂的主要缺点是异构化活性很高。(√) 二、填空题(每空1分,共10分) 1、磷肥的生产方法有酸法和热法两大类。 2、石油中的非烃化合物主要有硫化物、氮化物、含氧化合物和金属有机化物。P14 3、化工生产过程一般可概括为原料预处理、化学反应、和产品分离及精制三大步骤。P24 4、催化剂按催化反应体系的物相均一性可分为均相催化剂和非均相催化剂。 5、乙烯产量常作为衡量一个国家基本化学工业发展水平的标志。 6、工程中常以C5和C5以上液相产品氢含量不低于8%作为裂解深度的限度。 7、由于受炉管耐热程度的限制,管式裂解炉出口温度一般均限制在950℃以下。 8、乙烯生产中常采用脱除乙炔的方法有溶剂吸收法和催化加氢法。 9、裂解气深冷分离中,脱甲烷塔和乙烯精馏塔是两个关键的精馏塔。10、芳烃中的三苯和烯烃中的三烯是化学工业的基础原料,其中三苯是指苯、甲苯和二甲苯。 10、芳烃中的三苯和烯烃中的三烯是化学工业的基础原料,其中三烯是指乙烯、丙烯和丁二烯。 11、工业上分离对二甲苯的主要方法有:深冷结晶分离法、_ 络合分离法_和模拟移动床吸附分离法。 12、按脱硫剂的状态来分,脱硫方法有__ ___和__ __两大类。 13、烃类选择性氧化可分为:碳链不发生断裂的氧化反应、碳链发生断裂的氧化反应和氧化缩合反应三种。 14、氧化反应是一大类重要的化学反应,其特征为:反应放热量大、反应不可逆、氧化途径复杂多样、过程易燃易爆。 15、羰基合成的初级产品为醛 16、高压法甲醇羰化反应合成醋酸采用的催化剂为钴碘催化剂、低压法采用铑碘催化剂。 17、目前对乙烯氧氯化的反应机理主要有两种不同看法。一种认为是氧化-还原机理;另一种认为是环氧乙烷机理。 1、裂解炉在裂解过程中,由于有二次反应的存在,炉管会结焦,为了保持设备的正常运行,必须定期给裂解炉管清焦,清焦分清焦和清焦或蒸汽-空气清焦。 2、工业催化剂的使用性能指标为:、、寿命和其它廉价易得、无毒、易分离等。 3、裂解气中酸性气体脱除的方法有碱洗法和两种。 4、裂解气深冷分离中,和乙烯精馏塔是两个关键的精馏塔。 5、工业上分离对二甲苯的主要方法有:、_ _和模拟移动床吸附分离法。 6、按脱硫剂的状态来分,脱硫方法有__ ___和__ __两大类。 三、选择题(每小题1分,共10分) 1、下列哪个过程属于对石油的一次加工: A.烃类热裂解;B. 催化重整;C. 催化裂化;D.常压蒸馏和减压蒸馏 2、各族烃类的裂解反应难易顺序为:p61 A. 正烷烃>异烷烃>环烷烃>芳烃 B. 正烷烃<异烷烃<环烷烃<芳烃 ---------------------------------------- 装-------------------------------------- 订------------------------------------- 线----------------------------------------------------
金属乙二醇盐合成工艺的研究 沈国良1,2, 张晓辰1, 李银苹1, 刘红宇1, 宁桂玲2 (1.沈阳工业大学石油化工学院,辽宁辽阳111003;2.大连理工大学化工学院,辽宁大连116012) 摘 要:介绍了乙二醇盐催化剂的合成研究进展,详细介绍和评述了金属法、碱法、Nelles 法、醇交换法等制取乙二醇钠、乙二醇钾、乙二醇锑、乙二醇钛、乙二醇铝等二元醇盐催化剂的工艺技术,乙 二醇盐有着广阔的应用前景。 关键词:二元醇盐;乙二醇盐;金属醇盐;合成中图分类号:TQ 223.16 文献标志码:A 文章编号:0367-6358(2011)01-0049-04 S tudy on Sy nthesis T echnology of Ethy lene G lycol A lkoxides SH EN Guo -liang 1,2 , ZH ANG Xiao -chen 1, LI Yin -ping 1, LIU H ong -yu 1, N ING Gui -ling 2 (S chool o f P etrochemical E ngineer in g ,Shenyang Univer sity o f Technolog y ,Liaonin g Liaoy ang 111003,China ; S choo l o f Chemical E ng ineer in g ,Dalian Univer sity o f Technolog y ,Liaoning Da lian 116012,Ch ina ) Abstract :The development on study of ethy lene glycol alkoxides cataly st w as review ed .The sy nthesis techno logy of e thylene gly col so dium ,e thylene gly col po tassium ,ethylene gly co l antim ony ,e thylene g ly co l titanium and e thylene gly col aluminum cataly sts by m etal metho d ,alkaline method ,Nelles method and alcohol ex chang e method w as introduced .The e thylene gly co l alkoxides will find bro ad application in industry . Key words :dihy dro xy alcohol alko xides ;ethy lene g lycol alko xides ;metal alkoxides ;sy nthesis 收稿日期:2010-08-16 基金项目:辽宁省教育厅科技计划项目[2005303] 作者简介:沈国良(1960~),男,辽宁大连人,教授,从事化学工艺学科研究工作。E -mail :sg l6666@https://www.doczj.com/doc/7a11186124.html, 金属醇盐是介于无机化合物和有机化合物之间的广义金属有机化合物的一部分[1]。随着醇盐溶胶-凝胶法(S ol -Gel )的迅猛发展,极大地促进了金属醇盐化学的研究[2],并为开发醇盐新用途和制备新材料奠定了基础[3]。目前,开展醇盐合成、性能、应用的研究已成为研究的热点之一,既有较大的理论意义,又有重要的实用价值。 但到目前,所合成的金属醇盐大都为单金属、多金属的一元醇盐 [4] 。金属的一元醇盐是酯化反应、 酯(醇)交换反应、缩聚反应等重要反应的高效催化 剂,也可用作有机合成试剂、干燥剂,是近年来制备超细(纳米)氧化物的主要原料。但是,金属的一元醇盐非常容易水解,就连采用溶胶—凝胶法水解制 备超细(纳米)粉体时还需加入大量螯合剂以减缓水解程度 [5] ,以便于控制粒度和形貌,严重影响着金属 钛醇盐的应用。 在研究金属一元醇盐水解性能时,为控制金属一元醇盐水解速率,一种有效而普遍使用的方法是使用螯合剂,螯合剂能与高活性的金属醇盐反应形成螯合物,能够降低水解速率。可用作螯合剂的物质有二元醇、有机酸、β-二酮等,其中采用二元醇作 螯合剂时,反应通式如下: M (OR )n +x HO -G -O H ※(RO )n -2x M (OG O )x +2x RO H 金属二元醇化合物能产生高的分子缔合,通常比原醇盐难水解[6]。根据这一原理,后来人们制备 · 49·第1期化 学 世 界
2014 学年第 2 学期 函授 13化学工程(专升本)专业《化工工艺学》课程教案 4课时/次共10次 40课时 教师: 教研室:
§1 第一章合成氨原料气的制备 教学目的:掌握优质固体燃料气化、气态烃蒸汽转化、重油部分氧化等不同原料制气过程的基本原理;原料和工艺路线;主要设备和工艺条件的选择;消耗定额的计算和催化剂的使用条件。 教学重点:优质固体燃料气化、气态烃蒸汽转化、重油部分氧化等不同原料制气过程。教学难点:消耗定额的计算和催化剂的使用条件。 新课内容: 第一节固体燃料气化法 一、概述 固体燃料(煤、焦炭或水煤浆)气化:用氧或含氧气化剂对其进行热加工,使碳转变为可燃性气体的过程。气化所得的可燃气体称为煤气,进行气化的设备称为煤气发生炉。 二、基本概念 1、煤的固定碳;固体燃料煤除去灰分、挥发分、硫分和水分以外,其余的可燃物质称为固定碳。 2、煤的发热值:指1公斤煤在完全燃烧时所放出的热量。 3、标煤:低位发热值为7000kcal/kg的燃料4.空气煤气:以空气作为气化而生成的煤气其中含有大量的氮(50%以上)及一定量的一氧化碳和少量的二氧化碳和氢气。 5.混合煤气(发生炉煤气):以空气和适量的蒸汽的混合物为气化剂生成的煤气,其发热量比空气煤气为高。在工业上这种煤气一般作燃料用。 6.水煤气:以蒸汽作为气化剂而生成的煤气,其中氢及—氧化碳的含量高在85%以上,而氮含量较低。 7.半水煤气:以蒸汽加适量的空气或富氧空气同时作为气化剂所创得的煤气或适当加有发生炉煤气的水煤气,其含氮量为21—22%。 三、气化对煤质的基本要求 (1)保持高温和南气化剂流速 (2)使燃料层各处间一截而的气流速度和温度分布均匀。这两个条件的获得,除了与炉子结构(如加料、排渣等装置)的完善程度有关外,采用的燃料性质也具有重大影响。 1水分:<5% 2挥发份:<6% 煤中所含挥发分量和煤的碳化程度有关,含量少的可至I一2%,多的可达40%以上。它的含量依下列次序递减: 泥煤褐煤烟煤无烟煤焦炭 3灰份:15-20% 灰分中主要组分为二氧化硅、氧化铁、氧化铝、氧化钙和氧化镁等无机物质。这些物质的含量对灰熔点有决定性影响。 4硫分:<1.5g/m3 煤中的硫分在气化过程中,转化为含硫的气体,不仅对金属有腐蚀作用,而且会使催化剂中毒。在合成氨生产系统中,根据流程的特点,对含硫量有一定的要求,并应在气体净化过程中将其脱除。 5灰熔点:>1250℃ 6机械强度和热稳定性
由 煤 制 合 成 气 综 述 学院:化学化工学院班级:200 级化贸班姓名: 学号:09130
前言 传统的煤炭开发和利用对我国经济和环境产生了严重的影响,制约着国民经济的可持续发展。为了保证国民经济的可持续发展,必须提高煤炭的利用率,减少燃煤对大气的污染。发展洁净煤技术。 洁净煤技术(CCT——Clean Coal Technology)一词源于80年代的美国,是关于减少污染和提高效率的煤炭洗选加工及燃烧转化,烟气净化等一系列新技术的总称。1985年美国和加拿大曾就解决跨国界的酸雨问题进行谈判,关于1986年开始实施洁净煤技术计划(CCTP),其基本做法是把具有潜力的先进技术通过示范进入市场,所优选出的示范项目要有足够的普遍性和商业应用前景。现在已完成五轮计划项目,主要优选项目有:先进的选煤技术、先进的燃烧器、流化床燃烧、煤气联合循环发电、煤炭气化、煤油共炼、烟道气净化工艺及炼焦厂、水泥厂污染控制技术。该计划的实施将有助于扩大美国的煤炭生产和利用,减少石油进口、增强美国在高技术领域的国际竞争力。从长远看,也将对世界能源供应格局,煤炭工业的前景及改善环境产生重大影响。 由煤制合成气综述 摘要:论述了煤转化技术、煤气化工艺的技术特点、发展现状和工业应用;对比和分析了固定床、流化床和气流床气化炉的气化特点和工程应用概况;提出了目前国内可采用优先发展工业化成熟的Texaco气化技术和自主开发的对置式多喷嘴气化技术,适时发展具有广阔发展潜力的干煤粉气化技 术的参考性意见。 关键词:化工行业;煤制气;洁净煤技术 Abstract: Author has discussed the features, presently developing situation and industrial application of the coal conversion technology and coal gasification technology; has compared and analyzed gasification features and engineering application situation for gasifies of fixed bed, fluidized bed and gas flow bed technologies; has presented that it can be adopted in China at present to develop preferentially the ripped Texaco gasification and self-developed gasification technology with multi-burners oppositely arranged, has proposed to develop at the right moment the pulverized dry coal gasification technology which has wide development potential. Keyword: chemical industry; coal gasification; clean coal technology 煤制合成气,是指以煤或焦炭为原料,以氧气(空气、富氧或纯氧)、水蒸汽等为气化剂,在高温条件下,通过化学反应把煤或焦炭中的可燃部分转化为气体的过程。生产的气体作为生产工业燃料气、民用煤气和化工原料气。它是洁净、高效利用煤炭的最主要途径之一,是许多能源高新技术的关键技术和重要环节。如燃料电池、煤气联合循环发电技术等,煤制气应用领域非常广发。如图1-1示意图。
《化工工艺学》课程设计任务书 一、课程设计的目的 通过课程设计,旨在使学生了解化工工艺基本原理、重要工艺过程、设备的构造及工程设计基本内容,初步掌握化工工艺设计的主要程序及方法,锻炼和提高学生综合运用理论知识和技能的能力、收集和查阅文献资料的能力、分析和解决工程实际问题的能力、独立工作和创新能力。课程设计的任务是:学生能综合运用所学理论知识和所掌握的各种技能,通过独立思考和锐意创新,在规定的时间内完成指定的化工工艺的设计任务,并通过设计说明书及设计图形式正确表述。 二、设计任务及要求 1、设计题目 4.2/7.2/ 9.2万吨/年环氧烷生产工艺设计 2、设计条件 用N2作为惰性致稳气时的原料气组成 反应器的单程转化率: 12.3% 选择性:73.8% 环氧乙烷的吸收率:99.5% O2中夹带Ar 0.00856 mol/mol,循环排放气中含Ar为12.85%(10~15%,可自行调配),产品环氧乙烷中含Ar 0.00631 mol/mol。 年生产7440小时。 3、设计任务 1)设计方案简介:对给定或选定的工艺流程进行简要的论述。 2)主要设备的工艺设计计算:包括工艺参数的选定、物料衡算、热量衡算、设备的工艺尺寸计算及结构设计。对反应器和环氧乙烷精馏塔做详细设计计算(包括工艺参数和设备参数)。3)典型辅助设备的选型和计算:包括典型辅助设备的主要工艺尺寸计算和设备型号规格的选定。 4)工艺流程简图:以单线图的形式绘制,标出主要设备和辅助设备的物流量、能流量和主要化工参数测量点。 5)主要设备工艺条件图:包括设备的主要工艺尺寸。 6)编写设计说明书:包括设计任务书、目录、设计方案简介与评述、工艺设计及计算、主要设备设计、设计结果汇总表、参考资料等内容,并附带控制点的工艺流程图。 三、设计时间进程表 时间:2周(11-12周),时间分配大致如下:
第一章合成氨原料气的制备 1.何为固体燃料气化? 2.煤气的成分由哪些因素决定?(影响煤气组成的因素有哪些?) 3.常用的工业煤气有哪些?制合成氨所用的煤气是什么/ 4.何为独立反应数?如何计算/ 5.以煤和水蒸气反应,欲制得含CO和H2较高的水煤气,应在什么 条件下进行反应?欲制得CH4含量高的高热值煤气,应在什么条件下进行反应? 6.以空气和水蒸气为汽化剂,对煤进行热加工,在自热平衡条件下 获得的煤气是什么煤气? 7.什么是半水煤气? 8.固体燃料间歇气化的原因是什么? 9.如何进行煤气化过程的连续生产? 10.间歇制半水煤气的工作循环包括哪几个阶段?用于制气的阶段有 哪些?各阶段的作用是什么? 11.间歇制水煤气的工作循环包括哪几个阶段? 12.间歇制低氮煤气的工作循环包括哪几个阶段? 13.间歇制半水煤气中,炉内温度过高会造成什么影响? 14.分析间歇制半水煤气中的能耗问题。 15.气化炉的操作温度即炉温指的是何处的温度? 16.间歇制半水煤气各阶段时间分配的原则是什么? 17.间歇制半水煤气中,调节气体组成常用的方法有哪些? 18.燃烧室的作用是什么? 19.富氧空气—水蒸气连续气化过程中,用调节什么的方法,保持燃 料层在允许温度范围内维持系统的自热平衡? 20.富氧空气—水蒸气连续气化制半水煤气时,主要操作指标有哪 些? 21.天然气蒸汽转化反应过程的主副反应主要有哪些? 22.何为烃类蒸气转化? 23.生产合成氨最经济的原料气生产方法是什么? 24.影响天然气蒸汽转化反应平衡的因素有哪些?有何影响? 25.提高温度,降低压力,提高水碳比,均有利于降低烃类蒸气转化 的转化气中的哪种组分含量。 ①H2②CO ③CH4④CO2 26.烃类蒸气转化过程为何分两段进行?二段转化的目的是什么? 27.在天然气蒸气转化系统中,将水碳比从3.5~4降至2.5,试分析一 段转化炉可能出现的问题和解决的方法。 28.试分析烃类蒸气转化过程中加压的原因和确定操作温度的依据。
化学工艺学试卷(两套) 一、选择题(2分/题) 1.化学工业的基础原料有( ) A石油 B汽油 C乙烯 D酒精 2.化工生产中常用的“三酸二碱”是指( ) A硫酸、盐酸、硝酸和氢氧化钠、氢氧化钾 B硫酸、盐酸、磷酸和氢氧化钠、氢氧化钾 C硫酸、盐酸、硝酸和氢氧化钠、碳酸钠 D硫酸、盐酸、磷酸和氢氧化钾、碳酸钾 3.所谓“三烯、三苯、一炔、一萘”是最基本的有机化工原料,其中的三烯是指( ) A乙烯、丙烯、丁烯 B乙烯、丙烯、丁二烯 C乙烯、丙烯、戊烯 D丙烯、丁二烯、戊烯 4.天然气的主要成份是() A乙烷 B乙烯 C丁烷 D甲烷 5.化学工业的产品有( ) A钢铁 B煤炭 C酒精 D天然气 6.反应一个国家石油化学工业发展规模和水平的物质是( ) A石油 B乙烯 C苯乙烯 D丁二烯 7.在选择化工过程是否采用连续操作时,下述几个理由不正确的是( ) A操作稳定安全 B一般年产量大于4500t的产品 C反应速率极慢的化学反应过程 D工艺成熟 8.进料与出料连续不断地流过生产装置,进、出物料量相等。此生产方式为( ) A间歇式 B连续式 C半间歇式 D不确定 9.评价化工生产效果的常用指标有() A停留时间 B生产成本 C催化剂的活性 D生产能力 10.转化率指的是( ) A生产过程中转化掉的原料量占投入原料量的百分数 B生产过程中得到的产品量占理论上所应该得到的产品量的百分数 C生产过程中所得到的产品量占所投入原料量的百分比 D在催化剂作用下反应的收率 11.电解工艺条件中应控制盐水中Ca2+、Mg2+等杂质总量小于( ) A 10μg/L B 20mg/L C 40μg/L D 20μg/L 12.带有循环物流的化工生产过程中的单程转化率的统计数据()总转化率的统计数据。 A大于 B小于 C相同 D无法确定 13.()表达了主副反应进行程度的相对大小,能确切反映原料的利用是否合理。A转化率 B选择性 C收率 D生产能力 14.三合一石墨炉是将合成、吸收和()集为一体的炉子。 A 干燥 B 蒸发 C 冷却 D 过滤 15.转化率X、选择性S、收率Y的关系是() A Y=XS B X=YS C S=YX D以上关系都不是 16.化工生产一般包括以下( )组成 A原料处理和化学反应 B化学反应和产品精制
化学工艺学 第一章绪论 1、化学工业:运用化学工艺、化学工程及设备,通过各种化工单元操作,高效、节能、经济、环保和安全地将原料生产成化工产品的特定生产部门。 2、化学工艺即化工生产技术,是指将各种原料主要经过化学反应转变为产品的方法和过程,包括实现这种转变的全部化学的和物理的措施。 3、化学工艺学是根据化学、物理和其他科学的成就,研究综合利用各种原料生产化学产品的方法原理、操作条件、流程和设备,以创立技术先进、经济上合理、生产上安全的化工生产工艺的学科。 4、21世纪,化学工业的发展趋势? 答:(1)产品结构精细化和功能化;(2)生产装置微型化和柔性化;(3)生产过程绿色化和高科技化;(4)市场经营国际化、信息化。 5、绿色化工就是用先进的化工技术和方法减少或消除对人类健康、社区安全、生态环境有害的各种物质的一种技术手段。 6、化学工业的基础原料指可以用来加工生产化工基本原料或产品的在自然界天然存在的资源。 7、化工产品一般是指由原料经化学反应、化工单元操作等加工方法生产出来的新物料(品)。 8.煤化工:以煤为原料,经过化学加工转化为气体、液体和固体燃料及化学品的工业。 9.煤的干馏:是指在隔绝空气条件下将煤加热,使其分解生成焦炭、煤焦油、粗苯和焦炉气的过程。 10.一次加工方法主要包括一次加工和二次加工,一次加工方法主要包括常压蒸馏和减压蒸馏。 11.蒸馏是一种利用液体混合物中各组分挥发度的差别(沸点不同)进行分离的方法,是一种没有化学反应的传质、传热物理过程,主要设备是蒸馏塔。 12.常用的二次加工方法主要有催化重整、催化裂化、催化加氢裂化和烃类热裂解四种。 13.催化重整:是在铂催化剂作用下加热汽油馏分(石脑油),使其中的烃类分子
《化工工艺学》教学大纲 一、课程属性 1.课程的性质 《化工工艺学》课程是化学工程与工艺专业的核心课程。本课程从化工生产工艺角度出发,运用化工过程的基本原理,介绍典型化工产品的生产方法与原理、流程组织、关键设备、操作条件以及介绍生产中的设备材质安全技术、三废治理、节能降耗等问题。 2.课程定位 本课程在第6学期开设,是一门专业核心课程,在基础课和专业课之间起着承前启后、由理及工的桥梁作用。其前导课程是化工原理、物理化学、化工热力学等,与其平行学习的专业课为分离过程、化学反应工程等。 3.课程任务 本课程的主要任务是使学生全面的掌握石油化工生产方面的知识以及各个生产工艺流程。通过本课程的学习,培养学生分析和解决有关单元操作各种问题的能力,以便在石油化工生产、科研和设计工作中达到强化生产过程。为使学生在今后的学习和工作中能正确而有效的联系石油化工生产实际打下坚实的基础。 二、课程目标 知识目标 1.掌握化工工程的基本原理。 2.掌握化工工艺的基本概念和基本理论。 3.掌握典型化工产品的生产方法与工艺原理、典型流程与关键设备、工艺条件与节能降耗分析。 4.了解化工生产中设备材质、安全生产、三废治理等问题。 能力目标 培养学生应用已学过的基础理论解决实际工程问题的能力,使学生了解当今化学工业的概貌及发展方向,使学生在以后的生产与开发研究工作中能掌握基本的方法,做到触类旁通、灵活应用,不断开发应用新技术、新工艺、新产品和新设备,降低生产过程中的原料与能源消耗,提高经济效益,更好地满足社会需要。 素养目标 1.培养具有良好的职业道德、精湛的专业技能、较强的竞争能力和可持续发展的学习与适应能力的德、智、体等方面全面发展的高端高级技能型专门人才。 2.具备从事本专业领域实际工作的基本能力和基本技能,并且熟悉某些石油化工生产流程、某些化工车间管理的高素质技能型专门人才。 3.养成认真细致、积极探索的科学态度和工作作风,形成理论联系实际、自主学习和探索创新的良好习惯。 三、课程内容及实施 1、课程结构
课程设计任务书 课程名称:制药工艺课程设计 题目: 3.6万吨/年氯苯车间分离工段工艺设计 学院:环境与化学工程系:化学工程 专业班级:制药071班 学号: 5 8 0 1 3 0 7 0 3 0 学生姓名:晏金华 起讫日期:2010-10-25—2010-12-20 指导教师:杜军职称:副教授 学院审核(签名): 审核日期:
说明 1.课程设计任务书由指导教师填写,并经专业学科组审定,下达到学生。 2.学生根据指导教师下达的任务书独立完成课程设计。 3.本任务书在课程设计完成后,与论文一起交指导教师,作为论文评阅和课程 设计答辩的主要档案资料。 一、课程设计的主要内容和基本要求 (一)目的与要求 1.通过课程设计使学生树立正确的设计思想,培养学生理论联系实际的作 风;进一步提高学生综合利用所学的基础理论、专业知识和基本技能(包括查阅资料、运算和绘图等)的能力及分析解决专业范围内工程技术问题的能力;使学生初步掌握化工工艺设计的一般程序和方法,得到工艺设计方面的基本训练. 2.在课程设计期间,要求学生遵守设计纪律和考勤制度。 3.善于学习,勤于思考,充分发挥主观能动性,以严格的作风和认真负责的 态度,在老师的指导下,根据设计任务书,在规定的时间内独立地完成设计任务;学生所完成的设计,应体现设计方案正确、工艺技术可行、经济合理,并参考文献资料,结合生产实际,尽可能吸收最新科技成果,采用先进工艺技术,争取使设计具有一定的先进性和创新性。 (二)课程设计内容—1万吨/年氯苯车间反应工段工艺设计 1.设计说明书内容 (1)总论 ①设计依据;南昌市东北郊xx厂,厂内现有氯碱车间,可提供Cl ;且具备 2完善的公用工程系统。即可供最低-15℃冷冻盐水,20℃(平均)工业上水及 0.6MPa的蒸汽。 ②氯苯在国民经济中的地位和作用(用途),国内外氯苯生产发展概况; ③氯苯生产方法简述及论证; ④生产流程的选择及论证: (2)产品规格,主、辅原料规格及来源情况 (3)生产工艺流程说明 按生产工艺流程说明物料经过工艺设备的顺序及生成物的去向,物料输送及贮备方式,同时说明主要操作条件,如温度、压力、流量、配料比等。 (4)物料衡算 ①根据生产规模及其特点确定年生产时间(h)、单位时间产量及计算基准; ②物料衡算:选定计算方法,对车间所有有变化的过程及设备(或系统),按一定顺序和计算步骤,逐个进行物料衡算,确定每股进、出料的组分、流量及百分比含量。要求及时整理计算结果,对每个过程设备列物料平衡表。 (5)列表: ①工艺条件一览表; ②生产控制一览表; 2. 图纸内容及张数:反应工段工艺流程图,1张
化工工艺学期末考试总结 1. 二氧化硫接触氧化制三氧化硫。 (1)化学反应:SO2 + 1/2O2 SO3 (2)催化剂:活性组分:V2O5。载体:硅胶、硅藻土及其混合物。助催化剂:K2O、K2SO4、TiO2、MoO3等。(3)反应压力:常压。(4)反应温度:400~600℃ 2. 氧气氧化法乙烯环氧化制环氧乙烷。 (1)化学反应:C2H4 + 1/2O2 C2H4O (2)催化剂:活性组分:Ag。载体:碳化硅,α—Al2O3和含有少量SiO2的 α—Al2O3,助催化剂:碳酸钾、碳酸钡和稀土元素化合物。 (3)反应压力:1.0~3.0 MPa。(4)反应温度:204~270℃ 3. 氢氮气合成氨 (1)化学反应:N2 + 3H2 2NH3 (2)催化剂:α—Fe-Al2O3-MgO-K2O-CaO-SiO2 (1)反应压力:15MPa。(4)反应温度:390~520℃。 4.丙烯氨氧化制丙烯腈。 (1)化学反应:CH2=CHCH3 + NH3 + 3/2O2 CH2=CHCN + 3H2O (2)催化剂:①钼酸铋系:P-Mo-Bi-Fe-Co-Ni-K-O/Si2O;②锑系:Sb-Fe-O。 (3)反应压力:常压。(4)反应温度:最佳温度:440℃。 5.乙苯脱氢制苯乙烯 (1)化学反应:C2H5 CH=CH2 + H2 (2)催化剂:Fe2O3-Cr2O3-K2O (3)反应压力:常压。 (4)反应温度:600~630℃ 6..写出合成气制甲醇的主反应及主要副反应方程式。 答:主反应:CO +2H2CH3OH 当有二氧化碳存在时,二氧化碳按下列反应生成甲醇: CO2 + H2 CO + H2O CO + 2H2CH3OH 两步反应的总反应式为:CO2 + 3H2CH3OH+ H2O 副反应:(1)平行副反应 CO + 3H2CH4 + H2O 2CO + 2H2CO2 + CH4 4CO + 8H2C4H9OH+3 H2O 2CO + 4H2CH3OCH3+ H2O 当有金属铁、钴、镍等存在时,还可以发生生碳反应。 (2)连串副反应 2CH3OH CH3OCH3 + H2O CH3OH + nCO +2nH2CnH2n+1CH2OH + nH2O CH3OH + nCO +2(n-1)H2CnH2n+1COOH + (n-1)H2O 1. 什么叫烃类热裂解过程的一次反应和二次反应? 答:一次反应:由原料烃类热裂解生成乙烯和丙烯等低级烯烃的反应 二次反应:主要指由一次反应生成的低级烯烃进一步反应生成多种产物,直至最后生成焦或炭的反应。 2. 什么叫烃类的热裂解? 答:烃类热裂解法是将石油系烃类原料(天然气、炼厂气、轻油、柴油、重油等)经高温作用,使烃类分子发生碳链断裂或脱氢反应,生成分子量较小的烯烃、烷烃和其他分子量不同
《化工单元操作》 课程整体教学设计(2014~ 2015学年第二学期) 课程名称:化工单元操作 所属系部:化工学院 制定人:宋丽萍 合作人:吴晓滨 制定时间: 2015年1月20日 包头轻工职业技术学院
课程整体教学设计 一、课程基本信息 课程名称:化工单元操作 课程代码:181103 学分:20 学时:360 授课时间:第二学期授课对象:三年制专科 课程类型:应用化工技术专业职业能力必修课。 先修课程:化工机械基础后续课程:现代煤化工生产技术 二、课程定位 《化工单元操作》课程面向的岗位有:管路安装、泵及其他动设备操作、流量控制、压力控制、温度控制、DCS控制操作、设备保全等。《化工单元操作》安排在《化工机械基础》之后,《现代煤化工生产技术》之前的一门专业基础课,时间安排在第三学期。其主要内容是以化工生产中的物理加工过程为背景,依据操作原理的共性,分成为若干单元操作过程,通过项目训练,掌握各单元典型设备的操作技能及设备选用原则和技能,学习各单元操作的基本原理、基本计算。中职定位:单元设备简单操作 本科定位:单元设备工作原理及生产能力设计 培训地位:单元设备工作原理简介 三、课程目标设计 总体目标: 本课程是应用化工技术专业专业核心类课程,专业课程体系符合高技能人才培养目标和
专业相关技术领域职业岗位(群)的任职要求,本课程对学生职业能力培养和职业素养养成起主要支撑或明显促进作用,与高等数学、无机化学、有机化学、化工图纸识用与绘制、物理化学等前续课程密切衔接,为后续课程《化工设计概论》、《化工工艺学》、《化工顶岗实习》、《毕业设计》等打下坚实的基础。同时注重培养学生的方法能力、社会能力,最终形成化工生产的职业综合能力。 能力目标: 1、能运用流体力学知识,根据输送流体的性质,正确选用管道及安装。根据输送机械设备操作规范,操作常见泵的开启与调节。根据输送机械设备操作规范,操作常见泵的开启与调节。 2、能运热量传递知识,根据传热设备的操作要求,操作和维护传热设备。 3、能运用蒸发原理知识,根据蒸发设备的操作要求,操作和维护蒸发设备。 4、能运用蒸馏原理知识,根据蒸馏设备的操作要求,操作和维护蒸馏设备。 知识目标:(知道...;了解…;理解…;掌握…。) 1、知道流体力学,了解其基本内容,理解流体动力学的基本概念,掌握机理及基本计 算方法; 2、知道非均相物系分离的基本原理,重力沉降和过滤的基本概念及相关计算;掌握 3、知道传热单元,了解传热过程,理解传热原理,掌握热量传递过程中的传热单元操 作的基本概念及传热基本方程; 4、知道吸收,了解吸收过程,理解吸收原理,掌握气体吸收的基本原理及其相关计算; 5、掌握两组分溶液精馏的原理和流程,精馏塔的操作及设计计算方法; 6、掌握干燥过程的基本概念,熟悉湿空气的性质及湿度图的应用,干燥过程的相关计 算。 素质目标:(职业道德、职业素质、职业规范在本课中的具体表现) 1、进入工作环境,必须穿着工作服、安全帽、工作鞋等。 2、不能随意触动设备。 3、操作设备要严格按照操作规程进行操作。 4、保持工作环境的卫生。 5、保持节俭节约。 四、课程内容设计:(包括顶岗实习、项目实施等,项目小于内容)
课程设计 专业名称 班级 学生姓名 学号 课题名称化工工艺学课程设计指导教师
目录 1 课程设计任务书 2 概述 (6) 2.1乙醇的性质及质量标准 (6) 2.1.1物理性质 (6) 2.1.2化学性质 (6) 2.1.3生化性 (6) 2.1.4质量标准 (6) 2.2乙醇生产的意义及发展史 (7) 2.2.1乙醇生产的意义 (7) 2.2.2乙醇生产的发展 (7) 2.3乙醇的应用领域 (8) 2.4主要生产工艺 (8) 2.5 乙醇发酵常用的微生物 (10) 3 乙醇发酵工艺 3.1 乙醇发酵分类 (10) 3.2 操作要点 (12) 3.3 结果 (12) 4 参考文献 5 感谢
1 “精细化工工艺学”课程设计任务书 1.1课程设计的目的: 精细化工是化学或化工专业的一门专业课,是继无机化学、有机化学、化工原理等专业基础课之后,把基础知识用于具体化工生产的一个专业体现。而精细化工课程设计是继前面专业课之后的一个总结性教学环节,是化工类人才培养中进行的一次实践,它犹如学生搞毕业设计那样的一次“预演习”,无疑对学生毕业前进行毕业设计将有很大的帮助,而对于一些毕业前只搞毕业论文不搞毕业设计的学生,是使他们得到工程师训练的不可缺少的一环。 1.2课程设计的要求: 以表面活性剂、涂料、香料、化妆品、抗静电剂、热稳定剂、纳米材料以及新型功能材料等精细化工研究领域为基本方向,相应的组别选择相应的方向中具体的精细化学品作为设计目标,进行合成设计。 设计题目举例:
1.3 设计内容 课程设计的基本要求就是要对所选择的设计目标做出文献综述及实验方案的设计,具体要求为: 1、查阅至少四篇相关文献,写出文献综述,并设计相应的设计方案; 2、设计方案要求画出具体的设计工艺及参数,要求工艺及方案合理可行; 3、课程设计期间遵守有关规章制度; 1.4 设计数据基础 可查相关教材或工具手册 1.5 工作计划 1、领取设计任务书,查阅相关资料(3天); 2、确定设计方案,进行相关的工艺设计(5天); 3、校核验算,获取最终的设计结果(2天); 4、编写课程设计说明书(论文),绘制工艺流程图(3天)。 1.6设计成果要求 1、通过查阅资料、设计计算等最终提供课程设计说明书(论文)电子稿及
目录 一、设计任务书………………………………………………… 二、前言………………………………………………………… 三、确定设计方案……………………………………………… 四、概述……………………………………………………… 五、主要符号说明…………………………………………… 六、设计计算………………………………………………… 七、参考文献………………………………………………… 八、设计自评………………………………………………… 九、附图………………………………………………………
一、设计任务书 一、题目: 某常减压蒸溜装置31.82万吨/年原油预热系统工艺设计 二、任务给定条件: 某炼油厂用柴油将原油预热。定性温度下柴油和原油的有关参数如下表。要求两侧流体的压降都不超过50KPa,试选用适当的列管式换热器(一台或多台)。 物料温度℃质量流量平均比热容平均密度导热系数粘度 入口出口Kg/h kJ/(kg.K) kg/m3W/(m.K) ×103Pa.s 30000 2.48 715 0.13 0.64 柴油175 T 2 原油70 110 40000 2.20 815 0.128 3.0 1、柴油质量流量30吨/小时,原油40吨/小时【以学号25号为基准,1-24(30/40-学号×0.1吨/小时)。26-50号(30/40+学号×0.1吨/小时)。 2、换热设备可选择浮头式或U型管式换热器;换热器内外两侧的污垢热阻均可取 1.72×10-4m 2.℃/W;忽略管壁热阻。 3、节约成本核算参考:若采用4.855千克(力)/厘米2饱和水蒸气预热原油,饱 和水蒸气放热后出口为80℃水,水蒸气180元/吨,计算每年节省的费用。 三、设计说明书主要内容要求: 包括封面、目录、设计任务书、参考文献、符号说明和设计自评,其中正文包括下述内容: a)前言(说明设计题目——31.82万吨/年,设计进程及自认达到的目的) b)换热系统工艺流程设计和计算 冷却水用量,换热器进出口温度等热量衡算,包括根据换热流体的特性和操作参数决定流体走向(哪个走管程、哪个走壳程);计算平均温差。 c)根据换热器工艺设计及计算的结果,对换热器选型 i.换热器管程、折流挡板间距、管子排列方式 ii.换热器接管尺寸确定 iii.管、壳层压降校验 iv.年节约成本核算参考:以饱和水蒸气的年消耗量计算 v.设计结果汇总与评价 四、附图(手绘3号图,1张) 1.换热器结构图 2.管板(包括管子排列方式)剖面图 3.管板与壳体连接局部放大图 4.列管与管板连接局部放大图