
2015高考实验专题复第1课时
吴家山中学高三年级杨敦俊
一、重视《综合实验》中的新装置及操作方法
【案例1 】 (2014年普通高等学校招生全国统一考试浙江卷)
28.[15分]二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,
反应的化学方程式及装置图(部分装置省略)如下:
C O CH
OH +2FeCl 3C O O +2FeCl 2+2HCl
在反应装置中,加入原料及溶剂,搅拌下加热回流。反应结束后加热煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯。重结晶过程:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥 请回答下列问题:
(1)写出装置图中玻璃仪器的名称:a___________,b____________。
(2)趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体:____。
A .缓慢冷却溶液
B .溶液浓度较高
C .溶质溶解度较小
D .缓慢蒸发溶剂
如果溶液中发生过饱和现象,可采用__________等方法促进晶体析出。
(3)抽滤所用的滤纸应略_______(填“大于”或“小于”)布氏漏斗内径,将全部小孔盖住。
烧杯中的二苯基乙二酮晶体转入布氏漏斗时,杯壁上往往还粘有少量晶体,需选用液体将杯壁上的晶体冲洗下来后转入布氏漏斗,下列液体最合适的是________。 A .无水乙醇 B .饱和NaCl 溶液 C .70%乙醇水溶液 D .滤液 抽滤完毕或中途停止抽滤时,应先 ,然后 。
(4)上述重结晶过程中的哪一步操作除去了不溶性杂质:___________,哪一步操作除去了可溶性杂质:___________
[反思1]本题主要涉及了抽滤操作?抽滤操作的装置、原理、优点、使用注意事项你掌握了吗?
[反思2]本题主要涉及了重结晶、洗涤?这些操作的目的、使用注意事项你掌握了吗? 【反馈1】[2013高考样卷]苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钠水溶液中的歧化反应制得,反应式为:
+NaOH 2
COONa
CHO
+
CH 2OH
某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
COOH
CH 2OH
重结晶
重结晶过程:溶解—→活性炭脱色—→趁热过滤—→冷却结晶—→抽滤—→洗涤—→干燥 已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。 请根据以上信息,回答下列问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是 ,
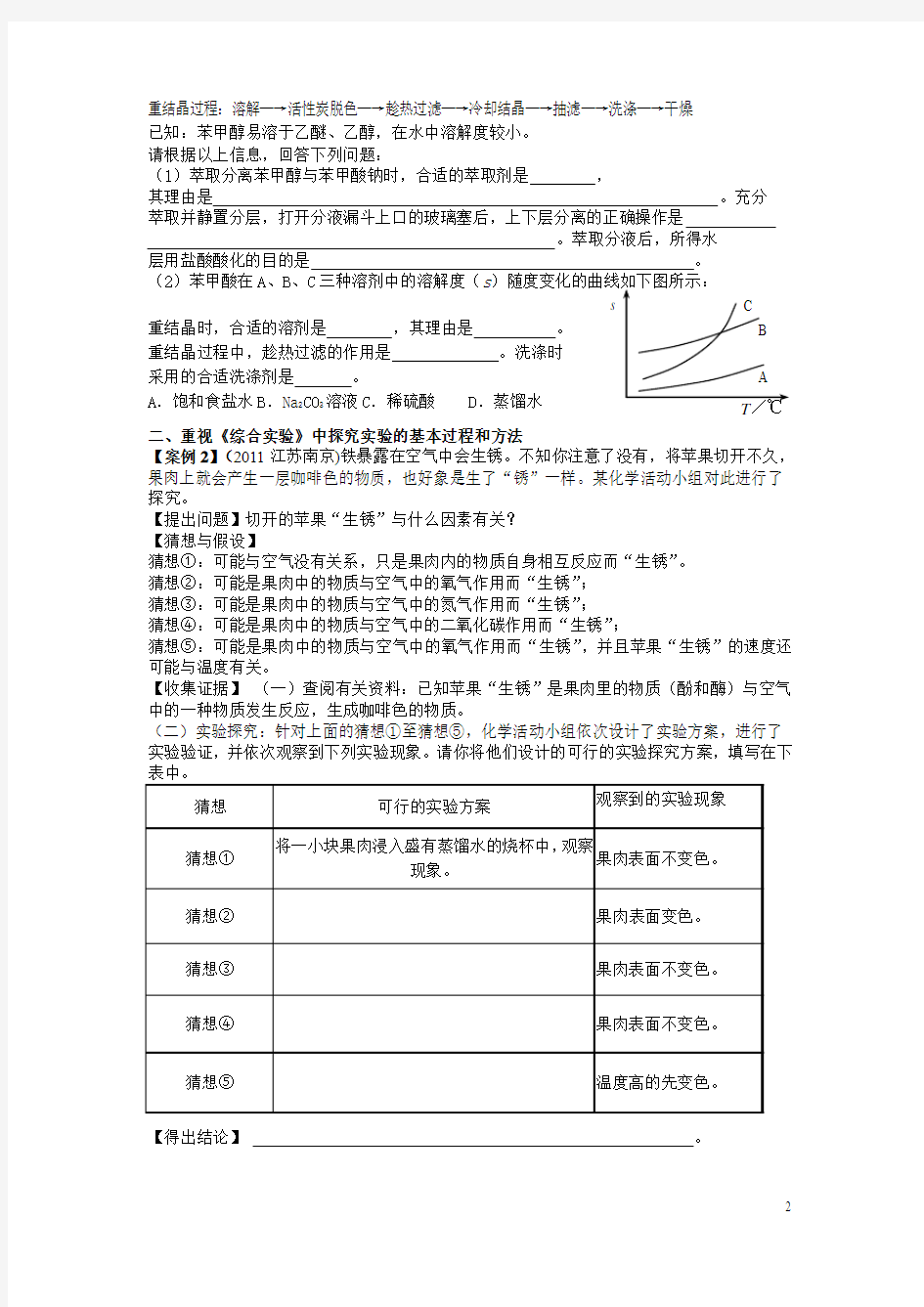
其理由是 。充分 萃取并静置分层,打开分液漏斗上口的玻璃塞后,上下层分离的正确操作是 。萃取分液后,所得水 层用盐酸酸化的目的是 。 (2)苯甲酸在A 、B 、C 三种溶剂中的溶解度(s 重结晶时,合适的溶剂是 ,其理由是 。 重结晶过程中,趁热过滤的作用是 。洗涤时
采用的合适洗涤剂是 。
A .饱和食盐水
B .Na 2CO 3溶液
C .稀硫酸
D .蒸馏水
二、重视《综合实验》中探究实验的基本过程和方法
【案例2】(2011江苏南京)铁暴露在空气中会生锈。不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,也好象是生了“锈”一样。某化学活动小组对此进行了探究。
【提出问题】切开的苹果“生锈”与什么因素有关? 【猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”。 猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”; 猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”; 猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”; 猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关。
【收集证据】 (一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质。
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象。请你将他们设计的可行的实验探究方案,填写在下
【得出结论】 。
【反思与评价】(1)在②—⑤四种猜想中,你认为猜想(填代号)最不合理,
理由是。
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变
色,其可能的原因是。
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是
。
[反思]本题是一道实验探究题,你了解实验探究的基本过程和主要方法吗?,你是否了
解可以通过控制哪些条件对实验进行探究吗?
【反馈2】某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72—转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究
有关因素对该反应速率的影响,探究如下:
(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和
一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化为________(填化学式)。
(3)实验①和②的结果表明________;实验①中0~t1时间段反应速率v(Cr3+)=________
答案(1)
(2)CO2
(3)溶液pH对该反应的速率有影响
(4)Al3+起催化作用SO42—起催化作用
(5)
(1)根据题意要求,调节不同初始pH和一定浓度草酸溶液用量,做对比实验,由此可知实验③改变的是草酸溶液用量,但应保持溶液总体积不变。(2)草酸中碳的化合价为+3价,与强氧化性物质K2Cr2O7反应后,草酸应被氧化为CO2。(3)根据实验①、②的曲线对比,在相同草酸用量不同pH时,反应速率不同,所以pH对该反应有一定的影响;在0~t1时间段内,v(Cr2O72—)=mol·L-1·min-1,由Δc(Cr3+)=2Δc(C r2O72—)所以v(Cr3+)=mol·L-1·min-1。(4)根据铁明矾组成离子可知,起催化作用的离子可能为Fe2+、Al3+、SO42—。(5)可通过在其他条件不变时,加入等物质的量的K2SO4·Al2(SO4)3·24H2O替代实验中的铁明矾,此时溶液中不存在Fe2+,但仍存在SO42—和Al3+,通过测定c(Cr2O72—)看是否仍然有催化效果来判断。
(1)乙醚(1分)
苯甲醇在乙醚中的溶解度大于在水中的溶解度,且乙醚与水互不相溶(2分)从下口放出下层液体,从上口倒出上层液体(2分)将苯甲酸钠转化为苯甲酸,析出晶体(2分)(2)C(1分)随温度升高溶解度增加较快(2分)除去不溶性杂质,防止苯甲酸冷却后结晶析出(2分)D(1分)(3)98.60 %
【答案】(1)CO2和CO
(2)利用焰色反应透过蓝色钴玻璃,观察到紫色的火焰
(3)①全部为铁单质全部为FeO 同时存在铁单质和FeO
③
【解析】(1)将产生的气体产物依次通过澄清石灰水,石灰水变混浊,说明产生的气体中含有CO2,然后再通过灼热氧化铜、澄清石灰水,观察到有红色固体生成,澄清石灰水都变浑浊,气体中含有CO;(2)碱金属元素的检验一般采用焰色反应;(3)依据信息:固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3,可推测铁元素只能以亚铁及铁单质的形式存在;在设计实验时,应注意Fe与FeO的性质的不同点。
【考点分析】:考查考生对元素及其化合物性质的掌握,对物质进行检验的实验技能,考查考生运用相关知识对实验提出假设及设计方案的能力。
第十一章化学实验基础 第一节化学实验基本方法 1.(2010·原创)不能用带橡皮塞的玻璃试剂瓶存放的药品是() ①浓硝酸②稀氢氧化钠溶液③液溴④纯碱溶液⑤水玻璃⑥氢氟酸 A.①③⑥B.①④⑥C.①⑤⑥D.除⑥外全部 解析:浓硝酸和液溴都具有强氧化性,能氧化橡胶塞,而氢氟酸会腐蚀玻璃,不能用玻璃试剂瓶存放,应保存在塑料瓶或铅皿容器中,故选A。 答案:A 2.下列仪器用酒精灯加热时,需垫石棉网的是() ①烧杯②坩埚③锥形瓶④蒸发皿⑤试管⑥烧瓶⑦表面皿 A.②④⑤B.①⑥⑦C.③④⑥D.①③⑥ 解析:加垫石棉网,目的是使仪器受热均匀,防止炸裂。可直接加热的仪器有:试管、坩埚、蒸发皿;隔石棉网可加热的仪器有烧杯、锥形瓶、烧瓶(圆底、平底和蒸馏烧瓶)表面皿不能加热。 答案:D 3.(2010·模拟精选,河北保定模拟)化学是以实验为基础的科学,化学实验设计和操作中必须十分重视师生安全问题和环境保护问题。下列操作方法不正确的是() A.制氧气时,用排水法收集氧气出现倒吸现象,立即松开试管上的橡皮塞 B.在气体发生装置上直接点燃乙炔气体时,必须先检验乙炔气体的纯度 C.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 D.给试管中的液体加热时不停移动试管或加入碎瓷片,以免爆沸伤人 解析:选项A,产生倒吸现象的原因是由于装臵内压力的降低,致使收集气体时,水槽中的水进入制气装臵中,松开试管上的橡皮塞可阻止倒吸的水进入制气装臵中。选项B,点燃可燃性气体之前,都要对气体进行验纯,防止出现爆炸事故。选项C,实验结束后的废液中有的含有有毒性的物质,不能直接倒入下水道,应倒入指定的容器中,经处理后再排放;选项D,给试管中的液体加热时,不停移动试管可使试管内的液体受热均匀,加入碎瓷片也能防止出现爆沸现象。 答案:C 4. 下列实验操作或仪器的用法正确的是()
高考综合题地理小专题答题模式 ----地理特征类【答题模式+高考真题+强化训练】 目录 引言------------------------------------------------------2 地理位置特征------------------------------------------3 气候特征------------------------------------------------8 气温特征------------------------------------------------11 降水特征------------------------------------------------15 地形特征------------------------------------------------18 地势特征------------------------------------------------21 河流水文特征------------------------------------------24 河流水系特征------------------------------------------28 自然地理环境特征------------------------------------33 等值线特征---------------------------------------------36 地理点状分布图特征---------------------------------40 地理面状分布图特征---------------------------------42 地理统计图特征---------------------------------------45 地理其它特征类题目---------------------------------50
高考化学专题:实验探究 1.)某中学化学实验小组为了证明和比较SO2和氯水的漂白性,设计了如下装置: 品红溶液NaOH溶液品红溶液 A B C D E ⑴实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质__________________ ⑵反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加 热,两个试管中的现象分别为:B D____________________ ⑶装置C的作用是________________________________________ ⑷该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验: SO2 NaOH溶液 通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。 试根据该实验装置和两名同学的实验结果回答问题。 ①指出在气体进入品红溶液之前,先将SO2和Cl2通过浓硫酸中的目的: 。 ②试分析甲同学实验过程中,品红溶液不褪色的原因是: 。(结合离子方程式说明) ③你认为乙同学是怎样做到让品红溶液变得越来越浅的? 。 2.((A).亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、 油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O。 ②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。 ③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。 (1)160 g/L NaOH溶液的物质的量浓度为。若要计算该溶液的质量分数,还需要的一个条件是(用文字说明)。(2)发生器中鼓入空气的作用可能是(选填序号)。 a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸; c.将NaClO3氧化成ClO2 (3)吸收塔内的反应的化学方程式为。 吸收塔的温度不能超过20℃,其目的是。(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是。(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是(选填序号)。 a.Na2O2b.Na2S c.FeCl2 (6)从滤液中得到NaClO2?3H2O粗晶体的实验操作依次是(选填序号)。 a.蒸馏b.蒸发c.灼烧d.过滤e.冷却结晶 要得到更纯的NaClO2?3H2O晶体必须进行的操作是(填操作名称)。 3..过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下: 2Na2CO3 + 3H2O2→2 Na2CO3·3H2O2 + Q (Q>0)
专题强化训练(九) 语言表达简明、得体题 1.阅读下面一段文字,按要求完成后面的题目。 或许是与我们从小接受的教育有关,从家庭教育到学校教学教育,都要求“让、让、让”,即便在家庭中一群孩子一起玩耍,大人们要求的都是“大的必须让小的”,不管“小的”有没有道理,在学校,一直被要求谦卑畏缩、先人后己,课本还有“孔融让梨”的故事,慢慢地这种不与世人争的观念就潜移默化,悄悄地成了思维观念和处事方式。不是“不好意思”的处事方式不好,而是凡事不能过度,一旦过了某个临界,所谓的“不好意思”就演变成了“死要面子”。其实,“不好意思”这类人大多本性善良,不忍伤害他人,总站在对方角度考虑思考问题,把委屈和困难留给自己,把方便和快乐留给别人。 (1)在不改变语意的前提下,为了表达简明,文中必须删掉两个词语,分别是“________”和“________”。 (2)文中使用不得体的两个词语,分别是“________”和“________”。 答案:(1)教学思考(2)畏缩潜移默化 2.阅读下面一段文字,按要求完成后面的题目。 心理问题,是农村留守儿童最值得被注意关注的问题。长期的单亲监护或隔代监护,甚至是他人监护、无人监护,使留守儿童无法像其他孩子那样得到父母的关爱,家长也不能随时了解、把握孩子的心理、思想变化。这种亲情的缺失使孩子变得孤僻、抑郁,甚至有一种被扔了的感觉,严重地影响到了孩子心理的健康发展。这些心理方面的问题,直接影响到孩子的办事,使他们不论是在家里,还是在学校、社会都经常出现一些与其他孩子不一样的举动行为,这些行为常常超越道德、法律底线。 (1)在不改变语意的前提下,为了表达简明,文中必须删掉两个词语,分别是“__________”和“____________”。 (2)文中使用不得体的两个词语,分别是“__________”和“____________”。 答案:(1)注意举动(2)扔了办事 3.下面是××公司开业庆典的贺词的正文,请阅读并按要求完成后面的题目。 今天是××公司值得纪念的喜庆日子,我们在这里庆祝××公司隆重进行开业,值此开业庆典之际,请允许我对××公司表示热烈的祝贺。××公司是一个朝气蓬勃、富有想象力和创造力的公司,我们相信在上级主管部门的领导下,在社会各界朋友的过问下,经过公司全体同仁的努力拼搏,××公司一定会逐渐成长壮大!××公司就像一艘刚刚起航的航船,让我们一起同仇敌忾,驶向更美好的明天! (1)在不改变语意的前提下,为了表达简明,文中必须删掉两个词语,分别是“__________”和“____________”。
12. ( 2011江苏高考10 ,15分)高氯酸铵(NH 4CIO 4)是复合火箭推进剂的重要成分,实 验室可通过下列反应制取 NaClO +(aq) + NH 4Cl(;aq) = NH 4CIO< (aq)+NaCl(aq) (1)若NH 4CI 用氨气和浓盐酸代替,上述反应不需要外界供热就能进行, 其原因是 ________ (2 )反应得到的混合溶液中 NH 4CIO 4和NaCI 的质量分数分别为 0.30和0.I5 (相关物质 的溶解度曲线见图 9)。从混合溶液中获得较多 NH 4CIO 4晶体的实验操作依次为(填操作名 称) _________ 、干燥。 (3 )样品中NH 4CIO 4的含量可用蒸馏法进行测定,蒸馏装置如图 10所示(加热和仪器固 定装置已略去),实验步骤如下: 步骤1:按图10所示组装仪器,检查装置气密性。 步骤2:准确称取样品a g (约0.5g )于蒸馏烧瓶中,加入约 150mL 水溶解。 步骤3:准确量取40.00mL 约0.1 moI ? L - 1 H 2SO 4溶解于锥形瓶中。 步骤4:经滴液漏斗向蒸馏瓶中加入 步骤5:加热蒸馏至蒸馏烧瓶中剩余约 步骤6:用新煮沸过的水冲洗冷凝装置 步骤7:向锥形瓶中加入酸碱指示剂, 标准溶液V 1mL 。 一 1 20mL3 mol ? L NaOH 溶液。 100mL 溶液。 2?3次,洗涤液并入锥形瓶中。 用c mol ? L _1 NaOH 标准溶液滴定至终点, 消耗NaOH
步骤8?将实验步骤1?7重复2次 IWH細 ①步骤3中,准确量取40.00ml H2SO4溶液的玻璃仪器是________________________________ 。 ②步骤1?7中确保生成的氨被稀硫酸完全吸收的实验是__________________________________ (填 写步骤号)。 ③为获得样品中NH4CIO4的含量,还需补充的实验是 _______________________________________ 。 【分析】本题以复合火箭推进剂的重要成分制取和分析为背景的综合实验题,涉及理论分析、阅读理解、读图看图、沉淀制备、沉淀洗涤、含量测定等多方面内容,考查学生对综合实验处理能力。 【备考提示】实验的基本操作、实验仪器的选择、实验误差分析、物质的除杂和检验等内容依然是高三复习的重点,也是我们能力培养的重要目标之一。 答案:(1)氨气与浓盐酸反应放出热量 (2 )蒸发浓缩,冷却结晶,过滤,冰水洗涤 (3)①酸式滴定管 ②1、5、6 ③用NaOH标准溶液标定H2SO4溶液的浓度(或不加高氯酸铵样品,保持其他条件相同,进行蒸馏和滴定实验) 13. (2011江苏高考,12分)草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解 液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)实验过程如下:
高考地理大题题型与答题模式 1特征描述类 设问形式: 描述事物即表现事物的形态或状态。高考中特征描述类试题,设问形式一般有“说明……特点”,“描述……状况”,“简述……特征”,“从……等方面归纳……主要特征”等。 思维建模 要准确描述地理事物特征必须把握正确的思维方式,建立解答该类试题的答题模式,并用规范而专业的语言准确地描述出来。具体答题思路是:首先要对题目涉及区域进行区域空间定位(经纬网定位法和区域特征定位法相结合),明确区域位置(海陆位置、经纬度位置、相对位置)和图文信息,然后结合所学知识进行特征分析;在描述时要注意梳理、组织语言,把握关键词,并且做到简洁、准确地描述。 模板典例 1.自然地理特征:地形、气候、土壤、水文(河流、湖泊)、植被(自然带) 2.地形特征: ①主要地形类型(高原、山地、平原、丘陵、盆地或河谷、冲积扇、三角洲); ②地势——海拔高低、地势起伏状况、地形倾斜方向、区域极值(地势最高、低值);③主要地形区及其分布。 3.地表环境特征: ①气候(湿、热、冷、干)②植被状况 ③土地类型(荒漠、草地、林地、耕地)④河流发育程度 4.气候特征: ①气温(气温高低、日较差和年较差大小) ②降水(总量、季节或年际变化) ③降水与热量的组合状况(如雨热同期) 5.河流水文特征:①年径流量;②汛期;③含沙量;④结冰期(凌汛);⑤流速。 6.河流水系特征: ①流向与长度②流域面积③支流多少及形态 ④河网形态、密度⑤河道深浅、弯曲、宽窄⑥落差或峡谷分布 7.农业生产特征: ①农业地域类型②农作物种类及分布③农业各部门结构(所占比重) ④生产水平(机械化水平、生产经营方式、专门化水平商品率)
高三化学实验 一、研究《考试说明》 1、对化学学习能力的要求 化学实验与探究能力(4项要求) ⑴了解并初步实践化学实验研究的一般过程,掌握化学实验的基本方法和技能。 ⑵在解决简单化学问题的过程中,运用科学的方法,初步了解化学变化规律,并对化学现象提出科学合理的解释。 2、考试范围与要求 化学实验基础 (1)实验要求 ①了解化学实验是科学探究过程中的一种重要方法。 ②了解化学实验室常用仪器的主要用途和使用方法。 ③掌握化学实验的基本操作。能识别化学品安全使用标识,了解实验室一般事故的预防和处理方法。 ④掌握常见气体的实验室制法(包括所用试剂、仪器,反应原理和收集方法)。 ⑤了解常见离子的检验方法,能对常见的物质进行检验、分离和提纯。 ⑥能根据要求配制一定溶质质量分数、物质的量浓度的溶液。了解测定溶液pH的方法。 ⑦能根据实验试题要求,做到: ⅰ.设计、评价或改进实验方案; ⅱ.了解控制实验条件的方法; ⅲ.分析或处理实验数据,得出合理结论; ⅳ.识别典型的实验仪器装置图。 ⑧以上各部分知识与技能的综合应用。 总结:1-6考查基础实验;7-8考查综合实验。 (2)实验内容(22) 化学1(9): 1、萃取与分液 2、离子的检验(Cl- Ag+ SO42- CO32- NH4+ Fe3+ ) 3、配制一定物质的量浓度的溶液 4、钠的性质 5、氢氧化铝的两性 6、铁及其化合物间的转化 8、碳酸钠与碳酸氢钠的性质 9、二氧化硫和浓硫酸的性质 化学2(7): 10、探究钠、镁、铝单质的金属性强弱 11、影响化学反应速率的因素 12、化学反应中的热量变化 13、原电池的工作原理 14、乙醇的主要性质 15、乙酸乙酯的制取和乙酸乙酯(或油脂)的水解 16、葡萄糖与新制氢氧化铜的反应
专题强化训练(一) Ⅰ. 语法填空 A One night four college kids 1. (stay) out late,partying and having a good time. They paid no mind 2. the test they had scheduled for the next day and didn't study. In the morning,they hatched a plan to get out of 3. (take) their test. They covered 4. (they) with grease (润滑油) and dirt and went to the Dean's office 5. (nervous). Once there, they said they 6. (be) to a wedding the previous night and on the way back they got 7. flat tire and had to push the car back to campus. The Dean listened to their sad story and got lost in deep 8. (think). Then he offered them a retest three days later. They thanked him and accepted his offer. 9. the test day arrived,they went to the Dean. The Dean put them all in separate 10. (room) for the test. They were fine with this since they had all studied hard. Then they saw the test. It had 2 questions. B Owing to the effect of traditional Chinese medicine and treatment, it becomes more and more popular now in the world. Traditional Chinese medicine originated in ancient and developed for 1. long time. It has collected various ways to treat 2. (differ) diseases. Traditional Chinese medicine pays attention 3. the balance of the body system. Once the body system balances, the disease 4. (disappear). The damage of the body system is the source of the disease. TCM is an important part of Chinese culture. Great 5. (success) have been made in many areas through TCM cure. As to acute stomachache, there is no need 6. (have) an operation; all you need is a cup of Chinese herbs, 7. the western way takes more time and money. You may even take the risk of 8. (infect) after operation. 9. (compare) with the western medicine high fees, TCM has a reasonable price that ordinary people can afford. I think TCM will be the mainstream in the health services in the future in China. And our country should invest more money on the 10. (develop) of TCM; make sure it is not going to fade away. Ⅱ. 短文改错 Early rising has many advantage. First, it helps us to keep health. We all need fresh air, and the air is freshest in the morning. Beside, we can improve our health by exercise regularly in the morning. Second, it can also benefits our study because in the morning we can learn more quickly. Third, it can make us to plan our work for the day. Only without a proper plan can we work well. Early rising can allow us enough time to get ready for your work. So we say that those who always gets up late should make an effort to get up early.
2011年普通高等学校招生全国统一考试(福建卷) 理科综合能力测试化学部分 6、下列关于化学与生产、生活的认识不正确 ...的是() A.CO2、CH4、N2等均是造成温室效应的气体 B.使用清洁能源是防止酸雨发生的重要措施之一 C.节能减排符合低碳经济的要求 D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 7、依据元素周期表及元素周期律,下列推断正确的是() A.H3BO3的酸性比H2CO3的强 B.Mg(OH)2的碱性比Be(OH)2的强 C.HCl、HBr、HI的热稳定性依次增强 D.若M+和R2-的核外电子层结构相同,则原子序数:R>M 8、下列关于有机化合物的认识不正确 ...的是() A.油脂在空气中完全燃烧转化为水和二氧化碳 B.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 C.在水溶液里,乙酸分子中的—CH3可以电离出H+ D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应 9 10、常温下) A.将溶液稀释到原体积的10倍 B.加入适量的醋酸钠固体 C.加入等体积0.2 mol·L-1盐酸 D.提高溶液的温度 11、研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料, 以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确 ...的是() A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成 C.放电时OH-向正极移动 D.总反应为:2Li+2H2O=== 2LiOH+H2↑ 12、25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应: Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。 下列判断正确的是() A.往平衡体系中加入金属铅后,c(Pb2+)增大 B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 D.25℃时,该反应的平衡常数K=2.2 23、(15分) I、磷、硫元素的单质和化合物应用广泛。 (1)磷元素的原子结构示意图是____________。 (2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为: 2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10 10C+P4O10===P4+10CO 每生成1 mol P4时,就有________mol电子发生转移。 (3)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
2013 高考地理综合题答题规范 简答题规范系列(一):地理计算专题1.经纬度计算: ①经度差与地方时差算经度——地方时每相差 1 小时,经度相差1°; ②纬差法与正午太阳高度算纬度——正午太阳相差多小,纬度相差多少; ③北极星的仰角即地平高度等于当地地理纬度; ④经纬线上长度算经纬度: 1 ° 经线长=111km ; 1 ° 纬线长=111cos?km(血为纬度)。 2.比例尺计算:比例尺=图上距离/实地距离 3?相对高度的计算:(n-1)d w" h v (n+1)d (其中n 表示两地间不同等高线的条数, d 表示等高距)。 4 ?流域面积的计算: ⑴ 作出流域的分水线即山脊线,由分水岭所围的区域即为流域的范围; ⑵ 因图形不规范,计算时一般算出图幅面积后,再分析流域面积占图幅面积的比重,相乘即可。 5.有关时间计算: ⑴ 某地时区数=该地经度十15,对商取整数部分,尾数部分四舍五入; ⑵ 根据各时区中央经线的地方时即为本时区区时,相邻的两个时区的区时相差 1 小时,即求某地区区时=已知地区时±两地时区,注意东加西减; ⑶ 根据东早西晚,经度每相差15°,地方时相差 1 小时。即求某地地方时=已知某地地方时± (两地 经度差X 4分钟/1°),注意东加西减; ⑷ 日期界线有两条: ①时间界线: 即地方时0时经线,以东早一天,为新的一天,以西晚一天,为旧的一天; ②空间界线: 即国际日期变更线,也就是180°经线(但两者并不完全重合), 规定日界线以东晚一天,为旧的一天,以西早一天, 为新的一天; ③新的一天的范围即从地方时0 时经线向东到180°经线的范围; 新的一天的范围=180°经线的地方时X 15。 ⑸ 日照图上晨线与赤道交点所在经线地方时为6:00,昏线与赤道交点所在经线的地方时为18:00;晨昏线与某纬线的切点所在经线为0:00(切点为极昼)或12:00(切点为极夜)。 6 .地球自转速度计算: ①地球上除南北极点外,其它各地角速度都相等,大致每小时15°; ②地球上赤道处线速度最大,南北极点为0, 任意纬线上线速度V ? =V 赤道cos? =1670cos ? km/h ; ③同步卫星的角速度与地球上除极点外的任一点都相等,线速度比地面对应点大。 延伸:卫星发射基地的选址条件: ①纬度低(可以节省火箭燃料,增加火箭的有效负载); ②天气稳定,大气能见度高; ③交通便利(铁路或海运); ④地形平坦开阔,地质稳定; ⑤从安全性来讲,以设在远离工业中心、居民稀少的地区为宜。 例1:酒泉卫星发射基地的优势条件是哪些?我国即将在海南文昌建立新的卫星发射中心,其优势条件又是哪些? ①酒泉发射基地地处巴丹吉林沙漠的绿洲之中,靠近兰新铁路,地势平坦开阔,人烟稀少,干燥少雨,大气能见度高,适于发射的天数多。 ②海南文昌卫星发射中心的优势:纬度低,有良好的海上运输条件,火箭航区和残骸落区可以避开地面人口稠密地区,安全性好。 例2:试分析神舟六号飞船返回舱着陆场的有利条件? ①当地人烟稀少; ②温带大陆性气候,晴天多,空气能见度高; ③地形平坦开阔。 7 ?太阳高度及正午太阳高度计算: A. 概念: ①太阳高度:太阳光线与地平面的夹角(锐角); ②正午太阳高度:一天中最大的太阳高度。 B. 日影朝向与太阳光线方向(太阳方位)相反,影长与太阳高度呈反比, 影长=h x ctga(h为物体高度,a为太阳高度)。 C. 太阳方位问题: ①若直射点在某地以南,该地正午太阳位于正南 方位; ②若直射点在某地以北,该地正午太阳位于正北 方位。 ③太阳直射的地方,正午太阳位于天顶。 D. 日出方位问题:
高三化学实验专题基础实验练习题 1.下图是一套实验室制取气体装置,用于发生、干燥、收集和吸收有毒气体,下列各组物质能利用这套装置进行实验的是〔〕 A.MnO2和浓盐酸 B.Na2SO3〔s〕和浓H2SO4 C.Cu片和稀HNO3 D.浓氨水和生石灰 2.关于下列各装置图的叙述中,正确的是 A.电解装置甲中,d为阳极、c为阴极 B.装置乙可用于收集NH3等密度比较小的气体,不可以收集CO2等密度较大的气体C.装置丙中X若为四氯化碳,可用于吸收氨气或氯化氢等易溶于水的气体D.装置丁可用于实验室制取并收集乙酸乙酯 3.下列实验中,能达到预期目的的是〔〕 A.用过滤法除去Fe 〔OH〕3胶体中的FeCl3 B.只需在淀粉KI溶液中滴加少量市售食盐配制的溶液,就可鉴别真假碘盐 C.用广泛试纸测得氯水的pH值为2.1 D.液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中 4.下列有关化学实验的叙述中,正确的是〔〕 A.中和滴定实验中应用待测液润洗锥形瓶 B.蒸馏操作时应将温度计的水银球插入液面下 C.NaOH溶液应保存在带玻璃塞的试剂瓶中 D.配制硫酸亚铁溶液,是将绿矾晶体溶于稀硫酸中,再加入一定量的铁粉 5.下列实验问题处理方法错误的是〔〕 ①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液 ②实验中,点燃CO前应首先检验CO的纯度 ③实验结束后,可将所有的废液倒入下水道排出实验室 ④给试管中的液体加热时加入碎瓷片,以免暴沸伤人 ⑤测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算 ⑥配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸 A.①② B.②④⑤ C.①③⑤ D.②④⑥ 6. 下列对实验现象或结论的预测正确的是〔〕 A.向苯酚钠溶液中通入CO2,溶液变浑浊,继续通入CO,至过量,又变澄清 B.向NaOH溶液中通入足量CO2,再加入少量Ba〔OH〕2溶液,CO32-浓度增大 C.向NaAlO2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 D.向银氨溶液中滴加盐酸至过量,开始有沉淀出现,后来沉淀又溶解 7.利用下列实验装置能完成相应实验的是〔〕
专题强化训练(三十) 小说探究题 一、阅读下面的文字,完成1~3题。 送不出去的祝福 吕啸天 临近新年还有三天,丰城莲花山来福寺住持喜福大师派弟子虚水下山,带着祥符把新年的美好祝愿送给丰城的百姓。虚水出家才几个月,做这样的事还是第一次。他问喜福大师:“师父,居住在山下的施主几十万人,弟子不知道该送给谁合适。” “一念之慈,万物皆善。福喜之愿,万人皆喜。”喜福大师微微一笑说,“新年的祝福当送给有缘之人。” 虚水一边下山一边想,居住在丰城的百姓有几十万,归纳起来只有两种:富人和穷人。于是他一路打听来到了丰城首富何有国的府上。年近半百的何有国抽着水烟在府上安排管家置办年货、搭戏台。听虚水道明来意,何有国冷冷一笑说:“何某经营商号顺风顺水,家大业大,富贵满门,何须寺里再来凑这个热闹?”让管家把放在桌上的祥符一把塞回虚水的手中,连推带送把虚水赶了出去。 虚水无奈,一路打听又来到了城北莲花村村民向喜莲家中。年过三十的向喜莲,丈夫暴病而亡,寡居的她一人带着两个孩子靠种几亩薄地度日,常常吃了上顿没下顿,为一日三餐操碎了心。眼下她正为过年饭菜和两个孩子的新衣服发愁。虚水递过来的祥符,她看都没看:“不能当饭吃,不能当衣穿,有什么用?你拿走。”她也把虚水赶了出去。 祥符和新年的美好祝愿送不出去,接连碰了两个钉子,虚水感到很憋屈,再也没有心思做下去了。回到寺里,虚水说了下山的经过。喜福大师微微一笑说:“出家之人,不拘俗世之念。明早你再下山,再找此两人送上祝福。” 师命难违。次日一早,虚水又带着祥符和新年的美好祝愿下山。他再次来到何有国的府上。虚水二次登门,何有国没有见他,也没有接受他的祥符。何有国这样做不是说他真的不需要美好祝愿。他是担心一旦接受了祥符,今后寺里借送祝福之名向他伸手要银子,就不好拒绝。何有国想了片刻,让管家拿了三两银子交给虚水,说是捐给寺里的香火钱。 虽然还是没有送出祥符,但得到了三两银子的捐赠,虚水心里好受了一些。他又走了两个时辰,来到了向喜莲的家中。年关更近,穷苦人的生活更显得艰难。向喜莲愁苦满脸,坐在旧房子角落里暗自垂泪,两个年幼的孩子躲在一边哭泣,显得很凄惶。 虚水叹了一声,心想:她这个样子再送上祥符,她肯定不要。他做出了新的决定:把何有国捐给寺里的三两银子转捐给向喜莲。 向喜莲接过银子,激动得放声大哭,让两个孩子给虚水磕头谢恩。虚水扶起孩子,逃也似的离开村里。
1.【2018新课标1卷】在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是 A.A B.B C.C D.D 【答案】D 【解析】分析:在浓硫酸的作用下乙酸与乙醇发生酯化反应生成乙酸乙酯,根据乙酸乙酯的性质、产品中含有的杂质,结合选项解答。 点睛:掌握乙酸乙酯的制备原理是解答的关键,难点是装置的作用分析,注意从乙酸乙酯的性质(包括物理性质和化学性质)特点的角度去解答和判断。 2.【2018新课标2卷】下列实验过程可以达到实验目的的是
A.A B.B C.C D.D 【答案】B 【解析】分析:A.氢氧化钠溶于水放热; B.根据铁离子具有氧化性结合溶液颜色变化分析; C.氢气中含有氯化氢和水蒸气,据此解答; D.根据双氧水与亚硫酸氢钠反应的实验现象分析。 点睛:明确相关物质的性质特点、发生的反应和实验原理是解答的关键。注意设计或评价实验时主要从正确与错误、严密与不严密、准确与不准确、可行与不可行等方面作出判断。另外有无干扰、是否经济、是否安全、有无污染等也是要考虑的。本题中选项D是解答的易错点,学生往往只考虑物质的浓度不同,而忽略了实验结论需要建立在实验现象的基础上。 3.【2018新课标2卷】实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是 A.A B.B C.C D.D 【答案】D 【解析】分析:在光照条件下氯气与甲烷发生取代反应生成氯化氢和四种氯代烃,结合有关物质的溶解性分析解答。 点睛:明确甲烷发生取代反应的原理和有关物质的溶解性是解答的关键,本题取自教材中学生比较熟悉的实验,难度不大,体现了依据大纲,回归教材,考查学科必备知识,体现高考评价体系中的基础性考查要求。 4.【2018新课标3卷】下列实验操作不当的是 A.用稀硫酸和锌粒制取H2时,加几滴CuSO4溶液以加快反应速率 B.用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂 C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+ D.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二 【答案】B
实验专题 1、某化学兴趣小组的甲、乙、丙三位同学在学习Na 2O2 与CO2的反应时,就提出SO2与Na2O2反应的问题。 同学们设计实验探究SO2与Na2O2的反应。 (1)甲同学认为Na2O2和SO2的反应与Na2O2和CO2的反应 类同,设计了下图实验装置,并将带火星的木条伸到导 管口,预期现象与结果相反,如果甲同学的观点是正确 的,请你分析实验失败的原因是 __________________________________________________________ (2)反应完毕后,综合大家的观点,认为硬质玻璃管中的固体成分有多种可能: 可能Ⅰ:全部为Na2SO3;可能Ⅱ:为Na2SO3和Na2O2的混合物;可能Ⅲ:________ 可能Ⅳ:为Na2SO3和Na2SO4的混合物;可能Ⅴ:为Na2O2和Na2SO4的混合物; 可能Ⅵ:为Na2O2、Na2SO3和Na2SO4的混合物。 (3)乙同学认为,无论哪种观点正确,甲同学设计的装置都有一个明显的缺陷,即 ________________________________________________________________________ (4)丙同学对可能Ⅳ持怀疑的态度。现有下列实验用品:几支试管、带胶塞的导管(单孔)、滴管、 药匙、品红溶液、蒸馏水、Ba(NO3)2溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝酸、请你帮 实验步 实验操作预期现象和结论骤编号 ①待硬质玻璃管冷却到室温后,用药匙取少量白色固体于试 管中。 ②向①的试管中加入_____ ,塞紧带导管的胶塞,并将导管 通入________。 ③ ④ 2、Fe2O3和Cu2O都是红色粉末,常用作颜料,某校一化学实验小组通过实验来探究—红色粉 末的成分,该粉末可能是Fe2O3或Cu2O或两者的混合物。探究过程如下: 查阅资料Cu2O溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。 提出假设 假设1:红色粉末是Fe2O3; 假设2:红色粉末是Cu2O; 假设3:红色粉末是Fe2O3和Cu2O混合物。 设计探究实验取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。 (1)若假设1成立,则实验现象是____________________。 (2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含氧化铁。你认为这种说法 合理吗?________。简述你的理由:__________________________________________ ___________________________________________________________________________ ___。 (3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红,则证明原固体粉末是 ________,写出发生反应的离子方程式:______________________________________。 延伸探究经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
2020年精品试题 芳草香出品
专题强化训练(四十一)散文探究题 [2017·河南省益阳市箴言中学三模]阅读下面的文字,完成1~3题。 桃园杂记 李广田 我的故乡在黄河与清河两流之间。县名齐东,济南府属。土质为白沙壤,宜种五谷与棉及落花生等。无山,多树,凡道旁田畔间均广植榆柳。县西境方圆数十里一带,则盛产桃。间有杏,不过于桃树行里添插些隙空而已。世之人只知有“肥桃”而不知尚有“齐东桃”,这应当说是见闻不广的过失。我这样说话,意在使自家人多卖些铜钱过日子,实在是因为年头不好,连家乡的桃树也遭了末运,现在是一年年地逐渐减少了。 故乡的桃李,是有着很好的景色的。计算时间,从三月花开时起,至八月拔园时止,差不多占去了半年日子。所谓拔园,就是把最后的桃子也都摘掉。最多也只剩着一种既不美观也少甘美的秋桃,这时候园里的篱笆也已除去,表示已不必再昼夜看守了。最好的时候大概还是春天吧,遍野红花,又恰好有绿柳相衬,早晚烟霞中,罩一片锦绣画图,一些用低矮土屋所组成的小村庄,这时候是恰如其分地显得好看了。到了夏天,有的桃实已届成熟,走在桃园路边,也许于茂密的秀长桃叶间,看见有刚刚点了一滴红唇的桃子,桃的香气,是无论走在什么地方都可以闻到的,尤其当早夜,或雨后。说起雨后,这使我想起布谷,这时候种谷的日子已过:是锄谷的时候了,布谷改声,鸣如“荒谷早锄”,我的故乡人却呼作“光光多锄”。这种鸟以午夜至清晨之间叫得最勤,再就是雨霁天晴的时候了。叫的时候又仿佛另有一个作吱吱鸣声在远方呼应,说这是雌雄唱和,也许是真实的事情。这种鸟也好像并无一定的宿处,只常见它们往来于桃树柳树间,忽地飞起,又且飞且鸣罢了。我永不能忘记的,是这时候的雨后天气,天空也许半阴半晴,有片片灰云在头上移动,禾田上冒着轻轻水汽,桃树柳树上还带着如烟的湿雾,停了工作的农人又继续着,看守桃园的也不再躲在园屋里。——这时候的每个桃园都已建起了一座临时的小屋,有的用土作为墙壁而以树枝之类作为顶篷,有的则只用芦席做成。守园人则多半是老人或年轻姑娘。他们看桃园,同时又做着种种事情,如织麻或纺线之类。落雨的时候便躲在那座小屋内,雨晴之后则出来各处走走,到别家园里找人闲话。孩子们呢,这时候都穿了最简单的衣服在泥道上跑来跑去,唱着歌,和“光光多锄”互相应答。 在大城市里,是不常听到这种鸟声的,但偶一听到,我就立刻被带到了故乡的桃园去,而且这极简单却又最能表现出孩子的快乐的歌唱,也同时很清脆地响在我的耳里。我听不到这种唱答已经有七八年之久了。 今次偶然回到家乡,是多少年唯一能看到桃花的一次,然而使我惊讶的,却是桃花已不再那么多了,有许多桃园都已变成了平坦的农田,这原因我不大明白,问乡里人,则只说这里的土地都已衰老,不能再生新的桃树了。当自己年幼时候,记得桃的种类是颇多的,有各
高三化学实验专题 HUA system office room 【HUA16H-TTMS2A-HUAS8Q8-HUAH1688】
实验专题 1、某化学兴趣小组的甲、乙、丙三位同学在学习Na 2O 2 与CO 2 的反应时,就提出SO 2 与 Na 2O 2 反应的问题。同学们设计实验探究SO 2 与Na 2 O 2 的反应。 (1)甲同学认为Na 2O 2 和SO 2 的反应与Na 2 O 2 和CO 2 的反应类同,设计了下图实验装置,并将 带火星的木条伸到导管口,预期现象与结果相反,如果甲同学的观点是正确的,请你分析实验失败的原因是__________________________________________________________ ________________________________________________________________________ (2)反应完毕后,综合大家的观点,认为硬质玻璃管中的固体成分有多种可能: 可能Ⅰ:全部为Na 2SO 3 ;可能Ⅱ:为Na 2 SO 3 和Na 2 O 2 的混合物;可能Ⅲ:________ 可能Ⅳ:为Na 2SO 3 和Na 2 SO 4 的混合物;可能Ⅴ:为Na 2 O 2 和Na 2 SO 4 的混合物; 可能Ⅵ:为Na 2O 2 、Na 2 SO 3 和Na 2 SO 4 的混合物。 (3)乙同学认为,无论哪种观点正确,甲同学设计的装置都有一个明显的缺陷,即 ________________________________________________________________________ (4)丙同学对可能Ⅳ持怀疑的态度。现有下列实验用品:几支试管、带胶塞的导管(单 孔)、滴管、药匙、品红溶液、蒸馏水、Ba(NO 3) 2 溶液、BaCl 2 溶液、稀硫酸、稀盐酸、稀 硝酸、请你帮助丙同学从中选出合适的用品对“可能Ⅳ”进行验证,完成下表(可以不填满):