
医疗器械产品技术要求
臂式全自动电子血压计
2015-07-01发布2015-07-01实施
- 0 -
医疗器械产品技术要求
医疗器械产品技术要求编号:
腕式全自动电子血压计
1.产品型号/规格及其划分说明
1.1 产品名称:臂式全自动电子血压计; 型号:FT-C09Y。
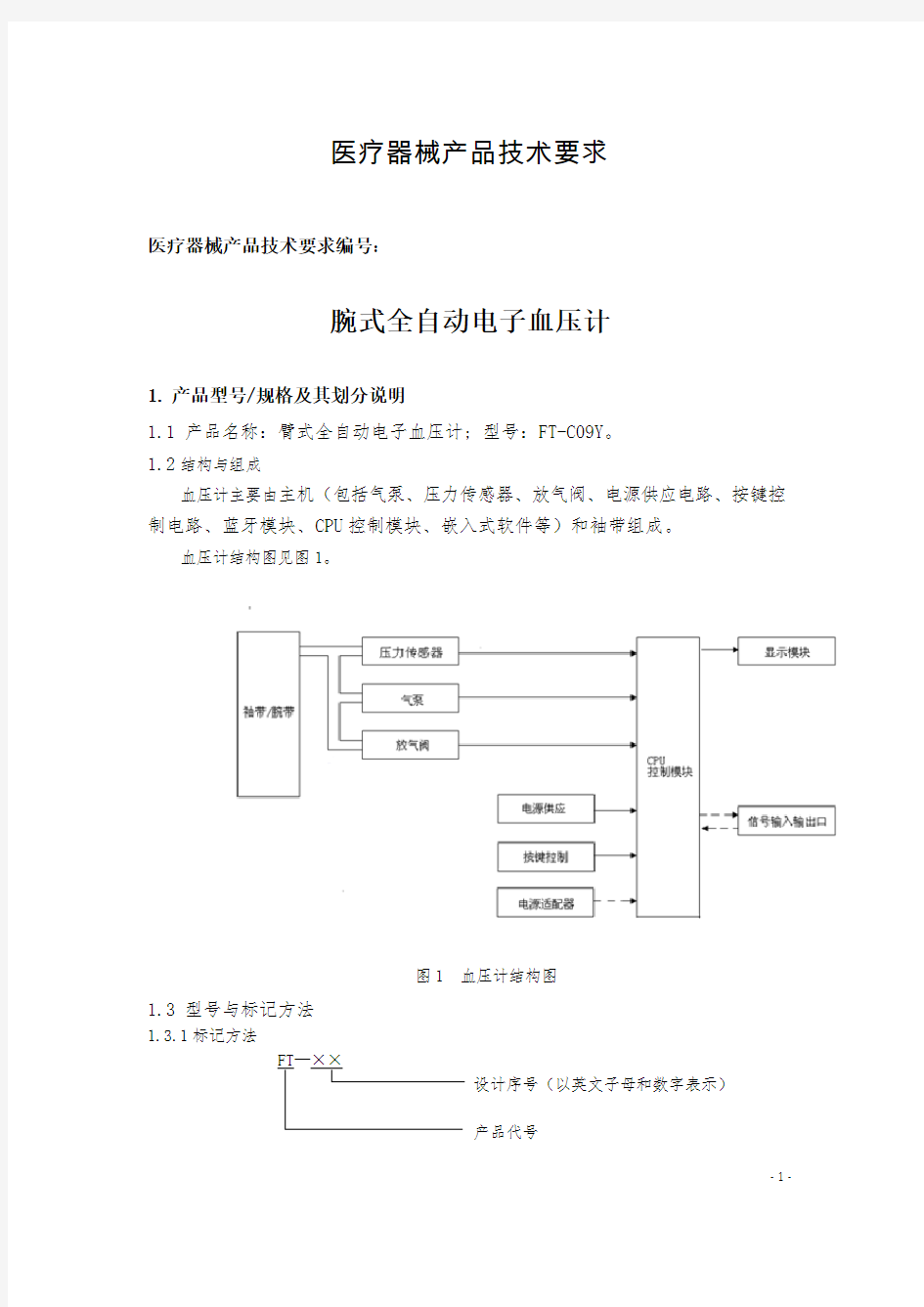
1.2结构与组成
血压计主要由主机(包括气泵、压力传感器、放气阀、电源供应电路、按键控制电路、蓝牙模块、CPU控制模块、嵌入式软件等)和袖带组成。
血压计结构图见图1。
图1 血压计结构图
1.3 型号与标记方法
1.3.1标记方法
设计序号(以英文子母和数字表示)
产品代号
- 1 -
2.性能要求
2.1工作条件
a) 环境温度:
1) 正常工作条件:5℃~40℃;
2) 运输和贮存:-20℃~+55℃。
b) 相对湿度:
1)正常工作条件:≤85%(无冷凝);
2)运输和贮存:≤93%(无冷凝)。
c) 大气压力:
1)正常工作条件:700hPa~1060hPa;
2)运输和贮存:500hPa~1060hPa。
d)使用电源:1)专用外接电源:输入AC100V-240V,50Hz/60Hz,120mA;输出DC6V,1A。
2)电池供电: d.c.6V具有-10%、+5%的相对误差(四节5号电池)。
2.2标示要求
2.2.1设备标示:设备本身要显示足够的信息,便于追溯和识别;还需要显示以
下信息:
a)使用警告,包括声明需要专业医师解释测量的血压值;
b)适当的操作指示;
c)腕带适用手腕的周长;
2.2.2外包装:外包装上至少包含以下信息:适用手臂的周长、限定的测量范围;
2.2.3说明书
说明书的编写应符合YY 0670-2008中4.2.3、GB/T 9969-2008、《医疗器械说明书、标签和包装标识管理规定》和GB 9706.1-2007的有关规定;
2..2.4 部件标识
2.2.4.1部件更换
如果某些部件(如臂带、压力传感器等)跟换后可能影响设备的性能等指标,那么该有一份如下措词:“注意:如果以非厂家提供的部件更换原有部件可能会引起测量错误”;
2.2.4.2 电池供电设备的标识
设备应标示正确的电池型号;
- 2 -
2.2.4.3 腕带标识
臂带上应标示或说明起适用的手腕周长的范围;
2.3寿命
设备经过至少10000次满量程循环后,任应满足技术要求中安全要求和性能指标;
2.4 安全要求
2.4.1 最大臂带压
a) 最大袖带压应为40kPa(300mmHg);
b)袖带压处在2kPa(15mmHg)以上的时间应不超过3min;
2.4.2 泄气
在充气系统阀门全开快速放气的情况下,压力从34.67 kPa(260mmHg)降到2kPa(15mmHg)的时间不应超购10秒。
2.5 性能要求
2.5.1 量程
血压计量程应为0kPa(0mmHg)~37.5kPa(280mmHg)。
2.5.2 分辨率
显示分辨率应为0.133 kPa(1mmHg)。
2.5.3 可重复性
在静态连续低压状态下测量,在刻度范围内每一点重复测量的读数之间,相差应不大于0.533 kPa(4mmHg).所有读数应符合压力传感器准确性中的要求。
2.5.4 压力传感器准确性
在量程中的任何测量点上,袖带内压力测量的最大误差应是±0.4 kPa(±3mmHg。
2.5.5 系统整体的有效性
制造商应提供针对自动血压测量准确性的临床评估报告。推荐的临床评估方案:在这个临床过程中应确保被评估系统的整体性能的评价方法符合YY0670-2008中第G.1章(听诊法)或第G.2章(有创法)的要求,而且符合标识要求,并确保整个体系在上述临床评价的统计结论应满足:
1)按YY0670-2008中G.1.1的方法,达到平均差不超过±0.67kPa(±5mmHg),标准偏差不超过1.067kPa(8mmHg);
2.6充气源和压力控制阀的要求
2.6.1 充气源
通常情况下,充气源应能在10s内提供足够的空气使得200cm3的容器内的压力达到40kPa(300mmHg)。
2.6.2 压力自控气阀
2.6.2.1 漏气
- 3 -
阀门关闭,在初始压力分别为33.33kPa(250mmHg)、20kPa(150mmHg)、6.67kPa(50mmHg)状态下,一个容积不超过80 cm3容器内的最大压降,在10s内应不超过0.133 kPa(1mmHg。
2.6.2.2 气阀/袖带放气率
当气阀处于压力自控位置(使用配套的袖带)时,从33.33 kPa(250mmHg)降到6.67kPa(50mmHg)的降压速度应不低于0.267 kPa/s(2mmHg/s)。
2.6.2.3 泄气
充满气体的系统在阀门全开时的快速放气,压力从34.67kPa(260mmHg)下降到2 kPa(15mmHg)的时间不应超过10秒。
2.7带气囊的袖带
2.7.1 尺寸
臂式袖带尺寸的长度480±5mm,袖带的宽度145±5mm。气囊长度220±3mm,气囊的宽度127±3mm。
2.7.2 耐压力
袖带、一体化气囊以及整个管路应能承受的内部压力为40kPa(300mmHg)。2.7.3 袖带接口/结构
在经过1000次开合循环和10000次40kPa(300mmHg)的压力循环后,袖带的闭合和密封性仍应完好到足以满足其他求。
2.8系统漏气
血压计整个系统的漏气造成压力下降的速率不应大于0.133kPa/s (1mmHg/s)。
2.9使用功能
a)血压计应能查询存储的数据,能存储用户人数和每人记忆组数见附录B;
b)血压计的显示屏应能显示收缩压、舒张压和脉率三行数据;
c)血压计应有WHO血压分类指标;
血压计应有心率不齐标记;
d)
e)血压计应能自动计算近三次测量的平均血压;
f)血压计应有毫米汞柱(mmHg)与千帕斯卡(kPa)单位切换功能;
g)血压计应有低电压提示功能:血压计电压低至5.2±0.2V 时,应有“”
的提示;
h)血压计应有自动关机功能:启动血压计,若不进行任何操作,血压计应在
1.0min±30s内自动关机;
i)血压计应有错误提示功能:血压计未能正确的测量时,均有“Er”加故障
代码的提示;
j)血压计测试完毕后可有语音提示或蜂鸣提示功能;
k)三色背光显示功能(若有,见附录B):开机时显示白色背光,血压异常时显示红色背光,血压正常时显示绿色背光;
l)串口功能(若有,见附录B):血压计应能通过USB数据线与指定设备进行连接,将该血压计数据传输到指定设备。
- 4 -
q)蓝牙功能(若有):血压计应能通过蓝牙连接功能与指定设备进行连接,将
该血压计测试数据传输到指定设备;
r)GPRS功能(若有):血压计应能通过自动传输或信息发送方式,将该血压计数据传输到指定后台或服务器
2.10 环境要求
血压计的环境试验应符合GB/T 14710-2009中气候环境试验Ⅱ组、机械环境试验Ⅱ组和表1的规定;运输试验、电源电压适应能力试验分别符合GB/T 14710-2009中4章、5章和表1的规定。
2.11 电气安全性
应符合GB 9706.1-2007的要求。
2.12 与人体接触的组件(腕带等)的生物性能要求
2.12.1应按GB/T 16886.1-2001进行生物学评价,评价结果应表明无生物学危
害。
2.12.2若需要进行试验时,应包括:
a)细胞毒性试验应不高于轻微细胞毒性;
b)皮肤刺激试验应为极轻微刺激;
c)迟发性超敏反应试验应无致敏反应。
2.13 外观与结构
2.1
3.1血压计的外观应整洁美观,表面色泽均匀,无明显划痕、破损、锋棱、毛刺及变形。
2.1
3.2血压计的配件应整洁美观,无破损、裂纹,相互连接可靠。
2.1
3.3血压计的控制和调节机构应动作可靠、灵活,紧固件无松动现象。
2.1
3.4血压计的文字和标记应清晰、准确、牢固。
2.14 脉率
血压计应有脉率测试功能,脉率测量范围应为(40~160)次/min,显示分辨率应为1次/min,测量误差应为±5%。
2.15 电磁兼容性
设备应满足YY0505-2005中规定的要求
3.试验方法
3.1试验条件
试验时,其环境应满足4.1的工作条件。
3.2标识
按4.2中的要求,通过观察验证。
3.3寿命
按YY 0670-2008中5.3规定的方法进行,结果应符合2.3的要求。
3.4安全要求
3.4.1 最大袖带压
- 5 -
在血压计动态模式下,用压力发生器加压到压力表读数应为40kPa(300mmHg)前;应马上急排泄压,起到超压保护的作用,结果应符合2.4.1的规定。
3.4.2 泄气
按YY 0670-2008中5.4.1.2规定的方法进行,结果应符合2.4.2的要求。
3.5性能要求
3.5.1 量程
按YY 0670-2008中5.5.1规定的方法进行,结果应符合2.5.1的要求。
3.5.2 分辨率
按YY 0670-2008中5.5.2规定的方法进行,结果应符合2.5.2的要求。
3.5.3 可重复性
按YY 0670-2008中5.5.3规定的方法进行,结果应符合2.5.3的要求。
3.5.4 压力传感器准确性
按YY 0670-2008中5.5.4规定的方法进行,结果应符合2.5.4的要求。
3.5.5 系统整体的有效性
按YY 0670-2008中5.5.5规定的方法进行,结果应符合2.5.5的要求。
3.6充气源和压力控制阀的要求
3.6.1 充气源
通常情况下,充气源应能在65s内提供足够的空气使得200cm3的容器内的压力达到38.8kPa(291mmHg)。结果应符合2.6.1的要求。
3.6.2 压力自控气阀
3.6.2.1 漏气
按YY 0670-2008中5.6.2.1规定的方法进行,结果应符合2.6.2.1的要求。
3.6.2.2 气阀/袖带放气率
按YY 0670-2008中5.6.2.2规定的方法进行,结果应符合2.6.2.2的要求。
3.6.2.3泄气
见2.4.2。
3.7带气囊的袖带
3.7.1 尺寸
使用通用量具测量,结果应符合2.7.1的要求。
3.7.2 耐压力
按照说明书规定的方法和实际操作检查,结果应符合2.7.2的要求。
3.7.3 袖带接口/结构
按YY 0670-2008中5.7.2.3规定的方法进行,结果应符合2.7.3的要求。
3.8系统漏气
按YY 0670-2008中5.8规定的方法进行,结果应符合2.8的要求。
3.9使用功能
按照说明书规定的方法和实际操作检查,结果应符合2.9的要求。
- 6 -
3.10环境试验
环境试验按GB/T 14710-2009规定的方法、顺序及表1的要求进行,结果应符合2.10的要求。
3.11 电气安全性
按GB 9706.1-2007规定的执行。
3.12 生物性能试验
- 7 -
按GB/T 16886.1-2001 进行生物学评价,或由制造商提供符合性的证明,应符合
2.12.1的要求。
3.12.1 细胞毒性试验
按GB/T 16886.5-2003中8.3的规定方法进行,应符合2.12.2 a)的要求。
3.12.2 致敏试验
按GB/T 16886.10-2005中第7章的规定方法进行,应符合2.12.2 b)的要求。
5.12.3 皮肤刺激试验
按GB/T 16886.10-2005中6.3的规定方法进行,应符合2.12.2 c)的要求。
3.13外观与结构试验
用手感和目力观察、并实际操作进行检查,结果应符合2.13的要求。
3.14 脉率试验
用模拟血压器输入(40、80、160)次/min的脉率,给血压计输入正常的血压测量范围内的信号值(收缩压120mmHg,舒张压80mmHg)进行测试,每个脉率值重复三次,结果应符合
2.14的规定。
3.15 电磁线兼容性
按照YY0505-2005中规定的要求执行。
4.术语
无
- 8 -
附录A(规范性附录)
电气安全特征及检验规则
A.1血压计主要安全特征
A.1.1按防电击类型分类:Ⅱ类、内部电源设备。
A.1.2按防电击程度分类:B型应用部分。
A.1.3按对进液的防护程度分类:不适用。
A.1.4按在与空气混合的易燃麻醉气或与氧或氧化亚氮混合的易燃麻醉气情况下使用时的
安全程度分类:不能在有与空气混合的易燃麻醉气或氧或氧化亚氮混合的易燃麻醉气情况下使用的设备。
A.1.5按运行模式分类:连续运行。
A.1.6血压计的电源类种: 1)专用外接电源:输入AC100V-240V,50Hz/60Hz,120mA;输出DC6V,1A。
2)电池供电: d.c.6V,具有+10%、-5%的相对误差(四节5号电池)。
A.1.7血压计的输入功率:120mA。
A.1.8血压计无具有对除颤放电效应防护的应用部分。
A.1.9血压计部分型号具有蓝牙或串口功能,见附录B。
A.1.10血压计属携带式普通设备。
A.1.11电气绝缘图:见图A.1
图A.1 血压计电气绝缘图
- 9 -
东莞市福达康实业有限公司
- 10 -
电子血压计 适用范围:适用于成人无创血压和脉搏的测量。 1.1.2型号列表及区别 表1型号列表及区别
1.1.3基本参数 表2 2.1 正常工作条件 a)环境温度:5℃~40℃;
b)相对湿度:15%~80%; c)大气压力:860hPa~1060hPa; d)电源条件:DC6V(干电池4节); 2.2 外观 2.2.1 血压计外观应平整光滑,表面不得有锋棱、毛刺、凹凸缺 陷。 2.2.2 血压计各部件连接应可靠,按键活动应自如,无卡键和影响 操作现象。显示数字应清晰可辨,不存在缺划断划现象。 2.3 量程(测量范围) 2.3.1 血压计压力测量范围满足0kPa~37.3kPa(0 mmHg~ 280mmHg)。 2.3.2 血压计脉搏数测量范围满足(30-160)次/分。 2.4 分辨率 2.4.1 显示血压值时:千帕斯卡为0.1 kPa ;毫米汞柱为1 mmHg。 2.4.2 显示脉搏数时:1次/分。 2.5 测量误差 2.5.1 压力传感器准确性 无论采用升压测量法还是降压测量法,在量程中的任何测量点上,袖带内压力测量的最大误差应是±0.4 kPa(±3mmHg)。 2.5.2 脉搏数误差 脉搏数误差±5%以内。 2.6 可重复性
在静态连续低压状态下测量,在刻度范围内每一点重复测量的读数之间,相差应不大于0.533 kPa(4mmHg).所有读数应符合压力传感器准确性中的要求。 2.7 漏气 血压计整个系统应有良好的气密性:血压计整个系统漏气造成的压力下降的速率不应大于0.133kPa/s(1mmHg/s)。 2.8 泄气 测量过程中按下电源开关按钮以及突然断电,系统应能立刻排气;测量时血压计加压值大于37.3kPa(280 mmHg)时,应能立即自动快速排气;压力从 34.67kPa(260mmHg)下降到2.0kPa(15mmHg)的时间不应超过10秒。2.9 气阀 2.9.1 阀门关闭时,在初始压差分别为3 3.33kPa(250mmHg)、 20kPa(150mmHg)和6.67kPa(50mmHg)状态下,一个容积不超过 200cm3容器内的最大压降,在10s内应不超过0.267kPa (2mmHg)。 2.9.2 充满气体的系统在阀门完全开放时的快速放气,压力从 34.67kPa(260mmHg)下降到2.0kPa(15mmHg)的时间不应超过 10s。 2.10 袖带和气囊 2.10.1 尺寸 袖带长度应大于34cm,气囊尺寸应满足:长度200mm以上;宽度 120mm以上。
产品技术规范书 设备名称:SF6气体定性检漏仪 型号:XP-1A 数量:1台套 一、产品应用: XP-1A SF6气体定性检漏仪是30年以来检漏仪制造经验的顶点。作为迄今制造的最稳定与最灵敏的负电晕检漏仪,我们为提供此种工具而骄傲。我们把所有的经验及多年客户的反馈溶入到此产品中,希望为用户提供最好的一切:价格、性能及可靠性。 XP-1A SF6气体定性检漏仪的核心是一台先进的微处理机。它采用的数字信号处理技术使得它比采用的操纵电路及传感头信号更好成为可能。此外,电路中使用的元件数量约减少40%,从而提高了可靠性及性能。微处理机实时监视传感头和电池电压值,每秒钟可达4000次,能及时补偿即使是最微小变动的信号脉动。这使得该仪表在几乎一切环境的应用中,成为一种稳定而可靠的检测工具。 XP-1A SF6气体定性检漏仪在设计上增加了许多方便用户使用的性能。灵敏度的七级自由设置,使仪表从一级到七级增加64倍的灵敏度;独特的三色发光二极管把渐进的及广范围的泄漏大小的指示出来;指示灵敏度的等级;并提供有关电池电量的实际电压指示。触摸式键盘控制所有使用功能;新颖的外壳设计供使用者紧握,方便操作;安装使用时目视的直观指示器。 二、采用标准 本SF6气体定性检漏仪的制造、试验和验收除了应满足本技术要求外,还应符合如下标准: ●GB191 包装储运图示标志EQVISO780:1997 ●GB/T5048防潮包装 ●GB/T5832.2—1986 气体中微量水分的测定露点法 ●GB/T6388 运输包装收发货标志 ●GB/T6587.1—1986 电子测量仪器环境试验总纲 ●GB/T6587.2 电子测量仪器温度试验 ●GB/T6587.3 电子测量仪器湿度试验 ●GB/T6587.4 电子测量仪器振动试验 ●GB/T6587.5 电子测量仪器冲击试验
臂式电子血压计使用方法 使用方法 (一)装入电池或外接电源 ●请务必使用碱性电池或DC6V 800mA以上的电源适配器。 1血压计翻过来,按箭头所指方向卸下电池盖。 2确认电池的极后,装入AA(5号)碱性电池4节。 注:血压计第一次装上电池或外接电源时,液晶屏全显约1秒,并伴有“嘀”声3盖上电池盖,直至听见“咔哒”声。 更换电池出现以下情况时请更换电池 ●测量过程中出现标记显示时。 ●按下“ON/OFF 开/关”键,液晶屏无任何显示。 【电池寿命】 ●使用一组新的LR6 AA碱性电池,约可进行300次测量。(环境温度22℃,加压180mmHg,手臂周长17cm时)●如果环境温度较低,则会缩短电池寿命。 ●碱性电池如果被充电、正负极置入不当、短路、与使用过的电池或不同种类的电池混用、投入火中等,都可能造成漏液或爆炸。请勿分解电池。若长时间不使用本血压计时,应从血压计中取出电池。 ●废弃电池请勿乱扔,注意回收。 (二)臂带之绑法
1将臂带卷绑在裸露的手臂上,胶管的出口应与手掌面的小手指 对齐. 2扎牢臂带后,请勿将衣服带入臂带,否则会影响测量精度. (※臂带不能捆綁太紧,也不能太松,能放进一根手指最为合适). 3 测量时姿势是将胳膊肘放在桌子上.手心向上,身体放松,将臂带与心脏高度保持一致. ※如不将臂带正确绑好,位置放置正確,可能无法测得正确血压. 测量 ●测量时请在身体放松的状态下进行测量,并不可抽烟、深呼吸、说话及蠕动,否则将影响测量结果。 1 单位转换:血压值单位KPa/mmHg转换(开机默认单位为mmHg) ●长按ON/OFF开/关键5秒 ●根据需要,当显示KPa时松开ON/OFF开/关键,此时所有测量数据为KPa单位;●同理,当显示mmHg时松开ON/OFF开/关键,此时所有测量数据为mmHg单位。
采购产品技术要求和验收标准 1.0 元器件入库前检验 1.1 严格执行采购控制程序,从合格的供方采购合格产品。 1.2 对进厂的采购产品都要按下面的检验项目、方法和标准进行 检验,。对安全件,至少应抽取10%的样品按表中的检验项目进行检验和试验:对关键元器件,至少应抽取5%的样品进行检验:对一般材料,只须进行确认。 检验/验证项目、方法和标准: 1.2.1 断路器: 依据标准:GB14048.2《低压断路器》 1.2.2 隔离开关、熔断器: 依据标准:GB14048.3《低压开关、隔离器、隔离开关及熔断器组合电器》
1.2.3 接触器: 依据标准:GB14048.6《接触器和电动机起动器》 1.2.4电流互感器: 依据标准:GB1208《电流互感器》 依据标准:GB14048.5《控制电路电器和开关元件》
检验/验证项目、方法和标准: 1.2.6母线: 依据标准:GB5585《电工用铜、铝及其合金母线》检验/验证项目、方法和标准:
依据标准:GB5023《额定电压450/750V及以下聚氯乙烯绝缘电缆》检验/验证项目、方法和标准: 1.2.8绝缘支撑件、母线框、母线夹板 依据标准:GB1408《固体绝缘材料工频电气强度试验方法》 检验/验证项目、方法和标准:
1.3凡符合1.2条的初步判定为合格品,如有一项不符即为不合格品,并 填 写入库前的检验记录。出现不合格则全检,合格放行,不合格退货。 1.4 如在出厂检验中出现机械或性能或电性能的缺陷时,最终判定为不合 格产 品,在出厂检验中作记录。 2.0 外协件入库前检验 2.1 外协的各种零部件必须按图纸检验相关尺寸及外观。 2.2 各种型号的低压柜柜体,到厂后都必须按图纸检验外型尺寸、漆的表面、 门的开启、接地螺栓的焊接、防护等级等,合格后方可入库。 3.0 生产过程中的自检 3.1 操作者在生产工程中应严格执行工艺文件,不得擅自更改或降低工艺标准,也不得随意执行未经批准而制定的其他标准。 3.2 在每个工序完成后,转入下道工序前,操作人应进行自检,确认该工序 合格后,在产品随工卡上加盖自己的工序章,并向检验员口头报验,检验员检验 合格,在随工卡盖章后,方可转入下道工序。 3.3 若检验人员检验后,判定某一项不合格,应进行返工,返工后必须重新检验,直到判定合格为止,加盖检验章,方可转入下道工序 4.0 对不合格品的处理方法 4.1 对采购产品和外协件初步判定为不合格品的,由检验员将检验结果(缺 陷描述)等,填写在采购产品进厂检验单中,做出标识,另行存放,按不合格品 控制程序执行。 4.2 过程产品发生不合格时,由检验员通知操作工返修,并在随工卡上作记 录,返工返修的产品重新报验合格为止,若产品确定为不合格,则应作好标识, 另行存放,按不合格品控制程序执行。 4.3 过程产品发生不合格时,由检验员将检验结果,填写在成品检验记录中, 按不合格品控制程序执行。
关于按键功能 在电子血压计上的操作可以通过按键完成。以下列出各按键: ●【ON/OFF】开关机按键。长按时开机或关机 ●【START/STOP】按下此键,仪器开始为袖带充气,进行血压测量。 在测量过程中,按下此键可以中止测量并放气。 ●左边按键【USER】用于用户切换 中间按键【SETUP】用于年、月、日和时间设置 右边按键【MEMORY】用于用户数据回顾 ●上下按键,分别执行向上或向下移动光标,更改数值及切换 状态的功能。 电子血压计外部接口 注意 在拆下NIBP袖带导气管时,请拿着导气管前部的导气管插头拔出。 ①电子血压计袖带插孔 左侧面 仪器右侧是USB插座和AC稳压电源插孔。 ①USB插座
②AC稳压电源插孔 右侧面
装入干电池/AC 稳压电源的使用方法 本产品既可以使用干电池又可以使用AC 稳压电源 ① ② 装入干电池 ③ ① 将电池盒盖沿箭头方向卸下 ② 将5号干电池按 极装入 ③ 将电池盒盖滑动关上 图标 “”:表示电池电量即将耗尽。 请同时更换4节新电池(相同种类)。 更换电池时请关闭本体电源。 使用后的电池的废弃方法请参照城市有关环境保护规定进行处理 AC 稳压电源的使用方法 ① 连接血压计与AC 稳压电源 请将AC 稳压电源的插头插入血压计本体右侧面的AC 稳压电源插孔 ② 请将AC 稳压电源的电源插头插入AC220V 插座 注意 切断电源时,先切断电源插座与稳压电源,再切断稳压电源与血压计 请务必使用专用AC 稳压电源(型号: ) 注意 当稳压电源与干电池同时使用时,不消耗干电池电量 ● 稳压电源与干电池切换时请在关机状态下进行,否则会使仪器因断电关机
保健食品产品技术要求规范(国食药监许[2010]423号) 发布日期:2011-02-10 来源:国家食品药品监督管理局 【发布单位】国家食品药品监督管理局 【发布文号】国食药监许[2010]423号 【发布日期】 2010-10-22 【生效日期】 2011-02-01 【效力】 【备注】各省、自治区、直辖市食品药品监督管理局(药品监督管理局):根据《食品安全法》及其实施条例对保健食品实行严格监管的要求,为进一步规范保健食品行政许可工作,提高保健食品质量安全控制水平,加强保健食品生产经营监督,指导保健食品产品技术要求编制工作,国家食品药品监督管理局组织制定了《保健食品产品技术要求规范》,现予印发,请遵照执行。国家食品药品监督管理局二○一○年十月二十二日 保健食品产品技术要求规范 一、根据《食品安全法》及其实施条例对保健食品实行严格监管的要求,为进一步规范保健食品行政许可工作,提高保健食品质量安全控制水平,加强保健食品生产经营监督,保障消费者食用安全,制定本规范。 二、国家食品药品监督管理局负责批准保健食品产品技术要求,并监督其执行。 三、保健食品产品技术要求应当符合国家有关法律法规、标准规范。 四、保健食品产品技术要求文本格式应当包括产品名称、配方、生产工艺、感官要求、鉴别、理化指标、微生物指标、功效或标志性成分含量测定、保健功能、适宜人群、不适宜人群、食用量及食用方法、规格、贮藏、保质期等序列(见附件1),并按照保健食品产品技术要求编制指南(见附件2)编制。 五、保健食品产品技术要求是产品质量安全的技术保障。生产企业应当按照保健食品产品技术要求组织生产经营,食品药品监督管理部门应当将保健食品产品技术要求作为开展监督执法的重要依据。 六、保健食品产品技术要求适用于保健食品新产品的注册申请和产品的再注册。
附件5 医疗软件产品技术审评规范(2017版) 本规范旨在指导企业提交医疗器械软件注册申报资料,同时规范医疗器械软件的技术审评要求。 本规范是对医疗器械软件的一般性要求,企业应根据医疗器械软件的特性提交注册申报资料,判断指导原则中的具体内容是否适用,不适用内容详述理由。企业也可采用其他满足法规要求的替代方法,但应提供详尽的研究资料和验证资料。 本规范是在现行法规和标准体系以及当前认知水平下、并参考了国外法规与指南、国际标准与技术报告制定的。随着法规和标准的不断完善,以及认知水平和技术能力的不断提高,相关内容也将适时进行修订。 本规范是对企业和审查人员的指导性文件,不包括审评审批所涉及的行政事项,亦不作为法规强制执行,应在遵循相关法规的前提下使用本规范。 本规范针对软件的特殊性,在现行法规要求下进一步明确了对医疗器械软件的要求,特别是对软件更新、软件版本的要求。本规范是医疗器械软件的通用规范,其他涉及软件医疗器械产品的规范可在本规范基础上进行有针对性的调整、修改和完善。 一、适用范围 本规范适用于第二类医疗器械软件的注册申报,适用的软件开发方式包括自主开发、部分采用现成软件和全部采用现成
软件。 医疗器械软件包括独立软件和软件组件。独立软件:作为医疗器械或其附件的软件;软件组件:作为医疗器械或其部件、附件组成的软件。 独立软件应同时具备以下三个特征:具有一个或多个医疗用途,无需医疗器械硬件即可完成预期用途,运行于通用计算平台。独立软件包括通用型软件和专用型软件,其中通用型软件基于通用数据接口与多个医疗器械产品联合使用,如PACS、中央监护软件等;而专用型软件基于通用、专用的数据接口与特定医疗器械产品联合使用,如Holter数据分析软件、眼科显微镜图像处理软件等。 软件组件应同时具备以下两个特征:具有一个或多个医疗用途,控制(驱动)医疗器械硬件或运行于专用(医用)计算平台。软件组件包括嵌入式软件和控制型软件,其中嵌入式软件(即固件)运行于专用(医用)计算平台,控制(驱动)医疗器械硬件,如心电图机所含软件、脑电图机所含软件等;而控制型软件运行于通用计算平台,控制(驱动)医疗器械硬件。 软件组件也可兼具处理功能。专用型独立软件可单独注册,也可随医疗器械产品注册,此时视为软件组件。 二、技术审查要点 (一)产品名称和结构组成的要求 1.独立软件 产品名称应为通用名称,并符合相关法规、规范性文件的要求,可以结合人体部位(如胸部、心脏等)、临床科室(如骨科、神经外科等)、处理对象(如CT图像、MRI图像、心电数
电子血压计使用说 明书四
关于按键功能 在电子血压计上的操作能够经过按键完成。以下列出各按键: ●【ON/OFF】开关机按键。长按时开机或关机 ●【START/STOP】按下此键, 仪器开始为袖带充气, 进行 血压测量。 在测量过程中, 按下此键能够中止测量并放气。 ●左边按键【USER】用于用户切换 中间按键【SETUP】用于年、月、日和时间设置 右边按键【MEMORY】用于用户数据回顾 ●上下按键, 分别执行向上或向下移动光标, 更改数值 及切换 状态的功能。 电子血压计外部接口 注意 在拆下NIBP袖带导气管时, 请拿着导气管前部的导气管插头拔出。
①电子血压计袖带插孔 左侧面 仪器右侧是USB插座和AC稳压电源插孔。 ① USB插座 ② AC稳压电源插孔 右侧面
装入干电池/AC稳压电源的使用方法 本产品既能够使用干电池又能够使用AC稳压电源 装入干电池 ①将电池盒盖沿箭头方向卸下 ②将5号干电池按极装入 ③将电池盒盖滑动关上 图标””: 表示电池电量即将耗尽。 请同时更换4节新电池( 相同种类) 。 更换电池时请关闭本体电源。 使用后的电池的废弃方法请参照城市有关环境保护规定进行处理AC稳压电源的使用方法 ①连接血压计与AC稳压电源 请将AC稳压电源的插头插入血压计本体右侧面的AC稳压电源插孔
②请将AC稳压电源的电源插头插入AC220V插座 注意 切断电源时, 先切断电源插座与稳压电源, 再切断稳压电源与血压计 请务必使用专用AC稳压电源( 型号: ) 注意 当稳压电源与干电池同时使用时, 不消耗干电池电量 ●稳压电源与干电池切换时请在关机状态下进行, 否则会使仪器 因断电关机 设定日期和时间 接通电源按开机键开机后, 需设置日期和时间 本血压计可自动存储测量结果及日期和时间 ●干电池能量耗尽, 或卸下电池等时, 计时停止。 此时, 请重新设定日期和时间 本血压计可自动记忆3位用户, 每位用户99组测量值, 并能将测量的结果经过USB传到PC机软件, 进行数据回放处理等。对日期和时间进行正确的设定, 则会存储正确的测量日期和时间。否则不能记忆正确的测量日期和时间。 注意若要正确使用数据上传功能: 1.当首次接通血压计电源时, 按开机键开机后
臂式电子血压计 适用范围:该产品以示波法测量成人舒张压、收缩压、脉搏,其数值供诊断参考。 1. 产品型号及其划分说明 1.1 产品型号:LY-701D、LY-702D、LY-703D、LY-706D、LY-706D-1、LY-708D。 1.2 型号标记 1.3 结构组成 血压计由主机(气泵、压力传感器、放气阀、电池供应电路、按键控制电路、显示模 块、CPU控制模块、嵌入式软件)和袖带以及电源适配器(选配)组成。 1.4 型号分类 血压计型号分类见表1。 2.1 工作条件: a)环境温度:5℃~40℃; b)相对湿度: 15%~80%; c)大气压力:860hPa ~1060hPa;
d)电源电压:a)LY-701D、LY-702D、LY-703D 为 d.c 6V 5 号电 池 4 节(AA)。 b)LY-706D、LY-706D-1、LY-708D 为 d.c 6V 7 号电池 4 节 (AAA)。 c)适配器:输入交流电压100V~240V,频率50Hz,输出直流5V,1000mA 2.2 标识要求 2.2.1 设备标识 设备本身应显示以下供追溯和识别的标识: a) 适当的操作指示; b) 与本标准的精度要求相关的仪器性能参数。 2.2.2 外包装标识 外包装上至少应包括以下信息: a) 适用的臂围范围 b) 测量范围。 2.2.3 说明书 说明书上至少应包括以下内容: a) 完备的使用说明,包括对使用警告总结的章节,此章节 能在目录中被索引,且指导用户关注说明书中的相关章节; b) 介绍如何拆包、安装、使用前检查,获取帮助服务的渠道、 标准操作程序、常规维护、再校准及清洗频次的建议; c) 制造商或服务商的联系方式 d) 当有普通心律失常(比如说房早、室早及房颤等)出现时, 设备是否能达到声称的性能;
医疗器械产品技术要求编号: XXXXXX 1产品型号/规格及其划分说明 1.1型号命名 P200 设计序号 产品代号 1.2结构组成(不同型号如有结构组成的差异,应分型号列明) XXXXXX(以下简称XX)主要由X射线管组件(组合式)、限束器、操作台、影像处 理系统、C形臂及可移动机架、医用X射线影像增强器组成。 1.3型号说明(如有多个型号此条适用,列表标明型号间差异) 表1型号说明 1.4工作条件 a)环境温度:10℃~40℃; b)相对湿度:30%~75%; c)大气压力:700hPa~1060hPa。 d)电源:AC220V±22V;50Hz±1Hz e)额定输入功率:xx VA。 2性能指标 2.1外观 2.2XXX ...... 2.X安全要求 XXX安全要求应符合GB9706.1-2007的要求,产品主要特征见附录C。(9706.1适用设备) XXX安全要求应符合GB4793.1-2007的要求,产品主要特征见附录C。(4793.1适用设备)
间(h )间(h ) 条件 中间 24 试验后通电 ※ 2.x 、2.x 、... - 2.x 、2.x 、... 72 试验后通电 ※ 2.X 电磁兼容 (9706.1适用设备) 电磁兼容应符合YY 0505-2012 的要求。 2.X 电磁兼容 (479 3.1适用设备) 电磁兼容应符合GB/T 18268.1-2010 的要求。 2.X 电磁兼容 (体外诊断类适用设备) 电磁兼容应符合GB/T 18268.1-2010及 GB/T 18268.26-2010 的要求。 2.X 环境试验 按 GB/T 14710-2009 中规定的气候环境Ⅱ组、机械环境Ⅱ组的要求及表 X 进行试验, 应符合要求。 表 X 试验要求及检验项目 试验要求 检测项目 电源电压(V ) 试验项目 持续时 恢复时 试验 通电 状态 初始检测 检测 最后 检测 额定值 额定值 -10% +10% 额定工作 低温试验 2 --- 试验时通电 ※ 全性能 - 2.x 、2.x 、... √ --- 低温贮 存试验 4 --- - AC220 额定工作 高温试验 2 --- 试验时通电 ※ --- 2.x 、2.x 、... --- √ 运行试验 4 --- 试验时通电 ※ --- 2.x 、2.x 、... --- √ 高温贮 存试验 4 4 试验后通电 ※ --- 2.x 、2.x 、... AC220 额定工作 湿热试验 4 --- 试验时通电 ※ --- AC220 湿热贮存 试验 48 --- 2.x 、2.x 、... AC220 振动试验 碰撞试验 运输试验 --- --- --- 试验后通电 ※ 试验后通电 ※ 试验后通电 ※ --- --- --- --- --- --- 2.x 、2.x 、... 2.x 、2.x 、... 2.x 、2.x 、... AC220 AC220 AC220 注:表中“※ ”按GB/T14710-2009的规定 3 检验方法 3.1 外观 用正常或矫正视力观察以及用手感检查,结果应符合2.1的要求。 1
手臂式全自动电子血压计 2.性能指标 2.1外观与结构 2.1.1血压计的外观应整洁美观,表面色泽均匀,无明显划痕、破损、锋棱、毛刺及变形。 2.1.2血压计的配件应整洁美观,无破损、裂纹,相互连接可靠。 2.1.3血压计的控制和调节机构应动作可靠、灵活,紧固件无松动现象。 2.1.4血压计的文字和标记应清晰、准确、牢固。 2.2显示功能 a)无压力时,应指示在零位。 b)在显示过程中,不应有缺笔划现象。 c)血压计应用“kPa”或“mmHg”计量单位的形式进行显示。(适用于 RAK263、RAK269、RAK289T、RAK289L、RAK283L、RAK288L、RAK263L、RAK268L)。 血压计应可以设置时间、语音开关及计量单位。(适用于 RAK266、RAK268、RAK283、RAK286、RAK288、RAK289) d)显示屏上应能正常显示收缩压、舒张压和心率的测量数值。 2.3脉搏 血压计的脉搏测量范围不窄于(40~199)次/分,允差±5%;显示分辨率为 1 次/ 分。 2.4自动关机功能 2.4.1启动血压计,若无任何操作,血压计应能在 70S 内自动关机。(适用于 RAK263.RAK269、RAK289T、RAK289L、RAK283L、RAK288L、RAK263L、RAK268L) 2.4.2启动血压计,测量出结果后或者设定状态下,若无任何操作,血压计应能在 75S 内自动关机。(适用于 RAK266、RAK268、RAK283、RAK286、RAK288、RAK289) 2.5自动归零功能 血压计每次启动时,应能自动归零一次。 2.6记忆功能 血压计具有数据存储、数据回放的功能。
医疗器械产品技术要求编号: 臂式电子血压计 1. 产品型号/规格及其划分说明 1.1 型号规格:G80-01、G80-02、G80-03,产品型号差异划分见表1。 表1:产品型号信息表SN 产品型号G80-01 G80-02 G80-03 1 量测部位手臂手臂手臂 2 工作原理示波法示波法示波法 3 测量方式降压式降压式降压式 4 显示方式VA屏液晶反显VA屏液晶反显VA屏液晶反显 5 电源种类d.c. 3.7V或a.c 100~240V d.c. 3.7V或a.c 100~240V d.c. 3.7V或a.c 100~240V 6 标称电压 3.7V 3.7V 3.7V 7 低电压规格 3.6V 3.6V 3.6V 8 自动关机时间120s 120s 120s 9 血压量测范围0~299mmHg 0~299mmHg 0~299mmHg 10 血压测量精度±3mmHg±3mmHg±3mmHg 11 脉搏范围40~180搏/分40~180搏/分40~180搏/分 12 脉搏测量精度±5%±5% ±5% 13 主机尺寸154×48×35mm 150×52×38mm150×53×42mm 14 袖带尺寸150*490mm 150*490mm 150*490mm 15 放气速率6~8mmHg/s 6~8mmHg/s 6~8mmHg/s 16 超压保护300mmHg 300mmHg 300mmHg 17 自动量测■■■ 18 语音提示■■■ 19 心率■■■ 20 模糊充气模式智能加压智能加压智能加压 21 按键个数1个1个1个 备注:■表示有该项功能 1.2 标记方法 G80- □□ 产品研发序号:01、02…… 产品类型代号 GREEN首字母缩写 1.3 软件信息
关于印发化妆品产品技术要求规范的通知 国食药监许[2010]454 号 2010 年11 月26 日发 布各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,指导化妆品 产品技术要求编制工作,国家食品药品监督管理局组织制定了《化妆品产品技术要求规范》,现予印发,请遵照执行。 附件:1.国家食品药品监督管理局化妆品产品技术要求(文本格式) 2.化妆品产品技术要求编制指南 国家食品药品监督管理局 二0一0年十一月二十六日 化妆品产品技术要求规范 一、根据《化妆品卫生监督条例》,为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,保障消费者使用安全,制定本规范。
二、国家食品药品监督管理局负责批准化妆品产品技术要求,并监督其执行。 三、化妆品产品技术要求应当符合国家有关法律法规、标准规范。 四、化妆品产品技术要求应符合其文本格式的规定。文本格式应当包括产品名称、配方成分、生产工艺、感官指标、卫生化学指标、微生物指标、检验方法、使用说明、贮存条件、保质期等序列(见附件1),并按照《化妆品产品技术要 求编制指南》(见附件2 )编制。 五、化妆品产品技术要求是产品卫生质量安全的技术保障。生产企业应当按照化妆品产品技术要求组织生产经营,食品药品监督管理部门应当将化妆品产品技术要求作为开展卫生监督执法的重要依据。 六、化妆品产品技术要求适用于化妆品新产品的许可和产品延续。 七、化妆品产品技术要求编号。国产特殊用途化妆品按照HZ+GT+ 年份+0000 编制;进口特殊用途化妆品按照HZ+JT +年份+0000编制;进口非特殊用途化妆品按照HZ+JF+年份+0000编制。"HZ"表示"化妆品”,"GT"表示"国产特殊用途”, "JT"表示"进口特殊用途”,”JF"表示"进口非特殊用途”,"年份+0000"为化妆品批准文号(或备案号)的年份和顺序号。 八、本规范自2011 年4 月1 日起施行。 附件1 国家食品药品监督管理局 化妆品产品技术要求(文本格式) 产品技术要求编号)
欧姆龙血压计 一、集团概要 集团概要 1933年,立石一真先生在大阪建立了一个名为立石电机制作所的小型工厂,当时只有两名职员。公司在起步阶段除了生产定时器外,后来一度专门生产保护继电器。这两种产品的制造成为欧姆龙株式会社的起点。为了适应时代的发展,在公司成立50周年纪念时,公司名称与品牌名称实现了统一,改为“欧姆龙株式会社”。 无触点接近开关,电子自动感应信号机,自动售货机,车站自动售检票系统,癌细胞自动诊断仪…欧姆龙在世界上率先开发并生产出一系列产品与设备系统。为社会的进步与提高人类的生活水平作出贡献。创造社会需求,构筑“安心”,“安全”,“环保”“健康”的社会是欧姆龙的企业发展目标。 自1933年5月10日创业至今的70多年中,通过不断创造新的社会需求,欧姆龙集团已经发展成为全球知名的自动化控制及电子设备制造厂商,掌握着世界领先的传感与控制核心技术。 截止到2009年度,欧姆龙集团已经拥有员工36,299人(2010年4月),全球营业额近5,300亿日元。产品品种达几十万种,涉及工业自动化控制系统、电子元器件、汽车电子、社会系统以及健康医疗设备等广泛领域。(详细请参看以下图表) 公司概要 本社: 欧姆龙株式会社 OMRON Corporation 本社所在地: 京都本社:〒600-8530京都市下京区塩小路通堀川東入 代表者: 代表取缔役社長 山田義仁 创业: 1933年(昭和8年)5月10日 设立: 1948年(昭和23年)5月19日 资本金: 641亿日元(2010年4月) 集团销售额: 6,178亿日元(2011年4月) 集团营业利益: 480亿日元(2011年4月) 职工人数 欧姆龙集 团 35,684人 日本合计 6,653人 海外总计 (中国合计 24,263人 17,020人) (截止至2011年4月)
保健食品产品技术要求规范 一、根据《食品安全法》及其实施条例对保健食品实行严格监管的要求,为进一步规范保健食品行政许可工作,提高保健食品质量安全控制水平,加强保健食品生产经营监督,保障消费者食用安全,制定本规范。 二、国家食品药品监督管理局负责批准保健食品产品技术要求,并监督其执行。 三、保健食品产品技术要求应当符合国家有关法律法规、标准规范。 四、保健食品产品技术要求文本格式应当包括产品名称、配方、生产工艺、感官要求、鉴别、理化指标、微生物指标、功效或标志性成分含量测定、保健功能、适宜人群、不适宜人群、食用量及食用方法、规格、贮藏、保质期等序列(见附件1),并按照保健食品产品技术要求编制指南(见附件2)编制。 五、保健食品产品技术要求是产品质量安全的技术保障。生产企业应当按照保健食品产品技术要求组织生产经营,食品药品监督管理部门应当将保健食品产品技术要求作为开展监督执法的重要依据。
六、保健食品产品技术要求适用于保健食品新产品的注册申请和产品的再注册。 七、保健食品产品技术要求编号按照BJ+G(或J)+年份+0000编制。“BJ”表示“保健食品”,“G(或J)”表示国产或进口,“年份+0000”为保健食品批准文号的年份和顺序号。 八、本规范自2011年2月1日起施行。 附件:1.国家食品药品监督管理局保健食品产品技术要求(文本格式) 2.保健食品产品技术要求编制指南
附件1: 国家食品药品监督管理局 保健食品产品技术要求(文本格式)(产品技术要求编号) 中文名称 汉语拼音名 【配方】 【生产工艺】 【感官要求】 【鉴别】 【理化指标】 【微生物指标】 【功效或标志性成分含量测定】 【保健功能】 【适宜人群】 【不适宜人群】 【食用量及食用方法】 【规格】 【贮藏】 【保质期】 ─────────────────────────────
1如何获得血压计的读数 概要 此款OMRONMX3Plus电子血压计不适合去测量心脏跳动的频率。 怀孕期间、脉搏无规律和动脉异常等类似影响测量的,请求教你的医生。 测量前避免吃饭、饮酒、吸烟、运动和洗澡。测量前和测量中应保持平静、放松。 你决不能不听从医生的吩咐而改变所服用的药剂剂量。 将此款血压计保存于温度–20℃至60℃之间的干燥、封闭的地方。 如果3个月或更长时间不使用,请将所有电池从电子血压计中取出。
使用时的劝告 一天至少检查你的血压两次(早餐前、工作后)。 当你在车上时,不要测量你的血压。 请始终在同一个手臂上测量血压。 在测量前,将“布袖口”缠好在手臂上。 警告 使用环境温度在10℃至40℃。 使用中避免剧烈振动、撞击、磁场、电器干扰及其它。不可在强烈日光下测量。 测量期间与移动电话保持至少5米远。 不要将“布袖口”缠绕在除手臂之外的其它物品上。不要将“布袖口”和管子折叠。
不要将OMRONMX3Plus血压计摔落。 2视图 A显示屏B记忆按钮C开始按钮 D开关按钮E交流电源插口F布袖口 G气管H气管插头J电池盒K气管插口 3准备工作 ⑴滑开电池盖。⑵按照图示插四节电池进电池盒, 并合上电池盒。
注意!必须是四 节相同的 AALR61.5V碱性电 池! 连接布袖口使布袖口缠绕好 注意!当布袖口没有 缠绕好手臂时,不要 使布袖口膨 胀! 如上图,将H(气管插头)插入K(气管插口) ⑴除去手臂上衣物 注意!卷起袖子时,切
勿压迫血液流动! ⑵将布袖口一端穿过H(金属环) 注意!不要将气管裹入⑶手臂穿过布袖口 布袖口内!注意!如测量左臂, 使气管与手臂、中指 保持平行!如上图; 如测量右臂,则将气 管与右手的小手指保 持平行!如左图。布 袖口下端与肘关 节保持1至2厘 米! ⑷捏住布袖口末 端,将它绕在手 臂上,如左图。
臂式全自动电子血压计使用说明书●感谢您购买本公司产品。●使用之前请您务必仔细阅读本使用说明书。●请您务必妥善保管本使用说明书。 录目 一) 规格( 二) 安全注意事项( 三) 各部名称( 四) 使用方法( ) 测量五( ) 其它(六) 异常状态之检定(七) 注意事项(八 格 (一) 规 ●本型号血压计为用于臂式测量的全自动电子血压计,能够快速简便地测量血压值和脉搏 臂式全自动电子血压计品名FT-A11-2 号型 数字式液晶显示示方式显 示波法检测方式式测量方分160)次/:(30压力:(20mmHg~300mmHg) 脉搏数~围测量范以内:±5%压力:(±5mmHg) 脉搏数度准确节DC6V (2A)4 源电 80%RH ≤度度 5℃~40℃湿正常工作环境温93%RH 10%RH~ -20℃~55℃湿度温度贮存运输环境195mm 可测量的手臂周长~约200mm) 含臂带,电池除外355克( 重量60mm ×厚长135mm×高93mm 主机)(外形尺寸安全分类内部电源B 型振动片式泵的加压调整方式式压加方急速排气阀开放方式快速排气方式半导体压力传感器测检压力半导体压力传感器博脉检测※本型号电子血压计不可用于幼儿。 (二) 安全注意事项 ※使用之前,请仔细阅读本“安全注意事项”,以便正确使用。 禁止一、自己判断测量结果而进行治疗十分危险。 1.请将测量结果交给了解您健康状况的医生并接受诊断。 2.如果服用药剂请遵医嘱。 对于那些因某些疾病引起的末梢循环障碍者,在手腕3.注和上臂部测量的血压值可能会出现较大差异。 二、请勿用于血压测量以外的用途。意否则,将有可能引起事故或发生故障。 三、请勿私自进行拆卸、修理和改造。否则将有可能发生事故和故障。 ※请将本说明书妥善保管。 称部名 (三) 各
关于印发化妆品产品技术要求规X的通知 国食药监许[2010]454号 各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为进一步规X化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,指导化妆品产品技术要求编制工作,国家食品药品监督管理局组织制定了《化妆品产品技术要求规X》,现予印发,请遵照执行。 附件:1.国家食品药品监督管理局化妆品产品技术要求(文本格式)2.化妆品产品技术要求编制指南 国家食品药品监督管理局二○一○年十一月二十六日 化妆品产品技术要求规X 一、根据《化妆品卫生监督条例》,为进一步规X化妆品行政许可工作,提高化妆品卫生质量
安全控制水平,加强化妆品生产经营卫生监督,保障消费者使用安全,制定本规X。 二、国家食品药品监督管理局负责批准化妆品产品技术要求,并监督其执行。 三、化妆品产品技术要求应当符合国家有关法律法规、标准规X。 四、化妆品产品技术要求应符合其文本格式的规定。文本格式应当包括产品名称、配方成分、生产工艺、感官指标、卫生化学指标、微生物指标、检验方法、使用说明、贮存条件、保质期等序列(见附件1),并按照《化妆品产品技术要求编制指南》(见附件2)编制。 五、化妆品产品技术要求是产品卫生质量安全的技术保障。生产企业应当按照化妆品产品技术要求组织生产经营,食品药品监督管理部门应当将化妆品产品技术要求作为开展卫生监督执法的重要依据。 六、化妆品产品技术要求适用于化妆品新产品的许可和产品延续。 七、化妆品产品技术要求编号。国产特殊用途化妆品按照HZ+GT+年份+0000编制;进口特殊用途化妆品按照HZ+JT+年份+0000编制;进口非特殊用途化妆品按照HZ+JF+年份+0000编制。"HZ"表示"化妆品","GT"表示"国产特殊用途","JT"表示"进口特殊用途","JF"表示"进口非特殊用途","年份+0000"为化妆品批准文号(或备案号)的年份和顺序号。 八、本规X自2011年4月1日起施行。 附件1 国家食品药品监督管理局化妆品产品技术要求(文本格式)(产品技术要求编号)_______
医学电子仪器原理与设计课程设计报告 设计名称:便携式电子血压计设计 2011-6-1
第一部分功能设计 1.1 电子血压计的设计目的 当今社会人们迫切希望一套成形的人体生理参数测量系统。血压是人体的重要生理参数,是人们了解人体生理状况的重要指标。测量血压的仪器称为血压计,血压计分为水银血压计、弹簧表式血压计、电子血压计三种。其中电子血压计是一种医用范围十分广泛的医疗设备,它外观轻巧、携带方便、操作简单、显示清晰,对提高人们的生活质量发挥了重要的作用。 我们想通过此设计来达到以下目的: 1.通过设计加深对单片机的认识、了解及掌握,掌握模数转换部分、中断部分以及数码显示部分的应用,能够达到软硬件相结合的程度。 2.加深对硬件电路的了解以及掌握,学会根据系统要求设计电路,学会动手焊接电路。 3.复习相关知识,加深对以往学过的知识点的理解程度(特别是软件编程的能力)。 4.锻炼自己发现问题、分析问题、解决问题的能力,培养团队意识,锻炼分工合作以及协调能力。 1.2电子血压计的主要功能 我们的血压计基于示波法原理,根据课程实验所发传感器US9116-006N实现较准确的压力传感,使用8位单片机ATmege16对信号进行处理,将收缩压和舒张压的值在LED上显示出来。 第二部分系统设计 2.1设计摘要 血压是人体重要的生理参数,准确的测量血压对人体的健康起着十分重要的作用。我们的血压计基于示波法原理,选用传感器US9116-006N实现压力传感,使用8位单片机ATmege16对信号进行处理,将收缩压和舒张压的值在LED上显示出来。整套仪器具有易于携带、测量方便的特点。 2.2血压测量原理 临床上血压测量技术一般分为直接法和间接法。前者的优点是测量值准确,并能连续监测,但它必须将导管置入血管内,是一种有创的测量方法;后者是利
日本精密测试器株式会社NISSEI 腕式血压计WS-540使用说明书 1.基本产品信息 本用户手册旨在帮助用户安全有效的使用WS-540型自动数码腕式电子血压计。用户需严格按照本手册的说明使用本产品,不得将产品用在其他用途。全面阅读并理解本手册具有重要意义。特别要仔细阅读并熟悉“用前须知”部分的内容。 使用提示 本产品是用来测量15岁以上成人的血压及心率,对被测量人不造成创伤。推荐血压不稳定或高血压的病人在家庭护理过程使用本产品,以作为医疗管理的补充。血压计袖带适用的手腕范围约为125-205毫米。测量的血压范围为0-300毫米汞柱,心率范围为40-160次/ 分钟。 注意,如果本产品在温度、湿度过高的环境中存放或使用,有可能造成测量值不够准确。 详见本手册产品规格部分。 测量方法 本产品采用示波(高频)测量法测量血压和心率。整个系统包括袖带是一个可放置于手腕的整体,袖带缠绕在手腕后可自动进行加压,袖带内的电路能感应每次心跳引发的手腕动脉血管的舒张与收缩,对箍袖带所产生的压力示波。系统自动测量每次压力示波的波幅并将其转化为毫米汞柱显示在电子屏幕上。内存线路可存储30次最新的测量结果以方便比较。 第1页 用前须知 1.在家测量的血压值通常比在医院、诊所和医务室的测量值偏低。 由于个人放松或压力程度不同,血压波动程度可在不知不觉中达到30-50毫米汞柱。 在医院测量的血压值可比在家测量的值高出25-30毫米汞柱。这是由于在家比较放松。因此了解在家测量的稳定血压值很有必要。 引起血压变动的原因: 运动精神压力情绪变动进食 环境或气温变化大小便谈话饮酒抽烟等 须知血压容易产生变动。 2.了解血压的本质 每天在同一时间进行测量。为了解血压的长期变动趋势,在家每天需在同一时间进行血压测量。 3.手腕上的血压可能与上臂的血压有所不同。 正常人这两个部位测量的血压值相差正负10毫米汞柱。 由于测量部位与血管厚薄的不同,手腕处测量的血压值可能与上臂处的有所差异。通
化妆品产品技术要求规范 一、根据《化妆品卫生监督条例》,为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,保障消费者使用安全,制定本规范。 二、国家食品药品监督管理局负责批准化妆品产品技术要求,并监督其执行。 三、化妆品产品技术要求应当符合国家有关法律法规、标准规范。 四、化妆品产品技术要求应符合其文本格式的规定。文本格式应当包括产品名称、配方成分、生产工艺、感官指标、卫生化学指标、微生物指标、检验方法、使用说明、贮存条件、保质期等序列(见附件1),并按照《化妆品产品技术要求编制指南》(见附件2)编制。 五、化妆品产品技术要求是产品卫生质量安全的技术保障。生产企业应当按照化妆品产品技术要求组织生产经营,食品药品监督管理部门应当将化妆品产品技术要求作为开展卫生监督执法的重要依据。 六、化妆品产品技术要求适用于化妆品新产品的许可和产品延续。 七、化妆品产品技术要求编号。国产特殊用途化妆品按照HZ+GT+年份+0000编制;进口特殊用途化妆品按照HZ+JT+年份+0000编制;进口非特殊用途化妆品按照HZ+JF+年份+0000编制。"HZ"表示"化妆品","GT"表示"国产特殊用途","JT"表示"进口特殊用途","JF"表示"进口非特殊用途","年份+0000"为化妆品批准文号(或备案号)的年份和顺序号。 八、本规范自2011年4月1日起施行。 附件1 国家食品药品监督管理局 化妆品产品技术要求(文本格式) (产品技术要求编号)_______________________________________ 中文名称 汉语拼音名 【配方成分】 【生产工艺】 【感官指标】 【卫生化学指标】 【微生物指标】