
加入20.0g Ca(OH)2
80.0g H
2
O 2013中考化学试题分类汇编-实验探究题
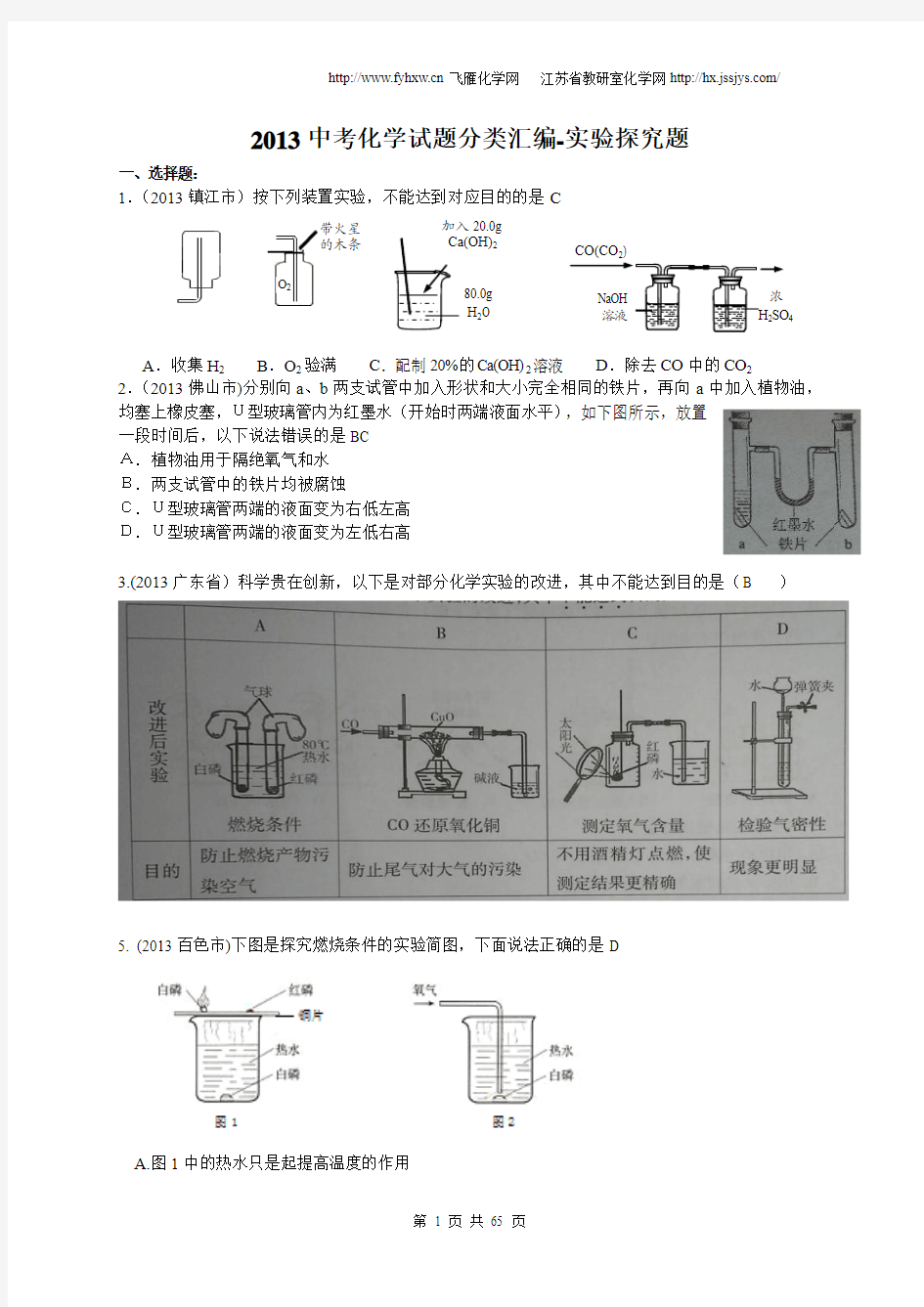
一、选择题: 1.(2013镇江市)按下列装置实验,不能达到对应目的的是C
A .收集H 2
B .O 2验满
C .配制20%的Ca(OH)2溶液
D .除去CO 中的CO 2 2.(2013佛山市)分别向a 、b 两支试管中加入形状和大小完全相同的铁片,再向a 中加入植物油,均塞上橡皮塞,U型玻璃管内为红墨水(开始时两端液面水平),如下图所示,放置一段时间后,以下说法错误的是BC A.植物油用于隔绝氧气和水 B.两支试管中的铁片均被腐蚀
C.U型玻璃管两端的液面变为右低左高 D.U型玻璃管两端的液面变为左低右高
3.(2013广东省)科学贵在创新,以下是对部分化学实验的改进,其中不能达到目的是(B )
5. (2013百色市)下图是探究燃烧条件的实验简图,下面说法正确的是D
A.图1中的热水只是起提高温度的作用
NaOH 溶液 浓 H 2SO 4 CO(CO 2)
带火星
的木条
B.图2中的白磷换成红磷也会有同样的现象
C.图1中的实验不能比较红磷和白磷着火点的高低
D.图1热水中的白磷不燃烧是因为没有与氧气接触
6.(2013邵阳市)小明通过化学方程式知道,电解水时生成氢气和氧气的体积比为2:1,但实验所得数据氢气和氧气的体积比略大于2:1.针对这一发现,你认为下列做法不可取的是(D)A.大胆提出假设:氧气比氢气易溶于水
B.反复多次实验查找原因
C.查找实验装置是否漏气
D.实验所得数据与理论相差不多,可以认为实验成功
7.(2013株洲市)用实验比较铜、锌、银的金属活动性,最好的方法是选用下列试剂中的 D A.ZnSO4溶液B.NaOH溶液C.稀硫酸D.CuSO4溶液8.(2013株洲市)下列实验操作、实验现象和实验结论均正确的一组是
实验操作实验现象实验结论
A 用带火星的木条伸入盛有某无色
气体的集气瓶中
木条复燃该无色气体为O2
B 将某气体燃烧,在火焰上方罩一
个冷而干燥的烧杯
烧杯内壁有水
珠生成
该气体一定为H2
C 向某无色溶液中滴加BaCl2溶液产生白色沉淀该无色溶液中一定含有H2SO4
D 将水注入盛有浓硫酸的烧杯中烧杯外壁发烫浓硫酸溶于水放出热量
9.(2013吉林省)下列实验设计方案合理的是(B)A.用碳酸钾和氢氧化镁制备氢氧化钾
B.用氯化钙溶液检验氢氧化钠是否部分变质
C.用氢氧化钡溶液区分硫酸铵、硫酸镁和硫酸钠
D.用氢氧化钠溶液和浓硫酸除去氢气中混有的氯化氢和水蒸气
10.(2013北京市)下列实验操作、现象与结论对应关系正确的是(D)
11.(2013泰州市)下列实验方案设计中,正确的是AB
A.除去NaCl中少量的Na2CO3杂质,先加入足量稀盐酸,再蒸发结晶
B.检验可燃性气体中是否含有氢元素,在其燃烧火焰上方罩上干冷的烧杯,观察有无水雾C.实验测定某矿石中碳酸钙的质量分数,先加入硫酸,再比较反应前后的质量变化
D.实验室制备干燥、纯净的氢气,用锌与浓盐酸反应,产生的气体经浓硫酸干燥后收集12.(2013苏州市)食品腐败是由于细菌或霉菌在潮湿、有氧、适温等条件下大量繁殖的结果。若要抑制食品中菌类的生长,下列措施不合理
...的是D
A.干燥B.密封后高温或低温冷藏
C.用盐腌渍D.加浓盐酸
13.(2013苏州市)为了验证铁、铜两种金属的活动性差异,如右图所示取2支试管分别进行有关实验,若要观察到现象的显著差异,所用液体合理的是B
A.蒸馏水B.稀盐酸
C.酒精水溶液D.硫酸钠溶液学科王
14. (2013沈阳市)下图是“一氧化碳与氧化铁反应”的部分实验装置,关于该实验说法正确的是A
A.充分反应后,向固体中加稀盐酸会产生气泡
B.在实验过程中,黑色的粉末会逐渐变成红色
C. 该实验的反应原理为FeO+ CO高温Fe+ CO2
D.在实验过程中,产生的尾气可以直接排放到空气中
15.(2013日照市)如图所示,实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响。经数小时实验后,U形管A、B两处的液面会出现下列哪种情况\C
A.A处下降,B处上升
B.A、B两处都下降
C.A处上升,B处下降
D.A、B两处都不变
16. (2013济宁市)某同学为探究镁、锌、铜、银的活动性顺序,设计如下实验流程:
依据该流程设计,下面对物质①、②的选择合理的是A
A. ①稀硫酸②硫酸铜
B. ①稀盐酸②硫酸锌
C. ①稀盐酸②硫酸亚铁
D. ①稀硫酸②氯化镁
17.(2013青岛市)控制变量法是实验探究的重要方法.利用如图所示的实验不能实现的探究目的
是(A)
A.甲图中①②对比可探究铁的锈蚀与植物油是否有关
B.甲图中①③对比可探究铁的锈蚀与水是否有关
C.乙可探究可燃物的燃烧是否需要达到一定温度
D.乙可探究可燃物的燃烧是否需要与氧气接触
18.(2013雅安市)蜡烛(足量)在如下左图密闭的集气瓶内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如下右图所示。下列判断正确的是B
A.蜡烛燃烧前瓶内只有氧气
B.氧气浓度小于一定值时,蜡烛无法燃烧
C.过程中瓶内物质总质量不断减少
D.蜡烛熄灭后瓶内只剩二氧化碳气体
19.(2013天津市)某研究性学习小组为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用下表中的不同试剂进行实
验.下列选项错误的是(BD)
选项所用试剂现象和结论
A 硫酸铜溶液出现蓝色沉淀,则氢氧化钠过量
B 氯化钡溶液出现白色沉淀,则硫酸过量
C 锌粒有气泡产生,则硫酸过量
D 无色酚酞溶液溶液不变色,则恰好完全反应
20.(2013昆明市)某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如下图所示的实验操作。其中可以达到实验目的的组合是D学D科王DD
A.①③B.②④C.④⑤D.②③
21.(2013迪庆州)实验室常用如图所示装置探究可燃物的燃烧条件.下列说法错误的是(A)
A.烧杯中的热水只起到加热作用
B.水中的白磷不能燃烧,是因为白磷没有与空气接触
C.对准烧杯中的白磷通入氧气,热水中的白磷能燃烧
D.铜片上的红磷不能燃烧,是因为温度没有达到着火点
二、填空与简答:
22.(2013北京市)化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
(1)步骤①中气球鼓起的原因可能是。
(2)步骤②中的操作是,其目的是。
(3)步骤④中发生反应的化学方程式为。
(4)本实验的结论是。
23.(2013北京市)四硫化钠()固体可替代红磷测定空气中氧气的体积分数,反应原理为:
。
【实验资料】
①受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢(水溶液呈酸性)。
②硫代硫酸钠()可溶于水,常温下与溶液不反应。
【实验过程】
①取碳酸钠、硫粉混合后置于试管中,加热(如图1所示,夹持装置已略去),
制得Na2S4,反应为,X 的化学式
为,蘸有浓NaOH 溶液的棉花的作用是。
②冷却后,取下棉花,入置一段时间,再向该试管中加入10ml 水,迅速塞紧橡胶塞,充分振荡,测量液面至橡胶塞下沿的距离,记录数据h 1(如图2所示) ③将该试管插入水中(如图3所求),按下橡胶塞,观察到_____,塞紧橡胶塞。将试管取出,倒过来,测量液面至橡胶塞下沿的距离,记录数据h 2,理论上h 1:h 2=____
24.(2013安徽省)某研究小组发现,维C 泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。 探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO 2、O 2、CO 、H 2、N 2。
小明说:不可能含有N 2,因为________________ _________________________________________。 小芳说:不可能含有CO 和H 2,因为从药品安全角度考虑,H 2易燃易爆,CO___________________________________________________。 该小组同学认为:该气体可能含有CO 2、O 2中的一种或两种。 【进行实验】
实验编
号
实验操作 实验现象
① 将气体通入澄清的石灰水
中
澄清石灰水变浑浊
②
将带火星的木条伸入该气
体中
带火星的木条没有
复燃
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的化学方程式 _____________________________________________________。
(2)由实验②_____________(填“能”或“不能”)确定该气体中不含氧气,理由是____ _____________________________________________________________________________。 探究二:维C 泡腾片溶液的酸碱性。
向维C 泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显_________性。 根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素。 有毒。
(1)二氧化碳;Ca (OH )2+CO 2=CaCO 3↓+H 2O 。
(2)不能;若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃。 酸。
主要成分
维生素C (C 6H 9O 6)
碳酸氢钠(NaHCO 3)
柠檬酸(C 6H 8O 7)
25.“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号硫酸的质量分数(均取
20mL)
锌的形状(均取1g)
氢气的体积(mL)(均
收集3分钟)
①20% 锌粒31.7
②20% 锌片50.9
③20% 锌粒61.7
④30% 锌片79.9
(1)写出稀硫酸与锌反应的化学方程式___________________________________________。
(2)小兵用右图装置收集并测量氢气的体积,其中量筒的作用是_______________________,氢气应从________(填e或f或g)管通入。
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________
____________________________________________________________________________。
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟)第1分
钟第2分
钟
第3分
钟
第4分
钟
第5分
钟
第6分
钟
H2的体积 3.1mL 16.7mL 11.9mL 9.6mL 7.6mL 6.0mL
请描述锌与硫酸反应的快慢的变化并解释原因______________________________________
______________________________________________________________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________
______________________________________________________________________________________ _______________________________________________________________________。
(1)Zn+H2SO4=ZnSO4+H2↑。
(2)根据进入量筒中水的体积,判断生成氢气的体积;F。
(3)①③或②④。
(4)硫酸的质量分数越大,反应速率越快/锌与硫酸的接触面积越大,反应速率越快。
(5)由慢到快然后逐渐减慢;随着反应的进行,硫酸被消耗,硫酸溶质质量分数变小。
(6)温度;取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间。(只要考生有控制变量的意识即可)
26. (2013厦门市)用Y 形管或Y 形导管完成以下实验。
(1)图9 中Y 形管左侧管中加入无色酚酞试液,右侧管中加入浓氨水,一段时间后,可观察到的
现象:________________________,用分子的观点解释这一现象:________________________。 (2)图 10 中 Y 形导管平放于桌面,实验中可观察到的现象;________________________,用化
学方程式解释结论:________________________;若把 Y 形导管固定在铁架台上(如图 11 ) , a 管位于上方, b 管位于下方,两石蕊试纸均湿润,可观察到 b 管中试纸变色比 a 管明显,原因:________________________。 (1)无色酚酞变红色,分子的不断运动。
(2)湿润的紫色石蕊试纸变红色,干燥的紫色石蕊试纸无明显变化。H 2O+CO 2=H 2CO 3;二氧化碳
的密度比空气大,主要从b 管中通过。
27. (2013厦门市)某化学兴趣小组回收利用废旧干电池。
实验 1 回收填料中的二氧化锰和氯化铵 查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。兴趣小组的同学们设计回收物质的流程如图 12 所示。
(1)操作 1 和操作 2 的名称都是____________,该操作中玻璃棒的作用是____________。 (2)灼烧滤渣 l 的目的是________________________ 。
(3)己知滤液 1 中氯化铵和氯化锌的浓度相近。在某温度下蒸发滤液 1 时,大量的氯化铵晶体先
析出,说明该温度下氯化铵溶解度____氯化锌的溶解度(填“<”、“=”或“>”)。 实验 2 利用外壳回收物锌制取氢气及相关探究
(4)用锌和稀硫酸制取氢气。己知氢气密度比空气小且难溶于水,提供装置如图 13 。
① 应选择:发生装置为____(填编号),排空气法收集装置为____(填编号)。
② 若用排水法收集并测定气体的体积,气体从装置 B 导管口____(填“ a ”或“ b ” ) 进;选用仪器 F 测量排出水的体积,仪器 F 名称是________。
(5)探究影响锌与稀硫酸反应快慢的因素。反应过程中,用前 10 min 内收集的氢气体积比较反应
的快慢。控制其他条件相同,进行下表四组实验,获得数据如下表。
验实号编 试剂
前 10 min 内产生的氢气体积(mL)
不同纯度的锌
不同体积和浓度的稀硫酸
a 纯锌 30 mL 30 % 564.3
b 含杂质的锌 30 InL 30 % 634.7
c 纯锌 30 mL 20 % 449.3 d
纯锌
40 mL 30 %
602.8
① 比较实验 a 和实验 b ,可以得到的结论是________________________。
② 为了研究硫酸浓度对反应快慢的影响,需比较实验_____和实验_____(填编号)。 ③ 控制其他条件相同,需控制的条件是______________________(例举一种条件即可)。 (1)过滤,搅拌。(2)除去炭粉。(3)<。(4)①B ,D 。 ② b ,量筒。 (5)① 与同体积同浓度的稀硫酸反应,含杂质的锌比纯锌反应速率要快。
② a 和d 。 ③ 温度(或锌粒形状大小)。
28.(2013福州市)四氧化三铁可用于医疗器械、电子等工业。某实验兴趣小组从工厂采集废液(含FeSO 4和少量ZnSO 4、MgSO 4),进行四氧化三铁的制备实验。 【阅读资料】
(1)25℃时,去氧化物沉淀的pH 范围如表3。
Zn (OH )2
Fe (OH )2
Mg (OH )2
开始沉淀的pH 5.7 7.6 10.4 沉淀完全的
pH
8.0
9.6
12.4
表3
(2)25℃时,Zn (OH )2可溶于pH >10.5的碱溶液。学科王 (3)制备Fe 3O 4的实验流程如下:
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为 (写一个即可)。
(2)操作a 的名称为 。该操作需要的玻璃仪器有烧杯、玻璃棒、 等。玻璃棒在此操作中的主要作用是 。
(3)溶液1所含溶质有 (至少写两种);溶液3所含溶质的主要成分为 。
(4)该实验取废液100g ,最终得到产品四氧化三铁质量为3.48g ,则原废液中硫酸亚铁溶质的质量分数不低于 (精确到0.01%)。
⑴2 NaOH+ ZnSO 4= Zn (OH )2↓ +Na 2SO 4【或2 NaOH+ FeSO 4= Fe (OH )2↓ +Na 2SO 4】⑵过滤、漏斗、引流(搅拌)⑶硫酸镁、硫酸钠、氢氧化钠、氢氧化镁(两种即可)、硫酸
29.(2013泉州市) 我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献。用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验。 资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应。
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳。 [方案一] 样品与氯化钙溶液反应,测定Na 2CO 3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的
CaCl 2溶液要过量..的原因:___________________;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量。利用沉淀物质量计算
实验操作
实验现象
实验结论
取一定量纯碱样品配成溶液后,滴加过量..
的CaCl 2溶液。 产生白色沉淀 反应的化学方程式:
Na 2CO 3的质量分数为91%。如果不洗涤沉淀物会造成测定结果大于91%,这是因为 _____ 。 [方案二] 样品与稀盐酸反应,测定Na 2CO 3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO 2气体的质量,计算Na 2CO 3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
(4) 打开止水夹K ,先对装置A 和B (已连接)通入已除去CO 2的空气一会儿,以排尽装置A 和B 中含有的 ,再接上装置C 和D 。
(5)关闭止水夹K ,加入足量的稀盐酸(杂质不与盐酸反应),装置A 中样品产生气体的化学方
程式为__________________。
(6)待装置A 中的反应结束后,再一次打开止水夹K ,继续往装置通入已除去CO 2的空气一会儿。根据 _______________ 定律,装置_________(填标号)在反应前后的质量差就是产生CO 2的质量,由此计算出该样品中Na 2CO 3的质量分数。若没有装置D ,将会使测定结果 ________(选填“偏大”或“偏小”)。
(1)Na 2CO 3+CaCl 2═CaCO 3↓+2NaCl (2)与碳酸钠充分反应
(3)不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大 (4)二氧化碳
(5)Na 2CO 3+2HCl═2NaCl+H 2O+CO 2↑ (6)质量守恒定律 C 偏大
30.(2013龙岩市)实验与探究是化学学习的重要方法和内容。
(1)今年5月,我市各学校进行了实验操作考查。小张同学进行的实验考查是“用稀盐酸鉴别氢氧化钠(NaOH )溶液和碳酸钠(Na 2CO 3)溶液,并测定碳酸钠溶液的pH”。
①小张同学的实验记录如下表,请补充完整:
②用pH 试纸测定碳酸钠溶液的酸碱度,简述操作的主要步骤: 。
(2)在实验台上有三瓶未贴标签的溶液,已知分别是碳酸钠溶液、氢氧化钠溶液和稀盐酸。为区别这三种溶液,在老师指导下,兴趣小组的同学把这三种溶液按A 、B 、C 进行编号,然后分别各取适量作为样品加入到三支试管中,进行了如下图所示的探究活动:
学科王
操作步骤 现象记录 反应的化学方程式
取两支试管,分别往试管中加入2mL 样品1、
2,再往其中滴入盐酸
样品1:无明显现象 ______________________
样品2:溶液中出现气泡 ______________________
H
2
5%
学科王 学科王
步骤一中,C 无明显现象,A 、B 溶液的颜色变成红色;
步骤二中,A 、B 溶液的颜色由红色变成无色,且B 溶液中有气泡冒出。 ①根据上述实验现象可知,B 、C 溶液分别是_________、__________。
②某小组同学在进行步骤一实验时出现异常现象:往A 溶液中加入酚酞试液时,溶液颜色先变成红色,振荡后迅速变成无色。老师指出这是因为溶液浓度过大....造成的。接着,老师往该试管的溶液中加入适量盐酸,观察到A 溶液的颜色又变成红色,此时..溶液中含有的溶质主要是_________________________(酚酞除外)。 (1)①样品1:NaOH+HCl=NaCl+H 2O
样品2:Na 2CO 3+2HCl=2NaCl+H 2O+CO 2↑
②用玻璃棒蘸取碳酸钠溶液滴在pH 试纸上,把试纸呈现的颜色 与标准比色卡对照①碳酸钠溶液 稀盐酸 ②氯化钠、氢氧化钠 学科王
31. (2013兰州市)实验室中有一瓶标签受损的无色液体,如右图所示。这瓶无色液体是什么呢? 实验
员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸和蒸馏水中的一种。 (1)大家讨论后一致认为不可能是蒸馏水,理由是 。 (2)为确定该液体成分,同学们继续进行了如下实验探究: 实验操作
实验现象 实验结论 步骤一:取该液体适量于试管中,向
其中加入少量 粉末。 没有气泡产生。 该液体不是过氧化氢溶液。 步骤二:取该液体适量于试管中,向其中滴加少量氯化钡溶液。
该液体是稀硫酸。
【反思交流】
(1)大家认为标签受损的原因可能是 ;
(2)如果该液体是过氧化氢溶液,则步骤一中产生的变化用化学方程式表示为
。 (1)由标签知该液体是混合物,而蒸馏水为纯净物(合理答案均可) (2)二氧化锰(或MnO 2)(合理答案均可) 产生白色沉淀 【反思交流】(1)倾倒液体时标签未朝向手心(合理答案均可) (2)2H 2O 2
2H 2O + O 2↑学科王
32.(2013广东省)仓库中有一包氮肥的包装标签模糊不清,有同学进行了以下探究:
(1)操作③用玻棒搅拌的目的是 。
(2)请完成下表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
假设和现象判断和化学方程式
a 若现象I为无氨味。则样品中不含________________(填名称)。
b 由操作②现象判断。该样品一定含有__________离子。
c 若现象Ⅲ为白色沉淀,现象Ⅳ为无
沉淀。则样品中含有(写名称),该反应的化学方程式为。
d 若现象Ⅲ为“无沉淀”,现象Ⅳ为白
色沉淀。则样品中含有(写化学式),该反应的化学方程式为。
(3)若现象Ⅲ、Ⅳ都无现象,则该氮肥可能是___________(写化学式);若操作②现象为无气味、现象Ⅲ、Ⅳ无现象,则该氮肥可能是(只写一种)。
(1) 加速溶解
(2) a.碳酸氢铵b.铵根(或铵、或
4
NH)
c.硫酸铵(NH4)2SO4 + Ba(NO3)2 =BaSO4↓+ 2NH4NO3
d. NH4Cl NH4Cl + AgNO3= AgCl↓+ NH4NO3
(3) NH4NO3尿素(或硝酸钾、硝酸钠等)
33. (2013广州市)某学习小组在如图所示的化学药品柜中发现一瓶标签模糊
不清的无色溶液,已知这瓶溶液是一下5瓶溶液中的一种:HNO3溶液、
Mg(NO3)2溶液、Ba(NO3)2溶液、Cu(NO3)2溶液、NaNO3溶液。
(1)根据上述信息判断,该无色溶液不可能是溶液和
溶液,只可能是其他3种溶液中的一种。学科王
(2)为了进一步确定该溶液是何种溶液,请你设计实验方案,叙述实
验操作、预期现象与结论。
限用试剂:稀H2SO4、NaOH溶液、Na2CO3溶液、酚酞溶液
实验操作预期现象与结论
(1)HNO3Cu(NO3)2
(2)
实验操作
预期现象与结论
(1)取少量溶液于试管中,加入适量的NaOH 溶液,振荡,观察(2分)
若出现白色沉淀,则原溶液为Mg(NO 3)2溶液 若无明显现象,则原溶液为Ba(NO 3)2溶液或NaNO 3 (2分)
(2)另取少量溶液于试管中,加入适量的稀H 2SO 4,振荡,观察 (2分)
若出现白色沉淀,则原溶液为Ba(NO 3)2溶液 若无明显现象,则原溶液为NaNO 3溶液 (2分)
(其他答案合理亦可)
34.(2013广州市)实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未密闭的KOH 固体,对其成分提出以下假设,并完成了实验探究。 假设1:只含KOH ; 假设2:含KOH 和K 2CO 3; 假设3:只含K 2CO 3
(1)成分中可能含有K 2CO 3的原因是(用化学方程式回答)________________________。
(2)取少量样品于试管中,加入足量稀盐酸,观察到_____________________,说明假设2或假设3成立。
(3)进一步探究的过程如下:
①“操作1”的名称是____________检验 ②“固体A”的化学式是___________。
③加入足量CaCl 2溶液的作用是_______________________________。
(4)变质试剂也有利用价值,从KOH 和K 2CO 3的组成和性质看,这瓶变质试剂的用途是 __________________________________________(写出一条)。 (1)2KOH + CO 2 === K 2CO 3 + H 2O (2分) (2)有气泡产生 (1分)
(3)①过滤 (1分) ②CaCO 3 (1分)
③ 将碳酸钾完全反应,防止对接下来的实验干扰 (2分)
(4)作钾肥(其他答案合理则可)(1分)
35.(2013佛山市)
我国大部分地区深受酸雨的危害,煤燃烧产生的SO 2是形成酸雨的主要污染物,SO 2与水结合生成弱酸性亚硫酸(H 2SO 3)。
已知:H 2SO 3易分解生成水和SO 2,也易与空气中的氧气或稀硝酸反应生成H 2SO 4;H 2SO 3和SO 2都能使红色的品红溶液褪色。
(1) 酸雨是pH 小于______的降雨。
(2) 常用脱硫方法减少废气中的SO 2,以生石灰(CaO )为脱硫剂,高温下与废气中的SO 2与
O 2化合生成CaSO 4,化学方程式为________________________
(3) 实验室常用亚硫酸盐与HCl 或H 2SO 4反应制备SO 2,Na 2SO 3与盐酸反应的化学方程式
____________________________。
(4)
小鸿同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH 约为3)中加入足量的
KOH ,并就反应后混合溶液的中盐成分进行如何探究: [提出猜想]反应后的混合溶液中盐的成份是什么? [进行猜想]猜想1:只有K 2SO 3 猜想2:___________
猜想3:既有K 2SO 4,也有K 2SO 3
[实验探究]限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液 步骤 实验操作
预期现象与结论
1 各取2mL 反应后的混合溶液分别加入A 、B 两只试管
2 向A 试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液
证明含有K 2SO 3
3
向B 试管中,加入_____________________,再加入足量的________________________
先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有K 2SO 4,则猜想3成立
(1)5.6 (2)2CaO+2SO 2+O 2==2CaSO 4 (分步写也给分)
(3)Na 2CO 3+2HCl=2NaCl+SO 2↑+H 2O (4)K 2SO 4
(5) 有气泡产生,品红溶液褪色(缺少“气泡产生”不扣分 足量的氯化钡溶液 稀盐酸(写化学式也给分)
36.(2013揭阳市)某化学兴趣小组根据右图所示进行模拟炼铁的实验,并对产物成分进行探究。 经初步分析:无色气体A 不含有单质气体,黑色粉末B 含有两种单质中的一种或者两种。
学科王
高炉炼铁的原理为:Fe 2O 3+3CO 高温2 Fe+3CO 2,请写出反应器中一氧化碳是如何产生的化学方程式: 。
兴趣小组又分成甲乙两组分别对无色气体A 和黑色粉末B 的成分进行探究。 【猜想与假设】
甲组在分析了炼铁的原理后,认为无色气体A 中可能有CO 2,也可能有未反应的 。 乙组认为黑色粉末的成分中存在以下三种情况:
假设一:只含有铁。 假设二:只含有 。 假设三:以上两种物质都含有。 【实验探究】
(1)为验证甲组的猜想,大家按下图示进行实验(箭头表示气体流向):
高温 O 2 Fe 2O 3、C 无色气体A 高温
黑色粉末B 无色气体A 澄清石灰水 Ⅰ 浓硫酸 Ⅱ 灼热氧化铜
Ⅲ
当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A的成分为:,Ⅱ中浓硫酸的作用是:。
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
实验方法实验操作实验现象实验结果
物理方法假设三成立
假设三成立化学方法取少量黑色粉末B于试管中,加入过量
的稀盐酸
写出黑色粉末B中加入过量的稀盐酸反应的化学方程式:。
【交流反思】
在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来。
C+O2点燃CO2 、CO2+ C高温2CO CO;C学科王
⑴CO2、CO;干燥作用
⑵
实验方法实验操作实验现象实验结果
物理方法取少量黑色粉末B,用磁铁吸引部分黑色粉末被
吸引上来
化学方法部分黑色粉末溶
解,产生气泡
Fe+2HCl= FeCl2+H2↑
没有进行尾气处理
37. (2013南宁市)某化学兴趣小组设计了如右下图所示的装置,对纯碱(Na2CO3)和小苏
打(NaHCO3)两种固体进行实验探究。
(1)写出甲、丙两种仪器的名称:甲__________,乙__________。
(2)在实验过程中,观察到乙仪器中的澄清石灰水变浑浊,请写出丙仪器
中发生反应的化学方程式
___________________________________________________。
(3)该实验探究利用的科学方法是________________________________(填“控制变量法”、“对比观察法”或“定量分析法”),实验目的是__________________________________________。
38. (2013百色市)探究(1)(4分)碳酸氢钠(NaHCO3)俗名小苏打,常用于食品和医学工业。某化学兴趣小组的同学对碳酸氢钠进行加热,发现有气泡,同时还剩余白色固体。他们对白色固体进行探究。
【提出问题】这白色固体是什么?
【查阅资料】碳酸氢钠受热易分解生成水、二氧化碳和一种常见的固体。
【提出猜想】猜想1:白色固体是碳酸钠,
猜想2:白色固体是氢氧化钠
猜想3:白色固体是氢氧化钠和碳酸钠的混合物
【实验探究】兴趣小组为了确定反应后的固体产物成分,进行了如下实验,请填写下表:
【实验总结】写出碳酸氢钠受热分解的化学方程式③ 。
探究2:某化学兴趣小组把金属钠投到硫酸铜溶液中,实验并非如想象的有红色铜析出,而是生成一种蓝色沉淀。同学们非常好奇并进行实验探究 。
【提出问题】金属钠投到硫酸铜溶液中到底发生了怎样的化学反应?
【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性 【提出猜想】猜想1:钠先与水反应生成氢气和某碱溶液,某碱再与硫酸铜反应生成蓝色沉淀;
猜想2:钠先与水反应生成某气体和某碱溶液,某碱再与硫酸铜反应生成蓝色沉淀;
【实验探究】实验一:同学们把一小块切干净的钠投到装有少量蒸馏水的试管中,点燃生成的气体 ,
听到“噗”的一声后燃烧起来;
实验二:在剩余的溶液中加入硫酸铜溶液,发现有蓝色沉淀。学科王
【实验总结】①两个猜想中的“某碱”是 ,猜想2中生成的气体是 ;②水与
金属钠反应的化学方程式 。③请你判断猜想 成立。
39.(2013河北省)小明设计的探究燃烧条件的实验如图9所示。请回答
下列问题。
(1)凸透镜对光有 作用。 (2)A 处红磷燃烧,B 处红磷不燃烧,由此得出的燃烧条件是
。
(3)熄灭A 处火焰,可采用的方法是(写出一种即可): 。 (1)会聚 (2)温度达到可燃物着火点 (3)盖湿抹布 40.(2013河北省)乙炔(C 2H 2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊
接金属。乙炔由碳化钙(块状固体,化学式为CaC 2)与水反应生成,同时生成一种白色固体。 【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO ;猜想二:
;猜想三:Ca(OH)2。
他的依据是 。 【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。 【进行实验】
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到 ,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液, ,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为:
实验方案
实验现象 结论
步骤一:取少量反应后的固体产物溶于水,加入过量的中性氯化钙溶液,过滤。
产生白色沉淀
学科王
猜想1成立学科王
步骤二:取滤液少许,往滤液中滴入:①
② 学科王 B
A 图9
红磷
。 结论:白色固体是Ca(OH)2。
【拓展应用】已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 (选填图15中装置序号)。
【做出猜想】CaCO 3 化学变化过程中元素不变 【交流反思】CaO 能与水反应 【进行实验】 (一)气泡放出
(二)通入二氧化碳气体 Ca(OH)2 + CO 2 = CaCO 3↓ + H 2O
[或滴加碳酸钠溶液 Ca(OH)2 + Na 2CO 3 = CaCO 3↓ + 2NaOH ] 【拓展应用】C 、 F
41.(2013河南省)酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应。
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有 生成。 (2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象。取反应后的部分溶液加热、蒸干、得到白色固体。
以下是探究白色固体成分的实验,已知CaCl 2溶液呈中性。请填写下表: 实验操作
测定结果
白色固体成分 用pH 试纸测定反应后溶液的酸碱度,操作方
法
是
pH >7
CaCl 2
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点。
(3)“粗盐提纯”指除去NaCl 中的泥沙和MgCl 2、CaCl 2、Na 2SO 4等杂质。
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl 2、NaOH 、Na 2CO 3溶液,充分反应后过滤,蒸发结晶。请回答:
部分物质的溶解性表(室温) OH -
Cl - SO -
24 CO -
23 H +
溶、挥
溶
溶、挥
A B C D E F
图15
①溶解、过滤和蒸发操作中都用到一种玻璃仪
器,该仪器在蒸发操作中的作用是什么?
②加入Na 2CO 3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充。
(4)LiOH 和NaOH 的化学性质相似。“神舟”飞船内,可用盛有LiOH 的过滤网吸收航天员呼出的气体,以降低CO 2含量。请计算:用LiOH 完全吸收176 g CO 2生成Li 2CO 3和H 2O ,理论上至少需要LiOH 的质量是多少? (1)水(或难电离物)(1分) ⑵
(3)①用玻璃棒不断搅拌,防止因局部温度过高造成液滴飞溅。(1分) ②除去CaCl 2杂质和过量的BaCl 2 (1分)
③过量的NaOH 和Na 2CO 3未除去,还应加人适量的盐酸。(1分) (4 )解:设理论上至少需要LiOH 的质量为-。 2LiOH + CO 2 =Li 2CO 3 + H 2O (1 分) 48 44 x 176 g
g
176x 4448= (1分) x=
44
g
17648? = 192 g (1 分) 答:理论上至少需要LiOH 的质量为192 g 。
42.(2013哈尔滨市)实验室有四瓶失去标签的溶液,现标为A 、B 、C 、D ,分别是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐酸中的一种。
【提出问题】如何区分出四种溶液?
Ba 2+ 溶 溶 不溶 不溶
Ca 2+ 微溶 溶 微溶 不溶
Mg 2+ 不溶 溶 溶 微溶
实验操作
测定结果 白色固体成分 用玻璃棒蘸取溶液滴到pH 试纸上,把 试纸显示的颜色与标准比色卡比较。 (1分)
CaCl 2、Ca(OH)2 (1分) pH ≤ 7 (1分)
【进行实验】甲同学实验如图所示:由此甲同学认为A一定不是(1)____________
【表达与交流】甲同学向实验后的溶液中滴加酚酞溶液,酚酞溶液由无色变为红色,则甲同学的结论:A是氯化钡溶液。
乙同学不同意甲同学的结论,乙同学的理由是(2)__________________________________。
于是乙同学另取少量A于试管中,向其中滴加一种试剂是(3)_________ _______溶液,
观察到的明显现象是(4)____________________.由此证明了甲同学的结论是错误的.同时确定了A。乙同学继续实验如图所示:
【收集证据】观察到C中产生气泡,D中产生白色沉淀。
【解释与结论】写出D中发生反应的化学方程式(5)__________________________________ 乙同学最终通过实验区分出了四种溶液。
【反思与评价】请指出甲同学区分上述四种溶液时,在实验方法上的一点不足之处(6)__________________________________。
43. (2013武汉市)某化学小组成功完成了下图所示实验(装置气密性良好),验证了二氧化碳的组成。探究过程如下:
1. 称量装有干燥块状木炭的试管D,质量为50.7g,装有碱石灰的装置C质量为11
2.3g,连接A、B、D装置;
2. 从长颈漏斗加入足量3%的过氧化氢溶液,连接C装置,点燃酒精灯;
3. 待D中发生反应,熄灭酒精灯,冷却;
4. 称量试管D及剩余固体的质量为50.1g,装置C的质量为114.5g
已知:碱石灰的成分是氧化钙和氢氧化钠,木炭中的杂质不参与反应,B、C中所装药品足量,能完全吸收相关物质。请回答下列问题:
装置A反应的化学方程式为_____________________,该反应属于_________反应
酒精灯加热的作用是_____________________
为减小误差,步骤Ⅲ冷却过程中需要注意的问题是_______________________
根据实验数据计算参加反应的氧气的质量为(列式并计算)_____________,从而计算出二氧化碳中碳、氧元素的质量比。
44. (2013孝感市)某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
【提出猜想】放出的气体可能是SO2、O2、H2,提出猜想的依据是。
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是_____________________________________。
(2)乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式________________________________。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
若拆去B装置,直接连接A和C装置进行实验,可能导致后果发生。
【实验探究】实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;
这样操作的目的是。
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色;
结论:铁粉与硫酸铜溶液反应时,产生的气体是_________________。
【思维拓展】由上述实验可以推出,硫酸铜溶液中可能含有____________。
45.(2013咸宁市)某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
Ⅰ、写出该中和反应的化学方程式:___①___。
Ⅱ、探究烧杯内溶液中溶质的成分。
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:___②___。
【查阅资料】氯化钙溶液呈中性。
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡
实验现象:___③___结论:猜想一不正确
实验步骤:实验步骤取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量
实验现象:__④__结论:猜想二不正确,猜想三正确
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑___⑤___。
2010高考化学试题分类汇编:化学计算 1.(2010全国卷1).下列叙述正确的是 A .在醋酸溶液的pH a =,将此溶液稀释1倍后,溶液的pH b =,则a b > B .在滴有酚酞溶液的氨水里,加入4NH Cl 至溶液恰好无色,则此时溶液的pH 7< C .31.010mol/L -?盐酸的pH 3.0=,81.010mol/L -?盐酸的pH 8.0= D .若1mL pH 1=的盐酸与100mL NaOH 溶液混合后,溶液的pH 7=则NaOH 溶液的pH 11= 【解析】A 若是稀醋酸溶液稀释则C(H +)减小,pH 增大,b >a ,故A 错误;B 酚酞的变色范围是pH= 8.0~10.0(无色→红色),现在使红色褪去,pH 不一定小于7,可能在7~8之间,故B 错误;C 常温下酸的pH 不可能大于7,只能无限的接近7;D 正确,直接代入计算可得是正确,也可用更一般的式子:设强酸pH=a ,体积为V 1;强碱的pH=b ,体积为V 2,则有10-a V 1=10-(14-b)V 210142 1-+=?b a V V ,现在V1/V2=10-2,又知a=1,所以b=11 【答案】D 【命题意图】考查弱电解质的稀释,强酸的无限稀释,指示剂的变色范围,强酸与强碱的混合pH 的计算等基本概念 【点评】本题在第一轮复习至第三轮复习无时不在强调的基本问题考查就是第二册第三章的问题,这次居然没有考离子浓度大小比较,而考这些,很简单,大家都喜欢! 2.(2010全国卷1)12.一定条件下磷与干燥氯气反应,若0.25g 磷消耗掉314mL 氯气(标准状况),则产物中PCl 3与PCl 5的物质的量之比接近于 A .1:2 B .2:3 C .3:1 D .5:3 【解析】设n(PCl 3)=X mol, n(PCl 5)=Y mol ,由P 元素守恒有:X+Y=0.25/31≈0.008……①;由Cl 元素守恒有3X+5Y=(0.314×2)/22.4≈0.028……②,联立之可解得:X=0.006,Y=0.002故选C 【命题意图】考查学生的基本化学计算能力,涉及一些方法技巧的问题,还涉及到过量问题等根据化学化学方程式的计算等 【点评】本题是个原题,用百度一搜就知道!做过多遍,用的方法很多,上面是最常见的据元素守恒来解方程法,还有十字交叉法,平均值法、得失电子守恒等多种方法,此题不
中考化学实验探究题归类 科学探究是学生自主学习的主要学习方式,贯穿与整个教学的各个环节。近几年的各地中考试卷中,以开放型的命题方式对探究能力的考查比重在逐年加大,尤其是实验探究题更呈现出多样、灵活和开放。现就该类考题归类解析如下: 一、物质成份的探究 例1、(05黄岗)室验室开放日,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体”之间的反应进行一些探究。 (1)小娜同学从一瓶固体和一瓶液体中各取少量试剂于试管中进行混合,立即 产生了一种无色气体,对气体是何物质,同学们进行了大胆的猜想,小佳同学的 猜想可能是①;②;……。 (2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如下: 实验步骤现象及结论 (3,则气体 由(填a或b)端进入。 (4)小丽同学从另外两瓶试剂中各取少量试剂于试管中,发现混合后,固体发生了变化,但无气泡放出。同学们对加入试管中的固体和液体从不同的反应类型、物质类别等方面进行了大胆的猜想: 猜想一:; 猜想二:; 猜想三:; ……。 例2、(03宜昌)“旺旺雪饼”袋内有一个小纸袋,上面写着“干燥剂,主要成分是生石灰”。 ⑴生石灰(CaO)可作干燥剂的理由是(用化学方程式表示)。 (2)我对它作了一系列探究,获得较多收益,其实验方案如下:
我对它还有 一个要再探 究的新问 题:。 分析:首先 是要清楚生 石灰可作干 燥剂的化学原理,同时要分析生石灰在空气中久置会发生一些什么变化以及变化后的产物,针对产物的性质特点设计实验方案进行探究。 例3、(05眉山)小李和小王两位同学对碱式碳酸铜[Cu2(OH)2CO3]受热完全分解后的黑色固体产物的成分进行探究。 (1)小李根据碱式碳酸铜的化学式对黑色固体产物做出以下猜想:①可能是碳,②可能是氧化铜,③可能是碳和氧化铜的混合物。他做出以上猜想的依据是; (2)小王根据碳的化学性质,认为猜想③可以排除,理由是; (3)为验证①、②猜想,他们设计如下实验方案:向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,待完全反应后静置观察现象。若猜想①正确,现象应该是 ;若猜想②正确,现象应该是。 分析:(1)反应物为碱式碳酸铜[Cu2(OH)2CO3],根据质量守恒定律,化学反应前后元素的种类和质量都不变,所以反应后物质也由铜、氧、氢、碳几种元素组成,据此可作出猜想; (2)猜想③碳和氧化铜的混合物受热会发生反应生成铜和二氧化碳,所以此猜想不合理; (3)鉴别碳和氧化铜,根据其化学性质不同,可向盛有少量黑色固体的试管中加入足量的稀硫酸,振荡,碳和稀硫酸不反应,氧化铜和稀硫酸反应生成硫酸铜和水,溶液变蓝色,据此可鉴别碳和氧化铜. 二、物质变化条件的探究
.实验探究题目 1为探究蚯蚓对土壤的影响,某同学做了如下实验:取一较大的玻璃缸,下层装颜色较深的粘土,中间装颜色较浅的沙土,上层再装颜色较深的粘土。每装一层稍加按压,使玻璃缸中的土保持一定湿度。三层土的总体积约占玻璃缸容积的四分之三,以保持玻璃缸内有足够的空气。选几条生长良好的蚯蚓放在上述盛土的玻璃缸内,并投放一定量的腐烂树叶,玻璃缸上盖一玻璃片(留一小孔通气)。将上述装置放入温暖、不直接见阳光处5~6日,观察土壤的分层情况及疏松状况。 (1) 请你预测所观察到的现象。 (2) 此实验结果能说明什么问题? (3) 该探究实验能成功的先决条件是什么? 2 土壤中含有植物生长所必需的各种无机盐,小明同学为了验证镁是甲种植物正常生长所必需的元素,设计了如下实验: 选择两盆生长状况相似的甲种植物,在一盆甲种植物的土壤中浇灌蒸馏水,在另一盆甲种植物的土壤中浇灌等量的含镁离子的蒸馏水,保持其他实验条件相同,观察比较两盆植物的生长情况。你认为这样的实验设计合理吗?___ _;理由是 。 3经测量,台州某地土壤中砂粒的含量约20%、粉砂 粒的含量约20%.黏粒的含量约60%。据图判断,该土壤 的类型为类土壤。 4 某同学取四份土壤,在①②③三个花盆中放入较肥沃的土壤,花盆④放入细砂石和碎石块,把长势相近的同种植物移栽盆中。并将花盆①放在盛满水的水盆中,水面与土面相平。同时每天给花盆①②④土壤浇相同的水,花盆③土壤不浇水。请回答: (1)从实验条件上看①②有什么不同?②③有什么不同?②④有什么不同? (2)从实验结果上看①②②比较说明了什么?②③比较说明了什么?②④比较又说明了什么? (3)请帮助该同学预测,哪一盆植株生长最好?并说明理由。 第二节各种各样的土壤 小明想知道“土壤性状和植物生长的关系”。他分别取等体积的砂土类土壤、黏土类土壤、壤
2020高考化学试题分类汇编电化学基础 1.〔2018全国卷1〕右图是一种染料敏化太阳能电池的示意图。电池的一个点极由有机光敏燃料〔S〕涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为: TiO2/S h TQ2/S 〔激发态〕 TiO 2/S TiO 2/S+ +e- l3+2e 3I 2TiO 2/S 3I 2TiO2/S+I3 以下关于该电池表达错误的选项是: A. 电池工作时,是将太阳能转化为电能 B. 电池工作时,I离子在镀铂导电玻璃电极上放电 C. 电池中镀铂导电玻璃为正极 D. 电池的电解质溶液中I-和I 3-的浓度可不能减少 【解析】B选项错误,从示意图可看在外电路中电子由负极流向正极,也即镀铂电极做 正极,发生还原反应:13-+2e-=3I -; A选项正确,这是个太阳能电池,从装置示意图可看出是个原电池,最终是将光能转化为化学能,应为把上面四个反应加起来可知,化学物质并没 有减少;C正确,见B选项的解析;D正确,此太阳能电池中总的反应一部分实质确实是: 还原. 氧化 I「3I-的转化〔还有I 2+| 一二|「〕,另一部分确实是光敏有机物从激发态与基态的 相互转化而已,所有化学物质最终均不被损耗! 【答案】B 【命题意图】考查新型原电池,原电池的两电极反应式,电子流向与电流流向,太阳能 电池的工作原理,原电池的总反应式等,还考查考生变通能力和心理素养,能否适应生疏的 情境下应用所学知识解决新的咨询题等 【点评】此题立意专门好,然而考查过为单薄,而且取材不是最新的,在3月份江苏省 盐都市高三第二次调研考试化学试题第17题〔3〕咨询,与此题极为相似的模型,这对一些考生显得不公平!
初 三 化 学 实 验 与 探 究 1.某化学探究小组准备用碳酸钠溶液与石灰水反应来制取氢氧化钠。 (1)实验过程: ①把石灰水加人盛有碳酸钠溶液的烧杯中充分搅拌,发生反应的化学方程式: ②再通过 操作,得到无色滤液。 ③将无色滤液通过 操作,得到白色固体。 (2)猜想:得到的白色固体是纯氢氧化钠吗?三位同学分别作出以下猜想: 小李:是纯净的氢氧化钠! 小强:可能还含有碳酸钠! 小陈:也可能含有 。 2.某化学兴趣小组的同学对一瓶久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动。 提出问题:这瓶熟石灰粉末是否已经变质生成了CaCO 3? 进行猜想 :猜想一:熟石灰全部变成了CaCO 3。 猜想二:熟石灰部分变成了CaCO 3。 猜想一:熟石灰没有变质。 设计实验: 该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表 ①要证明猜想二成立,可参照上述实验方案进行探究,在步骤②中产生的实验现象是_____________________。 ②熟石灰变质是由于_____________________的缘故。在初中化学我们所学过的物质中还有_____________________(举一例)等具有这样的性质,因此像熟石灰这类物质在实验室应_____________________保存。 ③称取1.0g 上述熟石灰样品,加适量水使之充分溶解,搅拌过滤后,往滤液中滴入酚酞试液,同时加入溶质质量分数为10%的盐酸至溶液刚好变为无色,消耗盐酸溶液7.3g 。求样品中Ca(OH)2的质量分数(写出计算过程)。 3.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一。某化学兴趣小组的同学探究金属腐蚀的原因,设计如下实验: (1)如图,取一根约10cm 的光亮铁钉放在自来水中,观察A 、B 、C 三处的变化。几天后,他们会发现 处最先出现铁锈,大家结合书本知识知道,铁在空气中生锈实际是铁和 、 等物质相 互作用发生一系列复杂的化学反应的过程。
中考最新实验探究题 1.在“测定物质的密度”实验中,所用的托盘天平如图10所示。实验时,应先向_______调节平衡螺母(选填“左”或“右”),使天平横梁水平平衡。称量物体质量时,Array被测物体应放在天平的_______盘(选填“左”或“右”),然后通过 _________________________________使天平横梁再次回到水平位置平 图10 衡。 2.某同学做“研究电流与电阻关系”的实验,在连接电路时,电键应处于_______状态(选填“闭合”或“断开”)。实验时,该同学要保持______________________不变。 3.某小组同学在“研究光的折射规律”的实验中,按正确的方法安装和调节好实验装置。他们使光从空气斜射入水中,按表一中的入射角i依次进行了三次实验,并将相应的折射角r记录在表一中。然后他们使光从空气斜射入玻璃中,重复上述实验,并将数据记录在表二 中。为了进一步探究入射角i和折射角r之间的关系,他们进行适量的运算,将结果分别 记录在表一和表二的后四列中。 (1)分析比较实验序号___________________________________数据中的入射角i与折射角r变化关系及相关条件,可得出的初步结论是:光从空气斜射入其它介质,折射角随入射角的增大而增大。 (2)分析比较每一次实验数据中的入射角i与折射角r的大小关系及相关条件,可得出的初步结论是:___________________________________________。 (3)分析比较实验序号1与4(或2与5、3与6)数据中的入射角i与折射角r的关系及相关条件,可得出的初步结论是:__________________________________________________。 (4)请进一步综合分析比较表一、表二中经运算后得到的数据及相关条件,并归纳得出结论。
图像试题 (2011烟台毕业)19.下列四个图像能正确反映其对应实验操作的是 ①②③④ (A)①高温煅烧一定质量的石灰石 (B)②用等质量、等浓度的双氧水分别制取氧气 (C)③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液 (D)④某温度下,向一定量饱和硝酸钾溶液中加人硝酸钾晶体 (2011潍坊毕业)16.下图是对四个实验绘制的图像,其中实验结果与图像对应正确的是 A.某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体 B.将稀H2SO4滴入一定量的BaCl2溶液中 C.将一定质量的氯酸钾和二氧化锰放入试管中充分加热 D.向pH=13的NaOH溶液中加水稀释 (2011南宁)19.下列图象与对应实验完全吻合的是 A.①往一定量的盐酸中滴加NaOH溶液至过量 B.②将一定量的不饱和KNO3溶液恒温蒸发水 C.③向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液 D.④用两份等质量等溶质质量分数的过氧化氢溶液制取氧气(甲加少量MnO2) (2011遂宁)32.下列四个图象分别对应四种操作(或治疗)过程,其中图象能正确表示对
应操作(或治疗)的是 A B C D A .将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出 B .常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸充分反应 C .向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量 D .服用胃舒平[主要成分Al(OH)3]治疗胃酸过多 (2011绥化)13.下列图像能正确反映其对应关系的是( ) A.向一定量pH=3的硫酸溶液中不断加水稀释 B.向一定量的饱和石灰水中不断加入生石灰 C.向盛有相同质量的镁和氧化镁的烧杯中分别加入相同溶质质量分数的稀盐酸至过量 D.将一定量的木炭放在盛有氧气的密闭容器中加热至燃烧 (2011黑龙江龙东地区)14.下列图像能正确反映所对应叙述关系的是 ( ) A.向pH=3的溶液中不断加水 B.向锌粒中逐渐加入稀硫酸 C.向H 2SO 4和CuSO 4混合液中滴加NaOH 溶液 加水的量/g A 反应时间/s B NaOH 溶液质量/g C 反应时间/s D A B C D
2013年中考英语真题分类汇编—词汇运用 2013年杭州市中考英语试卷 南京市2013年初中毕业生学业考试 四、填空(共16小题;每小题1分,满分16分) A)根据括号中所给的汉语写出单词,使句子意思完整正确,并将答案填写在答题卡标号 为46-50的相应位置上。 1.The school library is _ (开放的) Monday through Friday, 9a.m to 6 p.m. 2.I often _ (买)gifts for my parents on their birthdays. 3.The children all _ (跳)with joy when they heard the good news. 4.Where are you going to put your _ (自行车)? It’s so crowded here. 5.Some teenagers don’t know how to _ (处理)with their personal problems and they often go to therapy. B) 根据句子意思,用括号中所给单词的适当形式填空,并将答案填写在答题卡标号为 51-56的相应位置上。 6.If you don’t tell me what the problem is, I can’t _ (help) you. 7.Miss Li is a kind teacher and she always talks to us _ (gentle). 8.The teacher told us that the gravity on Mars _ (be) only about three-eighth of that on Earth. 9.Mr Black has been in China for three years and now he is used to _ (eat) Chinese food. 10.The Eiffel Tower, a cultural icon of France, was completed at the end of the _ (nineteen) century. 11.It is worth _ (mention) that Nanjing has entered Top 10 Appealing Chinese Cities. 四、填空(共16小题;每小题1分,满分16分) A)根据括号中所给的汉语写出单词,使句子意思完整正确 46.open 47.buy 48.jumped 49. bike(s)/bicycle(s) 50.deal B) 根据句子意思,用括号中所给单词的适当形式填空 51.help 52.gently 53. is 54.eating 55. nineteenth/19th56. mentioning C) 根据对话内容,从下面方框中选择适当的单词或短语填空 57. What 58. thousands of 59. so 60. turning off 61. hopeless 2013年苏州市初中毕业暨升学考试试卷 四、词汇检测(共10小题;每小题1分,满分10分) 根据下列句子及所给汉语注释或通过上下文,在答题卡上标有题号的横线上,写出空缺处各单词的正确形式。每空只写一词。 41.The local clubs are making every ▲ (努力)to interest more young people. 42.John went out and ▲ (锁住)the door behind him.
初中化学实验探究题专题训练 一、气体的制取、干燥及装置连接 1、某校化学兴趣小组学习了气体的制取和收集后,对相关知识进行总结,请你一起参与,并完成下面题目内容: (1)写出下列仪器名称:a ;b .图3 (2)若用E装置收集氧气,则氧气应从口通入(填“c”或“d”). (3)装置B、C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是。也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程 式,若用此法来制取CO2,应选用的发生装置为,收集装置为. (4)实验室制取氧气有以下主要操作步骤:①加热②把药品装入试管后固定在铁架台上③检查装置的气密性④熄灭酒精灯⑤用排水取气法收集气体⑥从水槽中取出导管。正确的操作顺序是(写序号)。(5)若用F收集CO2,要测量生成的CO2气体的体积,其中在水面上放一层植物油目的是;植物油上方原有的空气对实验结果(填“有”或“无”)明显影响. 2、图3所示装置有多种用途。请回答下列问题: (1)洗气:除去CO2中的水蒸气,装置内应盛的物质是,气体应从装置的端通入。 (2)检验:证明CO中混有CO2,装置内应盛。 (3)贮气:若用排空气法收集H2,气体应从装置的端通入(填“A”或“B”,下同。) 若用排空气法收集O2,气体应从装置的端通入。 若用排水法收集H2,瓶内先装满水,气体从端通入。 若用排水法收集O2,瓶内先装满水,气体从端通入。 3、下图是实验室常用的装置。请据图回答: (1)写出仪器①的名称。收集某气体只能采用E装置,由此推测该气体具有的性质; (2)用高锰酸钾制取氧气的装置组合是(填序号),反应的化学方程式为; (3)实验室制得的CO2气体中常含有HCl和水蒸气。为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是(填选项)。A.a→b→c→d B.b→a→c→d C.c→d→a→b D.d→c→b→a 4、实验室用图所示装置制取纯净、干燥的氢气,并进行还原氧化铜的实验。 (1)装置B、C内所盛的液体分别是浓硫酸和氢氧化钠中的一种,则装置B内所盛液体是,装置C的作用是。 (2)为检验氢气还原氧化铜有水生成,装置E中所盛试剂是,反应后装置E中观察到的实验现象是。(3)为证实生成的气体中混有氯化氢气体,装置B应改盛溶液。 (4)氢气还原氧化铜的主要操作步骤有:①加热氧化铜②检验氢气纯度③停止加热④通入氢气⑤停止通入氢气。正确的操作顺序(序号)是。
中考化学实验探究题归类及解法 实验探究活动是新课标理念中的一种全新的学习方法,也是中考考查的重点和热点,但不少同学对于实验探究类试题,往往不知如何入手去解答。实验探究题中的许多内容都是平时学习(实验)或生活中司空见惯的,只是命题形式新颖,选择素材陌生度高,但基础知识或原型实验来源于教材的演示实验或学生实验。很多同学做题时联想不到,这就要求我们在平时学习和生活中要多想多问几个为什么?要注意从化学的视角去观察思考学习和生产生活中的各种问题,并能根据自己已有的化学知识和经验对问题做出有意义的猜想和假设,并设法用实验去检验验证它。在解答实验探究类试题时要①通读全题划出关键的语句,审清题意,明确要求;②回归教材确定知识点;③细心分析明确设计意图,灵活应用基础知识解决探究题中的问题(关键是分析题中的设计方案和实验装置图)。现从近年来各地中考试题中选取数题,进行简要的归类与评析。 根据探究题的内容可分为以下几种类型: 一、气体成分的探究 如人吸入和呼出气体成分探究、酒精和蜡烛等可燃物燃烧后产生气体成分探究、两种物质反应后产生气体成分探究、鱼瞟内气体成分探究等。涉及的知识点有空气、O2、N2、H2、CO、CO2等这些物质的制法及检验,以及它们与氧气、水、碱溶液等反应产生的特有现象。
例1.(07长春)请你阅读下列短文后,回答有关问题。 “二氧化碳本身没有毒性,但当空气中的二氧化碳超过正常含量时,会对人体产生有害影响,所以在人群密集的地方,应该注意通风换气,保持空气新鲜。” (1)根据上述短文,提出一个你想探究的问题:。 (2)对你的问题做出一个比较合理的猜想:。 (3)请自选用品设计实验验证你的猜想,并填写下表。
09年高考化学试题分类汇编——物质的量 1.(09年福建理综·8)设N A为阿伏伽德罗常数,下列叙述正确的是 A.24g镁的原子量最外层电子数为N A B.1L0.1mol·L-1乙酸溶液中H+数为0.1N A C.1mol甲烷分子所含质子数为10N A D.标准状况下,22.4L乙醇的分子数为N A 答案:C 2.(09年广东化学·6)设N A 代表阿伏加德罗常数(N A )的数值,下列说法正确的是A.1 mol 硫酸钾中阴离子所带电荷数为N A B.乙烯和环丙烷(C3H6 )组成的28g混合气体中含有3N A 个氢原子 C.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为N A D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1N A Fe3+ 答案:C 3.(09年广东理基·20)设N A代表阿伏加德罗常数(N A)的数值,下列说法正确的是A.22.4 L Cl2中含有N A个C12分子 B.1 L 0.1 mol·L-1 Na2SO4溶液中有0.1 N A个Na+ C.1 mol H2与1 mol C12反应生成N A个HCl分子 D.1 mol Ca变成Ca2+时失去的电子数为2N A 答案:D 4.(09年海南化学·8)下列叙述正确的是(用N A代表阿伏加德罗常数的值)A.2.4g金属镁变为镁离子时失去的电子数为0.1N A B.1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 C.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 N A D.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 答案:C 5.(09年江苏化学·4)用N A表示阿伏加德罗常数的值。下列叙述正确的是A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2N A B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2N A C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5N A
2017年中考物理实验探究题专题解析
中考物理实验探究题专题解析 一、实验探究内容及考查点 1.课本实验探究(带※为中考的重点,带※※为中考的必考点) 考查内容考查知识点 平均速度的测量刻度尺的使用;停表的读数;平均速度公式的运用 音调和频率、响度与振幅的关系音调与频率的关系;响度与振幅的关系 改变频率和振幅的方法(振动物体的长度和拨动的力度) 光的反射光的反射的内容 ※平面镜成像的特点平面镜成像的特点 等大蜡烛的意图(便于比较物体和像的大小) 透明玻璃板的原因(便于确定像的位置) 图纸信息的处理(测量各点到平面镜的距离;连接对应点观察连线与平面镜的关系) ※凸透镜成像的规律凸透镜成像特点及应用;对焦点、焦距、物距、像距理解 实像和虚像的区分(是否呈现在光屏上) 蜡烛、凸透镜和光屏的位置和高低(中间放置凸透镜;三者中心在同一高度) ※晶体的熔化和凝固晶体熔化和凝固图像和条件(温度不变,需要继续吸热/放热)熔点和凝固点 ※水的沸腾水沸腾的图像和条件(温度不变,需要继续吸热) 沸点和气压的关系(气压高,沸点高) ※物体质量和密度的测量密度的计算 天平的使用(放、移、调、称、读的要点) 量筒的使用 质量和体积测量顺序的处理(注意测量时液体的残留) 重力与质量的关 系 重力与质量的关系 ※滑动摩擦力的影响因素滑动摩擦力的影响因素;控制变量法的运用 匀速拉动物块运动(便于读数、拉力等于摩擦力) 牛顿第一定律牛顿第一定律;控制变量法;实验加理论推导的实验思路二力平衡的条件二力平衡的条件;控制变量法 ※压力作用效果的影响因素压力作用效果的影响因素 压力作用效果的呈现(观察物体的凹陷程度) 液体压强的特点压强计的使用(观察U形管两边液面的高度差) 控制变量法;液体压强的特点 浮力的影响因素浮力的影响因素;弹簧测力计的使用;浮力的求解 ※阿基米德原理阿基米德原理的内容;测力计的读数 浮力的求解(两次测力计的示数差) 实验的步骤(称小桶重力;空中称物重;水中称读数;称小桶和水的重力) 杠杆的平衡条件杠杆的平衡条件 力臂的读取(杠杆水平时读杠杆上的刻度) ※滑轮组的机械效率机械效率的理解 有用功和总功的求解(有用功——重力做的功;总功——拉力做的功)拉力与物体重力的关系(F=(G+G 动 )/n;n——动滑轮上绳子的段数)匀速拉动绳子(便于读出拉力的示数)
烃 1.(全国理综I·8)下列各组物质不属于 ...同分异构体的是D A.2,2-二甲基丙醇和2-甲基丁醇B.邻氯甲苯和对氯甲苯 C.2-甲基丁烷和戊烷D.甲基丙烯酸和甲酸丙酯 2.(全国理综Ⅱ·6)20北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是C A.分子中碳原子不在一条直线上B.光照下能够发生取代反应 C.比丁烷更易液化D.是石油分馏的一种产 3.(天津理综·7)二十世纪化学合成技术的发展对人类健康平和生活质量的提高做出了巨大贡献。下列各组物质全部由化学合成得到的是C A.玻璃纤维素青霉素B.尿素食盐聚乙烯 C.涤沦洗衣粉阿斯匹林D.石英橡胶磷化铟 4.(山东理综·10)下列由事实得出的结论错误的是D A.维勒用无机物合成了尿素,突破了无机物与有机物的界限 B.门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新C.C60是英国和美国化学键共同发现的,体现了国际科技合作的重要性 D.科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研究为主的学科 5.(山东理综·12)下列叙述正确的是B A.汽油、柴油和植物油都是碳氢化合物 B.乙醇可以被氧化为乙酸,二者都能发生酯化反应 C.甲烷、乙烯和苯在工业上都可通过石油分馏得到 D.含5个碳原子的有机物,每个分子中最多科形成4个C—C单键 6.(重庆理综·8)下列实验装置图正确的是B
7.(宁夏理综·8)在①丙烯②氯乙烯③苯④甲苯四种有机化合物中,分子内所有原子均在同一平面的是B A.①②B.②③C.③④D.②④ 8.(广东理基·22)保护环境已经成为人类的共识。人类应以可持续发展的方式使用资源, 以合理的方式对废物进行处理并循环使用。下列做法不利于 ...环境保护的是D A.发电场的煤见脱硫处理 B.将煤转化为水煤气作燃料 C.回收并合理处理聚乙烯塑料废物 D.电镀废液经中和后直接排放 9.(广东理基·28)下列关于有机物说法正确的是B A.乙醇、乙烷和乙酸都可以与钠反应生成氢气 B.75%(体积分数)的乙醇溶液常用于医疗消毒 C.苯和乙烯都可以使溴的四氯化碳溶液褪色 D.石油分馏可获得乙酸、苯及其衍生物 10.(广东理基·34)根据陈述的知识,类推得出的结论正确的是 A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O B.乙烯可使酸性高锰酸钾溶液褪色,则丙烯也可以使其褪色 C.CO2和SiO2 化学式相似,则CO2与SiO2的物理性质也相似
2013中考全国100份试卷分类汇编列方程解应用题(一元一次方程不等式) 1、(2013?资阳)在芦山地震抢险时,太平镇部分村庄需8组战士步行运送物资,要求每组分配的人数相同,若按每组人数比预定人数多分配1人,则总数会超过100人;若按每组人 <, 2、(2013?宜昌)地球正面临第六次生物大灭绝,据科学家预测,到2050年,目前的四分之一到一半的物种将会灭绝或濒临灭绝,2012年底,长江江豚数量仅剩约1000头,其数量年平均下降的百分率在13%﹣15%范围内,由此预测,2013年底剩下江豚的数量可能为()头.
3、(2013?呼和浩特)某次知识竞赛共有20道题,每一题答对得10分,答错或不答都扣5分,小明得分要超过90分,他至少要答对多少道题? , 4、(2013?黔西南州)义洁中学计划从荣威公司购买A、B两种型号的小黑板,经洽谈,购买一块A型小黑板比买一块B型小黑板多用20元.且购买5块A型小黑板和4块B型小黑板共需820元. (1)求购买一块A型小黑板、一块B型小黑板各需要多少元? (2)根据义洁中学实际情况,需从荣威公司购买A、B两种型号的小黑板共60块,要求购买A、B两种型号小黑板的总费用不超过5240元.并且购买A型小黑板的数量应大于购买A、B种型号小黑板总数量的.请你通过计算,求出义洁中学从荣威公司购买A、B两种型号的小黑板有哪几种方案?
5、(2013?莱芜)某学校将周三“阳光体育”项目定为跳绳活动,为此学校准备购置长、短两种跳绳若干.已知长跳绳的单价比短跳绳单价的两倍多4元,且购买2条长跳绳与购买5条短跳绳的费用相同. (1)两种跳绳的单价各是多少元? (2)若学校准备用不超过2000元的现金购买200条长、短跳绳,且短跳绳的条数不超过长跳绳的6倍,问学校有几种购买方案可供选择? 由题意得:. 解得: 由题意得: 解得:
实验探究题 1、某学校实验室的废液缸中收集了学生在实验室制取二氧化碳后残留的废液。小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题: 【提出问题】废液中的溶质是什麽物质? 【做出猜想】小红认为废液中的溶质只有CaCl 2。你认为还可能含有的物质是 HCl 。(填化学式)。 【查阅资料】CaCl 2溶液呈中性。 【实验与结论】(1)小红取少量残留废液和少量氯化钙溶液分别加入到两支试管中,并分别滴入无色酚酞试液作对比试验,结果两支试管中溶液均无色,于是小红认为自己的猜想是正确的。 (2)你认为小红的实验 不能 (填“能”或“不能”)证明他的猜想是正确的,理由是 酸性、中性物质都不能使酚酞溶液变色 。 (3)如果要证明你的猜想是正确的,你选择的试剂是 石蕊试剂 ,当加入该试剂时观察到的现象是 溶液显红色 。 【拓展应用】(1)若实验证明你的猜想是正确的,想要处理废液只得到CaCl 2溶液,应向废液中加入过量的 碳酸钙 ,反应完全后过滤。 (2)通过以上探究你认为实验室的废液未经处理直接导入下水道,可能造成的危害是 腐蚀管道,污染环境等等 。(写一条) 2、某学习小组在探究CO 2与NaOH 溶液反应的实验中,先用铝制易拉罐收集满一罐CO 2气体,然后迅速向其中加入一定量的NaOH 浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计)。 【提出问题】易拉罐为什么先瘪后鼓? 【分析猜想】易拉罐开始时变瘪的原因 是 O H CO Na CO NaOH 23222+=+ (用化学方程式表示),易拉罐重新鼓起的原因是易拉罐中又生成了气体A ,其成分极有可能是CO 2或 H 2。 【查阅资料】①Na 2CO 3具有较强的热稳定性,只有在高温条件下才会分解; ②铝单质比较容易被酸、碱腐蚀。 【设计方案并进行实验】为了检验铝制易拉罐中重新生成的气体成分,小组又进行如下实验,并记录了相应的实验现象:
杭州各区中考化学实验探究题 30.(8分)铁粉在潮湿的空气中容易生锈。现 有m 1g生锈的铁粉样品,某兴趣小组同学 按如图所示装置进行实验,测定该样品中氧 化铁的质量分数(CO气体极难溶于水,铁 锈按氧化铁处理)。 (1)装置甲中发生反应的化学方程式 是。 (2)某同学欲通过乙装置反应前后的质量变化,测定该样品中氧化铁的质量分数。乙中的最佳试剂是。(选填序号)。 ①水②稀盐酸③氢氧化钠浓溶液④澄清石灰水 (3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:实验开始时,排尽装置中的空气,防止加热时发生爆炸;停止加热后,防止甲中生成物被氧化,防止乙中的溶液倒吸入甲中等。请你再写出一点CO气体在上述实验中起到的作用。 (4)完全反应后,该同学称得铁粉的质量为m2g,同时测得装置乙增重m3g,则铁粉样品中氧化铁的质量分数为。 31.(8分)物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却看不到明显的现象。 以下是同学们在学习过程中,为证明某些反应确实发生而从不同的角度设计的实验方案。 (1)为研究二氧化碳与氢氧化钠是否发生反应,甲小组的同学设计的下列四种方案,你认为不可行的是。(选填字母编号)。 (2)为证明NaOH溶液与H2SO4溶液发生了中和反应,乙小组同学和丙小组同学分别设计了两个不同的实验方案。 ①乙小组同学设计如图所示的实验证明二者之间确实发生了反应,所用的试剂有NaOH溶液、 H 2SO4溶液、CuSO4溶液。乙小组同学选择的试剂A的名称 是(并用“少量”、“足量”等指明试 剂的用量);CuSO4溶液与NaOH溶液的化学方程式 为。
②丙小组同学设计的实验方案是:先用pH试纸测定NaOH溶液的pH,再滴加H2SO4溶液,并不 断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与H2SO4溶液发生了化学反应。请简述该实验方案中强调“测得pH小于7”的理由 是。 33.(10分)天平两端托盘上的烧杯内各培养一株植物,烧杯中是全营养液。调节天平两边平衡,此时游码的位置恰好与支点正对。请回答下列问题: (1)全营养液中添加了很多营养物质,下列物质中,所含植物生长需要的主要营养元素种类最多的是。(选填字母编号) A.硝酸钠B.磷酸氢二钙C.硝酸钾D.硫酸镁 (选 (4)某同学移动游码将上述倾斜了的天平重新调节平衡,因横梁标尺上的读数无法看清,该同学测出了游码移动的距离为s,若游码的质量为m,天平的臂长为L,则光照后天平两边的质量差为。 30.(8分)泡菜,佐餐的小菜,烹饪的调料。自制泡菜,原料随意挑,卫生有保障,原料配比随意。但也有不尽人意之处,即保存时间稍长,味道变酸,刺激肠胃。那么酸味何来,可有解法? 【原料准备】新鲜的红辣椒、大蒜头、生姜、大白菜。 【制作过程】将原料与适量的食盐、白糖等混合均匀,装入泡菜坛,盖上坛盖,再向荷口装水至一半高度,这一过程叫腌制。 【提出问题】腌好的泡菜时间一长,味道就逐渐变酸。这酸味哪来?怎么控制? 【建立猜想】科学探究小组的同学经过分析判断, 认为该酸味物质可能是碳酸。理由为 坛内蔬菜是以C和H元素为主的化合 物,与久放菜窖的白菜一样,在密封 的有限空间里CO2浓度大。生物学知 识告诉我们,通过盐、糖腌制的蔬菜 细胞会失水。因此,坛内会出现少量 的液体(主要成分是H2O)。 【评价检测】 (1)坛顶荷口内装水至一半高度的目的是。 (2)请设计证明在做泡菜过程中,坛内CO2浓度大的实验(用 图示或文字表达均可):。 (3)通过探究,你觉得可以如何控制酸味。 (4)有酸味的物质不一定属酸性物质。要测定物质酸性的 强弱,最常用、最简单的方法是使用pH试纸,正确的 测定方法是,将试纸显示的颜色与标准比色卡对照。
化学高考题分类目录 A 单元 常用化学计量 A1 阿伏伽德罗常数和物质的量 5. [2014·四川卷] 设N A 为阿伏伽德罗常数的值。下列说法正确的是( ) A .高温下,0.2 mol Fe 与足量水蒸气反应,生成的H 2分子数目为0.3 N A B .室温下,1 L pH =13的NaOH 溶液中,由水电离的OH -数目为0.1N A C .氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2N A D .5NH 4NO 3=====△2HNO 3+4N 2↑+9H 2O 反应中,生成28 g N 2时,转移的电子数目为 3.75N A 5.D [解析] 根据3Fe +4H 2O(g)=====高温Fe 3O 4+4H 2,则0.2 mol Fe 参与反应生成415 mol H 2 ,A 项错误;pH =13的NaOH 溶液中,溶液中c (OH -)=0.1 mol/L ,c (H +)=K W c (OH -) =10-13 mol/L ,则水电离出来c (OH -)=c (H +)=10 -13 mol/L ,B 项错误;氢氧燃料电池正极的电极反应式为O 2 + 4H + + 4e -===2H 2O ,则1 mol O 2被消耗,电路中有4N A 的电子通过,C 项错误;根据化学方程式,-3价的氮元素升高到0价,失去3个电子。+5价的氮元素降低到0价,得到5个电子,即每生成4 mol 氮气,反应中转移电子的物质的量为15 mol ,则生成28 g N 2(即1 mol 氮气),转移电子的物质的量是15 mol÷4=3.75 mol ,D 项正确。 7. [2014·全国卷] N A 表示阿伏伽德罗常数,下列叙述正确的是( ) A .1 mol FeI 2与足量氯气反应时转移的电子数为2N A B .2 L 0.5 mol·L -1硫酸钾溶液中阴离子所带电荷数为N A C .1 mol Na 2O 2固体中含离子总数为4N A D .丙烯和环丙烷组成的42 g 混合气体中氢原子的个数为6N A 7.D [解析] 1 mol FeI 2与足量Cl 2反应时,Fe 2+被氧化为Fe 3+,I - 被氧化为I 2,转移电子3N A ,A 项错误;2 L0.5 mol·L -1的硫酸钾溶液中n (SO 2-4)=1 mol ,所带电荷数为2N A ,B 项错误;Na 2O 2由Na +和O 2-2(过氧根离子)构成,1 mol Na 2O 2中的离子总数为3N A ,C 项错误;丙烯和环丙烷为同分异构体,其分子式均为C 3H 6,最简式为CH 2,42 g 混合气中的氢原子个数为42 g 14 g·mol -1 ×2N A =6N A ,D 项正确。 27. [2014·安徽卷] LiPF 6是锂离子电池中广泛应用的电解质。某工厂用LiF 、PCl 5为原
2012北京各区初三一模化学实验探究题 东城32.(6分)老师用如图所示装置为同学们做了一个实验。A装置集气瓶中装有体积比约为1:1的氮气和气体a的混合气体,注射器中装有足量的无色溶液b;B装置中盛有少量紫色石蕊溶液;C装置中盛有适量生锈的铁钉;D装置中盛有足量的稀硫酸。 (1)关闭活塞K1、K2,将注射器中的溶液b挤入瓶中,打开活塞K1,看到B中溶液进入A中后溶液变为蓝色,B中长导管脱离液面。 请回答: ①若a气体是二氧化碳,则b 是溶液。 ②若b是水,则气体a具有的性质有。 (2)保持K1开启状态,并打开K2,一段时间后 关闭K2,整个过程中,观察到D中的现象是 ,C装置中反应的化学方程式是。 33.(8分)(1)某实验小组在研究二氧化碳的性质时,根据下图进行实验。 请回答:A中的现象是______,B中反应的化学方程式是______。 (2)该小组利用对比的方法研究二氧化硫的性质, 进行如下探究。 【提出问题】二氧化硫与二氧化碳均属于非金属氧 化物,是否具有相似的化学性质呢? 【查阅资料】二氧化硫具有漂白性,其原因是二氧 化硫与某些有色物质(如品红溶液)反应生成不稳 定的无色物质,实验室常用红色的品红溶液检验二 氧化硫的存在。 【实验探究】实验装置如右图所示。 ①装置C中紫色石蕊溶液变红,是由于二 氧化硫与水反应生成了亚硫酸(H2SO3);装 置D中澄清石灰水变浑浊,该反应的化学方 程式是______。 ②装置E的试管中溶液变无色,取该溶液 加热,溶液又变为红色,其原因是______。 ③此装置有一个明显的不足之处是 ______。 ④活性炭也能使品红溶液褪色,其褪色原理与二氧化硫 使品红溶液褪色的原理不相同,其理由是______。 【反思提高】某同学将二氧化硫通入到紫色的酸性高锰酸钾溶液中,观察到溶液由紫色变为无色,由此他得出的结论是:二氧化硫能将酸性高锰酸钾溶液漂白。请你设计实验证明此结论是否正确(要求写出操作、现象、结论):______。 二氧化硫与二氧化碳有相似的化学性质,但二氧化硫还具有某些特殊的化学性质。