
第十二章陶瓷的结构和特性
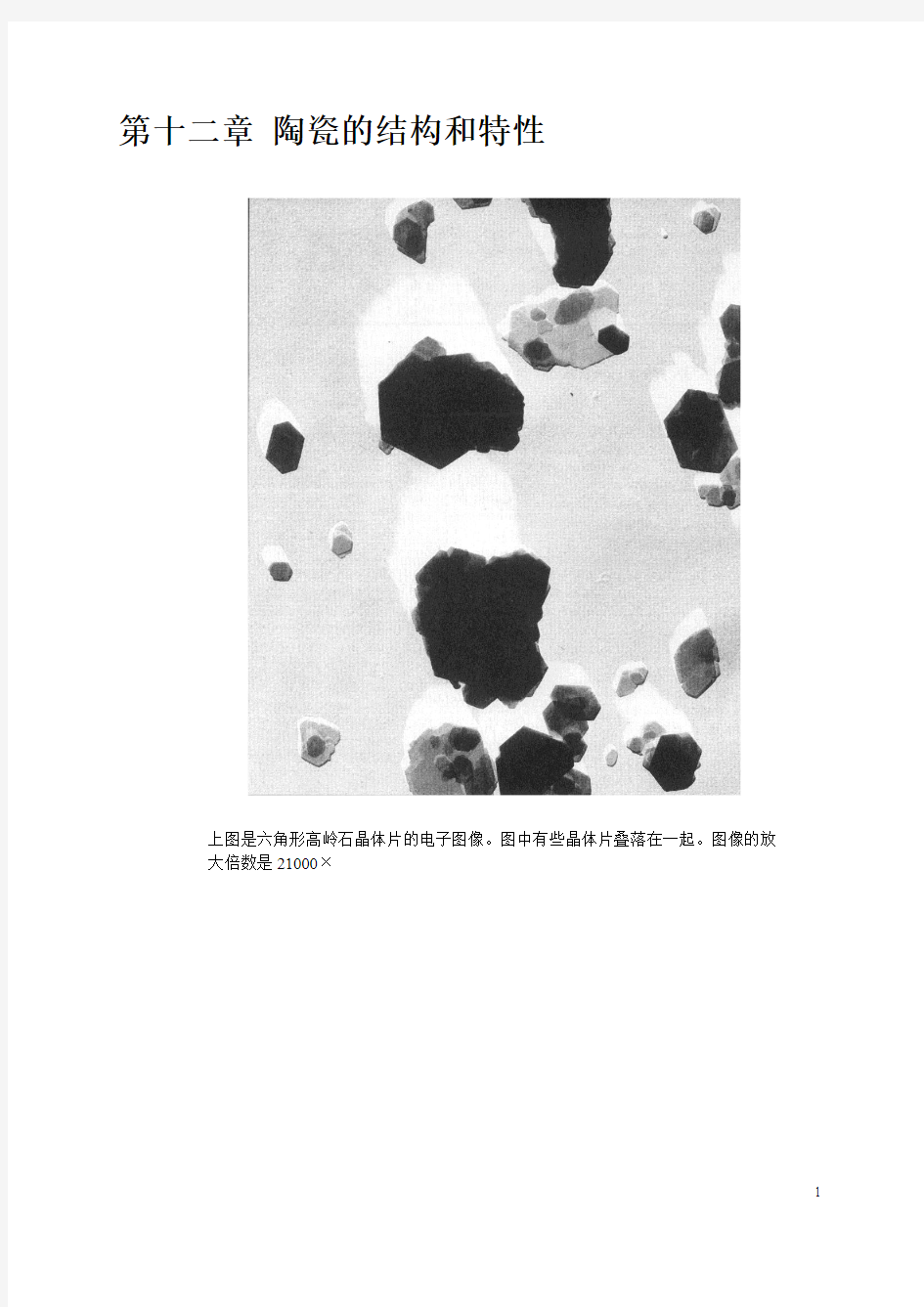
上图是六角形高岭石晶体片的电子图像。图中有些晶体片叠落在一起。图像的放
大倍数是21000×
为什么学习陶瓷的结构与特性?
陶瓷的某些特性可以通过其结构来解释。例如,(a)无机玻璃材料的透光性起因与其结构非晶性;(b) 陶土的水塑性(即水的加入量与塑性变化)与水分子和陶土结构的相互作用相联系;(c) 一些陶瓷材料的永磁性和铁磁行为可用其晶体结构来解释。
学习目的
认真学习了本章内容后,你能够解答下列问题:
1.用图或文字描述氯化钠、氯化铯、闪锌矿、金刚石、氟石和钙钛矿晶体的结构基元。同样地用图或文字描述石墨和石英玻璃的原子结构的相似性。
2.已知陶瓷复合材料的化学式,以及构成组元的离子半径,确定其晶体结构。
3.指出并描述在陶瓷复合材料中发现的八种不同的离子点缺陷。
4.简短解释为什么在完全相同的陶瓷材料试样中,断裂强度可以存在很大差异。
5.计算三点加载弯曲至断裂的陶瓷棒的抗弯强度。
6.利用滑移的基本概念解释为什么晶体陶瓷材料通常很脆。
12.1 前言
在本书第一章,我们曾对陶瓷材料进行了简单的讨论。指出:陶瓷材料是无机非金属材料。绝大多数陶瓷是金属元素和非金属元素组成的化合物,其原子间的键合或者完全是离子键,或者主要是离子键,同时具有一定共价键特征。陶瓷(Ceramic)来源于希腊词(Keramikos),它的原意是“烧结材料”,说明这类材料的理想特性通常是通过高温热处理或者叫高温烧结得到。
直到最近五十年左右,我们才对陶瓷材料中最重要的一类材料命名为“传统陶瓷材料”,其主要原材料是陶土。这类传统陶瓷材料有陶器,瓷器,砖瓦,瓷砖以及玻璃和高温陶瓷。此后,在对于这类材料的基本特征的理解以及与其独特特性相关的现象的理解方面取得了很大的进展,开始了陶瓷材料新的时代,陶瓷这一术语有了更为广泛的含义。不论从那一方面来说,这类材料对我们的生活有着巨大的影响;电子、计算机、通讯、宇航以及其它许多工业都有赖于这类材料的应用。
这一章主要讨论陶瓷材料的晶体结构类型、原子点缺陷类型、和力学特性。下一章将讨论这类材料的应用和加工技术。
陶瓷结构
陶瓷通常由两种或者两种以上的元素合成,因此其结构与金属相比一般要复杂的多,其原子键合可以从完全离子键到完全共价键。许多陶瓷同时表现出两种键合类型,离子键特征的程度依赖于原子的电负性。表12.1列出了几种普通陶瓷材料的离子特征的百分比,这一百分比是通过公式2.10和表2.7的电负性计算出来的。
12.2晶体结构
对于键合主要是离子键的陶瓷材料,其晶体结构可以看作是由带电的离子而非原子构成的。金属离子或阳离子带正电,因为它们将价电子贡献给了带负电荷的非金属离子或阴离子。
表12.1 几种陶瓷材料原子键合中,离子特征所占百分比
材料 离子键特征百分比
CaF 2 89
MgO 73
NaCl 67
Al 2O 3 63
SiO 2 51
Si 3N 4 30
ZnS 18
SiC 12
在晶体陶瓷材料中组元离子的两种特征会影响晶体结构:一是组元离子所带电荷的多少;二是阳离子和阴离子的相对尺寸大小。针对第一种特征,晶体必须是电中性。也就是说,全部阳离子带的正电荷一定要由阴离子带的等量负电荷进行平衡。化合物的化学式就表明了阳离子和阴离子的比例,或者说达到电荷平衡时化合物的组分。例如,在氟化钙中,每一个钙离子有两个正电荷(Ca +2),每一个氟离子有一个负电荷(F -),因此每一个钙离子必须与两个氟离子相结合,反映在化学式上就是CaF 2。
第二种特征涉及到阳离子和阴离子的大小或者说离子半径r C 和r A 。因为金属原子离子化以后失去电子,因此阳离子通常比阴离子小,比值A C r r 小于1 。每个阳离子希望有尽可能多的最近邻阴离子,阴离子也希望有尽可能多的最近邻阳离子。
当阳离子与所有的最近邻阴离子都保持接触时,如图12.1所示,陶瓷晶体结构达到稳定状态。相关数(即与阳离子最近邻的阴离子数)与阳离子和阴离子的半径比相关。对某个特定的相关数,为了保证阳离子和阴离子相互接触,阳离子与阴离子的半径比A C r r 有一个临界最小值(如图12.1)这一最小比值由纯几何学决定(见例题12.1)。
稳定 稳定 不稳定
表12.2列出了各种A C r r 比值下的相关数和最近邻几何关系。当比值A C r r 小在0.155到0.225之间,阳离子的相关数为3,小于0.155时,非常小的阳离子只能以直线排列方式与两个阴离子键合在一起。如果A C r r 的比值这意味着每一个阳离子由三个成平面等边三角形的阴离子包围,阳离子位于三角形中心。A C r r 的比值在0.225到0.414之间,阳离子相关数为4,阳离子位于四面体中心,阴离子占据四个角位。A C r r 的比值在0.414到0.732之间,阳离子可以被认为占据八面体体心位,周围有六个占据角位的阴离子,如表12.2所示。A C r r 的比值在0.732到1.0之间,相关数为8,阴 图12.1 稳定和不稳定的阴-阳离子相
关数组态。空心圆代表阴离子,实心
圆代表阳离子。
离子占据立方体的八个角位,阳离子占据体心位置。如果A C r r 的比值大于1,相关数是12。陶瓷材料中最常见的相关数是4,6,和8。表12.3给出了陶瓷材料中最
常见的几种阳离子和阴离子的离子半径。
表12.3 几种阳离子和阴离子的离子半径(相关数为6)
阳离子 离子半径 nm 阴离子 离子半径 nm
Al 3+ Ba 2+ Ca 2+ Cs + Fe 2+ Fe 3+ K + Mg 2+ Mn 2+ Na + Ni 2+ Si 4+ Ti 4+ 0.053 0.136 0.100 0.170 0.077 0.069 0.138 0.072
0.067
0.102
0.069
0.040
0.061
Br - Cl - F -
I -
O 2-
S 2- 0.196
0.181
0.133 0.220 0.140
0.184
表12.2 不同阳-阴离子半径比值的相关数和几何
相关数
阳离子-阴离子半径比值 相关几何
例题12.1
证明:当相关数为3时,阳离子与阴离子半径比值最小为0.155。
解答:
对这一相关数,当阳离子半径很小时,三个阴离子
形成等边三角形,如左图,三角形ABC ,四个离子的
中心在同一个平面上。因此问题简化为相对比较简单
的三角几何问题。由直角三角形APO 可以很清楚看到,
此三角形的边长与阳离子和阴离子半径r C 和 r A 有关。
A r AP =
C A r r AO += 边长比值AO AP 是角α的函数,
α=cos /AO AP
由于AO 平分60?角BAC ,所以α的大小为30?,因此我们有,
2
330cos ==+=o C A A r r r AO AP 求解上述等式,可以得到阳离子-阴离子半径比为,
155.02
32/31=-=A C r r AX 型晶体结构
一些常见的陶瓷材料具有相同数目的阳离子和阴离子,我们把这类材料称为AX 型化合物,其中A 代表阳离子,X 代表阴离子。AX 型化合物可以有几种不同的晶体结构,每一种结构的名称来源于具有这种特定结构的一种常见材料。
岩盐结构
在AX 型化合物中可能最常见的晶体结构就是氯化钠或岩盐型结构了。在这种结构中阳离子和阴离子的相关数都是6,因此阳离子和阴离子的半径比大约在0.414到0.732之间。这种晶体结构的
图12.2 岩盐结构或氯化钠晶体结构的结构基元
基元(见图12.2)由FCC 方式排列的阴离子,加上占据在体心位和和十二个立方边中心位的阳离子构成。面心排列的阳离子构成另一个等价的晶体结构。因此岩盐结构被认为是两个FCC 结构相互贯通而成,一个由阳离子形成,一个由阴离子形成。具有这种晶体结构的陶瓷材料有NaCl 、MgO 、MnS 、LiF 和FeO 。
氯化铯结构
图12.3是氯化铯晶体的结构基元示意图。对阳离子和阴离子而言,相关数都是8,阴离子占据立方体的角位,阳离子占据体心位。阳离子和阴离子相互交换得到相同的晶体结构。这种晶体结构不是体心立方(BCC )结构,因为结构基元中包含了两种不同的离子。
闪锌矿结构
第三种AX 型结构,离子相关数为4,所有的离子都是四面体相连,被称为闪锌矿(zinc blende or sphalerite) 结构---硫化锌的矿物学名称。图12.4是其结构基元示意图。在立方结构中,所有的角位和面心位都由S 原子占据,Zn 原子填充内部四面体位置。将S 和Zn 交换位置得到等价结构。因此每个Zn 原子与四个S 原子成键,同时每个S 原子与四个Zn 原子成键。具有这种晶体结构的化合物通常原子间键合是高度共价键。这类化合物有ZnS 、ZnTe 和SiC 。
A m X p 型晶体结构
图12.3 氯化铯晶体的结构基元
图12.4 闪锌矿ZnS 的结构基元
如果阳离子和阴离子所带电荷不相同,化合物具有A m X p 形式化学式,这里m 和p ≠1。例如AX 2,一类在氟化物中最常见的晶体结构。CaF 2的离子半径比A C r r 大约是0.8,根据表12.2,相关数为8。钙离子占据立方体的体心位,氟离子占据立方体的角位。化学式表明,钙离子的数目是氟离子的半数,也就是说氟化钙的结构与氯化铯结构相似,但是只有半数的体心位被钙离子占据,基元由八个立方体组成,如图12.5所示。具有这种晶体结构的其他化合物还有:UO 2、PuO 2和ThO 2。
A m
B n X p 型晶体结构
陶瓷化合物也可以具有一种以上阳离子,对于具有两种阳离子的化合物,阳离子标为A 和B ,其化学式可以写为A m B n X p 。钛酸钡(BaTiO3)具有Ba 2+和Ti 4+两种阳离子,属于这一类化合物。这类材料具有钙钛矿晶体结构,其电力学特性十分有趣(这将在以后讨论)。当温度高于120?C (248?F )时,晶体结构为立方体,基元组织见图12.6;Ba 2+离子占据立方体的八个角位,单个Ti 4+离子占据体
心位,O -2离子占据六个面心位置。
表12.4用阴阳离子比和相关数的形式总结了岩盐结构、氯化铯结构、闪锌矿结构、氟化物结构和钙钛矿结构,而且对每一种结构给出了一个例子。当然陶瓷也可能具有其他许多类型晶体结构。
表12.4 陶瓷的基本晶体结构小结
结构名称 结构类型 阴离子组织 相 关 数 阳离子 阴离子
典型材料
图12.5 CaF 2 晶体结构的结构基元
图12.6 钙钛矿晶体结构基元
岩盐(NaCl) AX FCC 6 6 NaCl,MgO,
FeO
氯化铯AX SC 8 8 CsCl
闪锌矿AX FCC 4 4 ZnS,SiO
氟化物AX2SC 8 4 CaF2,UO2,ThO2
钙钛矿ABX3FCC 12(A)
6(B) 6 BaTiO3,SrZrO3,
SrSnO3
尖晶石AB2X4FCC 4(A)
6(B) 4 MgAl2O4,
FeAl2O4
来源:W.D.Kingery, H.K.Bowen, and D.R.Uhlmann, Introduction to Ceramics, 2nd edition, copyright 1976 by John Wiley & Sons, New York.
阴离子密堆的晶体结构
在3.12我们曾经讨论过,对金属而言,密排原子面的相互堆叠构成了FCC和HCP晶体结构。类似的,某些陶瓷晶体结构也可以被认为是密堆离子面以及基元的堆叠。通常,密排面由尺寸较大的阴离子构成。当这些密排面相互堆叠时,它们中间就产生了可以被阳离子占据的小的间隙位置。这些间隙位置以两种形式存在,如图12.7所示。一种间隙位置由四个原子(三个原子属于同一个晶面,另一个原子在相邻晶面)包围构成,在图中标为T,称为四面体位置,因为四个包围原子的球心的联线构成四面体;另一种类型在图12.7中标为O,包含六个离子球,每三个在一个平面,因为这六个离子球心的联线构成八面体,所以这一间隙位置被称为八面体位置。所以,填充四面体和八面体位置的阳离子的相关数分别为4和6。而且,对每一个阴离子而言,存在一个八面体、两个四面体位置。
这种类型的陶瓷晶体结构与两个因素有关;1. 密排阴离子面的堆叠(FCC和HCP排列都有可能,也就是说ABCABC…排列和ABABAB…排列都有可能);2. 阳离子填充间隙位置的方式。例如,对岩盐晶体结构,基元具有立方对称性,每个阳离子(Na+)有六个最近邻Cl-离子(见图12.2),即体
心位的Na+有六个占据面心位的Cl-最近邻。晶体结构具有立方对称性,可以认为是密排阴离子面以FCC形式堆垛,所有的面都是{111}面。阳离子因为有六个阴离子最近邻,占据八面体位置。而且因
为每一个阴离子只有一个八面体位置,所有的八面体位置都被占据了,因此阳离子和阴离子的比率是1:1。这种晶体结构,基元和密排阴离子面的堆叠方式的关系如图12.8所示。
图12.7密排阴离子面的堆垛。堆垛面之间四面体和八面体位置分别标记为T和O。
其它陶瓷晶体结构,如闪锌矿和钙钛矿,也可以用的方式来处理。尖晶石结构具有A m B n X p 形式,这种形式结构是在铝酸镁或称尖晶石(MgAl 2 O 4)中发现的。在这种结构中,O -2构成FCC 晶格,Mg 2+离子填充四面体位置,Al 3+离子占据八面体位置。磁性陶瓷或者铁氧体具有稍微变型的尖晶石结构,其磁特性受四面体和八面体位置占据情况影响(见20.5节)。
例题12.2
基于离子半径,预测FeO 的晶体结构。
解:首先,FeO 是一种AX 型化合物。其次,由表12.3可知阳离子和阴离子半径比为:
550.0140.0077.022==-+
nm
nm r r O F e 这一比值在0.414和0.732之间,而且,由表13.2可知Fe 2+离子的相关数为6。既然阳离子和阴离子数目相同, 可以预测其结构一定是岩盐结构。岩盐结构具有AX 结构形式,相关数为6,见表12.4。 陶瓷密度计算
类似于3.5对金属的讨论,晶体陶瓷材料的理论密度可以通过基元的数据进行计算。在这种情形下,密度ρ可以用3.5式的改进形式来决定。 A C A C N V A A n ∑∑+=ρ)
(' (12.1)
其中,
n ' = 基元中化学式单位1的数目
∑A C = 化学式单位中阳离子的原子重量之和
∑A A = 化学式单位中阴离子的原子重量之和
V C = 基元体积
N A = 阿伏伽德罗常数(Avogadro’s number ),6.023×1023化学单位/摩尔
例题13.3
利用晶体结构知识,计算氯化钠的理论密度,并与测量密度进行比较。
解:利用公式12.1可以计算理论密度,其中,n '基元中NaCl 单位的数目为4,这是因为钠离子和氯离子都构成FCC 晶格结构。而且,
∑==mol
g A A Na C 99.22 mol
g A A Cl A 45.35==∑ 由于基元是立方体,V C = a 3, a 是基元的边长。对下图所示面心立方基元,
r Na +和r Cl -分别是钠离子和氯离子的离子半径,由表12.3可知分别是0.102和0.181nm 。 化学式单元,即化学式中包含的全部离子。例如,对BaTiO 3,一个化学式1
Na + Cl -
因此,
33)22(-++==Cl Na C r r a V
323377314.2)10*023.6()]10*181.0(2)10*102.0(2[)45.3599.22(4)22()(cm g N r r A A n A
Cl Na Cl Na =++=++'=---+ρ
这个结果与实验值2.16 g/cm 3相比非常接近。
12.3 硅酸盐陶瓷
硅酸盐是一类主要由硅和氧合成的材料。硅和氧是地表组织中储量最丰富的两种元素。土壤、岩石、陶土、和沙土都属于硅酸盐类材料。与用基元描述这类材料的晶体结构特征相比,用硅酸盐离子(SiO 44-四面体)的排列来描述更方便,见图12.9。每一个硅原子与四个占据四面体角位的氧离子成键,硅离子占据中心位置。由于这是硅酸盐的基本单元,因此经常被当作带负电的实体来处理。 通常人们认为硅酸盐不是离子晶体,因为在Si-O 键合中,共价键特征很明显(见表12.1),键合相对较强,具有方向性。除了Si-O 键合的特征外,每一个四面体SiO 44-携带有4个负电荷,因为四个氧原子中的每一个都需要一个额外电子才能达到电子结构平衡。四面体SiO 44-在一维、二维和-++=Cl Na r r a 22
三维的不同组合方式构成不同的硅酸盐结构。
硅石
从化学上讲,最简单的硅酸盐材料是二氧化硅,即硅石 (SiO 2)。从结构上讲,硅石具有三维网状结构,四面体角位的每一个氧原子都被相邻的四面体共享。因此,整个材料处于电中性,所有的
原子具有稳定的电子结构。在这种情况下,Si 原子与O 的原子比为1:2,如化学式所示。
如果这些四面体以某种规则的或有序的方式排列,就形成了晶体结构。硅石有三种主要的多态晶体,石英、方石英(图12.10)、鳞石英。它们的结构相对比较复杂,而且比较开放,也就是说原子不是密堆在一起。因此这种结构的晶体硅石具有比较低的密度。例如,室温下石英密度只有2.65 g/cm 3。Si-O 原子键合的强度可以通过高的融化温度(1710?C, 3110?F )来反映。
硅石玻璃
二氧化硅也可以以非晶态固体或称玻璃存在,其中原子有很高的无序度,具有液体的特征,这样一种材料被称为硅石玻璃或熔融石英。与晶体硅石相同之处在于硅石玻璃仍以SiO 44-四面体为基本单位,不同之处在于硅石玻璃具有很高的无序度。晶态和非晶态硅石的结构比较见图3.18。其它氧化物,如B 2O 3和GeO 2也可以形成玻璃结构以及类似图12.9所示的多面体氧结构。这类材料包括SiO 2被称为网络构造者。
通常用于容器、玻璃窗等的无机玻璃是填加了其它氧化物如CaO 和Na 2O 的硅石玻璃。这些氧化物不构成多面体网络,但其阳离子存在于SiO 44-四面体网络内并改造SiO 44-四面体网络。因此这类氧化物填加剂被称为网络改造者。例如,图12.11是钠硅石玻璃的结构示意图。还有一些其它的氧化物,如TiO 2和Al 2O 3,不是网络构造者,但是可以取代硅,成为网络的一部分并稳定网络,这类
氧化物叫中介物。从实际效果看,这类改造剂和中介物的加入降低了玻璃的熔化点和粘性,使得玻图12.9 硅-氧(SiO 44-)四
面体结构。
璃容易在更低温度成型(见13.8节)。
硅酸盐
在各种硅酸盐矿物质中,随着SiO44-四面体角位的一个、两个、三个氧原子被其它四面体共享,会形成一些非常复杂的结构。图12.12给出了其中五种结构的示意图。这五种结构的化学式分别是:SiO44-、Si2O76-、Si3O96-、Si6O1812-、(SiO3)n2n-。单链结构也是可能的,如图12.12e,带正电的阳离子如Ca2+ ,Mg2+ ,Al3+有两个作用:一是补偿SiO44-四面体基元所带的负电荷,使材料达到电中性;二是阳离子与SiO44-四面体元形成离子键,结合在一起。
简单硅酸盐
在硅酸盐中,结构最简单的是包含独立的SiO44-四面体的结构(见图12.12a)。例如,镁橄榄石(Mg2SiO4),一个四面体与两个Mg2+离子相结合,每个Mg2+离子周围有六个氧最近邻。
当两个四面体共享同一个氧原子时,就形成了Si2O76-离子,如图12.12b所示。钙镁黄长石(Ca2MgSi2O7)是一种具有此种结构的矿物质,每一个Si2O76-单元与两个Ca2+离子和一个Mg2+离子
成键,结合在一起。
层状硅酸盐
每一个四面体中的三个氧离子与其他四面体共享可以获得二维层状或片状结构(见图12.13)。对于这种结构,重复单元的化学式可以写为(Si 2O 5)2-,负电荷由突出纸面的未成键的氧原子提供,通常,这些未成键的氧原子与另一个极化的带多余阳离子的片状结构中的阳离子成键,从而达到电中性。这类材料称为片状或层状硅酸盐,它们的基本结构具有陶土和其它矿物质的特征。高岭石是最常见的陶土矿物质之一,具有比较简单的双层硅酸盐片状结构,高岭石的化学式为Al 2(Si 2O 5)(OH)4,其中硅石四面体层表示为(SiO 5)2-,所带负电荷通过相邻的Al 2(OH)42+层中和从而达到电中性。图12.14是这种结构单层的直视图,此图从竖直方向上很好地描述了离子占位,而且标出了高岭石的不同双层。中间阴离子面由来自(Si 2O 5)2-层的O 2-离子和来自Al 2(OH)42+层的OH -离子构成。在这种双层片内键合很强,介于离子键和共价键之间。相邻片间通过范德瓦尔斯力连接,键合较弱。
高岭石晶体是许多的这种双层片相互平行堆剁,形成直径小于1 m 的近六角形的薄片。本书383页有一张高放大倍数的高岭石晶体的电镜照片,由照片可见六角形晶体片,其中有些晶体片相互堆剁在一起。
这类硅酸盐片状结构并不限于陶土。其它矿物质,如滑石岩[Mg 3(Si 2O 5)2(OH)2]和云母(例如,钾云图12.12 五种硅酸盐离子由
SiO 44-四面体元形成结构示意图。
图12.13具有重复单元的化学式为(Si 2O 5)2-的
二维硅酸盐片层状结构示意图。
母KAl3Si3O10(OH)2)也具有这类结构,而且它们是重要的陶瓷原材料。正如化学式所示,有一些硅酸盐的结构属于所有的无机材料中最为复杂的一类。
图12.14 高岭石陶土结构
12.4碳
碳是一种可以以多种形态以及非晶态存在的元素。这一族材料在传统的金属、陶瓷、聚合物的分类图中找不到位置。但是,由于石墨(碳的多态形式中的一种)有时被归类于陶瓷,而且金刚石(另一种多态形式)晶体结构类似于12.2讨论的闪锌矿结构,因此本章也将对这类材料进行讨论。讨论主要集中于石墨、金刚石、富勒烃, 碳纳米管的结构和特征以及它们目前的主要用途和今后潜在的用途。
金刚石
在室温和大气条件下,金刚石是一种亚稳的碳多态。它的晶体结构是闪锌矿的一种变形,所有的位置(Zn,S)都由碳原子占据,基元如图12.15所示。每一个碳原子与周围四个碳原子成键,所成键为完全共价键,这种结构被称为金刚石立方晶体结构。具有此种结构的还有元素周期表中其他IV A 族元素(例如,锗,硅,和13 C以下的灰锡)。
金刚石因其物理特性而成为一种很有吸引力的材料。金刚石非常硬(是所有已知材料中最硬的材料),导电性很差。这些特性来自于它的晶体结构和原子间很强的共价键。此外,作为一种非金属材料具有很好的热导性,在电磁波谱的可见光波段和红外波段有好的透光性和高的折射率。比较大的金刚石单晶被当作宝石。在工业上,金刚石可以用来研磨和切割其它软材料(见13.5)。金刚石合成技术是从二十世纪五十年代中期开始发展起来的,目前这项技术已经非常精细,现在大多数工业用金刚石材料都是人造金刚石,其中还包括某些宝石。
最近几年,又生产出了金刚石薄膜。薄膜生长技术包括气相化学反应薄膜沉积,最大膜厚可以达到毫米量级。此外,目前生长的薄膜不具有天然金刚石的长程晶体周期性,金刚石是多晶,组织中既有比较小的晶粒,也有相对比较大的晶粒,还可能有非晶碳和石墨。图12.16是金刚石薄膜表面扫描电镜照片。金刚石薄膜的力学、电学、光学性能接近大块金刚石材料的性能。人们正在继续开发这些理想特性,创造出更新更好的材料。例如,在钻头、模具、轴承、刀具和其它工具的表面覆加金刚石薄膜涂层可以提高表面硬度。透镜和天线罩表面覆加金刚石涂层即可使其增强又可保持透明。金刚石涂层也应用到了扩音器高音喇叭和高精度测微器上。这类薄膜的潜在应用包括:机器部件如齿轮表面,光记录磁头和磁盘,以及用作半导体器件的基底。
石墨
碳的另一种多态是石墨。石墨的结构(见图12.17)与金刚石结构明显不同。在室温和大气条件下,石墨结构比金刚石结构更稳定。石墨结构是由六边形排列的碳原子层构成,在层内,碳原子与三个相邻共面原子成很强共价键,在层间,通过电子参与的弱的范德瓦尔斯力形成第四个键。由于层间键合弱,因此很容易发生层间劈裂,因此石墨是非常优秀的润滑剂,而且在平行六边形片的晶体学方向上具有比较高的导电性。
图12.15 金刚石立方晶体结构的基元
图12.16 金刚石薄膜的扫描电
镜照片,可以看到许多多面体
微晶。
石墨的其它特性包括:在高温非氧化气氛下强度高,化学稳定性好;除此之外,石墨热导率高,热膨胀系数低,抗热震性好,气体吸附率高,可加工性好。石墨通常被用作电炉中的加热元件,电弧焊中的电极,冶炼坩埚,金属、合金、和陶瓷的浇铸模具,高温耐火材料和绝缘材料,火箭喷嘴,化学反应容器,电子触件,电刷和电阻器,电池中的电极,以及用于空气净化器中。
富勒烯和碳纳米管
富勒烯
碳的另一种多态形式是1985年发现的,它以离散分子的形式存在,由60个碳原子组成一个中空的球状团簇,一个单分子标记为C 60。每一个分子由一组碳原子组成,碳原子间相互成键,构成六边形(六个原子)和五边形(五个原子)两种几何图案。图12.18是一个C 60分子的结构示意图,它包含20个六边形和12个五边形,排列方式为任何两个五边形之间没有公用边。分子表面表现出足球的对称性。由C 60分子构成的材料被成为巴可明斯特富勒烯,以纪念网格球顶的发明者R.Buckminster Fuller 。每一个C 60分子仅仅是这种球的一个复制品,因此也常被简称为巴基球。富勒烯是这类分子构成的材料系列的总称。
金刚石和石墨是所谓的网状固体,其中由碳原子和相邻原子构成的主键贯穿整个固体。相比较而言,巴可明斯特富勒烯中碳原子相互成键形成球状分子。在固态,C 60分子按照面心立方形式堆垛形成晶体结构。
纯净的C 60固体晶体是绝缘体,但是适当掺入杂质后可以成为半导体或者良导体。
碳纳米管
碳纳米管是近年新发现的另一种形式碳分子,碳纳米管既有独特的特性又有科学价值。碳纳米管由单层石墨卷成管状,两端是C 60富勒烯半球。碳纳米管的结构图见12.19。纳米表示管子的半径在纳米量级(也就是说,100 nm 以下)。每一个纳米管是一个分子,这个分子由上百万个原子构成。图12.17 石墨结构。
图12.18 C 60分子的结构。
纳米管的长度远远大于纳米管的半径(大约要大几千倍)。目前发现也存在由同心的圆柱构成的多重碳纳米管。
这些碳纳米管很强、很硬,同时延展性比较好。对单重纳米管,拉伸强度在50到200 GPa之间(大约比碳纤维高一个量级),是已知的最强的材料。弹性模量在一个TPa量级(1 TPa=103 GPa)断裂应变在5%到20%之间。此外,纳米管的密度比较低。基于这些特性碳纳米管被称为“终极纤维”,是复合材料中最有希望的增强相。
碳纳米管还具有独特的结构敏感电学特性。在graphene面(管壁)上的六角形单元和管轴的相对趋向决定纳米管表现出金属的导电性还是半导体导电性。有报道说,由碳纳米管作发射极的直板全色显示器(例如电视和计算机显示器)已经生产出来,这种显示器与CRT和液晶显示器相比成本低,能耗小。而且,可以预知碳纳米管将来还可以用于二级管和晶体管等电子领域。
图12.19 碳纳米管的结构
12.5陶瓷中的缺陷
原子点缺陷
在陶瓷化合物中存在包括宿主原子在内的原子点缺陷。正如金属,陶瓷中同样存在空位和间隙,但是由于陶瓷材料中存在两种以上的离子,每个离子都有可能产生两种类型缺陷。例如,在NaCl 中,可能存在Na间隙和Na空位以及Cl间隙和Cl空位,但是间隙阴离子的浓度很小不太可能测到。因为阴离子相对比较大,填充进入小的间隙位置时,会引起周围离子的较大应变。阴离子和阳离子空位以及阳离子间隙示于图12.20。
图12.20 阴离子和阳离子空位以及阳
离子间隙示意图。
缺陷结构常用来标志陶瓷中原子缺陷的类型和浓度。由于原子以带电离子的形式存在,因此考虑缺陷结构时,电中性条件必须满足。当离子贡献的正电荷数和负电荷数相等时达到电中性状态。因此在陶瓷中缺陷不可能单独出现。一种类型的缺陷是包括一个阳离子间隙和一个阳离子空位对,这种缺陷被称为弗兰克尔缺陷,如图12.21。可以认为阳离子离开正常位置进入间隙位置从而形成弗兰克尔缺陷。在此过程中电荷没有变化,因为阳离子处于间隙位置后所带正电荷不变。
在AX 型材料中发现的另一类缺陷是阳离子空位和阴离子空位成对出现,这类缺陷被称为肖特基缺陷,也示于图12.21。可以认为阳离子和阴离子从晶体内部被移到了晶体外表面形成了这类缺陷。由于阳离子和阴离子带相同电荷,而且对应每一个阴离子空位都存在一个阳离子空位,因此晶体保持电中性。
无论形成弗兰克缺陷还是肖特基缺陷,阳离子和阴离子的比值不发生变化。如果没有其他的缺陷,材料保持理想配比。化学配比的定义为:离子固体中,阳离子和阴离子的比值严格满足化学式给出的比值的状态。例如,如果Na +离子和Cl -离子的比例为严格1:1,那么NaCl 就为理想配比。如果阳离子和阴离子的比值偏离精确比值,那么陶瓷化合物就是非理想配比。
对某些陶瓷材料而言,当其中的一种离子存在两种价态时,就会出现非理想配比。氧化铁(方铁体)就是这样一种材料,因为铁可以以Fe 2+和Fe 3+状态存在,每种类型的离子的数量依赖于温度和氧压强。每形成一个Fe 3+离子,就引入一个多余正电荷,从而破坏了晶体的电中性,所以一定要有某种类型的缺陷来补偿。这种补偿可以是形成一个Fe 2+空位或者说每形成两个Fe 3+离子,就将两个正电荷移走(如图12.22),此时晶体不再是理想配比,因为氧离子数比铁离子数多出一个,但是整个晶体仍然保持电中性。这种现象在在铁的氧化物中很常见,事实上,它的化学式常被写为Fe 1-x O(其中x 是远小于1的可变的分数),表明处于一种缺铁的非理想配比状态。
陶瓷中的杂质 陶瓷材料中的杂质原子类似于金属中的杂质原子可以形成固溶体,即可能形成替代式固溶体又图12.21 离子固体中弗兰
克和肖特基缺陷的示意图。
图12.22 FeO 中两个Fe 3+离子形成从
而出现一个Fe 2+空位示意图。
可能形成间隙式固溶体。间隙式固溶体,杂质的离子半径必须小于阴离子半径。由于材料中即存在阴离子又存在阳离子,因此替代式杂质将替代电子性质最相近的宿主离子,也就是说,在陶瓷中如果杂质离子形成阳离子,那么此杂质离子将替代宿主阳离子。例如在氯化钠中,杂质Ca2+离子和O2-离子将分别替代Na+离子和Cl-离子。图12.23是间隙和替代式杂质阳离子和阴离子的示意图。要达到最佳固溶度,替代式杂质离子的离子半径和所带电荷必须与其中一种宿主离子非常相近或相同。如果杂质离子所带电荷与要替代的宿主离子的不同,为了保持整体电中性,晶体必须对这种电荷差别进行补偿。一种方法就是形成前面讨论过的空位或间隙晶格缺陷。
图12.23离子化合物中,间隙杂质原
子和杂质阴离子替代以及阳离子替
代的示意图。
例题12.4
在保持电中性的前提下,用Ca2+离子替换NaCl中的Na+离子可能引入那几种点缺陷?每引入一个Ca2+离子将同时引入多少这种点缺陷?
解答:一个Ca2+离子替换一个Na+离子同时引入一个多余的正电荷,要保持电中性,必须消除一个正电荷或者加入一个负电荷。可以通过形成Na+空位消除正电荷,也可以通过形成间隙Cl-离子引入一个负电荷,中和Ca2+离子的效应,但是正如前文所述,形成这种缺陷的可能性很小。12.6 离子性材料中的扩散
离子化合物中的扩散现象比金属要复杂的多,需要考虑带电相反的两种离子的扩散运动。这类材料中扩散通常是通过空位机制发生(如图5.3a)。在12.5节曾经指出,在离子性材料中,为了保持电中性,空位可以:(1) 成对出现(就象图12.21中的肖特基缺陷);(2) 形成非理想配比化合物(图12.22);(3) 当杂质离子的电荷状态和宿主离子的电荷状态不同时,产生空位(例题12.4)。在任何情况下,与一个单离子的扩散运动相关的是电荷的转移。为了维持移动离子附近的局部电中性,必须有与移动离子的电量相同,电性相反的另一种离子伴随这种离子的扩散运动。这些离子种类包括:另一种空位,杂质原子,或者载流子(自由电子或者孔穴)。带电对的扩散速率由其中运动最慢的那种带电子的扩散速率决定。
当在离子固体上施加一个电场时,带电离子响应外电场施加的力漂移(也就是扩散)。我们将在18.16节讨论,离子的运动会导致电流,而且,电导率是扩散系数的函数(18.20式)。因此,离子固体的许多扩散数据来源于电导率测量。
12.7陶瓷相图
很多陶瓷体系的相图已经通过实验得到。二元或者两种成分相图通常是两组元都是化合物,具有一个共同的元素,常常是氧。这类相图类似于金属-金属体系,解释也基本相同。读者可以查阅本书9.7,查阅关于相图的解释。
Al 2O 3-Cr 2O 3体系
氧化铝和氧化铬体系的相图是陶瓷中比较简单的相图之一,见图12.24。此相图与异质同形的铜-镍相图(见图9.2a )相同。存在一个单相液态区,一个单相固态区,固液两相之间由一个刀片状的固-液两相共存区隔开。Al 2O 3-Cr 2O 3固溶体是替代式固溶体,其中Al 3+离子和Cr 3+离子互相替代。在Al 2O 3熔点以下,可以存在任何成分固溶体,因为铝离子和铬离子带有相同电荷和相近的离子半径(分别是0.053nm 和0.062nm ),而且Al 2O 3和Cr 2O 3具有相同晶体结构。
MgO- Al 2O 3体系
MgO- Al 2O 3体系相图(见图12.25)在很多方面与铅镁体系相图(见9.18)相似,存在一个中间相,或者更确切的说,存在一个叫尖晶石的化合物,其化学式为MgAl 2O 4(或者MgO- Al 2O 3)。尽管尖晶石是一种化合物,组分为50mol% Al 2O 3和50mol% MgO 或者说72wt% Al 2O 3和28wt% MgO ,但是在相图上尖晶石以单相区存在,而不是以一条直线(如图9.18中Mg 2Pb )存在。这是因为在此成分范围内,尖晶石是一种稳定的化合物。当组分不满足50mol% Al 2O 3+50mol% MgO 时,尖晶石处于非理想化学配比。在1400?C 以下Al 2O 3在MgO 中有一个极限固溶度(如图12.25中的左边的极限),这主要是由于Mg 2+和Al 3+所带电荷不同,以及离子半径不同(0.072 nm 和 0.053 nm )造成的。由于同样的原因MgO 几乎不溶于Al 2O 3,这一点可从相图中最右边缺少固溶体看出。同时在尖晶石相区的两边有两种共晶体,理想化学配比的尖晶石在2100?C 融化。
图12.24氧化铝-氧
化铬相图。
本科专业目录中教育学包括教育学、体育学等2个学科类,共有9个本科专业。 据国务院学位办公室发表的统计数据,我国大学授予的教育学学士占学士总数的 3.61%,授予的教育学硕士占硕士总数的2.50%,教育学博士占博士总数的1.40%。另据教育部高校学生司发布的博士生导师资料统计,在全国大学37078名博士生导师中,有662名是教育学博导,占博导总数的1.79%。教育学是比较小的学科。 在本科专业分类中,心理学属于理学,而在研究生专业分类中,心理学属于教育学。为了使两者统一,本评价的教育学排名含心理学类的各本科专业的得分。 2017中国大学教育学60强名单 排名等级校名 1 A++ 北京师范大学 2 A++ 华东师范大学 3 A++ 华南师范大学 4 A+ 浙江大学 5 A+ 北京体育大学 6 A+ 南京师范大学 7 A 西南大学 8 A 华中师范大学 9 A 上海体育学院 10 A 东北师范大学 11 A 成都体育学院 12 A 武汉体育学院 13 A 湖南师范大学 14 A 浙江师范大学 15 A 首都师范大学 16 A 西北师范大学 17 A 上海师范大学 18 B+ 首都体育学院 19 B+ 陕西师范大学 20 B+ 辽宁师范大学 21 B+ 福建师范大学 22 B+ 苏州大学 23 B+ 天津师范大学 24 B+ 曲阜师范大学 25 B+ 山东师范大学 26 B+ 广州大学 27 B+ 江西师范大学 28 B+ 天津体育学院
29 B+ 安徽师范大学 30 B+ 南京大学 31 B+ 河北大学 32 B+ 吉林大学 33 B+ 沈阳师范大学 34 B+ 河南大学 35 B+ 湖北大学 36 B+ 宁波大学 37 B+ 山西大学 38 B 广西师范大学 39 B 河北师范大学 40 B 温州大学 41 B 北京航空航天大学 42 B 西安交通大学 43 B 广州体育学院 44 B 杭州师范学院 45 B 扬州大学 46 B 集美大学 47 B 深圳大学 48 B 聊城大学 49 B 北京理工大学 50 B 武汉理工大学 51 B 暨南大学 52 B 兰州大学 53 B 徐州师范大学 54 B 西安体育学院 55 B 山西师范大学 56 B 南通大学 57 B 北京联合大学 58 B 鲁东大学 59 B 淮阴师范学院 60 B 西华师范大学
兰州大学管理学院635西方经济学和855管理学考研真题及答案笔记模拟题 关于考研,2015你下定决心了吗?做好准备迎接它的到来了吗?愿意花上一年甚至更多的时间全心投入到这场艰苦的战役中了吗?也许你还在犹豫、也许你陷入迷茫,但千万不要让时间犹豫、迷茫中溜走。在学习上,历经了高考的拼搏,考研也许是最后的一次。未来的路在你脚下,要坚信自己认真的抉择永远是正确。 《弘毅胜卷》的特点: 1.“最全”:本资料把参考书可能考到的知识点都全部列出,并做了详细的讲解,并对历年真题进行透彻的解析; 2.“最简”:为不增加考生负担,对考点的讲解,尽量做到精简,除去了教材繁琐臃肿的语言,直击要害; 3.“最具实用性”:各高校考题的重复率非常高。针对此规律,本资料将专业涉及到的真题举例附在每个考点后面,方便大家查阅。 4.“最具时效性”:本资料会根据最新的招生简章和目录、最新的参考书目和考试大纲对资料进行及时调整、更新,让弘毅胜卷臻于完善! 提醒:为保证产品质量,我们在反盗版技术上投入了很大人力物力,首先在阅读体验上远远超越盗版资料(加了水印和红白页,复印基本看不清楚),同时弘毅考研每年均根据当年最新考试要求进行改版升级并提供超值的售后服务,并将后续重要资料分期发送,盗版将丢失这些重要资料,请考生务必谨慎辨别,不要为了省一点小钱购买其他机构或个人销售的盗版材料而耽误备考,甚至影响前途的大事情。同时也请大家支持正版,你们一如既往的支持,是我们一直大力度的投入开发的动力。 如果亲在考研路上需要小伙伴,欢迎加入兰州大学大学考研群:【54199212】 考试科目:635西方经济学(管理类)、855管理学 适用专业:行政管理、政府绩效管理、土地资源管理、教育经济与管理。855管理学还适用会计学、企业管理、旅游管理、情报学
兰州大学 管理学院 管理学2000——2006 西方经济学2000——2007,2010(2010为回忆版) 文学院 古代汉语和现代汉语2006 古代汉语2002——2005 文学概论2000——2002,2004——2005 现代汉语2002 现代汉语和语言学概论2003——2005 语言学概论2000——2002 中国文学2008 中国文学史2000——2007(注:2002,2003年试卷名称为“中国古代文学史”)中国现代文学史2002——2003 文学理论和外国文学2008 文学概论和外国文学2006 比较文学与世界文学2002——2003 汉语言文字学2000——2001 新闻与传播学院 传播学原理1999——2005(1999——2004有答案) 新闻理论(含中国新闻事业史) 1999——2005,2007(1999——2004有答案) 新闻写作1999——2002 历史文化学院 民族学概论2003——2005 民族学原理2000——2001 世界近现代史1995——2005 中国古代史2000——2005 中国近现代史1994——2005 中国历史文选2002——2005 中国少数民族史2003——2005 经济学院 高级微观与宏观经济学2006 西方经济学2000——2007,2010(2010为回忆版) 发展经济学2000——2005 金融学综合(含货币银行学、国际金融学)2005 政治经济学(资、社)2000——2005 中国近现代经济史(含中国近代经济史、中华人民共和国经济史)2005
法学院 法理学2003——2005 法理学(复试)2004 国际公法(复试)2004——2005 国际经济法2005 环境与资源保护法2002——2005 经济法2001——2005 民法2001——2002 民法(复试)2004——2005 民商法2003——2005 民事诉讼法(复试)2004——2005 宪法与行政法学2008 宪法(复试)2004 刑法2004——2005 刑事诉讼法(复试)2004——2005 行政法2002 行政法与行政诉讼法2004——2005 外国语学院 二外德语2002——2005 二外法语2002——2005 二外日语2001,2003(2001有答案) 翻译与写作2004——2005 英美文学2001——2005 英语语言学2002——2005 哲学社会学院 科学思想史2004——2005 马克思主义哲学2004——2005 西方哲学史2000——2005 中国哲学史2000——2005 社会调查方法2002——2005(注:2004年试卷共2页,缺第2页)社会学理论2007 社会学概论2002——2005 社会学专业2004年复试(笔试)试题 政治与行政学院 国际政治学2002——2006,2008(注:2008年试卷为回忆版) 马克思主义发展史2002——2006 政治学原理2002——2006,2008 科学社会主义原理2004 教育学院 高等教育学2002
2001年招收攻读硕士学位研究生考试试题 招生专业:管理类各专业考试科目:管理学注意:答案请一律写在答题纸上,写在试题上无效。 一、比较下列概念(每小题5分,共25分) 1、正式组织与非正式组织 2、管理跨度与管理层次 3、直接控制与间接控制 4、激励因素与保健因素 5、建设性冲突与破坏性冲突 二、简答题(每小题7分,共42分) 1、简述法约尔管理理论得主要内容。 2、选定计划目标时要注意哪些问题? 3、简述动态得组织设计原则。 4、简述管理审计工作得基本任务。 5、简述亚当斯公平理论得主要内容。 6、在管理沟通中存在着哪些障碍?如何克服? 三、论述题(共33分) 1、根据领导理论,谈谈对提高企业领导者素质得认识。(13分) 2、对建立与完善国有企业法人治理结构问题得思考。(20分) 2002年招收攻读硕士学位研究生考试试题 招生专业:管理类各专业考试科目:管理学注意:答案请一律写在答题纸上,写在试题上无效。 一、比较下列概念(每小题5分,共30分) 1、管理原理与管理原则 2、经济人与社会人 3、组织发展与组织变革 4、保健因素与激励因素 5、建设性冲突与破坏性冲突 6、零缺点质量管理与全面质量管理 二、简答题(每小题7分,共42分) 1、简述科学管理与管理科学得关系。 2、简述决策理论学派得主要内容。 3、简述三种领导理论得主要思路。 4、简述人本原理得主要内容。 5、画出计划管理得PDCA图并做解释。 6、简述价值工程得核心思想与主要内容。 三、论述题(每小题14分,共28分) 1、加强企业管理提高经济效益得思考。 2、试述现代企业制度条件下得管理创新问题。 2003年招收攻读硕士学位研究生考试试题 一、比较下列概念(每小题6分,共48分) 1、正强化激励与负强化激励 2、单向沟通与双向沟通 3、弹性预算与零基预算
兰州大学 2018年硕士学位研究生入学考试试题 (物理化学) ■需使用计算器□不使用计算器 一、选择题(每小题 2 分,共60 分,答案必须写在答题纸上) 1、从统计热力学的观点看,该图表示( ) (A) 体系吸热(B) 体系放热 (C) 体系对环境作功(D) 环境对体系作功 2、已知1mol HCl的无限稀释溶液与1mol NaOH 的无限稀释溶液在恒温恒压下完全反应,热效应Δr H m?=-55.9 kJ·mol-1,则1mol HNO3的无限稀释溶液与1mol KOH的无限稀释溶液在恒温恒压下完全反应的热效应Δr H m?为( ) (A) > -55.9 kJ·mol-1(B) < -55.9 kJ·mol-1 (C) = -55.9 kJ·mol-1(D) 不能确定 3、理想气体从相同始态分别经绝热可逆膨胀和绝热不可逆膨胀到达相同的压力,则其终态的温度、体积和体系的焓变必定是( ) (A) T可逆> T不可逆,V可逆> V不可逆,ΔH可逆> ΔH不可逆 (B) T可逆< T不可逆,V可逆< V不可逆,ΔH可逆< ΔH不可逆 (C) T可逆< T不可逆,V可逆> V不可逆,ΔH可逆< ΔH不可逆 (D) T可逆< T不可逆,V可逆< V不可逆,ΔH可逆> ΔH不可逆
4、已知均相纯物质的平衡稳定条件为(?p/?V)T < 0,则任一物质绝热可逆膨胀后压力必( ) (A)升高(B)降低(C)不变(D)不确定 5、273 K,0.5×101.3 kPa 时,水的化学势比冰的化学势( ) (A) 高(B) 低(C) 相等(D) 不可比较 6、沸点升高,说明在溶剂中加入非挥发性溶质后,该溶剂的化学势比纯溶剂的化学势( ) (A) 升高(B) 降低(C) 相等(D) 不确定 7、液体A与B混合形成非理想混合物,当A与B分子之间作用力大于同种分子之间作用力时,该混合物对拉乌尔定律而言() (A) 产生正偏差;(B) 产生负偏差; (C) 不产生偏差;(D) 无法确定。 8、关于标准态的选择,下列说法中错误的是( ) (1) 溶质选取不同的标准态,溶质的化学势也不同; (2) 实际气体与理想气体选取的标准态相同; (3) 液态理想混合物与液体非理想混合物选取的标准态相同; (4) 实际稀溶液的溶质,选取不同的标准态,得到得活度与活度系数也不同; (5) 纯液体与其蒸气选择的标准态相同。 (A) (1)(4) (B) (1)(5) (C) (2)(3) (D) (4)(5) 9、甲、乙、丙三个小孩共吃一支冰棍,三人约定:⑴各吃质量的三分之一;⑵只准吸,不准咬;⑶按年龄由小到大顺序先后吃。结果,乙认为这只冰棍没有放糖,甲则认为这冰棍非常甜,丙认为他俩看法太绝对化。则三人年龄( ) (A) 甲最大,乙最小;(B) 甲最小,乙最大; (C) 丙最大,甲最小;(D) 丙最小,乙最大。 10、有一形成不稳定化合物的双组分A与B凝聚体系,系统的组成刚巧与不稳定化合物 的组成相同,当其从液态冷却到不相称熔点,系统内建立如下平衡: 液相+ A(s) = A x B y(不稳定化合物) 如果在此时系统由外界吸取热时,则上述的平衡将( ) (A) 向左移动;(B) 向右移动;(C) 不移动;(D) 无法判定。 11、如图A与B是两组分恒压下固相部分互溶凝聚体系 相图,有几个两固相平衡区( ) (A) 1个; (B) 2个; (C) 3个; (D) 4个。
教育学考研学校排名及热门专业 凯程老师通过教育学考研辅导名师、及往届高分学员、职业经理人的意见,为有意向报考教育学专业的考研学子提供如下教育学择校及细分专业建议。 学校代码及名称学科整体水平得分 10027 北京师范大学95 10269 华东师范大学89 10319 南京师范大学81 10200 东北师范大学80 10511 华中师范大学78 10001 北京大学77 10028 首都师范大学77 10335 浙江大学77 10384 厦门大学77 10574 华南师范大学77 10635 西南大学77 热门专业: 1、教育学原理 教育学原理是研究教育现象及教育规律的核心学科,是指导教育活动和教育改革实践的理论源泉,教育学原理研究的每一个突破对我国教育事业的改革与发展都具有重要的影响作用。 本专业培养具有良好政治、思想和品德素质,较高的教育理论水平、教学和科学研究能力的高级专门人才。 随着中小学教师待遇的不断提高,再加上教师这个职业本身比较稳定,越来越多教育类专业的硕士毕业生开始进入中小学校,今年还出现了南京某中学几百个硕士竞争两个岗位的现象。 公务员招考很少,想当公务员的同学可以努力一把,但要做好心理准备,因为竞争的激烈程度会超乎你的想象。 推荐院校 教育学原理专业硕士全国较强的招生单位有:
华东师范大学、北京师范大学、南京师范大学、西南大学、东北师范大学、华南师范大学、北京大学、西北师范大学、辽宁师范大学、武汉大学、华中师范大学、山东师范大学。 2、高等教育学 高等教育学是教育学之下的一个二级学科硕士点,研究范围包括:高等教育与社会因素及高等教育内部之间关系的研究,高等教育管理与评估,中外高教史研究,高等教育课程与教学研究,国际高等教育研究和国际比较,大学生心理研究等。 但在人们传统的思维中,教育学的就业方向主要是去学校做老师,事实上有相当一部分教育学专业毕业的学生毕业后并没有从事教书行业。专业课教研室梳理了教育学的六大从业方向。 随着国家对教育的越来越重视和教师待遇的不断提高,教育学专业正在逐渐成为一门热门专业,但是随着部分高校改革高等教育学硕士研究生学制以及高等教育学硕士持续扩招以来高等教育学硕士生面临着严峻的就业压力高等教育学硕士就业难而高等教育女硕士就业更难。 推荐院校 以下学校本专业实力较强: 厦门大学、北京大学、华中科技大学、北京师范大学、西南大学、华东师范大学、清华大学、兰州大学、云南师范大学、广西师范大学、苏州大学、湖南师范大学、中国地质大学、南京师范大学、湖南大学、南京大学等。 3、基础心理学 顾名思义,基础心理学研究的是心理学的基础的东西。研究方向有认知心理学、实验心理学、生理心理学、认知神经科学等,其研究为心理学的应用打下良好的基础。基础心理学的研究生需要掌握一定的数学、生理学、计算机科学、语言学等方面的知识。本专业培养坚持党的基本路线,德智体全面发展,专业基础扎实,具备创新精神和实践能力的心理学理论、心理学科研和心理学教学的高级专门人才。 推荐院校
金属材料物理专业实验课程教学大纲 一、课程说明 (一)课程名称、所属专业、课程性质、学分; 课程名称:金属材料物理专业实验 所属专业:金属材料 课程性质:专业实验课 学分:4 (二)课程简介、目标与任务; 课程简介:金属材料物理专业实验是专业实验教学部的重要组成部分,其前身是原物理系金属物理专业,始建于1956年,是我国第一批设置的金属物理专业,是与吉林大学、北京大学、南京大学、中山大学同期先后设置的专业,也是建国初期按照地理区域和行政区域划分的全国八大金属材料研究基地之一。主要培养有色金属、复合材料、粉末冶金、材料热处理、材料腐蚀与防护及表面等领域从事科学研究、技术开发、工艺和设备设计、生产及经营管理等方面的人才。本专业实用性很强,研究成果可以直接应用到现实生产,所取得的进展和人民群众的日常生活密切相关,专业就业前景广阔。 目标和任务:从基础性的技能训练实验、综合性创新性实验和研究性科研训练等三个层次上进行实验内容、层层深入地培养与训练学生的综合实验素质及创新能力:精选基础性实验,建设并加强综合性实验和研究创新性实验。 (三)先修课程要求,与先修课与后续相关课程之间的逻辑关系和内容衔接; 《金属物理学》《金属热处理》 (四)教材与主要参考书。 教材:自编中
参考书: 1.《金属热处理综合实验指导书》,王志刚、刘科高主编,高等学校“十二五”实验实训规 划教材,冶金工业出版社; 2.《金属材料及热处理实验教程》,周小平主编,华中科技大学出版社; 3.《金属热处理原理与工艺》,王顺兴主编,哈尔滨工业大学出版社; 4.《金属热处理工艺学》,夏立方主编,哈尔滨工业大学出版社 (五)主讲教师。 主讲:卓仁富,闫徳 教师梯队:王君,耿柏松,门学虎,吴志国 二、课程内容与安排 第一章金属热处理(退火、正火、淬火) (一)教学方法与学时分配 8学时,必做实验。先讲授,然后自己动手完成实验 (二)内容及基本要求 主要内容:热处理是一种很重要的金属加工工艺方法,热处理的主要目的是改善钢材性能,提高工件使用寿命。钢的热处理工艺特点是将钢加热到一定的温度,经一定时间的保温,然后以某种速度冷却下来,通过这样的工艺过程能使钢的性能发生改变。 热处理之所以能使钢的性能发生显著变化,主要是由于钢的内部组织发生了质的变化。采用不同的热处理工艺过程,将会使钢得到不同的组织结构,从而获得所需要的性能。 普通热处理的基本操作有退火、正火、淬火及回火等。热处理操作中,加热温度、保温时间和冷却方式是最重要的三个关键工序,也称热处理三要素。正确选择这三种工艺参数,是热处理成功的基本保证。Fe-FeC相图和C-曲线是制定碳钢热处理工艺的重要依据。 【重点掌握】:含碳量、加热温度、冷却速度等因素与碳钢热处理后组织及性能的关系。
2016 年兰州大学管理学考研真题 一、名词解释(20 分,每小题 4 分) 1、指挥链 2、工作丰富化 3、成本领先策略 4、路径——目标理论 5、利益相关者 二、填空题(20 分,每空 2 分) 1、美国哈弗大学教授迈克尔·波特认为,一个行业的吸引力主要取决于五种基本竞争用:___________、____________、____________、____________和____________。 2、古典管理理论的代表人物有:弗雷德里克·泰勒、____________、____________ 。 3、尽管控制的内容各有不同,每项控工作的关键控制点和标准也可能不一样,但控制的过程基本一致的,大致可以分为三个步骤:_____________、______________、 ______________。 一、简答题。(本题 60 分,每题 12 分) 1、简述效率和效果的区别与联系。 2、试分析滚动计划法与有限理性决策的关联。 3、简述设计良好的目标的基本特征。 4、简述组织部门划分的方法。 5、简述管理学的系统观点及对管理实践的指导意义。 四、论述题。(本题 20 分) 有人认为“战略就是定位”,也有人认为“战略就是领导力” 1)请你谈谈你对两种观点的理解 2)你更同意哪个观点?为什么? 五、案例分析(本题 30 分) 郭仕纳与IBM IBM 是国际商用机器公司的英文简称。它是美国乃至世界最大的电子计算机制造和数据处理公司之一,总部设在美国纽约的阿蒙克。1997 年,IBM 销售额为 785 亿
美元,资产总额为 815 亿美元,名列世界 500 强第 14 位,在美国大公司排名第 6 位,被称为“蓝色巨人”。2002 年,在世界品牌资产价值分析中,IBM 名列第三,仅次于可口可乐公司和微软公司。然而就这样的一位“蓝色巨人”其发展也不是一帆风顺的,也曾陷入低潮和困境,其中在 1991~1993 年间累计亏损额高达 162 亿美元,时任公司董事长埃克斯引咎辞职。 IBM 公司董事会经过3个月的深思和挑选,让没有计算机行业经历的郭仕纳担任了 IBM 公司的新任董事长。从 1993 年开始,郭仕纳就开始大刀阔斧的改革。 首先,郭仕纳更换了 IBM 公司 2/3 的高层管理人员,使长期从事行业但眼睛向内的管理者、守业者离开主管岗位,让一批“外来者”担任公司的重要职务,从而使IBM 公司领导班子为之一新。 其次,以郭仕纳为首的 IBM 公司新管理层提出了 IBM 的经营理念和经营战略。经营理念包括:第一、市场是我们一切商业活动的动力。第二、质量使我们至高无上的承诺。第三、客户满意度和股东价值是衡量我们成功与否的基准。第四、不断创新,提高管理效能和生产率是我们不懈的追求。第五,重视人才培养和队伍建设,呵护员工,强调团队的紧密协同行动,使我们制胜的关键。经营战略包括:第一,确定网络计算机的领导地位。第二,在开发关键硬件和软件产品方面继续发挥领导作用,第三,为客户提供服务,帮助他们应用信息技术。第四,投资于新兴市场。 在确定了经营理念和经营战略后,郭仕纳在管理上开始了果断行为。他制止了其前任实行的分权管理制的扩大做法,他认为要使公司“停止流血”,必须制止分裂。他强调公司与用户之间以公司总部与分部之间要联系紧密,强调各部门之间在资源、技术和管理上更大程度的共享。 郭仕纳恢复了沃森时代重视科技开发投资的传统,他不仅将营业收入的 10%重新用于研究开发投资,而且明确指出,研究开发应着眼于用户和市场需要,而不是仅仅围绕着公司自身产品展开。这种创新式的管理思想,极大地促进了 IBM 公司产品的开发。 郭仕纳作为公司最高主管,既重视言传又重视身教。他上任后,有 40%的时间用在听取用户意见上,数年进行过 542 次飞行,亲自走访客户;他倡导移动办公,设立虚拟办公室;他动员公司底层员工通过电子邮件直接联系他,反映真实情况,提出建议和意见;他鼓励员工提高个人能力,在团队合作过程中不仅为公司创造财富,同时也为个人增加收入,他责令公司高层管理人员每月必须走访 5 个客户等。
兰州大学2017年教育学考研参考书 兰州大学只有教育学学硕,是统考,专业隶属于教育学院。兰州大学教育学院渊源于1979年成立的兰州大学高教研究室,是国内较早成立高等教育研究机构的高校之一,是筹备中国教育学会、中国高等教育学会的主要发起单位。2002年8月,兰州大学根据学校学科发展战略,成立了兰州大学教育学院。兰州大学教育学院的发展目标是成为在国内有重要影响力的高等教育管理、服务、研究类人才培养基地和高等教育科学研究中心之一;成为西部一流的高等教育研究和咨询服务中心;成为兰州大学建设发展的重要决策咨询机构之一;成为在区域内有较大影响力的基础教育研究与培训中心。 注:2017年招生信息一般在2016年9月左右发布,所以对于备考兰州大学2017年教育学学硕或者专硕研究生的同学们来说,现阶段的复习可以以2016年招生信息为准。 兰州大学教育学学硕招收方向很多,考试科目中外国语考察有不同,专业课是统考。考试科目:①101思想政治理论、②201英语一或202俄语或203日语、③311教育学专业基础综合或者312心理学专业基础综合。部分方向考试科目外国语考察英语一,备考同学需要提前了解好所报考方向的考试科目。 311教育学专业基础综合以及312心理学专业基础综合都是统考,有全国版大纲,但是并没有全国版大纲,博仁教育根据统考大纲以及历年统考真题推荐以下参考书目,备考同学可参考:311教育学专业基础综合 教育学原理: 《教育学基础》(第2版)教育科学出版社十二所重点师范合编; 《教育学》人民教育出版社王道俊、郭文安; 教育心理学: 《当代教育心理学》北师大出版社陈琦、刘儒德; 中外教育史: 《中国教育史》华东师范大学出版社孙培青; 《外国教育史教程》人民教育出版社吴式颖; 教育研究方法: 《教育研究方法导论》安徽教育出版社裴娣娜; 《教育研究导论》北京师范大学出版社,宁虹主编; 312心理学专业基础综合 《普通心理学》彭聃龄北京师范大学出版社
2020兰州大学教育学考研分数线 2020兰州大学教育学考研分数线已经公布,博仁考研为大家整理了教育学考研专业的分数线,帮助各位教育学考研人了解院校,高校备考。 兰州大学教育学专业隶属于高等教育研究院,学院秉承培养教育英才,创造教育知识,建设教育智库,服务社会发展的使命,坚持突出高等教育学科特色,积极发展教育信息化、教师教育、应用心理学等学科方向,形成了良性学科生态环境的学科战略,在人才培养、科学研究、服务社会、学术交流、师资队伍建设等方面取得较大进展。至2016年,全院教职员工47人,专任教师达到31人,其中教授7人,副教授11人,讲师13人,具有博士学位教师25人,占教师总数的80%。专职硕士生导师13人。教育对象总数达到988人,其中,全日制本科生312人,双学位学生602人,研究生74人。共承担国家自然科学基金、国家人文社科基金、全国教育科学规划项目、教育部人文社科项目、甘肃省社科基金项目等31项,横向项目43项。 兰州大学教育学考研备考如火如荼,考研复试分数线。不止关系着复试调剂,对于2021教育学考研人择校也有关系。为此博仁考研老师收集整理了兰州大学近3年的教育学考研分数线,仅供教育学考研学子参考。 兰州大学教育学考研近3年的考研复试分数线(兰州大学不招考教育专硕) 2020 2019 2018 教育学学硕考研50/50/155/355 50/50/150/350 50/50/150/340 2021教育学考研已经起航,你备考到哪里了呢?了解分数线后,确定了报考院校,只是第一步,随着考研时间的推进,考试有哪些科目?参考书有哪些?复习重点是什么?教育学考研真题怎么找…… 不要让这些问题成为你复习的阻碍,博仁考研老师将根据你的问题给予帮助,让考研复习事半功倍! 1
序号姓名考生编号外语能力考察 (占20%) 专业素质、综合素质 及能力考察(占 80%) 面试总成绩 复试笔 试成绩 面试+笔试初试成绩总成绩是否拟录取专业备注 1王猛10730902100158315.7565.6781.4286167.4238079.17拟录取材料工程 2雷雨田10730902100157716.1770.0086.1792178.1735378.97拟录取材料工程 3康世强10730902100162414.1769.3383.5092175.5036078.60拟录取材料工程 4杨文静10730902100155615.7566.6782.4287169.4236878.47拟录取材料工程 5周钰涵10730902100156816.2573.5089.7574163.7535178.40拟录取材料工程 6高鹏10730902100153814.5865.3379.9293172.9235877.07拟录取材料工程 7高继兵10730902100161314.8364.1779.0095174.0035576.60拟录取材料工程 8张虎山10730902100156615.2572.6787.9279166.9233376.37拟录取材料工程 9徐志彪10730902100163614.4264.3378.7588166.7535976.20拟录取材料工程10朱振兴10730902100158613.7565.0078.7595173.7535076.00拟录取材料工程11许淑容10730902100160013.8467.6681.5084165.5034775.70拟录取材料工程12卞嘉莉10730902100153913.5866.3379.9289168.9234875.67拟录取材料工程13毕鑫10730902100160514.8366.5081.3389170.3333875.23拟录取材料工程14鲁力10730902100162316.1671.6787.8397184.8329774.53拟录取材料工程15郑祖应10730902100155914.4265.1779.5883162.5833073.13拟录取材料工程16周洪宇10730902100160115.8368.1784.0088172.0030773.10拟录取材料工程17董文博10730902100161916.0065.1781.1791172.1731472.97拟录取材料工程18张可晴10730902100156915.2566.0081.2578159.2532572.80拟录取材料工程19王建军10730902100158115.8467.6683.5087170.5030472.50拟录取材料工程20陈玥10730902100160215.1662.0177.1793170.1732172.27拟录取材料工程21张乐乐10730902100163712.9259.8372.7579151.7535172.10拟录取材料工程22邵智鹏10730902100159812.4259.0071.4277148.4235071.27拟录取材料工程23郭洪州10730902100157514.5064.5079.0089168.0030771.20拟录取材料工程24杨永杰10730902100155414.8466.1681.0087168.0030071.10拟录取材料工程25蔡勇勇10730902100161711.0064.0075.0088163.0031570.30拟录取材料工程2019年物理科学与技术学院硕士研究生招生考试成绩及拟录取名单公示(一志愿)
2018年教育学考研院校汇总 听说你想报考教育学研究生却不知道有哪些院校可以报考?听说你想要了解哪些院校是211&985?听说你想报考北京的院校却不知道哪些能选择?来来来,让博仁考研老师给大家介绍一下2018年教育学考研院校。 PS:文末附赠2018年教育学考研九大牛校 招生单位名称所在地院校特性博士点 中国人民大学(11)北京市985211√ 清华大学(11)北京市985211√ 北京工业大学(11)北京市211√ 北京航空航天大学(11)北京市985211√ 北京理工大学(11)北京市985211√ 北京师范大学(11)北京市985211√ 首都师范大学(11)北京市√ 北京语言大学(11)北京市√ 中央民族大学(11)北京市985211√ 中国石油大学(北京)(11)北京市211√ 中国地质大学(北京)(11)北京市211√ 天津大学(12)天津市985211√ 天津师范大学(12)天津市√ 天津职业技术师范大学(12)天津市√ 天津体育学院(12)天津市√ 河北大学(13)河北省√ 河北科技大学(13)河北省 河北师范大学(13)河北省√ 河北科技师范学院(13)河北省 山西大学(14)山西省√ 山西师范大学(14)山西省√ 内蒙古师范大学(15)内蒙古自治区√ 大连理工大学(21)辽宁省985211√
辽宁师范大学(21)辽宁省√沈阳师范大学(21)辽宁省 渤海大学(21)辽宁省 大连大学(21)辽宁省 吉林大学(22)吉林省985211√延边大学(22)吉林省211√吉林农业大学(22)吉林省√东北师范大学(22)吉林省211√北华大学(22)吉林省 吉林师范大学(22)吉林省√长春师范大学(22)吉林省√黑龙江大学(23)黑龙江省√哈尔滨理工大学(23)黑龙江省√东北石油大学(23)黑龙江省√哈尔滨师范大学(23)黑龙江省√复旦大学(31)上海市985211√同济大学(31)上海市985211√上海交通大学(31)上海市985211√华东理工大学(31)上海市211√华东师范大学(31)上海市985211√上海师范大学(31)上海市√上海外国语大学(31)上海市211√南京大学(32)江苏省985211√苏州大学(32)江苏省211√东南大学(32)江苏省985211√南京航空航天大学(32)江苏省211√南京理工大学(32)江苏省211√中国矿业大学(32)江苏省211√南京邮电大学(32)江苏省√河海大学(32)江苏省211√江南大学(32)江苏省211√
考研过去很长时间了,突然想起来自己当初没有写过一篇像样子的考研经验贴,今天给大家分享出来,希望可以得到大家的借鉴。 政治 建议7月开始看政治,购买李凡《政治新时器》,每天看书1h左右,大概两三节的样子,同时配套做相关真题,优点是知识点比较全,讲解详细,这本书主要解决的是选择题的问题,真题的用法是反复做,做的时候不要直接把答案写上去了,可以找张纸写,第一次写可以翻书,第二次写尽量不看书,第三次写必须不能看书,每次写都把错的题目做上记号,三次下来会发现有的题目反复错,建议找一个笔记本,把相关知识点抄下来,哲学或者马政经部分答案完全看不懂,就直接把答案死背下来,政治的有些说法没有为什么,就是这样规定的,所以只能死背。第四遍,第五遍只做错题。选择题的分数决定你政治分数,大题分数大家差不多的,所以注重选择题的学习。考试的时候大题要分点作答,多角度答题,错了不扣分,字写大一点写清楚,间距注意,因为是电脑阅卷,卷面影响较大,然后尽量写满卷子。 最后,我上面说的书是我买的书,别的书我没有用过,我没有发言权。按照网上有的老师公布的答案,我的选择和主观题各拿了40分。主观题最重要的是多角度答题,有的人写了一大片,其实都是一个意思,只能得一个点的分,一个点写清楚了就不要再展开了,老师阅卷也不一定看,一般哲学是世界观加方法论加结合材料,别的科目是书上知识点加结合材料加联系实际,其实改卷子老师只看你的世界观对不对,对的就直接给分,后面应该没时间看了。务必把知识点整理成框架汇总成自己的东西,记在笔记本上,后期天天背。 英语 单词:英语是最早开始复习的一门课,从刚开始确定要考研还没确定学校的四月份就开始背英语单词。刚开始的四月到六月,用的是《一本单词》,配合它的视频完整的过了一遍这本书,说实话这本口碑很好的书确实有他的价值,在看了一遍之后对英语单词的掌握程度确实有了很大的提升,虽然本身英语基础不算好,但是对考研英语也算有了一点点自信。 七月,在刷完第二遍《一本单词》之后,还是一天不落的背单词,到十二月考试的时候这本书50个List来来回回背了8遍。我的英语成绩最后还算比较高,
兰州大学2018年工商管理硕士研究生招生简章 一、学院及项目简介 兰州大学创建于1909年,是教育部直属的全国重点综合性大学,是国家“985工程”和“211工程”重点建设高校之一,在海内外享有崇高的社会声誉和学术地位。1999年至今,先后有14位本科校友当选为两院院士。美国《科学》周刊曾评出了中国13所最杰出的大学,其中兰州大学位列第6。 兰州大学管理学院是综合性“985工程”大学中的综合型管理学院,拥有先进的学院文化和办学理念、相对齐全的管理学科、雄厚的师资力量,被誉为西部地区培养高级管理人才和学术精英的摇篮。1997年兰州大学获批开办MBA项目,同时开设MBA、国际MBA及EMBA多个项目,是中国大陆第22家、西北地区首家通过AMBA认证院校。2009-2016年连续8年荣获由诺贝尔经济学奖得主罗伯特?蒙代尔领导的世界经理人集团、《世界企业家》杂志主办的“中国最具影响力MBA排行榜”前十名!学院秉持开放办学的理念,建立了东西部合作与国际交流的机制,面向全国招生(东部生源超过60%),学生普遍具有良好的教育背景和工作经历,平均年龄31岁,平均工作经历7年以上。同时,学员在行业、专业等方面呈现多元化特点。2009年,学院与国际先进商学院合作创办国际MBA项目,接轨国际培养体制,投入全球一流商学教育师资,学员可在国内接受到国际先进的MBA教育,并可享受广泛的国际交流的机会。 二、招生计划 2018年,兰州大学工商管理硕士专业(代码:125100)分三个项目,具体招生人数以复试阶段兰州大学管理学院公布的招生计划为准: MBA项目兼收全日制、非全日制学生,招生规模参考上年度招生人数(2017年我校MBA实际录取414人,其中全日制278人,非全日制136人)。国际MBA为非全日制项目,暂定招生计划40人。EMBA为非全日制项目,暂定招生计划50人。 三、报考条件 (一)中华人民共和国公民。 (二)拥护中国共产党的领导,品德良好,遵纪守法。 (三)身体健康状况符合国家和兰州大学规定的体检要求。 (四)考生学历必须符合下列条件之一: 大学本科毕业后有3年以上(从毕业后到录取当年9月1日,下同)工作经验的人员;或获得国家承认的高职高专毕业学历后,有5年以上工作经验,达到与大学本科毕业生同等学力的人员;或已获硕士学位或博士学位并有2年以上工作经验的人员。 四、报名
(一)报考条件: 根据文件规定,兰州大学硕士研究生,本次考试选拔对象,应符合以下条件: 1.在校期间政治思想表现优秀,遵守校纪校规,文明礼貌,未受到任何处分。 2.学历要求:本科(或专科毕业两年),无重考,无重修记录,身心健康。 3.平时必修课程和限选课程学习成绩优秀和综合素质好。 4.以综合考试成绩为录取依据,首先按各专业实考人数划定分数资格线,再按成绩从高到低择优录取。 5.综合考试成绩将在录取前公示7天,录取过程中,如果有排名在录取名额内的考生自愿放弃,在名额外的学生按顺序递补。 (二)报考事项: 历年真题QQ在线咨询:363、916、816张老师。学校各相关学院成立工作小组,确定工作中的相关原则政策和办法研究重大事项;负责本学院考试工作的组织宣传事项和实施工作;完成报考成绩的统计及综合排名汇总材料并上报填表。 1.各学院要先完成报考专业的成绩进行排名,根据名单确定考生的具体范围。 2.符合上述条件的参加综合考试,根据报考专业并提交书面申请材料审核。 3.工作领导小组审核汇总名单后,将公示7天,期满后不再提示。 4.各相关专业按照考试科目的顺序依次进行。
5.考试成绩以书面通知形式发到学生本人。 (三)考试流程: 1.参加初试并获得复试资格的考生,应在复试前填写相关表格,按规定时间提供自身研究潜能的材料,攻读研究生阶段的研究计划、科研成果等。 2.报考考生的资格审查由领导小组进行审查,对考生料进行审阅符合报考条件的考生统计填表。 3.我校采取笔试、口试或两者相兼的方式进行差额复试,以进一步安排加强进行考察学生的专业基础、综合分析能力、解决实际问题的能力和各种应用能力等。具体比例由学校根据本学科、专业特点及生源状况安排。 (四)复习方略: 1.注重课本很多考生会安排各种各样的资料,其实关键要能保证你进行的系统性。因此整个阶段应该以教材为主,以精读的方式对教材重点章节相关要点,对课本有一个纲领性的认识。对课后题必须要掌握,很多知识点题都出自课后。加强相关科目关联性进行统筹考核安排。较为系统的了解都要以记忆为基础一定要做到对书的大体框架有全面的把握,把整个原理的前后概念贯穿起来。 2、在复习充分的情况下做完后对照答案进行对比,看看自己的差距在哪。接下来才是最重要的,你要了解往年的真题都会出什么题型,总结其考察重点是什么是哪一章节。整体掌握知识范围,一定要必须的题目都整理出来行理解背诵。为什么要这样做呢,因为通常前几年出现的题目会出现,根据相关专业考核对照问题的深度和广度,结合自己的知识结构知识存量,正确的安排答题技巧针对有限的知识来最好地回答。专业课的难度绝不亚于英语,往往在侧重点上、宣传上策
教育学考研到底哪个专业方向更适合你 作为教育学门类下的一级学科的教育学,究竟有哪些学科可供我们准备教育学考研的小可爱们进行选择呢?什么样的专业方向更适合你呢?今天就带各位学霸从各个专业的就业前景的方向上带大家看看,哪个专业更适合你! 课程与教学论就业前景 随着国家对文化教育事业的重视就业前景会更加广阔。近年来,同不少专业的大学毕业生比较严峻的就业形势相比,师范类毕业生的就业呈现出供不应求且经年不衰的可喜局面。这是因为我国教育事业相对落后,教育人才本来就比较缺乏。而目前,教育事业的迅速发展,更是给师范毕业生带来广阔的就业市场。从已经毕业的研究生就业去向来看,课程与教学论研究方向的研究生就业前景相对较好。 就业方向: 本专业毕业生可在基础教育教学和研究机构、各级各类教育培训机构、教育合作与交流机构从事相关教学、科研与各类课程的教学工作和管理工作。 课程与教学论考研实力院校推荐: 北京师范大学,西南大学,华东师范大学,西北师范大学,首都师范大学,东北师范大学,华中师范大学,华南师范大学,上海师范大学,四川师范大学,湖南师范大学,辽宁师范大学,南京师范大学,沈阳师范大学,山东师范大学,扬州大学等。 高等教育学就业方向 但在人们传统的思维中,教育学的就业方向主要是去学校做老师,事实上有相当一部分教育学专业毕业的学生毕业后并没有从事教书行业。下面梳理了教育学的六大从业方向。 1、普通高校,这是教育学原理、教育史、高等教育学、比较教育学、教育哲学等理论性比较强的专业的主要的去向,但现在硕士生进高校越来越难,基本上都要求博士学历,所以想考这些方向的研究生想去高校就要做好读博士的准备了。 2、出版社、报社,出版社、报社尤其是和教育相关的出版社和报社也是教育类专业毕业生的一个主要去处,主要从事教育类图书的策划和编辑工作。 3、政府单位,还有一些毕业生毕业后参加公务员考试进入了教育行政单位,但要求教育类专业的公务员招考很少,想当公务员的同学可以努力一把,但要做好心理准备,因为竞争的激烈程度会超乎你的想象。 4、中小学校,现在全国中小学校的新课程改革开展得轰轰烈烈,具有较强教育理论素养的人才特别缺乏,而且随着中小学教师待遇的不断提高,再加上教师这个职业本身比较稳定,越来越多教育类专业尤其是课程与教学论的硕士毕业生开始进入中小学校,今年还出现了南京某中学几百个硕士竞争两个岗位的现象。
我的考研之路各科复习还算是比较轻松的,下面把考研复习方法分享给大家。 政治的复习,我只跟随李凡老师,用的李凡《政治新时器》一套材料,几个复习注意点和大家说下: 1、选择题是不是决定性的,这个问题我个人觉得差不多是的,因为政治这个学科具有这样的特殊性,选择题确实拿分较大题容易,复习好了拿个40分的确不是很难,而大题不确定性较大,投入产出比也比选择题要小。既然如此,就当它是对的吧,选择题把握好,该拿的分到手,大题稳扎稳打,分数应该就很可观了。 2、一定要灵活。政治真的不像普遍认为的那样死板、背就好了,掌握一些技巧可以为自己省下很多时间,一定要在一些问题上灵活处理,低头死记硬背,很可能出力不讨好,别干傻事。比如某些章节里的一些事,你一个字不看我也包你没事,你说对吧。 3、各科目的策略。马哲主要靠理解,政经理解也很重要,尤其是一些计算的选择题,不理解真的没法做,而科社最好是结合着毛概来看。毛概是重中之重,看比例就知道,毛概加史纲就是史论结合,一定不要割裂开来看,尤其是史纲那个大题,终归还是要靠到毛概上去理解,孤立开搞不清的。至于思修法基,思修主要就是记忆,对于不学法律的同学还是好好啃下来吧,这样的分不难拿,丢不起。 英语前期我是看的《一本单词》,每天背单词,单词一定要大量的背诵,直到考试前一天都一直要背。单词是基础,地基不劳,地动山摇。 暑假的时候听蛋核英语的阅读课程,里面还是有挺多技巧的,到后来做题多了会越来越得心应手。同时进行阅读翻译,一开始翻译的时候写的乱七八糟,后来到40篇的时候就知道出题点在哪里了,等到翻译大题的时候就不需要做太多题了,一举两得。建议阅读直接就做真题的,我用的《木糖英语真题手译版》就很不错。 作文背背真题的大作文10篇,小作文10篇,自己再总结个模板,总结模板的时候记得多参考几个名师的作文,不要生搬硬套,要灵活变通,否则有抄袭嫌疑。有时间每天可以利用吃饭的工夫刷刷手机,看看木糖英语和蛋核英语公众号里的推文哦。