
班级姓名
第一章原子结构与元素周期律
第一节原子结构(第1课时)
【学习目标】
1.掌握原子的结构和组成,熟练掌握原子中各组成微粒之间的数量关系。
2.会表示原子的组成,明确表示式中各数字的含义,明确核素、同位素、元素的区别和
联系,了解同位素的应用。
【重点难点】原子中各组成微粒之间的数量关系;核素与元素的关系。
一、原子核(阅读课本第3页,完成下列内容)
1.原子的构成
2.原子内的等量关系
(1)质子数==。
(2)质量数=+。
【思考】1.原子为什么不显电性?离子呢?离子带电荷是什么原因?完成下表。
3.离子内的等量关系
(1)阳离子的核外电子数=质子数-。
(2)阴离子的核外电子数=质子数+。
【思考】2.有6个质子6个中子的原子质量数是;某种氧原子含有8个中子其质
量数是 ,要是有10个中子呢 ?
4.原子的表示 :通常用 X A
Z 表示一个原子,A 表示 Z 表示 。
【思考】3.完成下表。
表中的氧-16与氧-18是同样的原子吗?他们之间又是什么关系?
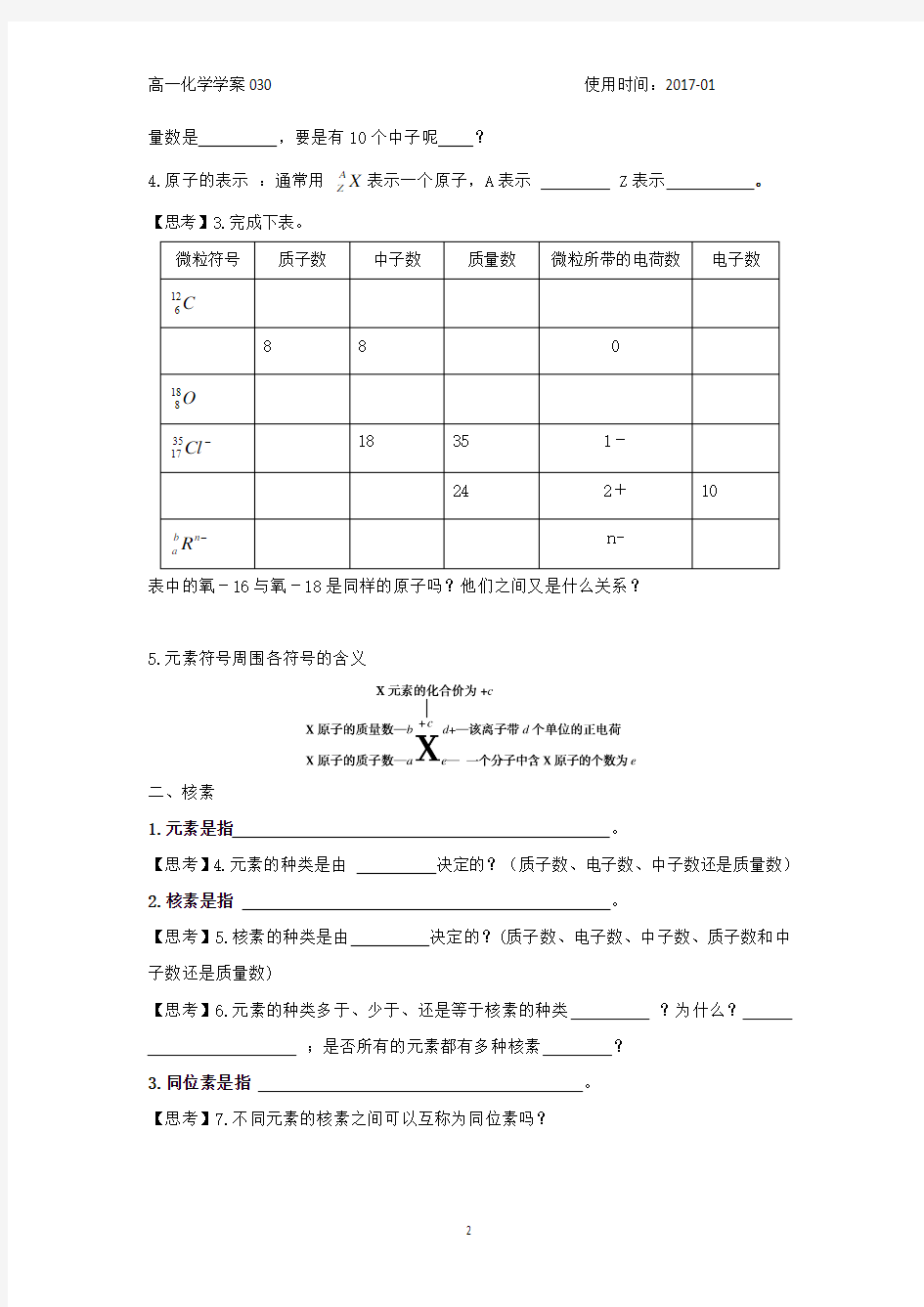
5.元素符号周围各符号的含义
二、核素
1.元素是指 。
【思考】4.元素的种类是由 决定的?(质子数、电子数、中子数还是质量数) 2.核素是指 。
【思考】5.核素的种类是由 决定的?(质子数、电子数、中子数、质子数和中子数还是质量数)
【思考】6.元素的种类多于、少于、还是等于核素的种类 ?为什么? ;是否所有的元素都有多种核素 ? 3.同位素是指 。 【思考】7.不同元素的核素之间可以互称为同位素吗?