
第七章络合滴定法练习题
1. EDTA二钠盐的水溶液的pH的最简式是()(EDTA相当于六元酸)
2. 络合滴定中一般不使用EDTA而用EDTA二钠盐(Na2H2Y), 这是由于(); 当在强酸性溶液中(pH<1),EDTA为六元酸, 这是因为()。
3.直接与金属离子配位的EDTA型体为()
(A)H6Y2+(B)H4Y (C)H2Y2-(D)Y4-
4. 指出下列EDTA络合物的颜色(填A,B,C,D)
(1) CuY2- ________ (A)无色
(2) MnY2- ________ (B)紫红色
(3) FeY-________ (C)黄色
(4) ZnY2- _______ (D)蓝色
5.一般情况下,EDTA与金属离子形成的络合物的络合比是()
(A)1:1 (B)2:1 (C)1:3 (D)1:2
6. 金属离子M与络合剂L形成逐级络合物, 溶液中各种存在型体的分布系数与络合剂的平衡浓度(); 与金属离子的总浓度()。(答有关或无关)
7. 已知乙酰丙酮(L)与Al3+络合物的lgβ1-lgβ3分别是8.6、15.5和21.3, 则AlL3为主要形式时的pL范围是(),pL为10.0时铝的主要形式是(),则[AlL]与[AlL2]相等时的pL值为()
8. 磺基水杨酸(L)与Cu2+络合物的lgβ1为9.5, lgβ2为16.5,[CuL]达最大的pL 为( )
(A) 9.5 (B) 16.5 (C) 7.0 (D) 8.3
9.αM(L)=1表示()
(A)M与L没有副反应(B)M与L的副反应相当严重
(C)M的副反应较小(D)[M]=[L]
10. 若络合滴定反应为
M + Y = MY
L│ │H+
ML H i Y(i=1~6)
则酸效应系数αY(H)的定义式为(),[Y']=()c(Y)=()。络合效应系数αM(L)的定义式为()。
11. 若EDTA滴定M反应为
M+Y=MY
↓A
MA
以下表示正确的是( )
(A) c(M)=[M']+[MY] (B) c(M)=[M]+[M']+[MY]
(C) c(M)=[MA]+[MY] (D) c(M)=[M]+[MA]
12. 用EDTA滴定金属M, 若M分别与A,B,C三者发生副反应,此时计算αM的公式是αM = (αM(A)+αM(B)+αM(C)-2 )。
13. 在一定酸度下,用EDTA滴定金属离子M。当溶液中存在干扰离子N时, 影响络合剂总副反应系数大小的因素是( )
(A) 酸效应系数αY(H)
(B) 共存离子副反应系数αY(N)
(C) 酸效应系数αY(H)和共存离子副反应系数αY(N)
(D) 络合物稳定常数K(MY)和K(NY)之比值
14. 指出下列叙述中错误的结论( )
(A) 络合剂的酸效应使络合物的稳定性降低
(B) 金属离子的水解效应使络合物的稳定性降低
(C) 辅助络合效应使络合物的稳定性降低
(D) 各种副反应均使络合物的稳定性降低
15. 在pH为10.0的氨性溶液中, 已计算出αZn(NH3)=104.7, αZn(OH)=102.4, αY(H)=100.5。则在此条件下lg K'(ZnY)为( )
[已知lg K(ZnY)=16.5]
(A) 8.9 (B) 11.8 (C) 14.3 (D) 11.3
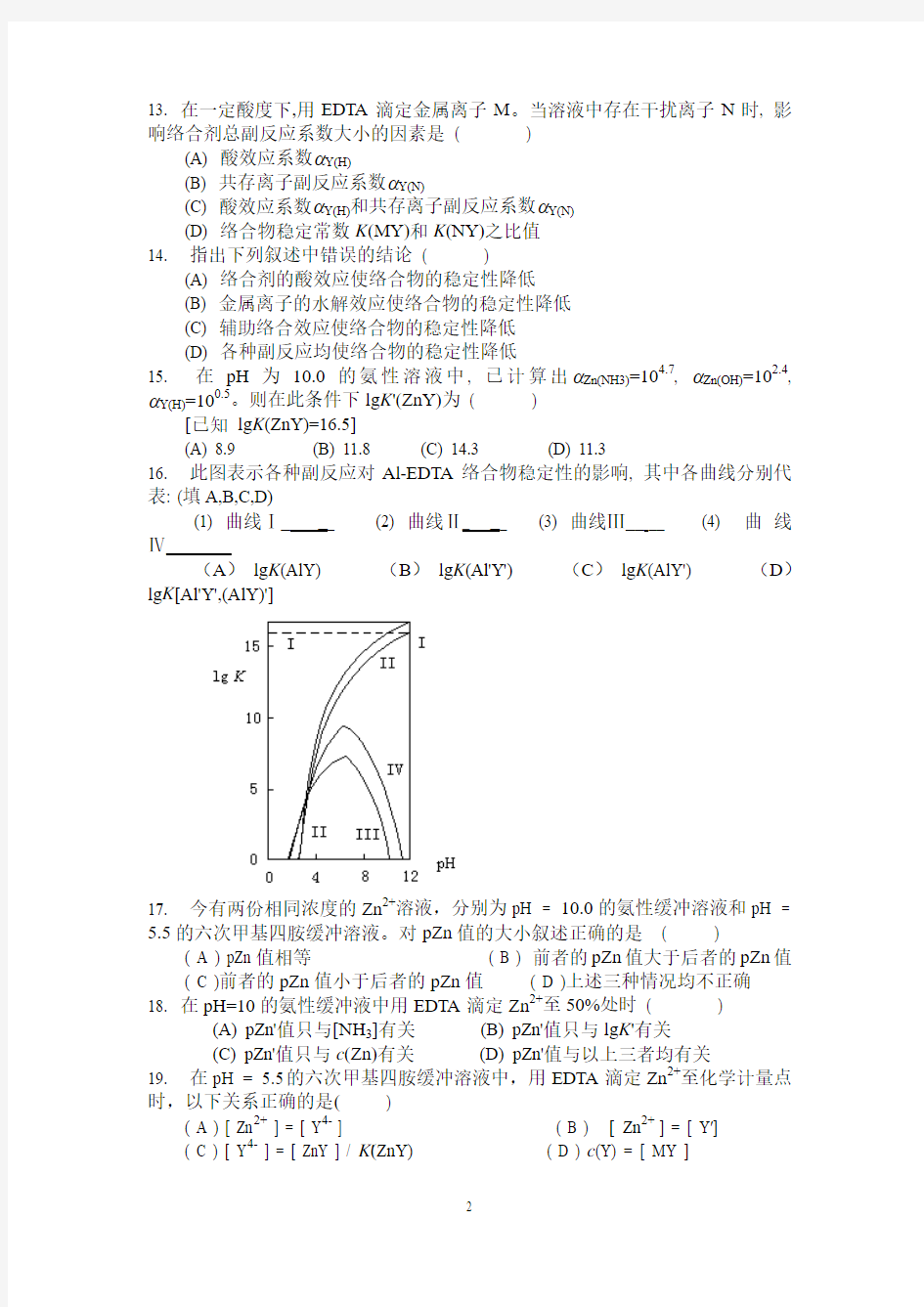
16. 此图表示各种副反应对Al-EDTA络合物稳定性的影响, 其中各曲线分别代表: (填A,B,C,D)
(1) 曲线Ⅰ___ (2) 曲线Ⅱ_ __ (3) 曲线Ⅲ____ (4) 曲线Ⅳ_
(A)lg K(AlY) (B)lg K(Al'Y') (C)lg K(AlY') (D)lg K[Al'Y',(AlY)']
17. 今有两份相同浓度的Zn2+溶液,分别为pH = 10.0的氨性缓冲溶液和pH = 5.5的六次甲基四胺缓冲溶液。对pZn值的大小叙述正确的是( )
( A ) pZn值相等( B ) 前者的pZn值大于后者的pZn值( C )前者的pZn值小于后者的pZn值( D )上述三种情况均不正确
18. 在pH=10的氨性缓冲液中用EDTA滴定Zn2+至50%处时( )
(A) pZn'值只与[NH3]有关(B) pZn'值只与lg K'有关
(C) pZn'值只与c(Zn)有关(D) pZn'值与以上三者均有关
19. 在pH = 5.5的六次甲基四胺缓冲溶液中,用EDTA滴定Zn2+至化学计量点时,以下关系正确的是()
( A ) [ Zn2+ ] = [ Y4- ] ( B ) [ Zn2+] = [ Y′]
( C ) [ Y4- ] = [ ZnY ] / K′(ZnY) ( D ) c(Y) = [ MY ]
20. 在pH=5.0的醋酸缓冲液中用0.002 mol/L的EDTA 滴定同浓度的Pb2+。已知: lg K(PbY)=18.0, lgαY(H)=6.6, lgαPb(Ac)=2.0, 化学计量点时溶液中pPb'应为( )
(A) 8.2 (B) 6.2 (C) 5.2 (D) 3.2
21. 在pH=10的氨性缓冲液中以EDTA滴定Zn2+至150%处时()
(A) pZn'只决定于lg K(ZnY) (B) pZn'只决定于lg K'(ZnY)
(C) pZn'只决定于c(Y) (D) pZn'与lg K'(ZnY)、c(Y)均有关
22. 在含有NH3-NH4Cl的pH=10.0的介质中, 以0.0200 mol/L EDTA 溶液滴定20.0 mL 0.0200 mol/L Zn2+溶液, 当加入40.0 mL EDTA溶液时, 在下列叙述中, 正确的是( )
(A) pZn'=lg K'(ZnY) (B) lg[Zn']=lg K ZnY
(C) lg[Zn']=lg K'(ZnY) (D) 都不正确
23. 以EDTA溶液滴定同浓度的某金属离子, 若保持其它条件不变, 仅将EDTA 和金属离子浓度增大10倍, 则两种滴定中pM值相同时所相应的滴定分数是( )
(A) 0% (B) 50% (C) 100% (D) 150%
24. 含有同浓度的Mg2+溶液A、B两份。A溶液的pH = 10.0,其中游离氨的浓度为0.1 mol /L;B溶液的pH = 9.5,其中游离氨的浓度为0.02 mol / L。今以等
的大小叙述正确的是浓度的EDTA溶液滴定上述溶液至化学计量点时。对pY'
计
()
( A ) A溶液的pY'计和B溶液的pY'计相等( B ) A溶液的pY'计比B溶液的pY'计大
( C ) A 溶液的pY'计比B溶液的pY'计小( D ) 不能确定
25. 在pH为10.0的氨性缓冲液中, 以0.01 mol/L EDTA 滴定同浓度Zn2+溶液两份。其中一份含有0.2 mol/L 游离NH3; 另一份含有0.5 mol/L 游离NH3。在上述两种情况下, 对pZn'叙述正确的是( )
(A) 在化学计量点前pZn'相等(B) 在化学计量点时pZn'相等
(C) 在化学计量点后pZn'相等(D) 在上述三种情况下pZn'都不相等
26. EDTA滴定金属离子时, 若仅浓度均增大10倍, pM突跃改变( )
(A) 1个单位(B) 2个单位(C) 10个单位(D) 不变化
27. EDTA滴定中, 介质pH越低, 则αY(H)值越____, K'(MY)值越____, 滴定的pM'突跃越____,化学计量点的pM'值越____。
28. 根据下表所给数据推断用EDTA滴定Ca2+(溶液的pH=13)时表中各点的pCa
29.
30. 试给出铬黑T用于EDTA滴定Mg2+的条件和现象
-H+-H+
H2In-HIn2-In3-
p K a1 =6.3 p K a2 =11.6
红色(_色) 橙色
+
Mg2+
|| pH=__
MgIn+Mg2+(_色)
|| +Y
MgY+HIn (终点__色)
31. 铬黑T指示剂在pH=8~11范围使用,其目的是为减少干扰离子的影响()。
32. 铬黑T(EBT)是有机弱酸,其p K a2=6.3,p K a3=11.6,Mg2+-EBT的lg K稳=7.0。在pH=10时, lg K'(Mg-EBT)的值是( )
(A) 6.4 (B) 5.4 (C) 4.4 (D) 7.0
33.配位滴定中,指示剂的封闭现象是由()引起的
(A)指示剂与金属离子生成的络合物不稳定
(B)被测溶液的酸度过高
(C)指示剂与金属离子生成的络合物稳定性小于MY的稳定性
(D)指示剂与金属离子生成的络合物稳定性大于MY的稳定性
34. 造成金属指示剂封闭的原因是指示剂本身不稳定()。
35.产生金属指示剂的僵化现象是因为()
(A)指示剂不稳定(B)MIn溶解度小(C)KˊMIn < KˊMY (D)KˊMIn > KˊMY
36. 金属指示剂的僵化现象是指滴定时终点没有出现( )。
37. 铬黑T指示剂常配成固体试剂而不是水溶液,其原因是_ _, 加入NaCl的目的是__ __。
38.金属指示剂PAN 在溶液中有如下平衡:
p K a1=1.9 p K a2=12.2
H2In+HIn In-
黄绿黄粉红
它与金属离子形成的络合物MIn为红色, 当使用PAN作指示剂时, pH范围应是( )。
若使用PAN-Cu指示剂以EDTA溶液滴定Ca2+, 化学计量点前溶液是( )颜色, 化学计量点后溶液呈( )颜色。
39. 在pH=10的氨性缓冲溶液中,以铬黑T(EBT)为指示剂, 用EDTA溶液滴定Ca2+时,终点变色不敏锐, 此时可加入少量( )作为间接金属指示剂, 在终点前溶液呈现( )色, 终点时溶液呈现( )色。
40. 在某一pH下,以2.0×10-4mol/L EDTA滴定2.0×10-4mol/L金属离子M, 设其条件稳定常数lg K'(MY)=10.0, 检测终点时的 pM=0.40, 则E t为( )%。41.配位滴定中加入缓冲溶液的原因是()
(A)EDTA配位能力与酸度有关(B)金属指示剂有其使用的酸度范围
(C)EDTA与金属离子反应过程中会释放出H+(D)K MY’会随酸度改变而改变
42. EDTA的酸效应曲线是()的关系曲线。
43.实际测定某金属离子时,应将pH控制在大于()且()的范围之内。
44. 络合滴定中,溶液的最佳酸度范围是由EDTA决定的()。
45. 在配位滴定中, 若溶液的pH值高于滴定M的最小pH值, 则无法准确滴定( )。
46. EDTA滴定某金属离子有一允许的最高酸度(pH值),溶液的pH再增大就不能准确滴定该金属离子了()。
47.在配位滴定中,直接滴定法的条件包括( )
(A)lgC M,sp K MY’≤8 (B)溶液中无干扰离子
(C)有变色敏锐无封闭作用的指示剂(D )反应在酸性溶液中进行
48.铝盐药物的测定常用配位滴定法。加入过量EDTA, 加热煮沸片刻后,再用标准锌溶液滴定。该滴定方式是()。
(A)直接滴定法(B)置换滴定法
(C)返滴定法(D)间接滴定法
49. EDTA滴定Al3+,Zn2+,Pb2+混合液中的Al3+应采用( )
(A) 直接滴定法(B) 回滴法(C) 置换滴定法(D) 间接法
50. 已知Ag+, Ni2+ 与EDTA络合物的稳定常数分别为lg K(AgY)=7.8, lg K(NiY)=18.6, Ag+-CN- 络合物的lgβ2=21.1, Ni2+-CN络合物的lgβ4=31.3。于含Ag+的试液中加入过量Ni(CN)42-络合物,然后在pH=10的缓冲溶液中以EDTA溶液滴定置换出的Ni2+量。在上述置换反应中,Ag+与Ni2+的物质的量之比n(Ag) : n(Ni)为( )。
51.若以金属锌为基准物, 以铬黑T为指示剂标定EDTA, 而配制此EDTA的水中含有少量Ca2+, 用此标定后的EDTA测定CaCO3试剂的纯度, 其结果将( )。(指偏高, 低或无影响)
络合滴定法 一、填空题 1. 采用EDTA为滴定剂测定水的硬度时,因水中含有少量的Fe3+, Al 3+。应加入作掩蔽剂; 滴定时控制溶液PH = 。 2. 以铬黑T为指示剂,溶液pH值必须维持;滴定到终点时溶液由色变为色。 3. EDTA的酸效应曲线是指,当溶液的pH越大,则越小。 4. EDTA滴定金属M时, 若?pM'=±0.2, 则要求lg[c(M计)K'(MY)]大于_______, 才能使滴定的终点误差小于0.1% 。 5. 用EDTA滴定金属离子M,若浓度增大10倍,突越大小变化为______ 。 6. 用EDTA滴定金属离子M和N的混合溶液时,已知αY(N)>αY(H),当被测离子M的浓度为干扰离子N浓度的10倍时, 欲采用控制酸度滴定 M 离子, 要求E t≤0.1%, ?pM=±0.20, 则lgK(MY)-lgK(NY)应____。 7. 在非缓冲溶液中,用EDTA滴定金属离子时溶液的pH值将升高、降低还是不变?_______。 8. 当M与Y反应时,溶液中有另一络合剂L存在,若αM(L)=1表示________。 9. 在pH=10.0的氨性溶液中,已计算出αZn(NH 3)=10 4.7, αZn(OH)=102.4,αY(H)=100.5,已知lgK ZnY=16.5;在此条件下, lgK’ZnY为___________。
10. 乙酰丙酮与Fe3+络合物的逐级累积稳定常数lgβ1~lgβ3分别为 11.4、22.1、26.7,则稳定常数lg K2=___ 不稳定常数lg K不(3)=__ __。 11. 在pH=5.0的醋酸缓冲溶液中用0.002 mol/L EDTA滴定同浓度的Pb2+,今知lg K(PbY) = 18.0, lgαY(H)=6.6,lgαPb(Ac)=2.0。则化学计量点时pPb'=___ ___ 。 二.选择题 1.EDTA的酸效应曲线是指---------------------------------------------------( ) (A) αY(H)-pH 曲线(B) pM-pH 曲线 (C) lg K'(MY)-pH 曲线(D) lgαY(H)-pH 曲线 2. 已知Ag+-S2O32-络合物的lgβ1~lgβ3分别是9.0,1 3.0,1 4.0。以下答案不正确的是---( ) (A) K1=109.0(B) K3=101.0 (C) K不(1)=10-9.0(D) K不(1)=10-1.0 3. 为了测定水中Ca2+,Mg2+的含量,以下消除少量Fe3+、Al3+干扰的方法中,哪一种是正确的?------------------------------------------( ) (A) 于pH=10的氨性溶液中直接加入三乙醇胺; (B) 加入三乙醇胺不需要考虑溶液的酸碱性。 (C) 于酸性溶液中加入KCN,然后调至pH=10; (D) 于酸性溶液中加入三乙醇胺, 然后调至pH=10的氨性溶液; 4. Fe3+,Al3+对铬黑T有-------------( )
第5章配位滴定法习题答案 1.EDTA与金属离子的配位反应有何特点? 答:广泛,EDTA几乎能与所有的金属离子形成络合物;稳定,一般lg K MY> 15; 络合反应速度快,水溶性好;EDTA与无色的金属离子形成无色的络合物,与有色的金属离子形成颜色更深的络合物;络合比简单,一般为1:1。 2. EDTA与金属离子配合物的稳定常数与条件稳定常数有什么不同?影响条件稳定常数大小的因素有哪些? 答:在无副反应存在的情况下用平衡常数来衡量反应进行的程度,在有副反应存在的情况下用条件平衡常数来衡量反应进行的程度;响条件稳定常数大小的因素有:酸效应、配位效应、干扰离子效应等。 3. 影响配位滴定图月范围大小的因素有哪些?是怎样影响的? 答:(1)lg K′的影响:K′增大10倍,lg K′增加1,滴定突跃增加一个单位。 (2)C M的影响:C M增大10倍,滴定突跃增加一个单位。 4. 为什么大多数的配位滴定需要在一定的缓冲溶液中进行? 答:络合滴定中广泛使用pH缓冲溶液来保持酸度相对稳定,因为:(1)滴定过程中的[H+]变化:M + H2Y = MY + 2H+ (2)K′MY与pH有关; (3)指示剂需在一定的酸度介质中使用 5. 金属指示剂的作用原理是什么?应当具备的主要条件是什么? 答:金属指示剂本身是弱的配位剂,在一定条件下,指示剂与金属离子形成有一定稳定性的配合物,该配合物与指示剂本身具有显著不同的颜色。 6. 指示剂为什么会被封闭?如何消除? 答:指示剂的封闭现象是指某些指示剂能与某些金属离子生成极为稳定的络合物,这些络合物较对应的MY络合物更稳定,以致到达化学计量点时滴入过量的EDTA,也不能夺取指示剂络合物(MIn)中的金属离子,指示剂不能释放出来,看不到颜色的变化,这种现象就叫指示剂的封闭现象。 可能原因:(1)MIn(或共存离子N的NIn)的稳定性大于MY。 (2)终点变色反应的可逆性差。 解决方法:(1)若封闭现象是滴定离子本身M引起的,则可采用返滴定法。例二甲酚橙XO,Al3+对其有封闭现象。可加过量EDTA,采用返滴法测定铝。
第6章 络合滴定法 2. 在PH=9.26的氨性缓冲溶液中,除氨络合物外的缓冲剂总浓度为0.20 mol ·L -1,游离C 2O 42-浓度为0.10 mol ·L -1。计算Cu 2+的αCu 。已知Cu(Ⅱ)- C 2O 42-络合物的lg β1=4.5,lg β2=8.9; Cu(Ⅱ)-OH -络合物的lg β1=6.0。 解: 3.铬黑T(EBT)是一种有机弱酸,它的lgK 1H =11.6,lgK 2H =6.3,Mg-EBT 的lgK MgIn =7.0,计算在PH=10.0时的lgK ’MgIn 值。 22433222 124224() 4.58.92 6.96.09.2614 1.26 1()14333()1321[][] 100.1010(0.10)101[]1101010[][]112[]0.10[][]1[][Cu C O Cu OH NH Cu NH C O C O OH C NH H NH mol L NH NH Ka NH N αββαβαββ------++ -=++=?+?==+=+?==+=+=?=??=++又23 24 259.35 3539.36 ()()()][]1010Cu Cu NH Cu C O Cu OH H NH βαααα-- ++=≈++=
4. 已知M(NH 3)42+的lg β1~ lg β4为2.0, 5.0,7.0,10.0,M(OH)42-的lg β1~ lg β4为4.0,8.0,14.0,15.0。在浓度为0.10 mol ·L -1的M 2+溶液中,滴加氨水至溶液中的游离NH 3浓度为0.010 mol ·L -1,PH=9.0试问溶液中的主要存在形式是那一种?浓度为多大?若将M 2+离子溶液用NaOH 和氨水调节至PH ≈13.0且游离氨浓度为0.010 mol ·L -1 ,则上述溶液中的主要存在形式是什麽?浓度又为多少? 解:用氨水调解时: 32()121(0.010)(0.010)122 M NH αββ=+++= 3 2.0 2.0 131()[]10100.0083 122 M NH NH βδα-?=== 32 5.0 4.0 232()[]10100.083 122 M NH NH βδα-?=== 7.0 6.0310100.083122δ-?== 10.08.0 410100.83 122δ-?== 故主要存在形式是M(NH 3)42+ ,其浓度为0.10×0.83=0.083 mol ·L -1 用氨水和NaOH 调节时: 34811 ()()11100.1100.01120210M M NH M OH ααα-=+-=+?+?++=? 49111100.1510210δ-?==?? 86 2 11100.01510210δ-?==?? 14311100.0010.5210δ?==? 15411 100.00010.5210δ?==? 故主要存在形式是M(OH)3-和M(OH)42-,其浓度均为0.050 mol ·L -1 5. 实验测得0.10 mol ·L -1Ag(H 2NCH 2CH 2NH 2)2+溶液中的乙二胺游离浓度为0.010mol ·L -1。计算溶液中C 乙二胺和δAg(H 2NCH 2CH 2NH 2)+ 。Ag +与乙二胺络合物的lg β1=4.7,lg β2=7.7。 解: 2 2 2 2 ()12222222224.77.723.74 1[][]11010(0.010)10Ag H NCH NH H NCH CH NH H NCH CH NH αββ=++=++?= 2 2 2 2 2 22.70 ()() 10 0.091 Ag H NCH NH Ag H NCH NH δα= =
第七章氧化还原滴定 1.条件电位和标准电位有什么不同?影响电位的外界因素有哪些? 答:标准电极电位E′是指在一定温度条件下(通常为25℃)半反应中各物质都处于标准状态,即离子、分子的浓度(严格讲应该是活度)都是1mol/l(或其比值为1)(如反应中有气体物质,则其分压等于1.013×105Pa,固体物质的活度为1)时相对于标准氢电极的电极电位。 电对的条件电极电位(E0f)是当半反应中氧化型和还原型的浓度都为1或浓度比为,并且溶液中其它组分的浓度都已确知时,该电对相对于标准氢电极电位(且校正了各种外界因素影响后的实际电极电位,它在条件不变时为一常数)。由上可知,显然条件电位是考虑了外界的各种影响,进行了校正。而标准电极电位则没有校正外界的各种外界的各种因素。 影响条件电位的外界因素有以下3个方面; (1)配位效应; (2)沉淀效应; (3)酸浓度。 2.是否平衡常数大的氧化还原反应就能应用于氧化还原中?为什么? 答:一般讲,两电对的标准电位大于0.4V(K>106),这样的氧化还原反应,可以用于滴定分析。 实际上,当外界条件(例如介质浓度变化、酸度等)改变时,电对的标准电位是要改变的,因此,只要能创造一个适当的外界条件,使两电对的电极电位超过0.4V ,那么这样的氧化还原反应也能应用于滴定分析。但是并不是平衡常数大的氧化还原反应都能应用于氧化还原滴定中。因为有的反应K虽然很大,但反应速度太慢,亦不符合滴定分析的要求。 3.影响氧化还原反应速率的主要因素有哪些? 答:影响氧化还原反应速度的主要因素有以下几个方面:1)反应物的浓度;2)温度;3)催化反应和诱导反应。 4.常用氧化还原滴定法有哪几类?这些方法的基本反应是什么? 答:1)高锰酸钾法.2MnO4+5H2O2+6H+==2Mn2++5O2↑+8H2O. MnO2+H2C2O4+2H+==Mn2++2CO2+2H2O 2) 重铬酸甲法. Cr2O72-+14H++Fe2+===2Cr3++Fe3++7H2O CH3OH+Cr2O72-+8H+===CO2↑+2Cr3++6H2O 3)碘量法3I2+6HO-===IO3-+3H2O, 2S2O32-+I2===2I-+2H2O Cr2O72-+6I-+14H+===3I2+3Cr3++7H2O 5.应用于氧化还原滴定法的反应具备什么条件? 答:应用于氧化还原滴定法的反应,必须具备以下几个主要条件: (1)反应平衡常数必须大于106,即△E>0.4V。 (2)反应迅速,且没有副反应发生,反应要完全,且有一定的计量关系。 (3)参加反应的物质必须具有氧化性和还原性或能与还原剂或氧化剂生成沉淀的物质。 (4)应有适当的指示剂确定终点。 6.化学计量点在滴定曲线上的位置与氧化剂和还原剂的电子转移数有什么关系? 答:氧化还原滴定曲线中突跃范围的长短和氧化剂与还原剂两电对的条件电位(或标准电位)相差的大小有关。电位差△E较大,突跃较长,一般讲,两个电对的条件电位或标准电位之差大于0.20V时,突跃范围才明显,才有可能进行滴定,△E值大于0.40V时,可选用氧化还原指示剂(当然也可以用电位法)指示滴定终点。 当氧化剂和还原剂两个半电池反应中,转移的电子数相等,即n1=n2时,则化学计量点的位
第三章 络合滴定法习题 一、填空题 1、在L m o l ??-3100.1铜氨溶液中,其中游离氨的浓度为L mol ??-2104.1。平衡时 ] )([243 + NH Cu = 1 -?L mol ,] )([233 + NH Cu = 1 -?L mol 。 (3 2NH Cu -+ 络合物的4 1lg ~lg ββ分别为4.30,8.0,11.0,13.3)。 2、二甲酚橙为一有机弱酸,在pH=5.0的缓冲介质中,) (XO ep pPb 为 。(XO 的3 .6=pKa ,3.8lg =-XO Pb K ) 3、某溶液含有M 和N 离子,且NY MY K K lg lg >>。MY K 'lg 先随溶液pH 增加而增 大,这是由于 。然后当pH 增加时,MY K 'lg 保持在某 一定值(N 在此条件下不水解),这是因为 。 4、在含有+ 2Zn 和+ 3Al 酸性混合溶液中,欲在pH=5~5.5的条件下,用EDTA 标 准溶液滴定其中的+ 2Zn 。加入一定量的六亚甲基四胺的作用是 ; 加入F NH 4 的作用是 。 5、在pH=5.0的- -Ac HAc 缓冲介质中,以EDTA 滴定+ 2Pb 至化学计量点时,当 溶液中 - Ac 浓度增大时,sp b pP '和 sp pPb 值的变化情况是:sp b pP ' ; sp pPb 。 6、采用EDTA 为滴定剂测定水的硬度时,因水中含有少量的+3Fe ,+ 3Al 。应加 入 作掩蔽剂;滴定时控制溶液pH= 。 7、EDTA 的酸效应曲线是指 ,当溶液的pH 越大,则 越小。 二、选择题 1、EDTA 的6 1 ~pKa pKa 分别为:0.9,1.6,2.0,2.67,6.16,10.26。今在pH=13时,以 EDTA 滴定同浓度的Ca 2+。以下叙述正确的是:( ) A 、滴定至50%时,pCa=pY ; B 、滴定至化学计量点时,pCa=pY ; C 、滴定至150%时,pCa=pY ; D 、以上说法都不正确。 2、当金属离子M 和N 共存时,欲以EDTA 滴定其中的M ,若N M c c 10=,TE=0.1%, 2 .0=?pM 。则要求K lg ?的大小是多少?( )
第6章 络合滴定法 2. 在PH=9.26的氨性缓冲溶液中,除氨络合物外的缓冲剂总浓度为0.20 mol·L -1 ,游离C 2O 42-浓度为0.10 mol·L -1 。计算Cu 2+ 的αCu 。已知Cu(Ⅱ)- C 2O 4 2- 络合物的lgβ1=4.5,lgβ2=8.9; Cu(Ⅱ)-OH -络合物的lgβ1=6.0。 解: 224 33222 124224() 4.58.92 6.96.09.2614 1.261()14333()1321[][] 100.1010(0.10)101[]1101010[][]112[]0.10[][]1[][Cu C O Cu OH NH Cu NH C O C O OH C NH H NH mol L NH NH Ka NH N αββαβαββ------+ +-=++=?+?==+=+?==+=+=?=??=++又23 24 259.35 3539.36 ()()()][]1010Cu Cu NH Cu C O Cu OH H NH βαααα- - ++=≈++=K
3.铬黑T(EBT)是一种有机弱酸,它的lgK 1H =11.6,lgK 2H =6.3,Mg-EBT 的lgK MgIn =7.0,计算在PH=10.0时的lgK ’MgIn 值。 4. 已知M(NH 3)42+ 的lgβ1~ lgβ4为 2.0,5.0,7.0,10.0,M(OH)42-的lgβ1~ lgβ4为4.0,8.0,14.0,15.0。在浓度为0.10 mol·L -1 的M 2+ 溶液中,滴加氨水至溶液中的游离NH 3浓度为0.010 mol·L -1 ,PH=9.0试问溶液中的主要存在形式是那一种?浓度为多大?若将M 2+ 离子溶液用NaOH 和氨水调节至PH≈13.0且游离氨浓度为0.010 mol·L -1,则上述溶液中的主要存在形式是什麽?浓度又为多少? 解:用氨水调解时: 3 2()121(0.010)(0.010)122 M NH αββ=+++=K 3 2.0 2.0 131()[] 10100.0083 122 M NH NH βδα-?=== 3 2 5.0 4.0 232()[]10100.083 122 M NH NH βδα-?=== 7.0 6.0310100.083122δ-?== 10.08.0 410100.83 122δ-?== 故主要存在形式是M(NH 3)42+ ,其浓度为0.10×0.83=0.083 mol·L -1 用氨水和NaOH 调节时: 3 4811 ()()11100.1100.01120210M M NH M OH ααα- =+-=+?+?++=?K 49 111100.1510210δ-?= =?? 8 6211 100.01510210δ-?==??
第七章氧化还原滴定法思考题与习题 1.条件电位和标准电位有什么不同?影响电位的外界因素有哪些? 答:标准电极电位E′是指在一定温度条件下(通常为25℃)半反应中各物质都处于标准状态,即离子、分子的浓度(严格讲应该是活度)都是1mol/l(或其比值为1)(如反应中有气体物质,则其分压等于1.013×105Pa,固体物质的活度为1)时相对于标准氢电极的电极电位。 电对的条件电极电位(E0f)是当半反应中氧化型和还原型的浓度都为1或浓度比为,并且溶液中其它组分的浓度都已确知时,该电对相对于标准氢电极电位(且校正了各种外界因素影响后的实际电极电位,它在条件不变时为一常数)。由上可知,显然条件电位是考虑了外界的各种影响,进行了校正。而标准电极电位则没有校正外界的各种外界的各种因素。 影响条件电位的外界因素有以下3个方面; (1)配位效应; (2)沉淀效应; (3)酸浓度。 2.是否平衡常数大的氧化还原反应就能应用于氧化还原中?为什么? 答:一般讲,两电对的标准电位大于0.4V(K>106),这样的氧化还原反应,可以用于滴定分析。 实际上,当外界条件(例如介质浓度变化、酸度等)改变时,电对的标准电位是要改变的,因此,只要能创造一个适当的外界条件,使两电对的电极电位超过0.4V ,那么这样的氧化还原反应也能应用于滴定分析。但是并不是平衡常数大的氧化还原反应都能应用于氧化还原滴定中。因为有的反应K虽然很大,但反应速度太慢,亦不符合滴定分析的要求。 3.影响氧化还原反应速率的主要因素有哪些? 答:影响氧化还原反应速度的主要因素有以下几个方面:1)反应物的浓度;2)温度;3)催化反应和诱导反应。 4.常用氧化还原滴定法有哪几类?这些方法的基本反应是什么? 答:1)高锰酸钾法.2MnO4+5H2O2+6H+==2Mn2++5O2↑+8H2O. MnO2+H2C2O4+2H+==Mn2++2CO2+2H2O 2) 重铬酸甲法. Cr2O72-+14H++Fe2+===2Cr3++Fe3++7H2O CH3OH+Cr2O72-+8H+===CO2↑+2Cr3++6H2O 3)碘量法3I2+6HO-===IO3-+3H2O,
第四章 配位滴定法 一、选择题 1.直接与金属离子配位的EDTA 型体为( ) (A )H 6Y 2+ (B )H 4Y (C )H 2Y 2- (D )Y 4- 2.一般情况下,EDTA 与金属离子形成的络合物的络合比是( ) (A )1:1 (B )2:1 (C )1:3 (D )1:2 3.铝盐药物的测定常用配位滴定法。加入过量EDTA,加热煮沸片刻后,再用标准锌溶液滴定。该滴定方式是( )。 (A )直接滴定法 (B )置换滴定法 (C )返滴定法 (D )间接滴定法 4.αM(L)=1表示( ) (A )M 与L 没有副反应 (B )M 与L 的副反应相当严重 (C )M 的副反应较小 (D )[M]=[L] 5.以下表达式中正确的是( ) (A )Y M MY MY c c c K =' (B )[][][]Y M MY K MY =' (C )[][][]Y M MY K MY = (D )[][][]MY Y M K MY = 6.用EDTA 直接滴定有色金属离子M ,终点所呈现的颜色是( ) (A )游离指示剂的颜色 (B )EDTA-M 络合物的颜色 (C )指示剂-M 络合物的颜色 (D )上述A+B 的混合色 7.配位滴定中,指示剂的封闭现象是由( )引起的 (A )指示剂与金属离子生成的络合物不稳定 (B )被测溶液的酸度过高 (C )指示剂与金属离子生成的络合物翁定性小于MY 的稳定性 (D )指示剂与金属离子生成的络合物稳定性大于MY 的稳定性 8.下列叙述中错误的是( ) (A )酸效应使络合物的稳定性降低 (B )共存离子使络合物的稳定性降低 (C )配位效应使络合物的稳定性降低 (D )各种副反应均使络合物的稳定性降低 9.用Zn 2+标准溶液标定EDTA 时,体系中加入六次甲基四胺的目的是( ) (A )中和过多的酸 (B )调节pH 值 (C )控制溶液的酸度 (D )起掩蔽作用 10.在配位滴定中,直接滴定法的条件包括( ) (A )MY K c '?lg ≤8 (B )溶液中无干扰离子 (C )有变色敏锐无封闭作用的指示剂 (D )反应在酸性溶液中进行 11.测定水中钙硬时,Mg 2+的干扰用的是( )消除的。 (A )控制酸度法 (B )配位掩蔽法 (C )氧化还原掩蔽法 (D )沉淀掩蔽法 12.配位滴定中加入缓冲溶液的原因是()
第6章 络合滴定法 2. 在PH=的氨性缓冲溶液中,除氨络合物外的缓冲剂总浓度为 mol ·L -1,游离C 2O 42-浓度为 mol ·L -1。计算Cu 2+的αCu 。已知Cu(Ⅱ)- C 2O 42-络合物的lg β1=,lg β2=; Cu(Ⅱ)-OH -络合物的lg β1=。 解: 22433222 124224() 4.58.92 6.96.09.2614 1.26 1()1 4333()1321[][] 100.1010(0.10)101[]1101010[][]112[]0.10[][]1[][Cu C O Cu OH NH Cu NH C O C O OH C NH H NH mol L NH NH Ka NH N αββαβαββ------+ +-=++=?+?==+=+?==+=+=?=??=++又2324 259.353539.36 ()()()][]1010Cu Cu NH Cu C O Cu OH H NH βαααα--++=≈++=K
3.铬黑T(EBT)是一种有机弱酸,它的lgK 1H =,lgK 2H =,Mg-EBT 的lgK MgIn =,计算在PH=时的lgK ’MgIn 值。 4. 已知M(NH 3)42+的lg β1~ lg β4为,,,,M(OH)42-的lg β1~ lg β4为,,,。在浓度为 mol ·L -1的M 2+溶液中,滴加氨水至溶液中的游离NH 3浓度为 mol ·L -1,PH=试问溶液中的主要存在形式是那一种浓度为多大若将M 2+离子溶液用NaOH 和氨水调节至PH ≈且游离氨浓度为 mol ·L -1,则上述溶液中的主要存在形式是什麽浓度又为多少 解:用氨水调解时: 32()121(0.010)(0.010)122M NH αββ=+++=K 3 2.0 2.0 131()[]10100.0083 122M NH NH βδα-?=== 32 5.0 4.0 232()[]10100.083 122 M NH NH βδα-?=== 7.0 6.0310100.083122δ-?==10.08.0 410100.83 122δ-?== 故主要存在形式是M(NH 3)42+,其浓度为×= mol ·L -1 用氨水和NaOH 调节时: 34811()()11100.1100.01120210M M NH M OH ααα-=+-=+?+?++=?K 49 111100.1510210δ-?==??86211 100.01510210δ-?==?? 14311100.0010.5210δ?==?15411 100.00010.5210δ?==? 故主要存在形式是M(OH)3-和M(OH)42-,其浓度均为 mol ·L -1 5. 实验测得 mol ·L -1Ag(H 2NCH 2CH 2NH 2)2+溶液中的乙二胺游离浓度为·L -1。计算溶液中C 乙二胺和δAg(H 2NCH 2CH 2NH 2)+ 。Ag +与乙二胺络合物的lg β1=,lg β2=。 解: 2 2 2 2 ()12222222224.77.72 3.74 1[][]11010(0.010)10Ag H NCH NH H NCH CH NH H NCH CH NH αββ=++=++?= 2 2 2 2 2 22.70 ()() 100.091 Ag H NCH NH Ag H NCH NH δα= =
1. EDTA二钠盐的水溶液的pH的最简式是(pH = (p K a4 + p K a5) /2)(EDTA相当于六元酸) 2. 络合滴定中一般不使用EDTA而用EDTA二钠盐(Na2H2Y), 这是由于(EDTA 在水中的溶解度小, 而Na2H2Y的溶解度较大); 当在强酸性溶液中(pH<1), EDTA为六元酸, 这是因为(两个N原子接受了两个质子)。 3.直接与金属离子配位的EDTA型体为(D) (A)H6Y2+(B)H4Y (C)H2Y2-(D)Y4- 4. 指出下列EDTA络合物的颜色(填A,B,C,D) (1) CuY2- ___ D _____ (A)无色 (2) MnY2- __ B ______ (B)紫红色 (3) FeY-___C _____ (C)黄色 (4) ZnY2- ___ A ____ (D)蓝色 5.一般情况下,EDTA与金属离子形成的络合物的络合比是(A) (A)1:1 (B)2:1 (C)1:3 (D)1:2 6. 金属离子M与络合剂L形成逐级络合物, 溶液中各种存在型体的分布系数与络合剂的平衡浓度(有关); 与金属离子的总浓度(无关)。(答有关或无关) 7. 已知乙酰丙酮(L)与Al3+络合物的lgβ1-lgβ3分别是 8.6、15.5和21.3, 则AlL3为主要形式时的pL范围是(pL < 5.8),pL为10.0时铝的主要形式是(Al3+),则[AlL]与[AlL2]相等时的pL值为(6.9) 8. 磺基水杨酸(L)与Cu2+络合物的lgβ1为9.5, lgβ2为16.5, [CuL]达最大的pL为( D) (A) 9.5 (B) 16.5 (C) 7.0 (D) 8.3 9.αM(L)=1表示(A) (A)M与L没有副反应(B)M与L的副反应相当严重 (C)M的副反应较小(D)[M]=[L] 10. 若络合滴定反应为 M + Y = MY L│ │H+ ML H i Y(i=1~6) 则酸效应系数αY(H)的定义式为(αY(H)=[Y']/[Y]),[Y']=([Y']=[Y]+∑[H i Y])c(Y)=([Y]+∑[H i Y]+[MY]或c(Y)=[Y']+[MY])。络合效应系数αM(L)的定义式为(αM(L)=[M']/[M])。 11. 若EDTA滴定M反应为 M+Y=MY ↓A MA 以下表示正确的是( A) (A) c(M)=[M']+[MY] (B) c(M)=[M]+[M']+[MY] (C) c(M)=[MA]+[MY] (D) c(M)=[M]+[MA] 12. 用EDTA滴定金属M, 若M分别与A,B,C三者发生副反应,此时计算αM的公式是αM = (αM(A)+αM(B)+αM(C)-2 )。 13. 在一定酸度下, 用EDTA滴定金属离子M。当溶液中存在干扰离子N时, 影响络合剂总副反应系数大小的因素是( C) (A) 酸效应系数αY(H)
分析化学练习题 第6章络合滴定法 一. 选择题 1.下列有关条件稳定常数的正确叙述是() A. 条件稳定常数只与酸效应有关 B. 条件稳定常数表示的是溶液中络合物实际的稳定常数 C. 条件稳定常数与温度无关 D. 条件稳定常数与络合物的稳定性无关 2. 对配位反应中的条件稳定常数,正确的叙述是() A. 条件稳定常数是理想状态下的稳定常数 B. 酸效应系数总是小于配位效应系数 C. 所有的副反应均使条件稳定常数减小 D. 条件稳定常数能更准确地描述配位化合物的稳定性 3. 已知lgK ZnY =16.5,若用0.020mol·L-1EDTA滴定0.020mol·L-1Zn2+溶液,要求△pM=±0.2, TE = 0.1%,已知pH = 4,5,6,7时,对应lgαY(H)分别为8.44,6.45,4.65,3.32,滴定时的最高允许酸度为() A. pH≈4 B. pH≈5 C. pH≈6 D. pH≈7 4. 现用Cmol·L-1EDTA滴定等浓度的Ca2+,Ca2+无副反应。已知此时滴定的突跃范围ΔpM, 若EDTA和Ca2+的浓度增加10倍,则此时滴定的突跃范围为ΔpM' () A.ΔpM'=ΔpM-2 B.ΔpM'=ΔpM+1 C. ΔpM'=ΔpM-1 D. ΔpM'=ΔpM+2 5. 以EDTA滴定Zn2+时,加入的氨性溶液无法起到的作用是() A. 控制溶液酸度 B. 防止Zn2+水解 C. 防止指示剂僵化 D. 保持Zn2+可滴定状态 6. 下列有关金属离子指示剂的不正确描述是() A.理论变色点与溶液的pH值有关 B.没有确定的变色范围 C.与金属离子形成的络合物稳定性要适当 D.能在任意pH值时使用 7. 在配位滴定中,当溶液中存在干扰测定的共存离子时,一般优先使用() A. 沉淀掩蔽法 B.氧化还原掩蔽法 C. 离子交换法分离 D. 配位掩蔽法 8. 用EDTA滴定Bi3+时,消除Fe3+干扰宜采用() A. 加NaOH B.加抗坏血酸 C.加三乙醇胺 D.加氰化钾 9. 某溶液中含有Ca2+、Mg2+及少量Al3+、Fe3+,欲以铬黑T为指示剂,用EDTA滴定Ca2+、 Mg2+的含量,正确的做法是() A.碱性条件下加入KCN和NaF,再测定 B.酸性条件下加入三乙醇胺,再调至碱性测定 C.酸性条件下加入KCN和NaF,再调至碱性测定 D.加入NH3沉淀掩蔽Al3+和Fe3+,再测定 10. 铬黑T(EBT)与Ca2+的配合物的稳定常数K Ca-EBT =105.4,已知EBT的逐级质子化常数 K1H =1011.5,K2H =106.3,在pH=10.0时,EBT作为滴定Ca2+的指示剂,在颜色转变点的pCa值为()
第6章 络合滴定法 一、填空题 1.EDTA 的化学名称为 ,当溶液酸度较高时,可作 元酸,有 种存在形式。 2. 采用EDTA 为滴定剂测定水的硬度时,因水中含有少量的 Fe 3+ , Al 3+ 。应加入 作掩蔽剂; 滴定时控制溶液PH = 。 3. EDTA 络合物的条件形成常数'MY K 随溶液的酸度的变化而改变。酸度越 则' MY K 越 ;络合物越 ,滴定突跃越 。 4.以铬黑T为指示剂,溶液pH 值必须维持 ;滴定到终点时溶液由 色变为 色。 5.EDTA 的酸效应曲线是指 ,当溶液的pH 越大,则 越小。 二、选择题 1. 以EDTA 为滴定剂,下列叙述中哪一种是错误的?( ) A. 在酸度较高的溶液中,可形成MHY 络合物; B. 在碱性较高的溶液中,可形成MOHY 络合物; C. 不论形成MHY 或MOHY ,均有利于滴定反应; D. 不论溶液pH 值的大小,只形成MY 一种形式络合物。 2.在pH=12时,以0.0100mol/LEDTA 滴定20.00mol/LCa2+。等当点时的pCa 值为( ) A.5.3 B.6.6 C.8.0 D.2.0 3. 在pH = 10 的氨性缓冲溶液中, 用EDTA 滴定同浓度的 Zn 2+ 至化学计量点时,下列关系式中哪一个是正确的?( ) A. [ Zn 2+ ] = [ Y 4 - ] ; B.[Zn 2+ ] = [ Y 4 -ˊ ] ; [ZnY 2 -] C. [ Zn 2+ ˊ ] 2 = K ˊ Zn Y [ZnY 2 - ] D. [ Zn 2+ ] 2 = K ˊZn Y ; 4.在pH= 5.7时,EDTA 是以( )形式存在的: A.H 6Y 2+ B.H 3Y - C.H 2Y 2- D.Y 4- 5. 在pH = 10 的氨性缓冲溶液中,以EDTA 滴定Zn 2+ 至化学计量点时,以下关系式中哪 一个是正确的( ) A.pZn sp = pZn ˊsp + lg α Zn ( NH 3 ) ; B. pZn sp = pZn ˊsp – lg αZn ( NH 3 ) ; C.pZn sp = lgZn ˊ sp + p α Zn ( NH 3 ) ; D. pZn sp = lg αZn ( NH 3 ) - pZn ˊsp 。 6.为了测定水中 Ca 2 + , Mg 2+ 的含量,以下消除少量 Fe 3+ , Al 3+ 干扰的方法中,哪一种是正确的?( ) A. 于pH =10 的氨性溶液中直接加入三乙醇胺; B. 于酸性溶液中加入KCN ,然后调至pH =10; C. 于酸性溶液中加入三乙醇胺,然后调至pH =10 的氨性溶液; D. 加入三乙醇胺时,不需要考虑溶液的酸碱性。 7. 今有 A ,B 相同浓度的Zn 2+ — EDTA 溶液两份;A 为PH = 10 的NaOH 溶液;B 为PH = 10 的氨性缓冲溶液。对叙述两溶液 K ˊZn Y 的大 小,哪一种是正确的?( ) A. A 溶液的K ˊZn Y 和B 溶液相等; B. A 溶液的K ˊZn Y 小于B 溶液的K ˊ Zn Y ; C. A 溶液的K ˊZn Y 大于 B 溶液的K ˊZn Y ; D. 无法确定。 8.EDTA 与Zn 2+ 形成的配合物在pH=10时的条件稳定常数' lg ZnY K =( ) A.16.50 B.0.45 C.16.05 D.16.95 三、 计算题
第七章络合滴定法练习题 1. EDTA二钠盐的水溶液的pH的最简式是()(EDTA相当于六元酸) 2. 络合滴定中一般不使用EDTA而用EDTA二钠盐(Na2H2Y), 这是由于(); 当在强酸性溶液中(pH<1),EDTA为六元酸, 这是因为()。 3.直接与金属离子配位的EDTA型体为() (A)H6Y2+(B)H4Y (C)H2Y2-(D)Y4- 4. 指出下列EDTA络合物的颜色 (1) CuY2- ___________ (2) MnY2- ___________ (3) FeY- ___________ (4) ZnY2-___________ 5.一般情况下,EDTA与金属离子形成的络合物的络合比是() (A)1:1 (B)2:1 (C)1:3 (D)1:2 6. 金属离子M与络合剂L形成逐级络合物, 溶液中各种存在型体的分布系数与络合剂的平衡浓度(); 与金属离子的总浓度()。(答有关或无关) 7. 已知乙酰丙酮(L)与Al3+络合物的lgβ1-lgβ3分别是8.6、15.5和21.3, 则AlL3为主要形式时的pL范围是(),pL为10.0时铝的主要形式是(),则[AlL]与[AlL2]相等时的pL值为() 8. 磺基水杨酸(L)与Cu2+络合物的lgβ1为9.5, lgβ2为16.5,[CuL]达最大的pL 为( ) (A) 9.5 (B) 16.5 (C) 7.0 (D) 8.3 9.αM(L)=1表示() (A)M与L没有副反应(B)M与L的副反应相当严重 (C)M的副反应较小(D)[M]=[L] 10. 若络合滴定反应为 M + Y = MY L│ │H+ ML H i Y(i=1~6) 则酸效应系数αY(H)的定义式为(),[Y']=()c(Y)=()。络合效应系数αM(L)的定义式为()。11. 若EDTA滴定M反应为 M+Y=MY ↓A MA 以下表示正确的是( ) (A) c(M)=[M']+[MY] (B) c(M)=[M]+[M']+[MY] (C) c(M)=[MA]+[MY] (D) c(M)=[M]+[MA] 12. 用EDTA滴定金属M, 若M分别与A,B,C三者发生副反应,此时计算αM的公式是αM = (αM(A)+αM(B)+αM(C)-2 )。 13. 在一定酸度下,用EDTA滴定金属离子M。当溶液中存在干扰离子N时, 影
第三章络合滴定法 一.选择题 1. EDTA的酸效应曲线是指------------------------------------------------------------------( ) (A) αY(H)-pH 曲线 (B) pM-pH 曲线 (C) lg K'(MY)-pH 曲线(D) lgαY(H)-pH 曲线 2. 已知Ag+-S2O32-络合物的lgβ1~lgβ3分别是9.0,1 3.0,1 4.0。以下答案不正确的是---( ) (A) K1=109.0(B) K3=101.0 (C) K不(1)=10-9.0(D) K不(1)=10-1.0 3. 在pH为10.0的氨性溶液中, 已计算出αZn(NH3)=10 4.7, αZn(OH)=102.4, αY(H)=100.5。则在此条件下lg K'(ZnY)为----------------------------------------------------------------------------------------- ( ) [已知lg K(ZnY)=16.5] (A) 8.9 (B) 11.8 (C) 14.3 (D) 11.3 4. αM(L)=1表示---------------------------------------------------------------------------------------( ) (A) M与L没有副反应(C) M与L的副反应相当严重 (C) M的副反应较小(D) [M]=[L] 5. 若用0.02 mol/L EDTA滴定0.02mol/L Zn溶液,(要求?pM=0.2,E t=0.1%)滴定时最高允许酸度是--------------------------------------------------------------------------------------------------( ) (A) pH≈4 (B) pH≈5 (C) pH≈6 (D) pH≈7 6. 当pH=10.0, 以0.010 mol/L EDTA溶液滴定0.010 mol/L Zn2+的溶液两份, 其中一份溶液中含有0.5 mol/L游离NH3; 另一份溶液中含有0.2 mol/L游离NH3。在上述两种情况下, 对pZn的叙述正确的是-----------------------------------------------------------------------------------( ) (A) 加入EDTA开始滴定时pZn相等(B) 滴定至一半时pZn相等 (C) 滴定至化学计量点时pZn相等(D) 上述说法都不正确 7. 用0.020 mol/L Zn2+溶液滴定0.020 mol/L EDTA溶液。已知lg K(ZnY)=16.5, lgαZn=1.5, lgαY=5.0,终点时pZn=8.5,则终点误差为--------------------------------------------------------( ) (A) +0.1% (B) -0.1% (C) +3% (D) -3% 8. 为了测定水中Ca2+,Mg2+的含量,以下消除少量Fe3+、Al3+干扰的方法中,哪一种是正确的?-------------------------------------------------------( ) (A) 于pH=10的氨性溶液中直接加入三乙醇胺; (B) 于酸性溶液中加入KCN,然后调至pH=10; (C) 于酸性溶液中加入三乙醇胺, 然后调至pH=10的氨性溶液; (D) 加入三乙醇胺不需要考虑溶液的酸碱性。
第六章 配位滴定法 思考题与习题 1.简答题: (1)何谓配位滴定法?配位滴定法对滴定反应有何要求? 答:以配位反应为基础的地点分析方法称为配位滴定法。配位滴定法要求配位反应按一定的反应式定量进行,且能进行完全;反应必须迅速;可以用适当的方法确定终点。 (2)EDTA 与其金属离子配合物的特点是什么? 答:EDTA 具有广泛的配位性能;EDTA 与金属离子配位时可生成的螯合物稳定性高,配位反应的完全程度高;EDTA 与金属离子形成配位化合物的配位比几乎均为1:1;EDTA 与金属离子形成的配合物大多能溶于水;配位反应迅速;EDTA 与无色离子形成的配合物也无色,便于用指示剂确定终点。 (3)配位滴定可行性的判断条件是什么? 答:MY M K c lg ≥6 (4)配位滴定中可能发生的副反应有哪些?从理论上看,哪些对滴定分析有利? 答:配位滴定副反应包括:EDTA 的酸效应,金属离子的水解效应,金属离子与其他配位剂的配位反应,干扰离子效应,配合物与氢离子、氢氧根离子的副反应等。配合物与氢离子、氢氧根离子的副反应对滴定分析有利。 (5)何谓指示剂的封闭现象?怎样消除封闭? 答:如果指示剂与某些金属离子形成的配位化合物极其稳定,以至于加入过量的滴定剂也不能将金属离子从金属-指示剂配合物中夺取出来,溶液在化学计量点附近就没有颜色变化,这种现象称为指示剂受到了封闭。可加掩蔽剂消除指示剂的封闭现象。 (6)提高配位滴定选择性的条件与措施有哪些? 答:1)控制酸度;2)分别采用配位掩蔽法、沉淀掩蔽法、氧化还原掩蔽法掩蔽干扰离子;3)分离干扰离子。 2.名词解释 (1)酸效应
答:由于H+的存在使配位剂参加主反应能力降低的现象。 (2)酸效应系数 答:定量表示酸效应进行的程度的系数称为酸效应系数。 (3) 配位效应 答:由于存在其他配位剂L 与金属离子M 配位使金属离子参加主反应能力降低的现象。 (4)配位效应系数 答:定量表示配位效应进行的程度的系数称为配位效应系数。 (5)金属指示剂的变色点 答:]n I []MIn ['=当点。变,此即指示剂的变色时,指示剂发生颜色突 3.计算题: (1)用EDTA 滴定法检验血清中的钙。取血清100μl ,加KOH 溶液2滴和钙红指示剂1~2滴,用0.001042mol/LEDTA 滴定至终点,用去0.2502ml 。计算此检品中Ca 2+含量(Ca 2+mg/100ml )。若健康成人血清中Ca 2+含量指标为 9~11mg/100ml ,此检品中Ca 2+含量是否正常?(尿中钙的测定与此相似,只是要用柠檬酸掩蔽Mg 2+) 解: E D T A C a S Ca ()100Ca%(0.0010420.2502)40.0810010.45(mg /100ml)(40.08g/mol)0.1 cV M V M ??=???=== (2)精密称取葡萄糖酸钙(C 12H 22O 14Ca·H 2O )0.5403g ,溶于水中,加入适量钙指示剂,用0.05000mol/LEDTA 滴定至终点,用去23.92ml 。计算此样品中葡萄糖酸钙含量。(1222142C H O Ca H O M =448.7) 解: