
2011年7月郑州大学学报(工学版)
Jul.2011第32卷第4期Journal of Zhengzhou University (Engineering Science )Vol.32No.4
收稿日期:2011-02-17;修订日期:2011-05-04
作者简介:邵蓓新(1965-),女,河南郑州人,本科,主要从事临床药学和药品的检验分析工作;通讯作者:屈凌波(1963-),
男,河南南阳人,博士,教授,主要从事药物分析和化学生物学研究,
E-mail :qulingbo@zzu.edu.cn.文章编号:1671-6833(2011)04-0099-04
毛细管电泳-电致化学发光法测定盐酸林可霉素
邵蓓新1
,张
颖2,李建军2,屈凌波
2,3(1.郑州大学第五附属医院药剂科,河南郑州450052;2.郑州大学化学系,河南郑州450001;
3.河南工业大学化学化工学院,河南郑州450001)
摘
要:基于盐酸林可霉素对联吡啶钌(Ru (bpy )2+
3)在铂电极上电化学信号的增敏作用,结合毛细管
电泳(CE ),建立了毛细管电泳-联吡啶钌电致化学发光(CE -Ru (bpy )
2+
-ECL )测定盐酸林可霉素的新方法.考察检测电位、检测缓冲液浓度和pH 值、分离电压、进样电压和进样时间、分离缓冲液的浓度和pH 值等实验条件对盐酸林可霉素分离检测条件的影响,确定了检测盐酸林可霉素的实验条件.在优化
的实验条件下,盐酸林可霉素在5?10-8 9?10-6g /mL 范围内呈良好线性,检出限为1.55?10-8
g /
mL.该方法可用于盐酸林可霉素注射液中林可霉素的含量测定,测定的回收率为99.62% 100.31%.
关键词:毛细管电泳(CE );电致化学发光(ECL );联吡啶钌(Ru (bpy )2+
3);盐酸林可霉素
中图分类号:R917文献标志码:A
0引言
盐酸林可霉素(Lincomycin Hydrochloride )又名盐酸洁霉素,结构如图1.对革兰阳性球菌有较高的抗菌活性,主要适应于敏感葡萄球菌属、链球菌属、肺炎链球菌及厌氧菌所致的呼吸道感染、皮肤软组织感染等疾病,在临床上得到了广泛的应用.
图1
盐酸林可霉素的结构
Fig.1
Molecular structure of lincomycin hydrochloride
林可霉素药物制剂的质量控制方法主要有微
生物测定法[1]、高效液相色谱法[2-4]
及分光光度法
[5,6]
.微生物测定法虽然测定准确,但测定周期
长,操作复杂且难以区分林可霉素及其它抗生素
药物;高效液相色谱法虽然准确,但成本昂贵,常使用大量的有毒试剂甲醇、已腈等,给环境带来
较大的污染;紫外分光光度法虽操作简便、快速,但灵敏度较低,一般只用做林可霉素兽药生产过程质量控制.
毛细管电泳-联吡啶钌-电致化学发光方法
(CE -Ru (bpy )2+
3-ECL )是20世纪90年代才发展起来一种现代分析技术,具有仪器简单低廉、样
品用量小、基本不使用有毒试剂等特点[7,8]
,非常符合当代提出的节能环保的分析理念.近年来,该技术成为药物分析领域的一个研究热点[9-11]
.实验发现,盐酸林可霉素对Ru (bpy )
2+
3
在铂电极上
的电化学反应具有明显的增敏效应.据此建立了
测定盐酸林可霉素CE -Ru (bpy )2+
3-ECL 新方法.结果表明,所建立的方法简便快速,准确度高,分析成本低且绿色环保,可用于各种林可霉素制剂的质量控制.
1
实验部分
1.1
仪器与试剂
MPI -A 型毛细管电泳电化学发光分析检测
系统(西安瑞迈电子科技有限公司),柱端检测池
采用传统三电极系统,铂盘工作电极(直径500μm ),辅助电极(铂电极)和参比电极(Ag /AgCl );雷磁PH 计(上海精科);石英毛细管(25μm i.d ,
40cm )(河北永年光导纤维厂).
100郑州大学学报(工学版)2011年
盐酸林可霉素标准品(河南天方药业股份有限公司提供,经HPLC 检测,纯度大于等于95%);盐酸林可霉素样品(上海禾丰制药有限公司);联吡啶钌纯品(美国Alfa Aesar 公司);实验所用缓冲溶液均由磷酸氢二钠、
磷酸二氢钠(天津市科密欧化学试剂公司,分析纯)配制而成;实验其余试剂均为分析纯,水为水森活纯净水(可口可乐公司).实验所用缓冲溶液均为磷酸缓冲液.1.2
实验方法
毛细管第一次使用前的活化:用0.1mol /L 的氢氧化钠溶液冲洗过夜,然后用纯净水冲洗至中性,再用15mmol (pH =7.0)的磷酸盐缓冲液平衡.工作电极使用前使用0.05μm 粒径的氧化铝粉末抛光,用纯净水冲洗干净并擦干后放置在正对毛细管出口末端处,在显微镜下调节工作电极和毛细管间的距离约为200?10μm ,进行检测
前,对工作电极进行循环伏安扫描处理至化学发光强度稳定.
光电倍增管的电压设置为+800V.检测电位为1.15V ,采用14kV ?10s 电驱动进样,分离电压12.5kV ,电泳缓冲溶液为15mmol /L (pH =6.5)的磷酸盐缓冲液.实验前检测池中充满5mmol /L 三联吡啶钌溶液和60mmol /L 磷酸盐缓
冲液(pH =7.0)350μL ,
3h 后更换新鲜的三联吡啶钌和磷酸盐缓冲溶液,以保证实验的重现性.
在样品进入检测池检测后,记录其毛细管电泳谱图,
以峰高定量.1.3溶液配制及样品处理
在暗室里准确称取盐酸林可霉素标准品0.0100g 于100.0mL 棕色容量瓶中溶解后用水森活纯净水定容,溶液用0.22μm 微孔滤膜过滤,于4?储存备用.然后逐级稀释配制出一系列浓度做工作曲线.
随机抽取标示量为0.3g /mL 的盐酸林可霉素注射液5支,取内容物注射液混匀后精密吸取
适量,配制为1.5?10-5g /mL 的储备液.向1.5?10-7g /mL 样品中分别加入盐酸林可霉素标准溶
液1.2?10-7g /mL 、
1.5?10-7
g /mL 、1.8?10
-7
g /mL 来测定样品回收率.
2
结果与讨论
2.1
检测电位的优化
在CE -ECL 体系中,检测电位是影响ECL
.,1.00
1.35V 范围内,盐酸林可霉素的ECL 强度随着检测电位的增大先增加后减小,当检测电位为1.15V 时,盐酸林可霉素的ECL 强度达到最大,而后随电压增大而减小.实验选择检测电位为1.15V.2.2
检测条件的优化
检测池中Ru (bpy )
2+3
的浓度以及检测池中
缓冲溶液的浓度和pH 是影响检测的主要因素.
电化学发光信号随检测池中Ru (bpy )2+
3的浓度的增大而增大,但同时仪器的噪声也会随之
增大.实验中以最大的信噪比(S /N )为指标,
考察了Ru (bpy )2+
3浓度在1 10mmol 变化中对S /N 的影响.实验表明:当Ru (bpy )2+
3
浓度为5mmol
时,有最大的信噪比.
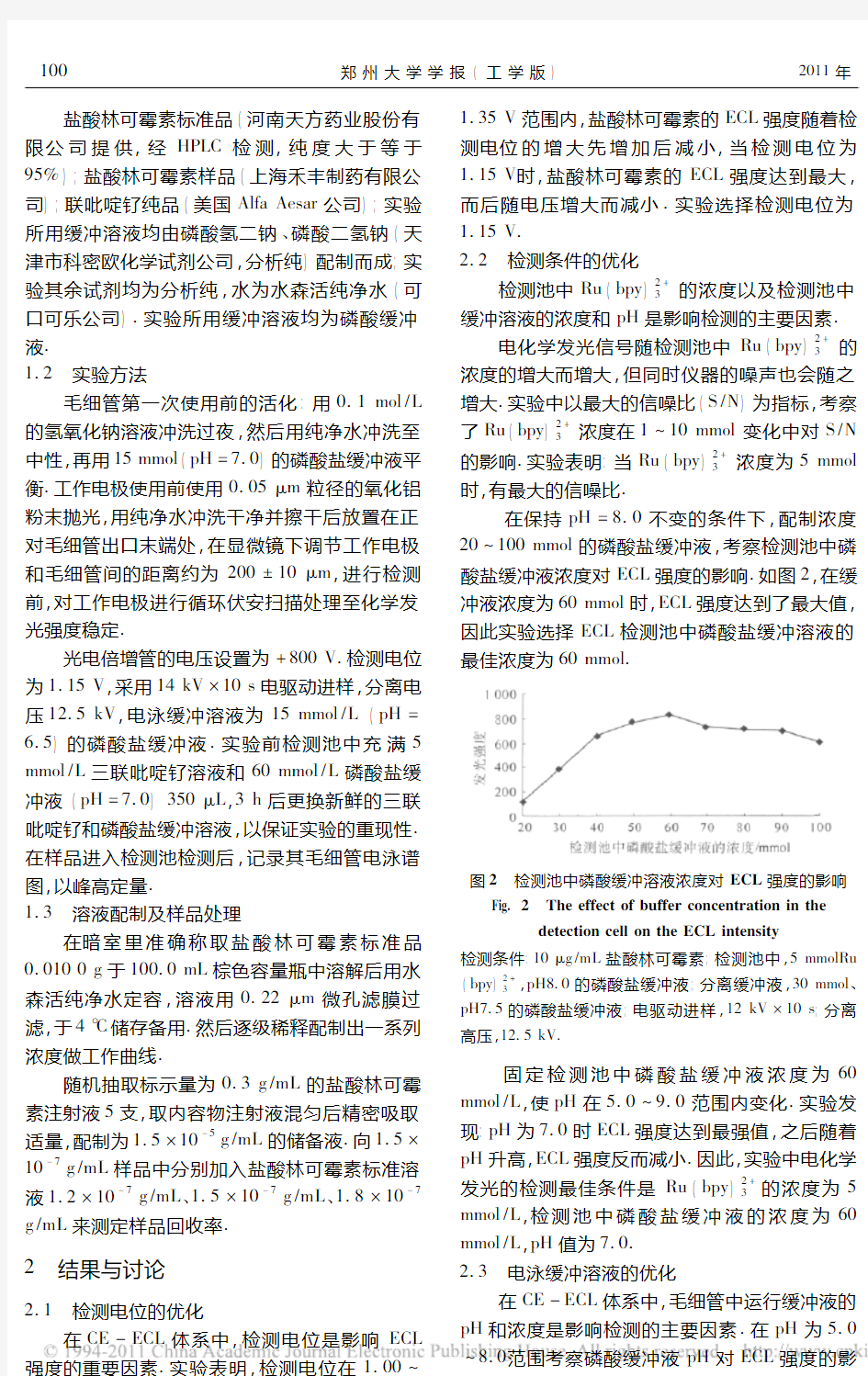
在保持pH =8.0不变的条件下,配制浓度20 100mmol 的磷酸盐缓冲液,考察检测池中磷酸盐缓冲液浓度对ECL 强度的影响.如图2,在缓
冲液浓度为60mmol 时,
ECL 强度达到了最大值,因此实验选择ECL 检测池中磷酸盐缓冲溶液的
最佳浓度为60mmol.
图2检测池中磷酸缓冲溶液浓度对ECL 强度的影响
Fig.2
The effect of buffer concentration in the detection cell on the ECL intensity
检测条件:10μg /mL 盐酸林可霉素;检测池中,5mmolRu (bpy )
2+
3
,pH8.0的磷酸盐缓冲液;分离缓冲液,30mmol 、
pH7.5的磷酸盐缓冲液;电驱动进样,12kV ?10s ;分离高压,
12.5kV.固定检测池中磷酸盐缓冲液浓度为60
mmol /L ,使pH 在5.0 9.0范围内变化.实验发现:pH 为7.0时ECL 强度达到最强值,之后随着pH 升高,ECL 强度反而减小.因此,实验中电化学
发光的检测最佳条件是Ru (bpy )2+
3的浓度为5mmol /L ,检测池中磷酸盐缓冲液的浓度为60
mmol /L ,pH 值为7.0.2.3
电泳缓冲溶液的优化
在CE -ECL 体系中,毛细管中运行缓冲液的
pH 和浓度是影响检测的主要因素.在pH 为5.0
8.0范围考察磷酸缓冲液pH 对ECL 强度的影
第4期邵蓓新,等:毛细管电泳-电致化学发光法测定盐酸林可霉素101
响.如图3所示,在pH 在5.0 6.5范围内,盐酸
林可霉素的ECL 强度随分离缓冲液pH 值的增加而增加,当分离缓冲液pH 值大于6.5后,
ECL 强度随分离缓冲液pH 值的增加反而减小.因此本实验选择pH 为6.5的分离缓冲液
.
图3分离缓冲溶液pH 对ECL 强度的影响
Fig.3
The effect of pH of separation buffer on the ECLintensity
检测条件:10μg /mL 盐酸林可霉素;检测池中,5mmol Ru (bpy )
2+
3
,60μmol pH7.0的磷酸盐缓冲液;分离缓冲液,
30mmol 的磷酸盐缓冲液;电驱动进样,12kV ?10s ;分离高压,
12.5kV.固定分离缓冲溶液的pH =6.5,考察分离缓
冲液浓度在5 40mmol 范围内,盐酸林可霉素ECL 强度的变化.随着分离缓冲液浓度的增大,盐酸林可霉素的ECL 强度先增加后减小,并在浓度为15mmol 处取得最大值.所以本实验选择分离缓冲溶液的最佳浓度为15mmol.2.4分离电压的优化
考察分离电压在5 20V 范围内分离电压对ECL 光强和迁移时间的影响.结果表明:随着分离电压增大,盐酸林可霉素的迁移时间逐渐缩短,但是ECL 强度先增加后减小,当电压为12.5kV 时电化学发光强度最大,实验选择分离电压为12.5kV.2.5
进样时间和进样高压的优化一般而言,采用电驱动进样时,随着进样时间
和进样高压的增加,系统的ECL 强度随之增加,但由于焦耳热效应,会使体系的理论塔板数下降.根据进样高压、进样时间以及理论踏板数的关系图(图4和图5),以获得较高的理论踏板数及较大的ECL 强度为原则,实验选择14kV 的进样高压和10s 的进样时间.2.6
线性范围、精密度和检出限按照实验方法,在所选的最优的实验条件下,
盐酸林可霉素的迁移时间为220s 左右.盐酸林
可霉素在5?10-8 9?10-6
g /mL 浓度范围内与.y =280.08x
+18.157,相关系数为0.9996(y 为峰高,x 单位为盐酸林可霉素的浓度,μg /mL ),得到盐酸盐酸林可霉素的CE -ECL 线性范围、相关系数和检出
限(S /N =3)分别为:5?10-8 9?10-6
g /mL ,
0.9996,1.55?10-8g /mL.对5?10-7g /mL 的盐酸林可霉素标准溶液连续测定7次,峰高和迁移时间的RSD 分别为3.16%和1.98%.
2.7
实际样品测定
盐酸林可霉素注射液的标示量为0.3g /mL (国家药典中规定其含量范围为90.0 110.0%).实测量是0.29g /mL (n =5),为标示量的96.7%,在国家药典规定含量范围内.向盐酸林可霉素注射液中添加一系列高、中、低浓度的盐酸林可霉素标准液,进行回收率实验.测定回收率在99.62% 100.31%之间,表明该方法准确可靠.在240s 时间内即可完成一个样品的测试,相对于盐酸林可霉素质量控制的HPLC 方法来说,分析时间缩短,且在实验过程中,没有使用任何有机有毒试剂,大大减少了对环境的污染.
102郑州大学学报(工学版)2011年
表1盐酸林可霉素注射液的回收率实验(n=4)
Tab.1Recoveries of Lincomycin hydrochloride in
Lincomycin hydrochloride injection(n=4)
样品编号
样品含量
/1?10-7
(g·mL-1)
加入量
/1?10-7
(g·mL-1)
测得总量
/1?10-7
(g·mL-1)
回收率
/%
RSD
/%
11.4501.454.12
21.451.202.6499.622.12
31.451.502.95100.000.39
41.451.803.26100.312.24 3结论
本研究通过实验条件的优化,建立了毛细管电泳-联吡啶钌电化学发光(CE-ECL)法测定盐酸林可霉素的新方法.该方法相对于药典规定的盐酸林可霉素检测的HPLC方法来说,该方法不仅可以达到HPLC测定的准确度要求,而且实验样品用量少,仪器简单便宜,运行成本低,实验过程中没有使用对环境有污染的有机试剂,为盐酸林可霉素制剂的质量控制提供了一种微量和环保的分析测定方法.
参考文献:
[1]冯学忠,吴广辉,方炳虎,等.盐酸林可霉素紫外分光光度测定方法的建立[J].动物医学进展,2009,
30(12):60-63.
[2]朱建平,张菁,高艳霞,等.分光光度法测定盐酸林
可霉素、盐酸麻黄碱和克林霉素磷酸酯三种胶囊剂
的含量[J].中国药学杂志,1999,34(7):498.
[3]魏国义,魏京海,钱春凤,等.RP-HPLC法测定林麻滴鼻剂中盐酸林可霉素和盐酸麻黄碱的含量
[J].药物分析杂志,2003,23(4):332-334.
[4]李红兵,仲娜.盐酸林可霉素滴眼液的HPLC法测定[J].中国药品标准,2002,3(3):42-43.
[5]陆进方.盐酸林可霉素滴眼液的HPLC测定[J].中国医药工业杂志,2003,34(12):627-628.
[6]中国药典,1990年版.二部[M].北京:中国医药科技出版社,1990:496.
[7]YIN Xue-bo,DONG Shao-jun,WANG Er-kang.Analyt-ical applications of the electrochemiluminescence of
tris(2,20-bipyridyl)ruthenium and its derivatives
[J].Trends in Analytical Chemistry.2004,23(6):432
-441.
[8]YIN Xue-bo,WANG Er-kang.Capillary electrophoresis coupling with electrochemiluminescence detection:a
review[J].Analytica Chimica Acta,2005,533:113–
120.
[9]任小娜,宋青云,付周周,等.毛细管电泳电致化学发光法测定洛贝林的研究[J].分析实验室,2008,
27(4):40-43.
[10]彭志兵,吴正平.毛细管电泳电致化学发光法测定氢溴酸右美沙芬[J].化学试剂,2008,30(12):915
-918.
[11]周兴旺,吕鉴泉,曾昭睿.毛细管电泳电致化学发光法测定阿替洛尔[J].分析科学学报.2007,23(1):
30-32.
Determination of Lincomycin Hydrochloride with Capillary
Electrophoresis-Electrochemiluminescence
SHAO Bei-xin1,ZHANG Ying2,LI Jian-jun2,QU Ling-bo2,3
(1.Department of Pharmacy,The Fifth Affiliated Hospital of Zhengzhou University,Zhengzhou450052,China;2.Department of Chemistry,Zhengzhou University,Zhengzhou450001,China;3.Chemistry and Chemical Engineering School,Henan University of Technology,Zhengzhou450001,China)
Abstract:A method of capillary eclctrophoresis(CE)with tris(2,2'-bipyridyl)ruthenium(Ⅱ)electro-chemiluminescence(ECL)detection has been developed for the determination of Lincomycin hydrochloride.The effects of detection potential,concentration and acidity of phosphate buffer,separation voltage,injection voltage of tris(2,2'-bipyridyl)and time,concentration and acidity of seperation buffer on the detection were investigated.Under optimized conditions,the calibration curve for Lincomycin hydrochloride showed a good lin-earity in the range of5?10-8 9?10-6g/mL,and the detection limits was1.55?10-8g/mL.The method was applied for the determination of lincomycin hydrochloride in the lincomycin hydrochloride injections with a recovery of99.62% 100.31%.
Key words:capillary electrophoresis;electrochemiluminescence;tris(2,2'-bipyridyl)ruthenium(Ⅱ);
lincomycin hydrochloride
cobas e411(Disk)操作手册 罗氏诊断产品(上海)有限公司广州分公司 第一章 一. 二. 三. 四. 五. 第二章 一. 二. 1. 2. 3. 三. 1. 2. 3. 四. 第三章 一. 二. 三. 四. 五. 第四章 一. A:操作开关 置)
C :测试区 D :消耗品区 E :显示及控制单元 位于仪器右侧面 位于仪器左侧面 A :主电源开关 B :电源线 A :USB 接口 C :HOST 接口 二. 控制单元 三. 样品/试剂区 A :取样区 B :样品盘保护盖 A :磁珠搅拌针 B :冲洗站 C :样本/试剂针 四. 测试区 A :孵育池(共32个孵育位) B :吸样位 B A :触摸屏 B :虚拟键盘(触摸屏幕 上需输入内容区域 时,自动在屏幕下方 跳出) C :数字键盘 A :定标/质控条形码阅读口 B :带开关盖装置的试剂仓 (18个位置) C B
A :系统试剂保护门 B :Sipple 针 C :CleanCell (黑盖) D :ProCell (白盖) 五. 消耗品区 废吸头/反应杯盒 A :蒸馏水桶 B :废液桶 第二章 基本操作 一. 开机 a . 检查蒸馏水桶,将SysWash 浓缩液配置 为1:100的系统用水 b . 清空废液桶 c . 打开ProCell 和CleanCell 盖子,关好系统试剂保护门。 注意:运行过程中不能打开系统试剂保护门,否则仪器将停止运行。 d . 打开仪器右面主电源开关,再打开仪器前面操作开关,等界面出现后,录入用户名和 密码,仪器自动初始化后进入待机状态 注意:仪器分不同级别及权限使用,可根据实际情况设定;添加用户名后,第 一次输入的密码即为以后的密码。 e. 待仪器进入待机后清空废吸头/反应杯盒。 二. 准备工作 仪器进入待机后,进行每日工作前准备。 1. 清除前日标本记录 B B D C A :吸头位1-2 B :反应杯位3-5 C :吸头丢弃位 D :反应杯丢弃位 A B A :抓手 B :抓手移动时的横纵轴 C :吸头/反应杯区1(120个吸头,60个反应杯) D :吸头/反应杯区2(120个吸头,60个反应杯) E :吸头/反应杯区3(120个吸头,60个反应杯)
电化学发光(Elecsys)检测项目及其临床应用 一、甲状腺功能 甲腺原氨酸(T3, triiodothyronine) T3是甲状腺激素对各种靶器官作用的主要激素。T3(3、5、3’-三碘酪氨酸)主要在甲状腺以外,尤其是在肝脏由T4经酶解脱碘生成。因此,血清T3浓度反映出甲状腺对周边组织的功能甚于反映甲状腺分泌状态。T4转变成T3的减少会导致T3浓度的下降。见于药物的影响,如丙醇、糖皮质类固醇、胺碘酮等以及严重的非甲状腺疾病(N TI),称为“T3低下综合征”。与T4一样,99%以上的T3与运输蛋白质结合,但T3的亲和力要低10倍左右。T3测定可用于T3-甲亢的诊断,早期甲亢的查明和假性甲状腺毒症的诊断。 检测范围:0.300─10.00nmol/l或O.195-6.51ng/ml 正常参考值:1.3-3.1nmol/l或0.8-2.0ng/ml 甲状腺素(T4, thyroxine) T4是甲状腺分泌的主要产物,也是构成下丘脑-垂体前叶-甲状腺调节系统完整性不可缺少的成份。对合成代谢有影响作用。T4由二分子的二碘酪氨酸(DIT)在甲状腺内偶联生成。T4与甲状腺球蛋白结合贮存在甲状腺滤泡的残腔中,在TSH的调节下分泌释放。血清中99%以上的T4以与其它蛋白质结合的形式存在。由于血清中运输蛋白质的浓度易受外源性和内源性作用的影响,因此,在检测血清T4浓度的过程中需考虑到结合蛋白质的状况。如果忽略这一点,结合蛋白质浓度的变化(如怀孕期、服用雌激素或者患肾病综合征等),会导致反映甲状腺代谢状况检测的错误结果。T4测定可用于甲亢、原发性和继发性甲状腺功能减退的诊断以及TSH抑制治疗的监测。 检测范围:5.40─320.0nmol/l或O.420-24.86μg/dl 正常参考值: I. 66-181nmol/l或5.1-14.1μg/dl(标本取自德国和日本) II. 59-154nmol/l或4.6-12.0μg/dl, FT4指数57-147nmol/l或4.4-11.4ug/dl (标本取至美国) 游离T3(FT3- free triiodothyronine) 三碘甲腺原氨酸(T3)是血清中的甲状腺激素之一,起调节代谢作用。测定该激素的含量对鉴别诊断甲状腺功能是否正常、亢进或低下有重要意义。绝大多数的T3与其转运蛋白质(TBG、前白蛋白、白蛋白)结合,fT3是T3的生理活性形式。fT3测定的优点是不受其结合蛋白质浓度和结合特性变化的影响。因此不需另加测定结合参数(T -uptake,TBG)。 检测范围:0.400─50.00pmol/l或O.260-32.55pg/ml 正常参考值:2.8-7.1pmol/l或1.8-4.6pg/ml 游离T4(FT4- free thyroxine)
cobas e411(Disk)操作手册罗氏诊断产品(上海)有限公司广州分公司 第一章 一. 二. 三. 四. 五. 第二章 一. 二. 1. 2. 3. 三. 1. 2. 3. 四. 第三章 一. 二. 三. 四. 五. 第四章 一. A:操作开关 B) C:测试区 D 位于仪器右侧面 A:主电源开关 B:电源线 A:USB接口 C:HOST接口 二.控制单元
三. 样品/试剂区 A :取样区 B :样品盘保护盖 A :磁珠搅拌针 B :冲洗站 C :样本/试剂针 四. 测试区 A :孵育池(共32个孵育位) B :吸样位 A :系统试剂保护门 B :Sipple 针 C :CleanCell (黑盖) D :ProCell (白盖) B A :触摸屏 B :虚拟键盘(触摸屏幕 上需输入内容区域 时,自动在屏幕下方 跳出) C :数字键盘 A :定标/质控条形码阅读口 B :带开关盖装置的试剂仓 (18个位置) C B
五. 消耗品区 废吸头/反应杯盒 A :蒸馏水桶 B :废液桶 第二章 基本操作 一. 开机 a . 检查蒸馏水桶,将SysWash 浓缩液配置为1:100的系统 用水 b . 清空废液桶 c . 打开ProCell 和CleanCell 盖子,关好系统试剂保护门。 注意:运行过程中不能打开系统试剂保护门,否则仪器将停止运行。 d . 打开仪器右面主电源开关,再打开仪器前面操作开关,等界面出现后,录入用户名和密码,仪器自动初始 化后进入待机状态 注意:仪器分不同级别及权限使用,可根据实际情况设定;添加用户名后,第 一次输入的密码即为以后的密码。 e. 待仪器进入待机后清空废吸头/反应杯盒。 二. 准备工作 仪器进入待机后,进行每日工作前准备。 1. 清除前日标本记录 定标: 1.录入定标物参数(扫描定标物BC 卡): 将BC 卡插入扫描位2.分配定标品位置 a :使用定标瓶上条形码 直接将定标瓶放上标本盘,并将定标瓶上的条码对准读码器即可。 b .手工安排定标品位置 B A :吸头位1-2 B :反应杯位3-5 C :吸头丢弃位 D :反应杯丢弃位 A B A :抓手 B :抓手移动时的横纵轴 C :吸头/反应杯区1(120个吸头,60个反应杯) D :吸头/反应杯区2(120个吸头,60个反应杯) E :吸头/反应杯区3(120个吸头,60个反应杯)
信阳师范学院 研究生课程论文 2014—2015学年第1学期 毛细管电泳电化学发光联用技术及应用新进展提交日期:2015 年 1 月 6 日研究生签名:
毛细管电泳电化学发光联用技术及应用新进展 姓名:学号:2 摘要:生命与健康是关系人类生活和可持续发展的永恒话题。为了检测食品中的有毒物质和人类身体内的有害物质,并达到快速检测和灵敏度高的目的,毛细管电泳(CE)和电化学发光(ECL)技术相结合的方法应运而生。这种方法充分利用了CE技术快速、灵敏、需样量少的优点及ECL线性范围宽和仪器简单的特点,使其在生命和医药等方面得到了广泛的应用。 关键词:毛细管电泳;电化学发光;生命;医药 引言 毛细管电泳法(Capillary Electrophoresis,CE)也叫做高效毛细管电泳(HPCE),是二十世纪八十年代问世的高效液相分离法之一[1],是将经典的电泳技术和现代微柱分离相结合的产物。它是一类以毛细管为分离通道,以高压直流电场为驱动力,以样品的多种特性(大小、电荷、等电点、极性、亲和行为、相分配特性等)为依据的液相微分离分析技术。与传统的分离分析方法相比,毛细管电泳显著特点是简单、高效、快速和微量。另外,毛细管电泳还有经济、清洁、易于自动化和环境污染小等优点。因此,毛细管电泳迅速发展为高效的分离和检测技术,广泛应用于物质的检测与分离。 电化学发光(electrochemiluminescence,ECL)是指电极表面通过电子的转移形成激发态,电子从激发态返回基态而产生的发光过程[2],由电极上施加的电压所引发和控制[3],以电激发为驱动力,通过电化学反应产生光信号。因此,电化学发光兼有化学发光的特点,是一种可控性强,灵敏度高的检测方法。 将毛细管电泳和电化学发光技术联用,产生了毛细管电泳-电化学发光检测技术(CE-ECL),该技术兼有CE微量、迅速、高效及ECL高选择性、高灵敏等特点。这些特点使CE-ECL检测技术在药物分析、生命分析等领域应用越来越广泛,在实际样品的分离和分析工作中也发挥着重要的作用。本文主要简述毛细管电泳-电化学发光联用技术在各个领域的应用进展。 1. 毛细管电泳-电化学发光联用技术
荧光和化学发光免疫分析方法 免疫分析是利用抗原抗体反应进行的检测方法,即利用抗原与抗体的特异性反应, 应用制备好的抗原或抗体作为试剂,以检测标本中的相应抗体或抗原。由于免疫的特异性结合,免疫分析方法具有很好的选择性,荧光免疫分析和化学发光免疫分析是其中典型的两种。本文将对这两种免疫分析方法进行详细的介绍。 一、免疫 免疫是指机体免疫系统识别自身与异己物质,并通过免疫应答排除抗原性异物,以维持机体生理平衡的功能。免疫是人体的一种生理功能,人体依靠这种功能识别“自己”和“非己”成分,从而破坏和排斥进入人体的抗原物质,或人体本身所产生的损伤细胞和肿瘤细胞等,以维持人体的健康。 特异性免疫系统,是一个专一性的免疫机制,针对一种抗原所生成的免疫淋巴细胞(浆细胞)分泌的抗体,只能对同一种抗原发挥免疫功能。而对变异或其他抗原毫无作用。 1、抗原 1.1抗原的定义 抗原:是一类能刺激机体免疫系统使之产生特异性免疫应答(免疫原性) ,并能与相应抗体在体内或体外发生特异性结合的物质(免疫反应性)。 抗原一般为大分子物质,其分子量在10kD以上。 1.2抗原的分类
完全抗原:同时具有免疫原性和免疫反应性的抗原,如细菌、病毒、异种动物血清等。 半抗原:仅具有与相应抗原或致敏淋巴细胞结合的免疫反应性,而无免疫原性的物质。如大多数的多糖、类脂及一些简单的化学物质,它们本身不具免疫原性,但当与蛋白质大分子结合后形成复合物,便获得了免疫原性, 1.3抗原的性质 决定簇是指抗原分子表面的基团,它直接决定免疫学反映的特异性。 抗原通过抗原决定簇与相应淋巴细胞表面抗原受体结合,从而激活淋巴细胞,引起免疫应答,抗原也藉此与相应抗体或致敏淋巴细胞发生特异性结合。 因此,抗原决定簇是被免疫细胞识别的靶结构,也是免疫反应具有特异性的物质基础。 2、抗体 2.1抗体的定义 抗体:是机体受抗原刺激后,由淋巴细胞合成的一类能与相应抗原发生特异性结合的球蛋白。 2.2抗体的结构 抗体是机体受抗原刺激后,由淋巴细胞特别是浆细胞合成的一类能与相应抗原发生特异性结合的球蛋白,因其具有免疫活性故又称作免疫球蛋白。 人免疫球蛋白有五类,分别为IgG、IgA、IgM、IgD和IgE。 3、抗原抗体的结合
罗氏电化学发光免疫分 析 标准化管理处编码[BBX968T-XBB8968-NNJ668-MM9N]
罗氏电化学发光免疫分析 技术是罗氏公司开发的,但全自动机械制造却由日本的日立公司承担,所以仪器上还有Hitachi的标志。这个仪器让大家吃惊的一大原因就在于一直在实验室研究的电致化学发光居然已经真正地产业化了,其中我们一直无法解决的诸多问题(尤其是重现性)均已得到解答,看来罗氏的确花了不少心血开发这款仪器。 罗氏电化学发光免疫分析技术的性能特点——创新的技术,与众不同 一、最先进的检测原理 电化学发光免疫测定,是目前最先进的标记免疫测定技术,是继放射免疫、酶免疫、荧光免疫、化学发光免疫测定以后的新一代标记免疫测定技术,具有敏感、快速和稳定的特点,在固相标记免疫测定中技术上居领先地位。 电化学发光(ECL)是一种在电极表面由电化学引发的特异性化学发光反应,实际上是电化学和化学发光两个过程的完美结合。电化学发光与普通化学发光的主要差异在于前者是电启动发光反应,循环及多次发光,后者是通过化合物混合启动发光反应,是单次瞬间发光。因此ECL反应易精确控制,重复性极好。 电化学发光免疫测定是电化学发光(ECL)和免疫测定相结合的产物,直接以[Ru(bpy)3]2+标记抗体,反应时标记物直接发光。且[Ru(bpy)3]2+在电极表面的反应过程可以周而复始进行,产生许多光子,使光信号得以增强。 二、专利的包被技术 链霉亲和素(streptoavidin,SA)和生物素(biotin,B)是具有很强的非共价相互作用的一对化合物,特异性强且结合紧密。一分子SA可与四分子B 相结合,增大了抗体结合量,达到放大效果。在ECL的试剂中,SA通过特殊的蛋白结合物均匀牢固地包被在磁性微粒上,形成通用的能与B结合的固相载体,另一试剂为活化的B衍生物化合的抗原或抗体。两种试剂混合时,抗原或抗体即包被在磁性微粒上。
毕业设计(论文)外文翻译 Electrochemical detection methods in capillary electrophoresis and applications to inorganic species 毛细管电泳电化学检测方法 在无机元素中的应用
电化学检测法在毛细管电泳 和无机元素中的应用 摘要:本文论述了毛细管电泳的三种电化学检测即电导检测法、安培检测法和电位检测法,并与较常见的光学检测方法进行了比较。详细介绍了三种检测方法的原理及其实现方法,同时介绍了它们在无机元素分析物中的应用情况。 关键字:电化学检测、毛细管电泳;无机阴离子、金属阳离子。 目录: 1.简介--------------------------------------------------------------1 2.电导检测法--------------------------------------------------------2 2.1原理----------------------------------------------------------2 2.2实现方法------------------------------------------------------3 3安培检测法--------------------------------------------------------6 3.1原理----------------------------------------------------------6 3.2实现方法------------------------------------------------------6 4电位检测法--------------------------------------------------------5 4.1原理----------------------------------------------------------9 4.2实现方法------------------------------------------------------9 5在无机元素中的应用------------------------------------------------9 6总结-------------------------------------------------------------10 7参考文献---------------------------------------------------------10 1.简介 毛细管电泳的检测方法通常采用光学方法(激光诱导荧光检测法),而毛细管电泳的三种电化学检测法即电导测定法、安培检测法、和电位测定法是非常有吸引力的一种替代方法,尽管目前开发的还相对较少。相对套色板离子法来说(其他和以前一般化的检测方法)他主要借助于电导性能而不是运用光学方法。由与针对毛细管中更小体积细胞的光学检测变得更加困难,而且事实上许多离子也不能直接由光学方法直接检测到,或许当人们意识到这些的时候会感到很惊讶。关于这一情况或许有两种解释。首先由于高性能流体套色板的广泛应用,我们在毛细管电泳中通常采用光学吸收检测法,许多毛细管电泳仪器制造商似乎已经走上
罗氏电化学发光免疫分析 技术是罗氏公司开发的,但全自动机械制造却由日本的日立公司承担,所以仪器上还有Hitachi的标志。这个仪器让大家吃惊的一大原因就在于一直在实验室研究的电致化学发光居然已经真正地产业化了,其中我们一直无法解决的诸多问题(尤其是重现性均已得到解答,看来罗氏的确花了不少心血开发这款仪器。 罗氏电化学发光免疫分析技术的性能特点——创新的技术,与众不同 一、最先进的检测原理 电化学发光免疫测定,是目前最先进的标记免疫测定技术,是继放射免疫、酶免疫、荧光免疫、化学发光免疫测定以后的新一代标记免疫测定技术,具有敏感、快速和稳定的特点,在固相标记免疫测定中技术上居领先地位。 电化学发光(ECL是一种在电极表面由电化学引发的特异性化学发光反应,实际上是电化学和化学发光两个过程的完美结合。电化学发光与普通化学发光的主要差异在于前者是电启动发光反应,循环及多次发光,后者是通过化合物混合启动发光反应,是单次瞬间发光。因此ECL反应易精确控制,重复性极好。 电化学发光免疫测定是电化学发光(ECL和免疫测定相结合的产物,直接以[Ru(bpy3]2+标记抗体,反应时标记物直接发光。且[Ru(bpy3]2+在电极表面的反应过程可以周而复始进行,产生许多光子,使光信号得以增强。 二、专利的包被技术 链霉亲和素(streptoavidin,SA和生物素(biotin,B是具有很强的非共价相互作用的一对化合物,特异性强且结合紧密。一分子SA可与四分子B 相结合,增大了抗体结合量,达到放大效果。在ECL的试剂中,SA通过特殊的蛋白结合物均匀牢固地包被在磁性微粒上,形成通用的能与B结合的固相载体,另一试剂为活化的B衍生物化合的抗原或抗体。两种试剂混合时,抗原或抗体即包被在磁性微粒上。 三、独特的载体
促肾上腺皮质激素(ACTH)测定试剂盒(电化学发光免疫分析法) 适用范围:本试剂盒用于体外定量测定人体血清样本中促肾上腺皮质激素(ACTH)的含量。 1.1包装规格:50人份/盒、100人份/盒。 1.2主要组成成分 试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(ACTH-Cal)(选配)组成。组成及含量见下表: 注:1、定标品靶值批特异,详见靶值单。 2、试剂盒条码卡内含主校准曲线。 2.1 外观 2.1.1 试剂盒各组分应齐全、完整、液体无渗漏; 2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物; 2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物; 2.1.4 包装标签应清晰、无磨损、易识别。 2.2 空白限
应不大于1.0pg/mL。 2.3 准确度 将已知浓度的ACTH标准溶液加入到血清中,其回收率应在(85%~115%)范围内。 2.4 线性 在[3.00,2000.0]pg/mL范围内,线性相关系数(r)应不小于0.9900。 2.5 精密度 2.5.1 重复性 在试剂盒的线性范围内,测定高、低两个水平的样品,检测结果的变异系数(CV)应不大于8%。 2.5.2 批间差 在试剂盒的线性范围内,用3个批号试剂盒分别测定高、低两个水平的样品,检测结果的变异系数(CV)应不大于15%。 2.6 效期末稳定性 本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。 2.7 溯源性 依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求提供促肾上腺皮质激素(ACTH)定标品的来源、赋值过程以及测量不确定度等内容,定标品溯源至企业工作校准品。
中文5300字 毕业设计(论文)外文翻译 Electrochemical detection methods in capillary electrophoresis and applications to inorganic species 毛细管电泳电化学检测方法 在无机元素中的应用 出处:Journal of Chromatography A, 1999, 834(1): 89-101
电化学检测法在毛细管电泳 和无机元素中的应用 Thomas Kappes, Peter C. Hauser 摘要: 本文论述了毛细管电泳的三种电化学检测即电导检测法、安培检测法和电位检测法,并与较常见的光学检测方法进行了比较。详细介绍了三种检测方法的原理及其实现方法,同时介绍了它们在无机元素分析物中的应用情况。 关键字:电化学检测、毛细管电泳;无机阴离子、金属阳离子。 目录: 1.简介--------------------------------------------------------------1 2.电导检测法--------------------------------------------------------2 2.1原理----------------------------------------------------------2 2.2实现方法------------------------------------------------------3 3安培检测法--------------------------------------------------------6 3.1原理----------------------------------------------------------6 3.2实现方法------------------------------------------------------6 4电位检测法--------------------------------------------------------5 4.1原理----------------------------------------------------------9 4.2实现方法------------------------------------------------------9 5在无机元素中的应用------------------------------------------------9 6总结-------------------------------------------------------------10 7参考文献---------------------------------------------------------10
化学发光免疫分析技术原理简介 20 世纪60 年代即有人利用化学发光法测定水样中细菌含量和菌尿症患者尿液检查。1977 年Halman 等将化学发光系统与抗原抗体反应系统相结合,创建了化学发光免疫分析法,保留了化学发光的高度灵敏性,又克服了它特异性不足的缺陷。近年来对技术与仪器的不断改进,使此技术已成为一种特异,灵敏,准确的自动化的免疫学检测方法。1996 年推出的电化学发光免疫技术,在反应原理上又具有一些新的特点。这两种技术目前已在国内一些大型医院实验室用于常规免疫学检验。 一、化学发光免疫分析法 化学发光免疫分析法( chemiluminescence immunoassay , CLlA) 是把免疫反应与发光反应结合起来的一种定量分析技术,既具有发光检测的高度灵敏性,又具有免疫分析法的高度特异性。在CLIA中,主要有两个部分,即免疫反应系统和化学发光系统。免疫反应系统与放射免疫测定中的抗原抗体反应系统相同化学发光系统则是利用某些化合物如鲁米诺( luminol) 、异鲁米诺(isolu-minol) 、金刚烷( AMPPD) 及吖啶酯( AE) 等经氧化剂氧化或催化剂催化后成为激发态产物,当其回到基态时就会将剩余能量转变为光子,随后利用发光信号测量仪器测量光量子的产额。将发光物质直接标记于抗原(称为化学发光免疫分析)或抗体上(称为免疫化学发光分析) ,经氧化剂或催化剂的激发后,即可快速稳定的发光,其产生的光量子的强度与所测抗原的浓度可成比例。亦可将氧化剂(如碱性磷酸酶等)或催化剂标记于抗原或 抗体上,当抗原抗体反应结束后分离多余的标记物,再与发光底物反应,其产生的光量子的强度也与待测抗原的浓度成比例。发光免疫分析的灵敏度高于包括RIA 在内的传统检测方法,检测范围宽,测试时间短,仅需30 - 60min 即可。试
总甲状腺素(TT4)测定试剂盒(电化学发光免疫分析法) 适用范围:本试剂盒用于体外定量测定人体血清样本中总甲状腺素(TT4)的含量。 1.1产品型号/规格:100人份/盒、200人份/盒。 1.2主要组成 试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(TT4-Cal)(选配)组成。组成及含量如下: 2.1 外观 2.1.1 试剂盒各组分应齐全、完整、液体无渗漏; 2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物; 2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物; 2.1.4 包装标签应清晰、无磨损、易识别。 2.2 空白限 应不大于0.420μg/dL 。 2.3 准确度 用T4国家标准品(150551)进行检测,实测值与理论值之比应在0.850-1.150之间。 2.4 线性 在[1.0,24.86]μg/dL范围内,线性相关系数的绝对值(|r|)应不小于0.9900。 2.5 精密度 2.5.1 分析内精密度
在试剂盒的线性范围内,浓度为(5.0±1.0μg/dL)和(20.0±4.0μg/dL)的样品检测结果的变异系数(CV)应不大于8%。 2.5.2 批间精密度 在试剂盒的线性范围内,用3个批号试剂盒分别检测浓度为(5.0±1.0μg/dL)和(20.0±4.0μg/dL)的样品,检测结果的变异系数(CV)应不大于15%。 2.6 特异性 2.6.1与三碘甲状腺原氨酸(T3) 测定浓度不低于500ng/mL的T3样品,其测定结果应不高于1.5μg/dL; 2.6.2 与反三碘甲状腺原氨酸(rT3) 测定浓度不低于50ng/mL的rT3样品,其测定结果应不高于1.5μg/dL。 2.7 效期末稳定性 本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。 2.8 溯源性 依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至国家标准品(编号150551)。
促甲状腺激素(TSH)测定试剂盒(电化学发光免疫分析法) 组成: 适用范围:本试剂盒用于体外定量测定人体血清样本中促甲状腺激素(TSH)的含量。 2.1 外观 2.1.1 试剂盒各组分应齐全、完整、液体无渗漏; 2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物; 2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物; 2.1.4 包装标签应清晰、无磨损、易识别。 2.2 空白限 应不大于0.01μIU/mL。 2.3 准确度 用TSH国家标准品(150530)进行检测,其测量结果的相对偏差应在±10%范围内。 2.4 线性 在[0.01,100.0]μIU/mL范围内,线性相关系数(r)应不小于0.9900。 2.5 精密度
2.5.1 分析内精密度 在试剂盒的线性范围内,浓度为(5.0±1.0μIU/mL)和(30.0±6.0μIU/mL)的样品检测结果的变异系数(CV)应不大于8%。 2.5.2 批间精密度 在试剂盒的线性范围内,用3个批号试剂盒分别检测浓度为(5.0±1.0μIU/mL)和(30.0±6.0μIU/mL)的样品,检测结果的变异系数(CV)应不大于15%。2.6 特异性 2.6.1 与促卵泡生成激素(FSH) 浓度不低于200mIU/mL促卵泡生成激素(FSH)样品,在本试剂盒测定结果应不大于0.01μIU/mL; 2.6.2 与促黄体生成素(LH) 浓度不低于200mIU/mL促黄体生成素(LH)样品,在本试剂盒测定结果应不大于0.01μIU/mL; 2.6.3 与人绒毛促性腺激素(HCG) 浓度不低于1000mIU/mL人绒毛膜促性腺激素(HCG)样品,在本试剂盒测定结果应不大于0.01μIU/mL。 2.7 效期末稳定性 本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。 2.8 溯源性 依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至TSH国家标准品(编号150530)。
毛细管电泳电化学检测分离测定毛发中的色氨酸酪氨酸和半胱氨酸 1.试验部分 1.1仪器与试剂 毛细管电泳-电化学检测系统(CE - ED) 为自组装, 包括±30 kV 高压电源(上海原子核研究所) ;三电极工作系统(直径为300μm的碳圆盘电极为检测电极、铂丝为辅助电极、饱和甘汞电极为参比电极);三维定位调节器(上海联谊光纤激光 器械厂);BAS LC- 3D 安培检测器(Bioanalytical Systems , USA) ;HW色谱工作 站(上海千谱软件有限公司);熔融石英毛细管(长70cm,内径25μm,河北永年光导纤维厂);超声波清洗器;毛细管清洗器(上海医科大学仪器厂);分析天平色氨酸,酪氨酸,半胱氨酸;头发样品:志愿者提供;其它试剂为分析纯。 1.2标准溶液及样品溶液的制备 标准溶液:色氨酸,半胱氨酸储备液:1.0×10- 3 g/m L,酪氨酸储备液:0.5×10- 3 g/m L,用50mmol/L硼砂-20mmol/L氢氧化钠溶液配置,再用运行缓冲液稀 释至所需浓度。 样品溶液:将头发用石油醚脱脂,干燥后称取50mg置于水解管中,加入3mL6mol/L氢氧化钠(含0.5%可溶性淀粉);水解管用真空泵抽真空3min,在酒精 喷灯上封管;然后,将封好的水解管置于110o C烘箱中水解20小时。将水解液置于已 加有2.9mL6mol/L盐酸溶液的25mL容量瓶中,用蒸馏水洗涤水解管3~4次,最后用 蒸馏水定容。 1.3 试验方法 毛细管使用前依次用0.1mol/L的NaOH、二次水、缓冲液各冲洗5min、2min、10min。自制碳圆盘电极使用前要用细砂纸打磨,并用超声波清洗2min,使用自组装的CE-ED检测系统,通过三维定位调节器使工作电极与毛细管的出口在同一直线上,并尽可能靠近毛细管的末端,以50mmol/L的硼砂(pH =8.98)缓冲液为运行液,采用电动进样,检测池内为0.1mol/L的NaO H溶液,阴极电泳槽为检测端。所有溶液使用前均用0.25μm聚丙烯滤膜过滤。 2 结果与讨论 2.1 3种氨基酸的分子量及等电点的比较 3种氨基酸的分子量:色氨酸(M r=204.11)>酪氨酸(M r=181.09)》半胱氨酸(M r=121.12);等电点:色氨酸(pI=5.89)> 酪氨酸(pI=5.66)> 半胱氨酸(pI=5.07);毛细管电泳的分
、概念 电化学发光免疫测定Electrochemiluminescence immunoassay,ECLI。 ECLI 是继放射免疫、酶免疫、荧光免疫、化学发光免疫测定以后的新一代标记免疫测定技术。电化学发光法源于电化学法和化学发光法,而ECLI 是电化学发光ECL和免疫测定相结合的产物,是一种在电极表面由电化学引发的特异性化学发光反应,包括了电化学和化学发光二个过程。 ECL 不仅可以应用于所有的免疫测定,而且还可用于DNA/RNA探针检测。 二、反应底物 ECL 反应底物有两种: ·三氯联吡啶钌[Rubpy3]2+络合物: 钌Ruthenium, Ru,原子序数44,原子量101.07。元素名来自拉丁文,原意是"俄罗斯"。1827年俄国化学家奥赞在铂矿中发现钌;1844年俄国化学家克劳斯肯定它是一种新元素。钌在地壳中的含量约为十亿分之一,是铂系元素中含量最少的一个。钌常与其它铂系元素一起分散于冲积矿床和砂积矿床中。钌有7种天然稳定同位素:钌96、98、99、100、101、102、104。 钌为银白色金属,熔点2310℃,沸点3900℃,密度12.37×103/m3。 钌的化学性质不活泼,在空气和潮湿环境中稳定;不溶于酸和王水,溶于熔融的强碱、碳酸盐、氰化物等;加热到900℃,时能与氧反应;加热时能与氟、氯、溴反应;钌有形成配位化合物的强烈倾向,还有良好的催化性能。 钌是铂和钯的有效硬化剂;金属钛中加入0.1%的钌就可大大提高耐腐蚀性;钌钼合金是一种超导体;含钌的催化剂多用于石油化工。 ·三丙胺Tripropylamine,TPA: 结构式: 点击浏览/下载该文件 三、电化学发光反应原理 电化学反应过程:在工作电极上阳极加一定的电压能量作用下,二价的三氯联吡啶钌 [Rubpy3]2+ 释放电子发生氧化反应而成为三价的三氯联吡啶 钌 [Rubpy3]3+,同时,电极表面的TPA也释放电子发生氧化反应而成为阳离子自由基 TPA+ ,并迅速自发脱去一个质子而形成三丙胺自由基 TPA·,这样,在反应体系中就存在具有强氧化性的三价的三氯联吡啶钌 [Rubpy3]3+ 和具有强还原性的三丙胺自由基 TPA·。 化学发光过程:具有强氧化性的三价的三氯联吡啶钌 [Rubpy3]3+ 和具有强还原性的三丙胺自由基 TPA·发生氧化还原反应,结果使三价的三氯联吡啶
电化学发光检测项目及其临床应用 一、甲状腺功能 甲腺原氨酸(T3, triiodothyronine) T3是甲状腺激素对各种靶器官作用的主要激素。T3(3、5、3’-三碘酪氨酸)主要在甲状腺以外,尤其是在肝脏由T4经酶解脱碘生成。因此,血清T3浓度反映出甲状腺对周边组织的功能甚于反映甲状腺分泌状态。T4转变成T3的减少会导致T3浓度的下降。见于药物的影响,如丙醇、糖皮质类固醇、胺碘酮等以及严重的非甲状腺疾病(NT I),称为“T3低下综合征”。与T4一样,99%以上的T3与运输蛋白质结合,但T3的亲和力要低10倍左右。T3测定可用于T3-甲亢的诊断,早期甲亢的查明和假性甲状腺毒症的诊断。 甲状腺素(T4, thyroxine) T4是甲状腺分泌的主要产物,也是构成下丘脑-垂体前叶-甲状腺调节系统完整性不可缺少的成份。对合成代谢有影响作用。T4由二分子的二碘酪氨酸(DIT)在甲状腺内偶联生成。T4与甲状腺球蛋白结合贮存在甲状腺滤泡的残腔中,在TSH的调节下分泌释放。血清中99%以上的T4以与其它蛋白质结合的形式存在。由于血清中运输蛋白质的浓度易受外源性和内源性作用的影响,因此,在检测血清T4浓度的过程中需考虑到结合蛋白质的状况。如果忽略这一点,结合蛋白质浓度的变化(如怀孕期、服用雌激素或者患肾病综合征等),会导致反映甲状腺代谢状况检测的错误结果。T4测定可用于甲亢、原发性和继发性甲状腺功能减退的诊断以及TSH抑制治疗的监测。 游离T3(FT3- free triiodothyronine) 三碘甲腺原氨酸(T3)是血清中的甲状腺激素之一,起调节代谢作用。测定该激素的含量对鉴别诊断甲状腺功能是否正常、亢进或低下有重要意义。绝大多数的T3与其转运蛋白质(TBG、前白蛋白、白蛋白)结合,fT3是T3的生理活性形式。fT3测定的优点
毛细管电泳中常用的检测方法 毛细管电泳(C E 以其高效、快速的分离, 成为一种令人瞩目的分析手段。为了便于热量散失和进行柱上检$lJ , 采用了极小内径的毛细管(≤50 umi.d. , 这样允许进样量就很小(10 一9 g 。如此小的进样量要求有高灵敏的检测方法, 才能进行定性、定量分析。 紫外吸收法: 一般, 常用于C E 的检测器是市售的紫外和荧光检测器。当采用紫外一可见吸收法时, 石英毛细管壁的内涂层常常用有机溶剂溶解或灼烧而刮去, 使出现一个“小窗口” , 作为柱上检测的流通池。内径很小的毛细管使得流通池的长度也相应很小, 检测灵敏度相当有限, 尤其在生物样品分析中常常需要先行样品预富集然后再检测, 以提高灵敏度。在使用长方形徽面的毛细管进行电泳分离分析时,柱上检测的光学流通池长度明显增大, 使检测灵敏度提高7 1 5 倍。采用高能量的光源, 如氨灯、激光等, 可较大地提高检测灵敏度, 但费用较高, 又因可供选择使用的人射光波长范围较窄, 限制了它的应用。 荧光检测法: 荧光检测的灵敏度比紫外吸收法高几个数量级。对于有适当的激发荧光和发射荧光的供试品, 采用激光诱导荧光检测法和光电倍增管, 可使检测灵敏度大大提高, 而对于绝大多数无自然荧光的化合物, 则必须进行柱前或柱后衍生化, 才能进行荧光检测。 间接检测法: 对供试品进行衍生化的操作繁琐, 且易引入误差, 对于被测浓度极低的生物样品更是如此。于是, 间接检测法应运而生。间接检测就是在电泳缓冲液中加入具有检测响应的检测剂, 如发色团、荧光物质等, 作为本底响应,以产生基线信号。供试品进样后, 供试品离子与反电荷的检测剂离子形成离子对, 或置换了检测剂的同电荷离子, 分别产生正峰和负峰,使基线信号发生改变而被检测。在间接荧光法中, 被分析
常见化学发光免疫分析技术比较 1、化学发光免疫分析 化学发光免疫分析(chemiluminescence immunoassay,CLIA),英音:[,kemi,lju:mi'nes?ns] [,imju:n?u?'sei] 是将具有高灵敏度的化学发光测定技术与高特异性的免疫反应相结合,用于各种抗原、半抗原、抗体、激素、酶、脂肪酸、维生素和药物等的检测分析技术。是继放免分析、酶免分析、荧光免疫分析和时间分辨荧光免疫分析之后发展起来的一项最新免疫测定技术。 CLIA是将具有高灵敏度的化学发光测定技术与高特异性的免疫反应相结合,用于各种抗原、半抗原、抗体、激素、酶、脂肪酸、维生素和药物等的检测分析技术。是继放免分析、酶免分析、荧光免疫分析和时间分辨荧光免疫分析之后发展起来的一项最新免疫测定技术。 1.1、化学发光免疫分析原理 化学发光免疫分析包含两个部分, 即免疫反应系统和化学发光分析系统。化学发光分析系统是利用化学发光物质经催化剂的催化和氧化剂的氧化, 形成一个激发态的中间体, 当这种激发态中间体回到稳定的基态时, 同时发射出光子(hv) , 利用发光信号测量仪器测量光量子产额。免疫反应系统是将发光物质(在反应剂激发下生成激发态中间体) 直接标记在抗原(化学发光免疫分析) 或抗体(免疫化学发光分析) 上, 或酶作用于发光底物。 1.2、化学发光免疫分析类型
化学发光免疫分析法以标记方法的不同而分为两种: (1)化学发光标记免疫分析法; (2)酶标记、以化学发光底物作信号试剂的化学发光酶免疫分析法 1.2.1化学发光标记免疫分析 化学发光标记免疫分析又称化学发光免疫分析(CL IA ) , 是用化学发光剂直接标记抗原或抗体的免疫分析方法。常用于标记的化学发光物质有吖啶酯类化合物-acridiniumester (AE) , 是有效的发光标记物,其通过起动发光试剂(NaOH-H2O2) 作用而发光, 强烈的直接发光在一秒钟内完成, 为快速的闪烁发光。吖啶酯作为标记物用于免疫分析, 其化学反应简单、快速、无须催化剂; 检测小分子抗原采用竞争法, 大分子抗原则采用夹心法, 非特异性结合少, 本底低; 与大分子的结合不会减小所产生的光量, 从而增加灵敏度。 1.2.2化学发光酶免疫分析 从标记免疫分析角度, 化学发光酶免疫分析(chemiluminescent enzyme immunoassay,CLEIA ) , 应属酶免疫分析, 只是酶反应的底物是发光剂, 操作步骤与酶免分析完全相同: 以酶标记生物活性物质(如酶标记的抗原或抗体) 进行免疫反应, 免疫反应复合物上的酶再作用于发光底物, 在信号试剂作用下发光, 用发光信号测定仪进行发光测定。目前常用的标记酶为辣根过氧化物酶(HRP) 和碱性磷酸酶(AL P) , 它们有各自的发光底物。 12.2.1HRP 标记的CLEIA
电化学发光的基本原理 电化学发光免疫测定(ECLI)是一种在电极表面由电化学引发 的特异性发光反应,包括电化学和化学发光两个部分。分析中应用 的标记物为电化学发光的底物三联吡啶钌或其衍生N-羟基琥珀酰胺(NHS)酯,可通过化学反应与抗体或不同化学结构抗原分子结合,制成标记的抗体或抗原。ECLL的测定模式与ELISA相似。 基本原理:发光底物二价的三联吡啶钉及反应参与物三丙胺在 电极表面失去电子而被氧化。氧化的三丙胺失去一个H+而成为强还原剂,将氧化型的三价钌还原为激发态的二价钌,随即释放光子而 恢复为基态的发光底物。医学教育网搜|集整理这一过程在电极表面 周而复始地进行,不断地发出光子而常保持底物浓度的恒定。 电化学发光是化学发光方法与电化学方法相互结合的产物,是 指通过电化学方法来产生一些特殊的物质,然后这些电生的物质之 间或电生物质与其它物质之间进一步反应而产生的一种发光现象。 电化学发光保留了化学发光方法所具有的灵敏度高、线性范围宽、观察方便和仪器简单等优点;同物时具有许多化学发光方法无 法比拟的优点,如重现性好、试剂稳定、控制容易和一些试剂可以 重复使用等优点,广泛地应用于生物、医学、药学、临床、环境、 食品、免疫和核酸杂交分析和工业分析等领域。在21世纪中必将继 续为解决人类面临的各种重大问题发挥更加显著的作用。因此有必 要对电化学发光在分析中的应用有更加全面的了解。
电化学发光的应用 1、电极表面活性分布的表征 利用电化学发光成像法可以很好地观察电极表面电化学发光强度的分布情况,而电化学发光强度对电极表面的活性具有很大的依赖性,因此利用电化学发光成像法可以直观地反映电极表面活性分布。 该方法是由Engstrom等于1987年提出的,他们观察到在新抛光的玻碳电极上电化学发光强度分布十分均匀,而在环氧树脂浸渍过的网状玻碳电极上,电化学发光强度的分布不均匀,通过与其它方法相对照,发现电化学发光强度分布能够很好地反映出电极表面活性分布,并且具有微米级的空间分辨能力。在此基础上,他们把电化学发光成像法用于研究碳糊电极表面活性点的分布,观察到碳糊电极表面存在。着活性区域和非活性区域,对于了解碳糊电极的电化学行为具有一定的意义。 由于电化学发光成像法具有直观和简单等优点,许多科学工作者先后将该方法用于表征化学修饰电极表面的活性分布。如Hopper 等用该方法研究了电极表面的电荷对电子转移性质的影响;Pantano 等用该方法研究了电极表面羧基的分布对电子转移性质的影响;ShuItz等用该方法研究了聚合物在电极上的附着情况。从上面的文献可以看出,电化学发光成像法对于了解电极表面的活性分布及其与电极性能之间的关系,进而制备出具有特定功能的电极具有较好的参考价值。