
水果中总酸度的测定
一、目的要求:
1.学会水果样品的预处理方法
2.掌握用酸碱滴定法测水果样品中总酸度的原理和方法
3、学会合理制定分析项目的顺序,做到合理安排分析时间,合理处理样品。
4、能熟练制备实训过程中所需要的标准溶液。
5、能规范记录数据并进行数据处理。
二、原理:
,因此,不能用直接法配制标准1. NaOH标准溶液的标定 NaOH 易吸收水分及空气中的 CO
2
溶液。需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。以酚酞为指示剂,当滴定至终点溶液呈浅红色,且 30S不褪色时。反应如下:
KHC8H4O4+NaOH=KNaC8H4O4+ H2O
2.水果总酸度的测定根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。当滴定至终点溶液呈浅红色,且 30S不褪色时,根据滴定时消耗的标准 NaOH 溶液的体积,可算出试样中的总酸度。其反应如下:
HAC+NaOH→NaAc+H2O
三、所需仪器、试剂:
仪器:酸碱式滴定管、锥形瓶、移液管、量筒、烧杯、容量瓶、胶头滴管、洗耳球、水浴锅、铁架台、电子天平、玻璃棒、小纸片、干燥的纱布
的蒸试剂: 0.1000mol/L NaOH 溶液、邻苯二甲酸氢钾、酚酞指示剂、水果试样、无CO
2
馏水
四、实验步骤:
1. 0.1000mol/LNaOH 标准溶液的配制和标定
称取固体NaOH约2g放置在500mL的烧杯中,先加入100ml溶解,再加水稀释成 500mL 溶液,混匀,放入烧杯中,待标定。
用减量法准确称取0.41~0.45g邻苯二甲酸氢钾3份,分别放入250mL锥形瓶中,加25mL 无CO2蒸馏水溶解。然后加1~2滴酚酞指示剂,用 NaOH 标准溶液滴定至终点(至粉红色,并保持30s不褪色为终点)。记录每次消耗 NaOH 溶液的体积。
2.试样处理:
取水果试样,需去皮、去柄、去核,切成块状,置于搅拌机中捣碎并混匀。准确移取 25mL 水果试样,加100mL无CO
的蒸馏水,稀释定容为250mL溶液。然后倒入烧杯中在 75~80℃
2
水浴上加热30分钟。冷却后过滤,滤液倒入容量瓶中备用。
3.滴定:
准确吸取20mL滤液三份于250mL锥形瓶中,各加25mL水稀释。加1-2滴酚酞指示剂,用NaOH标准溶液滴定至终点,至粉红色30S不褪色。记录NaOH消耗量的体积,平行三次。
五、计算公式
C NaOH=m KHC8H4O4/(V NaOH×M KHC8H4O4)X1000
ρHAc=(C NaOH×V NaOH×M Hac×10-3)/(20.00/250.0×25.00)
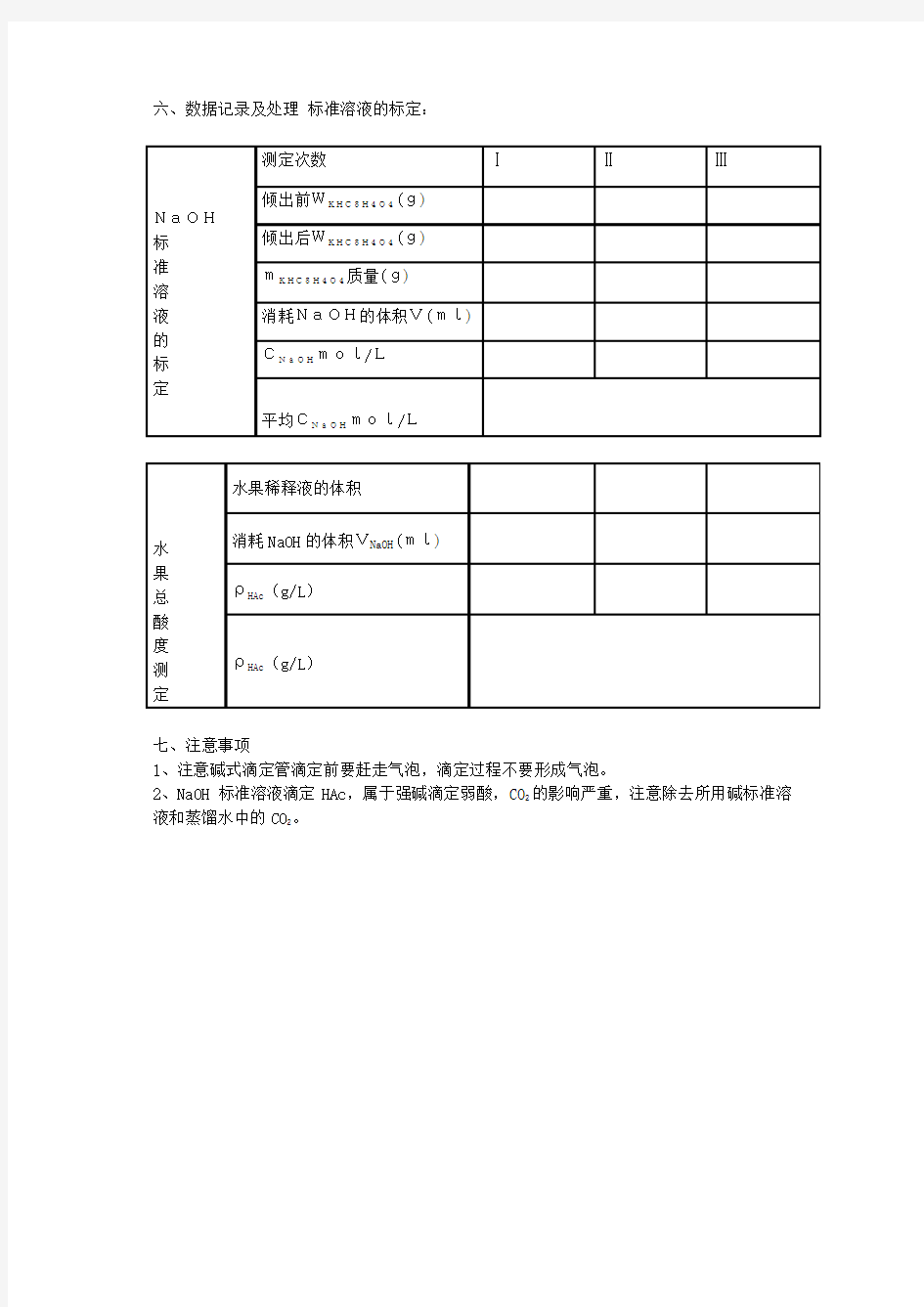
六、数据记录及处理标准溶液的标定:
七、注意事项
1、注意碱式滴定管滴定前要赶走气泡,滴定过程不要形成气泡。
的影响严重,注意除去所用碱标准溶2、NaOH 标准溶液滴定HAc,属于强碱滴定弱酸,CO
2
。
液和蒸馏水中的CO
2
食醋中总酸量的测定 实验目的 1、学习强碱滴定弱酸的基本原理及指示剂的选择原则。 2、掌握食醋中总酸量的测定原理和方法。 3、熟悉移液管和容量瓶的正确使用方法。 实验原理 食醋中的主要成分是醋酸(CH 3COOH )常简写为HAc ,此外还含有少量其他有机弱 酸,如乳酸等。当以NaOH 标准溶液滴定时,凡是C 810-?θ a K 的弱酸均可以被滴定,因 此测出的是总酸量,但分析结果通常用含量最多的HAc 表示。CH 3COOH 与NaOH 的反应为:NaOH + CH 3COOH = CH 3COONa + H 2O 由于这是强碱滴定弱酸,计量点时生成CH 3COONa ,溶液的pH 大约为8.7,故可选用酚酞作指示剂,但必须注意CO 2对反应的影响。食醋是液体样品,通常是量其体积而不是称其质量,因而测定结果一般以每升或每100mL 样品所含CH 3COOH 的质量表示,即以醋酸的密度ρ(HAc)表示,其单位为g 〃L -1或g/100mL 。 食用醋往往有颜色,会干扰滴定,应先经稀释或加入活性炭脱色后,再进行测定。食醋中含CH 3COOH 的质量分数一般在3%~5%,应适当稀释后再进行滴定。 仪器与试剂 碱式滴定管(50mL ),移液管(10mL ,25 mL ),容量瓶(250mL ),锥形瓶(250mL ),洗耳球。 0.1 mol 〃L -1 NaOH 标准溶液(要求实验前标定),0.2%酚酞乙醇溶液, 食醋(白醋)样品。 实验步骤 用移液管吸取25.00 mL 食醋样品,放入250 mL 容量瓶中,然后用无CO 2的蒸馏水稀释容至刻度,摇匀备用。 用移液管吸取25.00 mL 已稀释的食醋样品于250mL 锥形瓶中,滴加2~3滴酚酞指示剂。 用NaOH 标准溶液滴定到溶液呈微红色,30s 内不褪色即为终点,记录所消耗NaOH 标准溶液的体积。平行测定3次,要求每次测定结果的相对平均偏差不大于0.3%,计算食醋的总酸量ρ(HAc),ρ(HAc)按下式计算: ρ(HAc)= )(1) ()()(-????L g f V HAc M NaOH V NaOH c 样
酸度测定操作方法 一. 总酸度的测定 本法采用酸碱滴定法。取试样10ml,用0.1mol/L氢氧化钠标准溶液滴定, 所消耗的毫升数用点数表示。 A.1 试剂 氢氧化钠:0.1mol/L标准溶液按GB/T 601规定; 酚酞指示剂:1.0/L 按GB/T 603规定。 A.2 试验方法 吸取10ml试液于250ml锥形烧瓶中,加50ml蒸馏水,加3~4滴酚酞指 示剂。用0.1mol/L氢氧化钠标准溶液滴至溶液由无色变为粉红色为终点。 记下消耗氢氧化钠标准溶液毫升数V1。 A.3 计算方法 总酸度点数按下列公式计算: 总酸度(点)= 10V1 c/ 0.1V 式中: V1 —滴定时耗去氢氧化钠标准溶液毫升数,mL; c—氢氧化钠标准溶液实际浓度,mol/L; V—取样毫升数,mL。 二. 游离酸度的测定 本法采用酸碱滴定法。取试样10ml,用0.1mol/L氢氧化钠标 准溶液滴定,所消耗的毫升数用点数表示。 A.1试剂 氢氧化钠:0.1mol/L标准溶液按GB/T 601规定; 溴酚蓝指示剂:0.4mol/L 按GB/T 603规定。 A.2试验方法 吸取10ml试液于250ml锥形烧瓶中,加50ml蒸馏水,加2~3滴溴酚 蓝指示剂。用0.1mol/L氢氧化钠标准溶液滴至溶液由黄色变至蓝紫色 为终点。记下消耗氢氧化钠标准溶液毫升数A。 A.3计算方法 游离酸度点数按下列公式计算: 游离酸度(点)= 10Ac/ 0.1V 式中: A —滴定时耗去氢氧化钠标准溶液毫升数,mL; c—氢氧化钠标准溶液实际浓度,mol/L; V—取样毫升数,mL。 编制苏辉审核韩娟批准 山东金泰机械制造有限公司
实训一:水果中总酸度的测定 一、目的要求: 1.学会水果样品的预处理方法 2.掌握用酸碱滴定法测水果样品中总酸度的原理和方法 3、学会合理制定分析项目的顺序,做到合理安排分析时间,合理处理样品。 4、能熟练制备实训过程中所需要的标准溶液。 5、能规范记录数据并进行数据处理。 二、实训原理: 1. NaOH标准溶液的标定 NaOH易吸收水分及空气中的CO2,因此,不能用直接法配制标准溶液。需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。以酚酞为指示剂,当滴定至终点溶液呈浅红色,且30S不褪色时。反应如下: KHC8H4O4+NaOH=KNaC8H4O4+ H2O 2.水果总酸度的测定 根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。当滴定至终点溶液呈浅红色,且30S不褪色时,根据滴定时消耗的标准NaOH溶液的体积,可算出试样中的总酸度。其反应如下: HAC+NaOH→NaAc+H2O 三、实训所需仪器、试剂:洗仪器:袁驰 仪器:酸碱式滴定管、锥形瓶、移液管、量筒、烧杯、容量瓶、胶头滴管、洗耳球、水浴锅、铁架台、电子天平、玻璃棒、小纸片、干燥的纱布、试剂: 0.1000mol/LNaOH溶液、邻苯二甲酸氢钾、酚酞指示剂、水果试样、的蒸馏水、 无水CO 2 四、实验步骤: 1. 0.1000mol/LNaOH标准溶液的配制和标定配制:马佳红 称取固体NaOH约2g放置在500ml的烧杯中,先加入100ml少溶解,再加水稀释成500ml溶液,混匀,放入烧杯中,待标定。标定:曹芬芳用减量法准确称取0.41~0.45g邻苯二甲酸氢钾3份,分别放入250ml锥形瓶中,加25mL无CO2蒸馏水溶解。
一、总酸度的测定(滴定法) (根据GB/T12456-1990) 1.原理 用标准碱液滴定食品中的酸,中和生成盐,用酚酞做指示剂。当滴定终点 (pH=8.2,指示剂显红色)时,根据耗用的标准碱液的体积,计算出总酸的含量。 反应式:RCOOH+NaOH →RCOONa+H2O 2. 适用范围 本法适用于各类色浅的食品中总酸含量的测定。 3.试剂 ①0.1000mol/L NaOH 标准溶液 称取110g NaOH 于250mL 烧杯中,加入100mL 无CO 2的蒸馏水振摇使其溶解,冷却后倒入聚乙烯塑料瓶中静止数日,澄清后备用。量取上清液5.4mL ,加入无CO 2的蒸馏水稀释至1000毫升,摇匀。 ②1%酚酞乙醇溶液 称取酚酞1g 溶于60mL 95% 乙醇中,用水稀释至100 mL 。 4、仪器: 碱式滴定管 水浴锅 5、分析步骤 (1)样液的制备 液体试样:不含CO2的试样混合均匀后直接取样。含CO2的试样,如饮料、酒等,将试样置于40℃水浴上加热30min ,以除去CO2,冷却后备用。 (2)测定准确吸取50mL 试样制备液,于250mL 的锥形瓶内,加3~4滴酚酞指示液,以0.1mol/L NaOH 标准溶液滴定至浅红色,30S 内不褪色,记录消耗0.1mol/L 氢氧化钠滴定液的体积V1,同一试样必须平行测定两次,以其平均值作为测定结果。同时做空白试验。 两个平行样的测定值相差不得大于平均值的 2%。 式中: c------标准NaOH 溶液的浓度,mol/L V -----滴定消耗标准NaOH 溶液的体积,mL m------样品质量或体积,g 或ml V 0 ----样品稀释液总体积,mL; ) 1.......(%.........10025050K c 21???-=m V V X )(
实训一:水果总酸度的测定 一、实验目的 1、学会水果样品的预处理方法 2、掌握用酸碱滴定法测定水果样品中总酸度的原理和方法 3、学会合理指定分析项目的顺序,做到合理安排分析时间,合理处理样品。 4、能熟练纸杯实过程中所需要的标准溶液。 5、能规范记录数据并进行数据处理。 二、实验原理 ? 1. NaOH标准溶液的标定 NaOH易吸收水分及空气中的CO2,因此,不能用直接法配制标准溶液。需需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。以酚酞为指示剂,当滴定至终点溶液呈浅红色,且30S不褪色时。反应如下:?KHC8H4O4+NaOH=KNaC8H4O4+ H2O ? 2.水果总酸度的测定 根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞为指示剂。当滴定至终点溶液呈浅红色,30s不褪色时,根据滴定时消耗的标准碱溶液的体积,可算出试样中的总酸度。其反应如下: ?HAc+NaOH →NaAc+H2O 三、实验仪器及试剂 ?试剂:0.1000mol/LNaOH标准溶液、邻苯二甲酸氢钾、酚酞指示剂、无CO2的蒸馏水、水果试样(梨) ?仪器:洗耳球、玻璃棒、量筒、移液管、电子天平、 ?水浴锅、锥形瓶、容量瓶、酸碱滴定管、烧杯、小纸片、胶头滴管、干燥的纱布、铁架台 四、实验步骤 ?1、0.1000mol/LNaOH标准溶液的标定:(顾嘉俊王英权) ?0.1000mol/lNaoH标准溶液已经配制好,待标定。 ?用减量法准确称取0.4—0.45g邻苯二甲酸氢钾三份,分别放入250ml锥形瓶中,加25ml无CO2的蒸馏水溶解。 ?然后加1—2d 酚酞指示剂,用NaOH溶液滴定至终点(至粉红色,并保持30s不褪色为终点)。 ?记录每次消耗NaOH溶液的体积。 ?2、试样的处理:(朱方灵、陈鹏)
第五章酸度的测定 ●食品中的有机酸影响食品的香味、颜色、稳定性和质量的品质。果实蔬菜中含有的 酸种类很多。有机酸、无机酸、酸式盐以及某些酸性有机化合物。(如单宁、pro分解物、果胶质分解物等) ●果蔬中的有机酸主要是苹果酸、柠檬酸、酒石酸(通常称为果酸)还含有少量 草酸、鞣酸、苯甲酸、醋酸和蚁酸等。 第一节总酸度的测定 ●一、概念: ●1、酸度:已离解的酸的浓度(有效酸度)指溶液中H+的浓度。正确讲是H+的活度。 常用PH值表示,可用酸度计测量。 ●2、总酸度:包括未离解的酸的浓度和已离解的酸的浓度。用当量浓度表示,用滴定 法来确定。用滴定法测定总酸度,可将样品直接滴定,或将样品用水浸浦后,不断摇动滴定其滤液. ●二、测定方法 ●1、测定原理: ●食品中的酒石酸、苹果酸、柠檬酸、草酸等有机酸其电离常数均大于10-8, 可以用强碱标准溶液直接滴定。反应如下 ●RCOOH+NaOH——RCOONa+H2O ●用酚酞作指示剂,滴定至溶液呈现浅红色,30秒不褪色为终点。根据所消耗标准碱 溶液的浓度和体积,计算样品中酸的百分含量(%) ●2、测定方法: ●(1)样品处理: ●固态样品:果蔬原料等除去非可食部分。放于组织捣碎机中捣碎。 ●液态样品:如碳酸饮料先在50℃水浴加热驱除CO2。牛乳、果汁可直接滴定。●(2)制取滤液:精确称取10—20g捣碎的样品,加少量水混匀,定容至250ml, 在70—80℃水浴上加热半小时,冷却加水至刻度,以干燥滤纸过滤。 ●样品——溶解——定容——加热——冷却——加水至刻度——干燥滤纸过滤 ●(3)滴定:用移液管移取50ml滤液+酚酞(3—4滴)用0.1mol NaOH标准溶液滴 定至浅红色,30秒不褪色为终点,记录NaOH用量。 ●(4)计算:X(%)=V×N×K×5/W ×100 ●X——总酸度的百分含量V——滴定时消耗NaOH的毫升数 ●N——NaOH的当量浓度W——样品重量 ●K——换算为适当酸之系数,苹果酸——0.067 醋酸——0.060 酒石酸 ——0.075 柠檬酸0.070 乳酸0.090 ●说明1、一般情况下,橘子、柚子、柠檬其总酸以柠檬酸汁;葡萄以酒石酸计;苹 果、桃、李子以苹果酸汁;肉、鱼、乳、酱油以乳酸汁。 ●总挥发酸主要是醋酸和痕量的甲酸可用直接法和间接法测定。 ●一、测定方法: ●直接法:通过水蒸汽蒸馏或溶剂萃取把挥发酸分离出来,然后用标准碱液滴定的方 法。 ●间接法:将挥发酸蒸发除去后,滴定不挥发酸,最后从总酸度中减去不挥发酸,即 得出挥发酸的含量。 ●二、测定原理:挥发酸可用水蒸汽蒸馏使之分离,冷凝收集后,用标准碱液滴定。
酸度测定方法 1、原理 在水中,由于溶质的解离或水解 (无机酸类硫酸亚铁和硫酸铝等而产生氢离子,它们与碱标准溶液作用至一定 pH 值所消耗的量,定为酸度。酸度数值的大小,随所用指示剂指示终点 pH 值的不同而异。滴定终点的 pH 值有两种规定,即 8.3 和 3.7。用氢氧化钠溶液滴定到 pH8.3(以酚酞作指示剂的酸度,称为“酚酞酸度”,又称总酸度,它包括强酸和弱酸。 2、试剂 无二氧化碳水 氢氧化钠标准溶液 酚酞指示剂 邻苯二甲酸氢钾 3、实验仪器 50mL 碱式滴定管 250mL 锥形瓶 20mL 移液管 100mL 量筒 铁架台 4、实验内容和步骤 (1氢氧化钠标准溶液标定
称取在 105~110℃干燥过的基准试剂级苯二甲酸氢钾 (KHC8H 4O 4 约 0 5g(称准至 0.0001g 置于 250mL 锥形瓶中,加无二氧化碳水 l00mL 使之溶解,加入 4滴酚 酞指示剂, 用待标定的氢氧化钠标准溶液滴定至浅红色为终点。同时用无二氧化碳水做空白滴定按下式进行计算。 氢氧化钠标准溶液浓度 c (mol/L = m ×1000 / [ (V 1-V 0×204.23 ] 式中 m —— 称取苯二甲酸氢钾的质量 (g V 0——滴定空白时所耗氢氧化钠标准溶液体积 (mL V 1 ——滴定苯二甲酸氢钾时所耗氢氧化钠标准溶液的体积 (mL 204.23——苯二甲酸氨钾 (KHC8H 4O 4 摩尔质量 (g/mol (2测定酸度 取水样 20mL 于 250mL 锥形瓶中,用无二氧化碳水稀释至 100mL , 加入 4滴酚酞指示剂,用氢氧化钠标淮溶液滴定至溶液刚变为浅红色为终点记录用量 V2。 5、结果计算 酚酞酸度 (总酸度 CaCO 3, mg/L= c ×V 2×50×1000 / V 式中:c ——标准氢氧化钠溶液浓度 (mol/L V 2———用酚酞作滴定指示剂时消耗氢氧化钠标准溶液的体积 (mL V ——水样体积 (mL 50——碳酸钙 (1/2CaCO3 摩尔质量 (g/mol 附:碱式滴定管使用方法 (1试漏。给碱式滴定管装满水后夹在滴定管架上静量 1-2分钟。若有漏水应更换橡皮管或管内玻璃珠,直至不漏水且能灵活控制液滴为止。
学号姓名 实验三食品中总酸的测定(滴定法) 一、实验原理 果汁具有酸性反应,这些反应取决于游离态的酸以及酸式盐存在的数量。总酸度包括未解离酸的浓度和已解离酸的浓度。酸的浓度以摩尔浓度表示时,称为总酸度。含量用滴定法测定。果蔬中含有各种有机酸,主要有苹果酸、柠檬酸、酒石酸、草酸……。果蔬种类不同,含有机酸的种类和数量也不同,食品中酸的测定是根据酸碱中和的原理,即用标定的氢氧化钠溶液进行滴定。 二、材料、仪器与试剂 (一)材料:西红柿、苹果、果汁等 (二)仪器:碱式滴定管(20mL)、容量瓶(100mL)、移液管(10mL)、烧杯(100mL)、研钵或组织捣碎机、100ml量筒(量酒精)、1%酚酞指示剂、胶头滴管/滴瓶、容量瓶(1000mL)、布氏漏斗+滤纸、天平、三角烧瓶、洗瓶、活性炭(脱色)、和板、蒸馏水。 (三)试剂 1).0.1mol/L氢氧化钠:称4.0g氢氧化钠定容至1000mL,然后用0.1mol/L邻苯二甲酸氢钾标定,若浓度太高可酌情稀释。 2).1%酚酞指示剂:称1.0g酚酞,加入100mL50%的乙醇溶解。 三、操作步骤 1)0.1mol/L NaOH标准溶液的标定:将基准邻苯二甲酸氢钾加入干燥的称量瓶内,于105-110℃烘至恒重,用减量法准确称取邻苯二甲酸氢钾约0.6000克,置于250 mL锥形瓶中,加50 mL无CO2蒸馏水,温热使之溶解,冷却,加酚酞指示剂2-3滴,用欲标定的0.1mol/L NaOH溶液滴定,直到溶液呈粉红色,半分钟不褪色。同时做空白试验。 2)样品的处理与测定:准确称取混合均匀磨碎的样品10.0g(或吸10.0mL样品液),转移到100mL容量瓶中,加蒸馏水至刻度、摇匀。用滤纸过滤,准确吸取滤液20mL放入100mL 三角瓶中,加入1%酚酞2滴,用标定的氢氧化钠滴定至初显粉色在0.5min内不褪色为终点,记下氢氧化钠用量,重复三次,取平均值。 四、实验结果 式中:V——样品稀释总体积(mL)V1——滴定时取样液体积V2——消耗氢氧化
水果中总酸度的测定 一、目的要求: 1.学会水果样品的预处理方法 2.掌握用酸碱滴定法测水果样品中总酸度的原理和方法 3、学会合理制定分析项目的顺序,做到合理安排分析时间,合理处理样品。 4、能熟练制备实训过程中所需要的标准溶液。 5、能规范记录数据并进行数据处理。 二、原理: ,因此,不能用直接法配制标准1. NaOH标准溶液的标定 NaOH 易吸收水分及空气中的 CO 2 溶液。需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。以酚酞为指示剂,当滴定至终点溶液呈浅红色,且 30S不褪色时。反应如下: KHC8H4O4+NaOH=KNaC8H4O4+ H2O 2.水果总酸度的测定根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。当滴定至终点溶液呈浅红色,且 30S不褪色时,根据滴定时消耗的标准 NaOH 溶液的体积,可算出试样中的总酸度。其反应如下: HAC+NaOH→NaAc+H2O 三、所需仪器、试剂: 仪器:酸碱式滴定管、锥形瓶、移液管、量筒、烧杯、容量瓶、胶头滴管、洗耳球、水浴锅、铁架台、电子天平、玻璃棒、小纸片、干燥的纱布 的蒸试剂: 0.1000mol/L NaOH 溶液、邻苯二甲酸氢钾、酚酞指示剂、水果试样、无CO 2 馏水 四、实验步骤: 1. 0.1000mol/LNaOH 标准溶液的配制和标定 称取固体NaOH约2g放置在500mL的烧杯中,先加入100ml溶解,再加水稀释成 500mL 溶液,混匀,放入烧杯中,待标定。 用减量法准确称取0.41~0.45g邻苯二甲酸氢钾3份,分别放入250mL锥形瓶中,加25mL 无CO2蒸馏水溶解。然后加1~2滴酚酞指示剂,用 NaOH 标准溶液滴定至终点(至粉红色,并保持30s不褪色为终点)。记录每次消耗 NaOH 溶液的体积。 2.试样处理: 取水果试样,需去皮、去柄、去核,切成块状,置于搅拌机中捣碎并混匀。准确移取 25mL 水果试样,加100mL无CO 的蒸馏水,稀释定容为250mL溶液。然后倒入烧杯中在 75~80℃ 2 水浴上加热30分钟。冷却后过滤,滤液倒入容量瓶中备用。 3.滴定: 准确吸取20mL滤液三份于250mL锥形瓶中,各加25mL水稀释。加1-2滴酚酞指示剂,用NaOH标准溶液滴定至终点,至粉红色30S不褪色。记录NaOH消耗量的体积,平行三次。 五、计算公式 C NaOH=m KHC8H4O4/(V NaOH×M KHC8H4O4)X1000 ρHAc=(C NaOH×V NaOH×M Hac×10-3)/(20.00/250.0×25.00)
食用醋中总酸度的测定 一、【实验目的与要求】 1. 熟练掌握酸碱滴定的操作技术; 2. 掌握碱标准溶液的配制和标定方法,对基准物质的性质和应用有所了解; 3. 掌握食用醋总酸度的测定原理及方法; 4. 掌握指示剂的选择原则; 5. 了解强碱滴定弱酸滴定过程中pH值变化、滴定突跃及指示剂的选择。 二、【实验原理】 化学分析中的酸碱滴定是将已知准确浓度的溶液(称作标准溶液)滴加到待测定物质的溶液中,到标准溶液与待测溶液按一定的化学计量关系完全反应为止,然后根据标准溶液的消耗量和化学计量关系来计算待测组分的量,这种方法快速迅速,而且操作简单,因此非常适用于一般酸碱浓度的测定。 食用醋的主要成分是醋酸(HAc,含量大约为3%~5%)和少量的其它有机弱酸等。用NaOH作标准溶液滴定食用醋时,滴定反应为: NaOH + HAc == NaAc + H2O n NaOH + H n A (有机弱酸) == Na n A + n H2O 本滴定反应类型为强碱滴定弱酸,产物是弱酸强碱盐,测定结果为食用醋中醋酸的总酸度,用ρHAc (g·L-1)表示。由于滴定突跃范围在碱性范围,故指示剂可选用酚酞、百里酚酞等,本实验选择酚酞作为滴定反应指示剂。 三、【仪器、试剂与材料】 1. 仪器: 电子天平,碱式滴定管,试剂瓶,移液管,锥形瓶,烧杯,量筒,台秤。 2. 试剂和材料: NaOH标准溶液(0.1 mol·L-1),邻苯二甲酸氢钾(基准物质),酚酞指示剂(0.2%的乙醇溶液),食用醋。 四、【实验步骤】 1. NaOH标准溶液(0.1 mol·L-1)的配制和标定 用烧杯在台秤上称取固体NaOH 4.3 g左右,加入煮沸除去CO2的蒸馏水少许,快速冲
食品中总酸的测定 1.实验原理 食品中的酒石酸、苹果酸、柠檬酸、草酸、醋酸等有机酸,其电离常数Ka均大于10^(-8),可以用强碱标准溶液直接滴定试样中的酸,以酚酞为指示剂确定滴定终点。按碱液的消耗量计算食品中的总酸含量。测定结果包括了未离解的酸的浓度和已离解的酸的浓度。 2.仪器与试剂 (1)仪器酸碱滴定装置;分析天平,感量分别为0.0001g及0.001g;组织捣碎机;研钵。 (2)实验用水实验用水应符合GB/T6682规定的二级水规格或蒸馏水,使用前应经煮沸,冷却。 (3)试剂 ①NaOH标准滴定溶液(0.1mol/L) ②1%酚酞溶液称取1g酚酞,溶于60ml95%乙醇中,用水稀释 至100ml。 3.实验步骤 (1)样品预处理 ①固体样品。取有代表性的固体样品至少200g,用捣碎机捣碎 至均匀,置于密闭玻璃容器内。 ②固、液样品。取按比例组成的固、液样品至少200g,用研 钵或组织捣碎机捣碎混匀后置于密闭的玻璃容器内。
③含二氧化碳的液体样品。至少取200g样品至500ml烧杯中置于电炉上,边搅拌边加热至微沸腾,保持2min,冷却,称量,用煮沸过的水补至煮沸前的质量,置于密闭玻璃容器中。 ④不含二氧化碳的液体样品。充分混匀均匀,置于密闭玻璃容器内。 (2)测定试液的制备 ①液体样品。若总酸含量小于或等于4g/kg,将试液用快速滤纸过滤。收集滤液,用于测定。若总酸含量大于4g/kg,称取10~50g 样品,用煮沸过的水定容至250ml,过滤。收集滤液,用于测定。 ②固体、半固体样品。称取均匀样品10~50g,精确至0.001g,置于烧杯中。用约80 煮沸过的水150ml将烧杯中的内容物转移到250ml容量瓶中,置于沸水浴中煮沸30min(摇动2~3次,使试样中的有机酸全部溶解于溶液中),取出,冷却至室温,用煮沸过的水定容至250ml。用快速滤纸过滤。收集滤液,用于测定。 (3)样品测定 ①准确吸取试样滤液25~50ml,使之含0.035~0.07g酸,置于250ml 锥形瓶中,加水40~60ml及0.2 1%的酚酞指示剂,用0.1mol/L NaOH 标准溶液滴定至微红色且30s不褪色。记录消耗0.1mol/L NaOH标准滴定溶液的体积(V1)。同一被测样品须滴定两次。 ②用水代替样品做空白试验,操作相同。记录消耗0.1mol/L NaOH 标准滴定溶液的体积(V2)。 (4)实验数据记录见表
-总酸的测定(滴定法)- 一、原理 果汁具有酸性反应,这些反应取决于游离态的酸以及酸式盐存在的数量。总酸度包括未解离酸的浓度和已解离酸的浓度。酸的浓度以摩尔浓度表示时,称为总酸度。含量用滴定法测定。果蔬中含有各种有机酸,主要有苹果酸、柠檬酸、酒石酸、草酸……。果蔬种类不同,含有机酸的种类和数量也不同,食品中酸的测定是根据酸碱中和的原理,即用标定的氢氧化钠溶液进行滴定。 二、材料、仪器与试剂 (一)材料:桃、杏、苹果、蔬菜等 (二)仪器:碱式滴定管(20ml)、容量瓶(100ml)、移液管(10ml)、烧杯(100ml)、研钵或组织捣碎机、天平、漏斗、滤纸等。 (三)试剂 1.0.1mol/L氢氧化钠:称4.0g氢氧化钠定容至1000ml,然后用0.1mol/L 邻苯二甲酸氢钾标定,若浓度太高可酌情稀释。 2.1%酚酞指示剂:称1.0g酚酞,加入100ml 50%的乙醇溶解。 三、操作步骤 准确称取混合均匀磨碎的样品10.0g(或吸10.0ml样品液),转移到100ml 容量瓶中,加蒸馏水至刻度、摇匀。用滤纸过滤,准确吸取滤液20ml放入100ml 三角瓶中,加入1%酚酞2滴,用标定的氢氧化钠滴定至初显粉色在0.5min内不褪色为终点,记下氢氧化钠用量,重复三次,取平均值。 四、计算 V C×N×折算系数 总酸度(%)=——×————————×100 W V1 式中:V——样品稀释总体积(ml) V1——滴定时取样液体积 C——消耗氢氧化钠标准液毫升数 N——氢氧化钠标准液摩尔浓度 W——样品重量(g) 折算系数:即不同有机酸的毫摩尔质量(g/mmol),食品中的总酸度往往根据所含酸的不同,而取其中一种主要有机酸计量。食品中常见的有机酸以及其毫摩尔质量折算系数加下: 苹果酸——0.067(苹果、梨、桃、杏、李子、番茄、莴苣) 醋酸——0.060(蔬菜罐头) 酒石酸——0.075(葡萄) 柠檬酸——0.070(柑橘类) 乳酸——0.090(鱼、肉罐头、牛奶)
实验六水果中总酸及pH的测定 一、目的要求? 1.?进一步熟悉及规范滴定操作。? 2.?学习及了解碱滴定法测定总酸及有效酸度的原理及操作要点。? 3.?掌握水果中总酸度及有效酸度的测定方法和操作技能。? 4.?掌握pH计的维护和使用方法。 二、实验原理? 1.?总酸测定原理 水果中的有机酸在用标准碱液滴定时,被中和成盐类。以酚酞为指示剂,滴定至溶液呈现微红色,? 30s不褪色为终点。根据消耗标准碱液的浓度和体积,计算水果中总酸的含量。? 2.?有效酸测定原理 利用pH计测定水果中的有效酸度?(pH),是将玻璃电极、饱和甘汞电极插入榨取的果汁中组成原电池,该电池电动势的大小与果汁pH有关。即在25℃时,每相差一个pH单位就产生的电池电动势,利用酸度计测量电池电动势并直接以pH表示,故可从酸度计上直接读出果汁的pH。 三、仪器与试剂? 1.?仪器 水浴锅,酸度计,玻璃电极,饱和甘汞电极,现在多用复合电极。? 2.?试剂? ?/?L?NaOH标准溶液,酚酞乙醇溶液,pH=?标准缓冲溶液。 四、实验步骤? 1.?总酸度的测定? (1)?样液制备将样品用组织捣碎机捣碎并混合均匀。称取适量样品,用15mL无CO2?蒸馏水将其移入250mL容量瓶中,在75~80℃水浴上加热,冷却后定容,用干滤纸过滤,弃去初始滤液25mL,收集滤液备用。? (2)?滴定准确吸取上述制备滤液50mL加入酚酞指示剂3~4滴,用/LNaOH标准溶液滴定至微红色30s不褪为终点。记录消耗NaOH标准溶液的体积。? 2.?水果中有效酸度?(pH)?的测定? (1)?样品处理将水果样品榨汁后,取汁液直接进行pH测定。? (2)?酸度计的校正 ①开启酸度计电源,预热30min,连接玻璃及甘汞电极,在读数开关放开的情况下调零。 ②测量标准缓冲溶液的温度,调节酸度计温度补偿旋钮。
酸度的测定概述 食品中的酸味物质,主要是溶于水的一些有机酸和无机酸。在果蔬及其制品中,以苹果酸,柠檬酸,酒石酸,琥珀酸和醋酸为主;在肉,鱼类食品中则以乳酸为例。此外,还有一些无机酸,像盐酸,磷酸等。这些酸味物质,有的是食品中的天然成分,像葡萄中的酒石酸,苹果中的苹果酸;有的是人为的加进去的,像配制型饮料中加入的柠檬酸;还有的是在发酵中产生的,像酸牛奶中的乳酸。酸在食品中主要有以下三个方面的作用。 1、显味剂 不论是哪种途径得到的酸味物质,都是食品重要的显味剂,对食品的风味有很大的影响。其中大多数的有机酸具有很浓的水果香味,能刺激食欲,促进消化,有机酸在维持人体体液酸碱平衡方面起着重要的作用。 2、保持颜色稳定 食品中的酸味物质的存在,即pH值的高低,对保持食品的颜色的稳定性,也起着一定的作用。在水果加工过程中,如果加酸降低介质的pH值,可抑制水果的酶促褐度;选用pH6.5-7.2的沸水热烫蔬菜,能很好地保持绿色蔬菜特有的鲜绿色。 3、防腐作用
酸味物质在食品中还能起到一定的防腐作用。当食品的pH小于2.5时,一般除霉菌外,大部分微生物的生长都受到了抑制;若将醋酸的浓度控制在6%时,可有效地抑制腐败菌的生长。 食品中酸度测定的意义 1.测定酸度可判断果蔬的成熟程度 例如:如果测定出葡萄所含的有机酸中苹果酸高于酒石酸时,说明葡萄还未成熟,因为成熟的葡萄含大量的酒石酸。不同种类的水果和蔬菜,酸的含量因成熟度、生长条件而异,一般成熟度越高,酸的含量越低。如番茄在成熟过程中,总酸度从绿熟期的0.94%下降到完熟期的0.64%,同时糖的含量增加,糖酸比增大,具有良好的口感,故通过对酸度的测定可判断原料的成熟度。 2.可判断食品的新鲜程度 例如:新鲜牛奶中的乳酸含量过高,说明牛奶已腐败变质;水果制品中有游离的半乳糖醛酸,说明受到霉烂水果的污染。 3.酸度反映了食品的质量指标 食品中有机酸含量的多少,直接影响食品的风味、色泽、稳定性和品质的高低。酸的测定对微生物发酵过程具有一定的指导意义。如:酒和酒精生产中,对麦芽汁、发酵液、酒曲等的酸度都有一定的要求。
实验水果、蔬菜中总酸的测定 (学号:030212011031,030212011026 李欣钰和郎琳) 【实验目的】 1、利用标准液滴定水果蔬菜,测定不同水果蔬菜中总酸度 2、练习利用滴定管滴定溶液 3、练习移液管的使用 4、练习pH计的使用 【实验原理】 1、水果和蔬菜中含有各种不同的有机酸,主要为苹果酸,柠檬酸,酒石酸,草酸等。果树的种类不同,含有机酸的种类和数量也不同。果汁或菜汁的酸性取决于游离态的酸或酸式盐的存在数量。这些算都是有机弱酸,所以在测定时,有氢氧化钠标准溶液滴定就能测出酸度。这样测得的数据是总酸度,包含了未离解酸和已离解酸的浓度。用下式计算: 总酸度(%)=(V 样/W 样 )x(V NaOH xc NaOH x折算系数/V取样)x100 式子中V样为样品稀释总体积;V取样为滴定时取样体积;W样为样品的质量。折算系数为不同有机酸的毫摩尔质量 2、食品中的总算度往往根据算韩算的不同,而取其中某种主要有机酸计量。食品中常见的有机酸及其毫摩尔质量折算系数如下 苹果酸——0.067(苹果,梨,西红柿) 酒石酸——0.075(葡萄) 柠檬酸——0.090(柑橘类) 【仪器试剂】 烧杯(100ml)(3-5只),洗耳球,移液管(25ml),容量瓶(250ml)(3只),滤纸,铁架台,滴定管夹,碱式滴定管,玻璃棒,胶头滴管,电子天平,研钵,酚酞指示剂,NaOH标准溶液(约为0.2mol/l),西红柿,葡萄,橘子(自备),塑料袋若干(自备),小刀(自备) 【实验内容】 1.准确称取混合均匀磨碎的样品10g 2.转移到250ml容量瓶中,加纯水至刻度线,摇匀 3.吸取50ml溶液于锥形瓶中,加入两滴酚酞试剂 4.用NaOH标准溶液滴定溶液至淡红色,并且在30s内不退色,即到达终点。 5.记下所用的NaOH体积。重复测定三次取平均值。 6.利用同样的方法测定剩余的两种水果或蔬菜。并记录实验数据 7.用pH计测出样品稀释液的pH 8.处理实验数据,比较所测的西红柿,葡萄,橘子的总酸度的不同 实验数据处理表
实训一:水果中总酸度的测定 一.目的要求: 1.学会水果样品的预处理方法 2.掌握用酸碱滴定法测水果样品中总酸度的原理和方法 3、学会合理制定分析项目的顺序,做到合理安排分析时间,合理处理样品。 4、能熟练制备实训过程中所需要的标准溶液。 5、能规范记录数据并进行数据处理。 二、实训原理: 1. NaOH标准溶液的标定 NaOH易吸收水分及空气中的CO2,因此,不能用直接法配制标准溶液。需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。以酚酞为指示剂,当滴定至终点溶液呈浅红色,且30S不褪色时。 反应如下:KHC8H4O4+NaOH=KNaC8H4O4+ H2O 2.水果总酸度的测定 根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。当滴定至终点溶液呈浅红色,且30S不褪色时,根据滴定时消耗的标准NaOH溶液的体积,可算出试样中的总酸度。 其反应如下:HAC+NaOH→NaAc+H2O 三、实训所需仪器、试剂:洗仪器:CCC 仪器:酸碱式滴定管、锥形瓶、移液管、量筒、烧杯、容量瓶、胶头滴管、洗耳球、水浴锅、铁架台、电子天平、玻璃棒、小纸片、干燥的纱布、 试剂:0.1000mol/LNaOH溶液、邻苯二甲酸氢钾、酚酞指示剂、水果试样、无水CO2的蒸馏水、 四、实验步骤: 1. 0.1000mol/LNaOH标准溶液的配制和标定 配制:BBB
称取固体NaOH约2g放置在500ml的烧杯中,先加入100ml少溶解,再加水稀释成500ml溶液,混匀,放入烧杯中,待标定。 标定:AAA 用减量法准确称取0.41~0.45g邻苯二甲酸氢钾3份,分别放入250ml锥形瓶中,加25mL无CO2蒸馏水溶解。然后加1-2滴酚酞指示剂,用NaOH标准溶液滴定至终点(至粉红色,并保持30s不褪色为终点)。记录每次消耗NaOH 溶液的体积。 2.试样处理: 榨汁:CCC 取水果试样,需去皮、去柄、去核,切成块状,置于搅拌机中捣碎并混匀。准确移取25ml水果试样,加100mL无CO2的蒸馏水,稀释定容为250ml溶液。然后倒入烧杯中在75~80℃水浴上加热30分钟。冷却后过滤,滤液倒入容量瓶中备用。 3.滴定: 滴定:AAA BBB 准确吸取20mL滤液三份于250mL锥形瓶中,各加25ml水稀释。加1-2滴酚酞指示剂,用NaOH标准溶液滴定至终点,至粉红色30s不褪色。记录NaOH 消耗量的体积,平行三次。 五、计算公式 C NaOH = mKHC8H4O4×1000/VNaOH MKHC8H4O4 ρHAcc =(CNaOH×VNaOH×MHac×10-3)/(20.00/250.0×25.00) 七、注意事项 1、注意碱式滴定管滴定前要赶走气泡,滴定过程不要形成气泡。 2、NaOH标准溶液滴定HAc,属于强碱滴定弱酸,CO2的影响严重,注意出去所用碱标准溶液和蒸馏水中的CO2。
酸度的测定 一、判断题。 1、普通酸度计通电后可立即开始测量。× 2、使用甘汞电极时,不应取下电极上、下端的胶帽和胶塞。× 3、使用甘汞电极时,应注意勿使气泡进入盛饱和氯化钾的细管中,以免造成断路。√ 4、食品中有机酸的种类和含量是判断其质量好坏的一个重要指标。√ 5、有机酸可以提高维生素C的稳定性,防止其氧化。√ 6、挥发酸可用直接法或间接法测定。√ 7、pH的测定方法有多种,最常用的方法是比色法。× 二、选择题。 1、使用酸度计前,必须熟悉其使用说明书,其目的在于( A ) A.掌握仪器性能,了解操作规程 B.了解电路原理图 C.掌握仪器的电子构件 D.了解仪器结构 2、用酸度计以浓度直读法测试液的pH,先用与试液pH相近的标准溶液 ( C )。 A.调零 B.消除干扰离子 C.定位 D.减免迟滞效应 3、酸度计测量出来的是(A),而刻度指的是pH。 A.电池的电动势 B.电对的强弱 C.标准电极电位 D.离子的活度 4、用酸度计测定试液的pH之前,要先用标准( D )溶液进行定位。 A.酸性 B.碱性 C.中性 D.缓冲 5、电位法中的指示电极,其电位与被测离子的浓度( D )。 A.成正比 B.的对数成正比 C.无关 D.符合能斯特公式的关系 6、面包的酸度为( B )。 A.2~8oT B.3~9oT C.4~10oT D.5~11oT 7、下列说法不正确的是( AB )。 酸度指水中能与强碱发生中和作用的全部物质。 单位体积水中所含能提供(解离出)氢离子与强碱(如NaOH、KOH)等发生中和反应的物质总量。酸度指的是酸溶液中H离子的含量,而酸的浓度是指的酸在溶液中的含量 A.酸度就是pH B.酸度就是酸的浓度
10粉体徐明明一.实验题目:食醋中总酸度的测定 二.实验目的: 1、学会食醋中总酸度的测定原理和方法。 2、掌握指示剂的选择原则。 3、比较不同指示剂对滴定结果的影响。 4、加强移液管的使用; 5、掌握强碱滴定弱酸的滴定过程,突跃范围及指示剂的选择原理。 三、实验基本原理 食醋是混合酸,其主要成分是HAc(有机弱酸,K a=1.8×10-5),与NaOH反应产物为弱酸强碱盐NaAc: HAc + NaOH = NaAc + H2O HAc与NaOH反应产物为弱酸强碱盐NaAc,化学计量点时pH≈8.7,滴定突跃在碱性范围内(如:0.1mol·L-1NaOH 滴定0.1mol·L-1HAc突跃范围为PH:7.74~9.70),在此若使用在酸性范围内变色的指示剂如甲基橙,将引起很大的滴定误差(该反应化学计量点时溶液呈弱碱性,酸性范围内变色的指示剂变色时,溶液呈弱酸性,则滴定不完全)。因此在此应选择在碱性范围内变色的指示剂酚酞(8.0~9.6)。(指示剂的选择主要以滴定突跃范围为依据,指示剂的变色范围应全部或一部分在滴定突跃范围内,则终点误差小于0.1%)
因此可选用酚酞作指示剂,利用NaOH 标准溶液测定HAc 含量。食醋中总酸度用HAc 含量的含量来表示。 四、实验基本步骤 1、进入实验室,将实验要用到的有关仪器从仪器橱中取出,把玻璃器皿按洗涤要求洗涤干净备用。 2、用配制且已标定好的NaOH 溶液润洗洗涤好的碱式滴定管,然后装入NaOH 溶液。 3、用移液管吸取食醋试样5.00mL ,移入250mL 锥形瓶中,加入20mL 蒸馏水稀释(思考题1),加酚酞指示剂2滴(思考题 2),用NaOH 标准溶液滴定至终点。平行测定2~3次。记录NaOH 标准溶液的用量,按下式计算食醋中总酸量。 ()()()s r V HAc M NaOH V NaOH c HAc =)(ρ 4、用甲基红作指示剂,用上法滴定,计算结果,比较两种指示剂结果之间的差别(思考题3)。 五、注意事项 1、注意食醋取后应立即将试剂瓶盖盖好,防止挥发。 2、甲基红作指示剂时,注意观察终点颜色的变化。 3、数据处理时应注意最终结果的表示方式。 六、思考题和测试题 思考题1、加入20mL 蒸馏水的作用是什么? 思考题2、为什么使用酚酞作指示剂?
2020 食品中总酸的测定实验报告范文 Contract Template
食品中总酸的测定实验报告范文 前言语料:温馨提醒,报告一般是指适用于下级向上级机关汇报工作,反映情况,答复上级机关的询问。按性质的不同,报告可划分为:综合报告和专题报告;按行文的直接目的不同,可将报告划分为:呈报性报告和呈转性报告。体会指的是接触一件事、一篇文章、或者其他什么东西之后,对你接触的事物产生的一些内心的想法和自己的理解 本文内容如下:【下载该文档后使用Word打开】 篇一:食品中总酸度的测定实验报告 1.方法提要 总酸度是食品中所有酸性物质的总量,包括已离解的酸和未离解的酸,常采用酸碱滴定法进行测定,即用标准碱溶液进行滴定,以酚酞为指示剂来判断终点,并以样品中主要代表酸的百分含量表示。 样品中若颜色较深,不易观察终点时,常采用自动电位滴定仪进行测定,本实验终点PH控制在8.2。 2.要求 1)要求学会酸碱滴定法测定食品中的总酸度; 2)要求掌握酸碱电位滴定仪的调节和使用。 3.仪器、设备 1)ZD―2型自动电位滴定仪一套。 4.试剂
1)1000mol/L的氢氧化钠标准溶液; 2)PH9.18的缓冲溶液; 3)PH6.88的缓冲溶液。 5.实验步骤 1)按说明书接好电源及连线,打开电源开关; 2)定位调节:将PH旋钮指向测量挡,温度补偿旋钮指向所测溶液的温度,将PH复合电极插入PH6.88的缓冲溶液中,打开磁力搅拌器开关,缓慢旋转定位旋钮,使其PH到达所对应温度的PH值,固定好定位旋钮不动。 3)斜率校正:定位调节好后,将PH复合电极插入PH9.18的缓冲溶液中,打开磁力搅拌器开关,缓慢旋转斜率旋钮,使其PH 到达所对应温度的PH值,固定好斜率旋钮不动。 4)零位调节:按定量分析实验要求,在滴定管中装入标准氢氧化钠溶液,将“一般、自动、手动”调节旋钮指向“手动”位,不断的按启动按钮,排除橡皮管中的气泡,并使滴定管中的液位到达零位。 5)样品测定:准确吸取处理好的样品溶液50ml于100ml烧杯中,按下PH终点调节按钮,旋转PH终点调节旋钮,将终点设定在PH8.20。将电极插入溶液中,打开搅拌器开关,调节合适的搅拌速度,将PH旋钮指向滴定挡,将“一般、自动、手动”调节旋钮指向“一般”位,按下启动按钮开始滴定,到达终点后电磁阀会自动关闭,此时读出所用氢氧化钠的体积(ml)数。要求做两次平行试验,误差不大于0.05%
综合性、设计性实验报告 (本科学生) 姓名:毛修林学号:2010021141 专业:化学班级:1班 实验课程名称:《分析化学实验》 指导教师及职称:郭红老师(高级实验师) 开课学期:2011 至2012 学年上学期 上课时间:2011 年12 月 6 日 资源环境学院编印
一、实验设计方案: 实验序号及名称:柠檬中总酸度的测定实验时间:2011年12月6日 小组合作:是小组号:一成员:毛修林、鲁静宁、杨全、 李丽霞 (一).【实验目的】: 1.学会水果样品的预处理方法。 2.掌握酸碱滴定法测定水果样品中总酸度的原理和方法。 3.掌握强碱滴定弱酸的滴定过程,突跃范围及指示剂的选择原理。 4.柠檬总酸含量的测定。 5.规范记录数据并进行数据处理。 (二).【主要试剂和仪器】: 1.试剂:KHP基准试剂,固体NaOH,酚酞指示剂,新 鲜柠檬2个。 2.仪器:榨汁机,50.00mL碱式滴定管,25 .00mL移液 管,250 mL锥形瓶3只,电子天平,250 mL容量瓶2只。
(三).【实验原理】: 柠檬主要含有柠檬酸,其结构式为: ,各级解离常数分别为:K a1=7.4×10-4,K a2=1.7×10-5,K a3=4.0×10-7。由于柠檬酸各相邻解离常数之间相差不大,故不能分步滴定,但由于最后一级解离常数并不小,因此可以用NaOH标准溶液作滴定剂,按多元酸一次进行滴定。反应式为:HOOCCH2C(OH)(COOH)CH2COOH+3NaOH=NaOOCCH2C(OH)(COONa)CH2COONa+3H2O。反应产物为弱酸弱碱盐,滴定范围在碱性范围内,因此可选用酚酞作指示剂,滴定至溶液由无色变为微红色即达到终点,再根据消耗NaOH标准溶液的体积计算柠檬总酸含量。 计算式为:总算度(g/100g)=(K(CV)NaOH×100)/(V试液×m试样/250)(其中:K=0.064)。
食品中总酸度的测定 方法一指示剂法 一、实验原理 根据酸碱中和原理,用碱液滴定试液中的酸,以酚酞为指示剂确定滴定终点,按碱液的消耗量计算食品中的总酸含量。 二、试剂与仪器 1.试剂 所有试剂均为分析纯,水为蒸馏水或同等纯度的水(以下简称水),使用前须经煮沸,冷却。 0.1mol/L氢氧化钠标准滴定溶液 0.01mol/L或0.05mol/L氢氧化钠标准滴定溶液 1%酚酞指示剂溶液:1g酚酞溶于60mL 95%乙醇中,用水稀释至100mL。 2.仪器、设备 试验室常用仪器及下列各项: 组织捣碎机;水浴锅;研钵;冷凝管。 三、分析步骤 1.试样的制备 (1)液体样品 不含二氧化碳的样品充分混匀。含二氧化碳的样品按下述方法排除二氧化碳:取至少200mL充分混匀的样品,置于500mL锥形瓶中,旋摇至基本无气泡装上冷凝管,置于水浴锅中。待水沸腾后保持10min,取出,冷却。 啤洒中的二氧化碳按GB4928规定的方法排除。 (2)固体样品 去除不可食部分,取有代表性的样品至少200g,置于研钵或组织捣碎机中,加入与试样等量的水,研碎或捣碎,混匀。 面包应取其中心部分,充分混匀,直接供制备试液。 (3)固液体样品 按样品的固、液体比例至少取200g,去除不可食部分,用研钵或组织捣碎机研碎或捣碎,混匀。
2.试液的制备 取25~50g试样,精确至0.001g,置于250mL容量瓶中,用水稀释至刻度,含固体的样品至少放置30min(摇动2~3次)。用快速滤纸或脱脂棉过滤,收集滤液于250mL锥形瓶中备用。 总酸度低于0.7g/kg的液体样品,混匀后可直接取样测定。 3.样品测定 取25.00~50.00mL试液,使之含0.035~0.070g酸,置于150mL烧杯中。加40~60mL水及0.2mL1%酚酞指示剂,用0.1mol/L氢氧化钠标准滴定溶液(如样品酸度较低,可用0.01mol/L或0.05mol/L氢氧化钠标准滴定溶液)滴定至微红色30s不褪色。记录消耗0.1mol/L氢氧化钠标准滴定溶液的毫升数(V1)。 同一被测样品须测定两次。 4.空白试验 用水代替试液。记录消耗0.1mol/L氢氧化钠标准滴定溶液的毫升数(V2)。 四、结果计算 总酸以每公斤(或每升)样品中酸的克数表示,按式(1)计算: C(V1—V2)×K×F×1000 X= (1) m 式中: X——每公斤(或每升)样品中酸的克数,g/kg(或g/L); C——氢氧化钠标准滴定溶液的浓度,mol/L; V1——滴定试液时消耗氢氧化钠标准滴定溶液的体积,mL; V2——空白试验时消耗氢氧化钠标准滴定溶液的体积,mL; F——试液的稀释倍数; m——试样质量,g或mL; K——酸的换算系数。各种酸的换算系数分别为:苹果酸,0.067; 乙酸,0.060; 酒石酸,0.075; 柠檬酸,0.064; 柠檬酸,0.070; (含一分子结晶水);乳酸,0.090;盐酸,0.036; 磷酸,0.033。 五、注意事项