
2015~2016学年度高一上学期月考化学试卷(10月份)
一、选择题(共20小题)
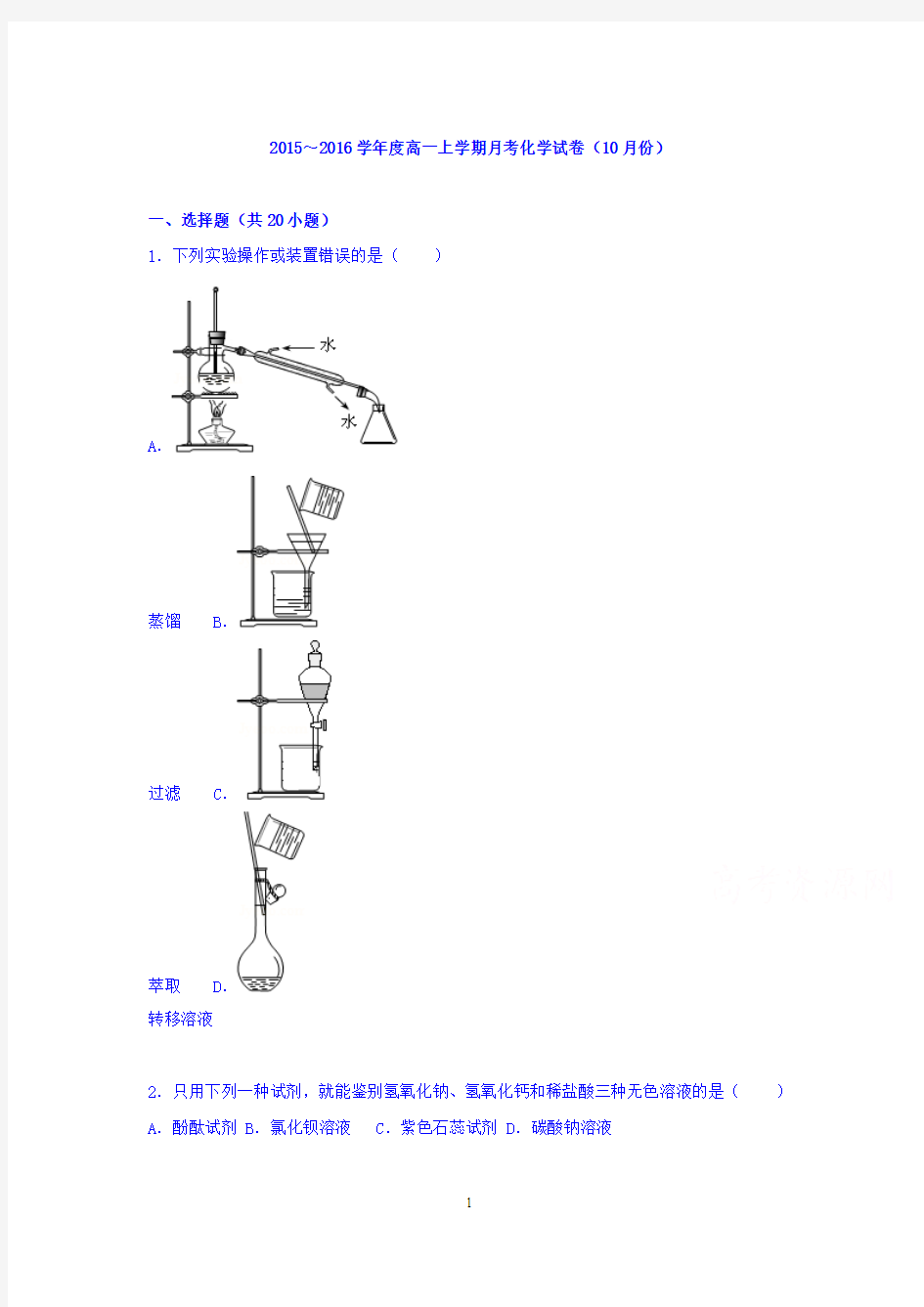
1.下列实验操作或装置错误的是()
A.
蒸馏B.
过滤C.
萃取D.
转移溶液
2.只用下列一种试剂,就能鉴别氢氧化钠、氢氧化钙和稀盐酸三种无色溶液的是()A.酚酞试剂 B.氯化钡溶液C.紫色石蕊试剂 D.碳酸钠溶液
3.下列状态的物质,既能导电又属于电解质的是()
A.KCl溶液B.液态HCl C.熔融的NaOH D.蔗糖溶液
4.下列叙述正确的是()
A.氯化钠溶液能导电,所以氯化钠溶液是电解质
B.化合反应不一定是氧化还原反应
C.盐、碱一定含有金属元素
D.在水溶液中电离产生H+的化合物一定是酸
5.燃放烟花爆竹增强春节喜庆,但也造成大气严重污染.烟花中含有的KNO3属于()A.酸B.碱C.盐D.氧化物
6.厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中发生的变化不属于氧化还原反应的是()
A.食物长时间放置后变质腐败
B.燃烧液化石油气为炒菜提供热量
C.用活性炭除去冰箱中的异味
D.烧菜用过的铁锅出现红棕色斑迹
7.传统的引爆炸药由于其中含Pb,使用时将产生污染,同时其引爆后的剩余炸药还严重危害接触者的人身安全,美国UNC化学教授Thomas J.Meyer等研发了环境友好、安全型的“绿色”引爆炸药,其中一种可表示为Na2R,它保存在水中可以失去活性,爆炸后不会产生危害性残留物.已知10mL Na2R溶液含Na+的微粒数为N个,该Na2R溶液的物质的量浓度为()A.N×10﹣2 mol/L B.mol/L
C.mol/L D.mol/L
8.做焰色反应实验用的铂丝,每试验一种样品后都必须()
A.用水洗涤2~3次后再使用
B.用盐酸洗涤后,经蒸馏水冲洗,方可使用
C.用滤纸擦干后才可使用
D.用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用
9.下列溶液与20mL 1mol?L﹣1 NaNO3溶液中NO3﹣物质的量浓度相等的是()A.10mL 1mol?L﹣1 Mg(NO3)2溶液
B.5mL 0.8mol?L﹣1 Al(NO3)3溶液
C.10mL 2mol?L﹣1AgNO3溶液
D.10mL 0.5mol?L﹣1 Cu(NO3)2溶液
10.下列反应既属于氧化还原反应,又属于置换反应的是()
A.2Fe+3Cl22FeCl3 B.Fe2O3+3CO2Fe+3CO2
C.CaO+CO2═CaCO3D.2H2O+2Na═2NaOH+H2↑
11.下列关于物质的检验说法正确的是()
A.加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定有硫酸根离子B.用四氯化碳萃取某溶液时,分层且下层显紫红色,可能存在碘单质
C.加入AgNO3溶液,有白色沉淀生成,证明含有Cl﹣
D.加入盐酸,放出能使澄清的石灰水变浑浊的无色无味的气体,证明一定含有CO32﹣
12.下列电离方程式正确的是()
A.NaHCO3═Na++H++CO32﹣B.Al2(SO4)3═2Al3++3SO42﹣
C.H2SO4═H2++SO42﹣D.Ba(OH)2═Ba2++OH﹣
13.V L浓度为1mol?L﹣1的盐酸,欲使其浓度增大1倍,采取的措施合理的是()A.通入标准状况下的HCl气体22.4VL
B.将溶液加热浓缩到0.5VL
C.加入10mol?L﹣1的盐酸0.2V L,再稀释至1.5VL
D.加入VL3mol?L﹣1的盐酸混合均匀
14.下列实验操作中错误的是()
A.蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
15.下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)()
选项待提纯的物质选用的试剂操作方法
A NaCl(Na2CO3)稀硫酸蒸发结晶
B CO2(CO) O2点燃
C Zn (Ag)稀盐酸过滤
D 自来水(Cl﹣)﹣﹣﹣蒸馏
A.A B.B C.C D.D
16.用N A表示阿伏加德罗常数的值.下列说法正确的是()
A.标准状况下,1 mol CO2、CO的混合气中含有的氧原子数为1.5N A
B.常温常压下,11.2 L 氯化氢气体中含有的分子数为0.5N A
C.N A个甲烷分子和1mol甲烷的质量相等
D.1 mol?L﹣1 CuCl2溶液中含有的氯离子数为2N A
17.为了除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液.不正确的操作顺序是()
A.⑤②④①③B.⑤④②①③C.②⑤④①③D.①④②⑤③
18.与0.2mol H2O含有相同氢原子数的是()
A.0.2molHNO3B.标况下2.24L CH4
C.1.7g NH3D.1.505×1022个HCl分子
19.宜兴竹海风景区被称为天然氧吧,其原因是空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”.O2﹣就是一种空气负离子,其摩尔质量为()A.32 g B.33 g C.33 g?molˉ1D.32 g?molˉ1
20.“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质()
①是溶液
②是胶体
③能产生丁达尔效应
④能透过滤纸
⑤不能透过滤纸
⑥静置后,会析出黑色沉淀.
A.①④⑥B.②③⑤C.②③④D.①③④⑥
二、解答题(共6小题)(选答题,不自动判卷)
21.取100mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出.计算:
(1)原混合液中Na2SO4的物质的量浓度是多少?
产生的气体在标准状况下的体积为多少L?
(3)过滤出沉淀后,所得滤液的物质的量浓度为多少?(写出计算过程).
22.实验室里需要纯净的氯化钠晶体,但现在只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案:
请回答下列问题:
(1)操作①加热的目的是,发生的反应(填“是”或“不是”)氧化还原反应.
操作②除用BaCl2溶液外,还可以用.
(3)操作③的目的是,发生反应的离子方程式为:.
(4)操作④应在(填仪器名称)中进行.
23.下列各组物质的分离或提纯,应选用下述方法的哪一种?(填选项字母)
A.分液B.过滤 C.萃取D.蒸馏E.蒸发结晶F.高温分解
(1)分离CCl4和H2O:;
除去CaO固体中少量的CaCO3固体:;
(3)除去澄清石灰水中悬浮的CaCO3:;
(4)从碘水中提取碘:;
(5)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:.
24.(1)现有①铁片②饱和食盐水③液态氯化氢④乙醇⑤干冰⑥熔融KNO3⑦BaSO4固体⑧石墨⑨氢氧化钠,
其中属于非电解质的是(填序号,下同),能导电的是.
写出下列物质的电离方程式:
①Na3PO4:
②NH4NO3:.
25.(1)标况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为;
某金属氯化物为MCl29.5g,含有0.200molCl﹣,则该氯化物的摩尔质量,金属M的相对原子质量为.
(3)71.5g碳酸钠晶体(Na2CO3?10H2O)溶于水,配成500ml溶液,此溶液的物质的量浓度为.
(4)质量都是10g的HCl、NH3、CO2、H2四种气体在标准状况下,体积最小的是;密度最小的是.(填化学式)
26.某同学欲用KMnO4固体配制100mL0.5mol.L﹣1的溶液.回答下列问题:
(1)配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量
筒、、.
应用托盘天平称取KMnO4固体g.
(3)不规范的实验操作会导致实验结果的误差.分析下列操作对实验结果的影响偏小的是(请填序号).
A.颠倒摇匀后发现凹液面低于刻度线又加水补上 B.加水定容时俯视刻度线
C.容量瓶内壁附有水珠而未干燥处理 D.在溶解过程中有少量液体溅出烧杯外.
2015~2016学年度高一上学期月考化学试卷(10月份)
参考答案与试题解析
一、选择题(共20小题)
1.下列实验操作或装置错误的是()
A.
蒸馏B.
过滤C.
萃取D.
转移溶液
【考点】蒸馏与分馏;过滤;分液和萃取;配制一定物质的量浓度的溶液.
【专题】化学实验基本操作.
【分析】A.温度计用于测量馏分的温度;
B.过滤可用于分离不溶性固体和液体;
C.萃取后通过分液漏斗分离;
D.转移液体时要防止液体飞溅.
【解答】解:A.蒸馏时,温度计水银球应位于蒸馏烧瓶的支管口附近,用于测量馏分的温度,故A错误;
B.过滤可用于分离不溶性固体和液体,装置图符合操作要求,故B正确;
C.萃取后通过分液漏斗分离,装置图符合操作要求,故C正确;
D.转移液体时要为防止液体飞溅,需通过玻璃棒引流,装置图符合操作要求,故D正确.故选A.
【点评】本题考查较为综合,涉及物质的分离、提纯实验等知识,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握物质的性质的异同以及实验操作的严密性、可行性的评价,难度中等.
2.只用下列一种试剂,就能鉴别氢氧化钠、氢氧化钙和稀盐酸三种无色溶液的是()A.酚酞试剂 B.氯化钡溶液C.紫色石蕊试剂 D.碳酸钠溶液
【考点】物质的检验和鉴别的基本方法选择及应用.
【分析】根据氢氧化钠和氢氧化钙都是强碱,只是阳离子不同,盐酸是酸进行分析.
A.酚酞遇碱变红色;
B.氯化钡和三者都不反应;
C.石蕊遇碱变蓝;
D.碳酸钠会与盐酸和氢氧化钙反应.
【解答】解:A.将酚酞滴入三种溶液中,在氢氧化钠和氢氧化钙中都显红色,现象相同,不能鉴别,故A错误,
B.将氯化钡滴入三种溶液中都不会反应,不能鉴别,故B错误,
C.将石蕊滴入三种溶液中,在氢氧化钠和氢氧化钙中都显蓝色,现象相同,不能鉴别,故C错误,
D.碳酸钠和氢氧化钙反应会生成沉淀,和氢氧化钠不会反应,和盐酸反应生成气体,三种物质中的反应现象不同,可以鉴别,故D正确,
故选D.
【点评】本题考查物质的检验及鉴别,明确物质的性质是解答本题的关键,注意物质性质的差异即可解答,题目难度不大.
3.下列状态的物质,既能导电又属于电解质的是()
A.KCl溶液B.液态HCl C.熔融的NaOH D.蔗糖溶液
【考点】电解质与非电解质.
【专题】电离平衡与溶液的pH专题.
【分析】在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液中和熔融状态下都不导电的化合物;能导电的物质中含有自由电子或离子,据此分析解答.
【解答】解:A.KCl溶液能导电,但是混合物,不是电解质,故A不符合;
B.液态氯化氢是电解质,但不能导电,故B不符合;
C.NaOH固体是电解质,熔融时电离出自由移动的离子,能导电,故C符合;
D.蔗糖属于非电解质,溶液不导电,故D不符合;
故选:C.
【点评】本题考查了电解质、非电解质概念的分析判断,物质组成和概念理解是解题关键,题目较简单.
4.下列叙述正确的是()
A.氯化钠溶液能导电,所以氯化钠溶液是电解质
B.化合反应不一定是氧化还原反应
C.盐、碱一定含有金属元素
D.在水溶液中电离产生H+的化合物一定是酸
【考点】电解质与非电解质;酸、碱、盐、氧化物的概念及其相互联系;化学基本反应类型.【专题】基本概念与基本理论.
【分析】A.电解质必须是化合物;
B.有化合价变化的反应是氧化还原反应;
C.非金属元素之间也可以形成盐;
D.电离时生成的阳离子全部是氢离子的化合物是酸.
【解答】解:A.氯化钠溶液是混合物,不是电解质,故A错误;
B.化合反应不一定有化合价的变化,例如二氧化硫与水反应生成亚硫酸属于化合反应,但是不是氧化还原反应,故B正确;
C.非金属元素之间也可以形成盐,例如:氯化铵、硝酸铵等,故C错误;
D.在水溶液中电离产生H+的化合物一定是酸,例如:硫酸氢钠电离产生氢离子,但是属于盐,故D错误;
故选:B.
【点评】本题考查学生对基本概念掌握的熟练程度,题目难度不大,注意四种基本反应类型与氧化还原反应的关系.
5.燃放烟花爆竹增强春节喜庆,但也造成大气严重污染.烟花中含有的KNO3属于()A.酸B.碱C.盐D.氧化物
【考点】常见的生活环境的污染及治理.
【专题】化学应用.
【分析】酸是指在电离时产生的阳离子全部是氢离子的化合物;
碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;
盐是指一类金属离子或铵根离子与酸根离子或非金属离子结合的化合物;
氧化物是由两种元素组成,其中一种元素是氧元素的化合物,据此进行分析判断.
【解答】解:KNO3是由钾离子和硝酸酸根离子组成的化合物,属于盐,故选:C.
【点评】本题考查了物质的分类,难度不大,根据概念即可解答.
6.厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中发生的变化不属于氧化还原反应的是()
A.食物长时间放置后变质腐败
B.燃烧液化石油气为炒菜提供热量
C.用活性炭除去冰箱中的异味
D.烧菜用过的铁锅出现红棕色斑迹
【考点】氧化还原反应.
【专题】氧化还原反应专题.
【分析】氧化还原反应的特征是化合价的升降,从化合价变化的角度分析氧化还原反应.【解答】解:A.食物长时间放置易被空气中氧气氧化,发生氧化还原反应,故A不选;B.液化石油气的燃烧属于氧化还原反应,故B不选;
C.用活性炭除去冰箱中的异味是利用了活性炭的吸附性,属于物理变化,故C选;
D.烧菜用过的铁锅出现红棕色斑迹,属于铁被氧化为生锈的过程,故D不选.
故选C.
【点评】本题考查氧化还原反应,题目难度不大,注意把握常见化学反应,从化合价的角度分析氧化还原反应.
7.传统的引爆炸药由于其中含Pb,使用时将产生污染,同时其引爆后的剩余炸药还严重危害接触者的人身安全,美国UNC化学教授Thomas J.Meyer等研发了环境友好、安全型的“绿色”引爆炸药,其中一种可表示为Na2R,它保存在水中可以失去活性,爆炸后不会产生危害性残留物.已知10mL Na2R溶液含Na+的微粒数为N个,该Na2R溶液的物质的量浓度为()A.N×10﹣2 mol/L B.mol/L
C.mol/L D.mol/L
【考点】物质的量浓度的相关计算.
【专题】计算题.
【分析】根据n=计算Na+的物质的量,n(Na2R)=n(Na+),根据c=计算该Na2R溶液的物质的量浓度.
【解答】解:N个Na+的物质的量为=mol,
所以n(Na2R)=n(Na+)=×mol=mol,
该Na2R溶液的物质的量浓度为=mol/L,
故选B.
【点评】本题考查物质的量浓度的有关计算,难度不大,注意电解质离子浓度与电解质浓度的关系.
8.做焰色反应实验用的铂丝,每试验一种样品后都必须()
A.用水洗涤2~3次后再使用
B.用盐酸洗涤后,经蒸馏水冲洗,方可使用
C.用滤纸擦干后才可使用
D.用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用
【考点】焰色反应.
【专题】金属概论与碱元素.
【分析】焰色反应最主要的就是无其他离子干扰,每次做完焰色反应实验后,铂丝会留有实验的物质,为除去实验物质用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用,盐酸可以溶解氧化物等杂质且易挥发,不会残留痕迹,所以选用盐酸洗涤.
【解答】解:A、用水洗涤,铂丝上残留的物质不能全部清除,对实验造成干扰,故A错误;
B、用盐酸洗涤,再用蒸馏水冲洗后使用,不能完全去除其它离子的干扰,故B错误;
C、用滤纸擦干净,铂丝上残留的物质不能全部清除,对实验造成干扰,故C错误;
D、用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用,去除了其它离子的干扰,且HCL 受热以后会挥发,无残留,故D正确;
【点评】本题考查了焰色反应实验,难度不大,根据教材基础知识解答即可;明确焰色反应是元素的性质,不是原子或离子的性质.
9.下列溶液与20mL 1mol?L﹣1 NaNO3溶液中NO3﹣物质的量浓度相等的是()
A.10mL 1mol?L﹣1 Mg(NO3)2溶液
B.5mL 0.8mol?L﹣1 Al(NO3)3溶液
C.10mL 2mol?L﹣1AgNO3溶液
D.10mL 0.5mol?L﹣1 Cu(NO3)2溶液
【考点】物质的量浓度的相关计算.
【专题】计算题.
【分析】根据化学式可知,20mL 1mol?L﹣1 NaNO3溶液中NO3﹣物质的量浓度为1mol/L,溶液中溶质离子浓度与溶液体积无关,与电解质强弱、溶质电离出的相应离子数目及溶质的浓度有关.
【解答】解:20mL 1mol?L﹣1 NaNO3溶液中NO3﹣物质的量浓度为1mol/L.
A、1 mol?L﹣1 Mg(NO3)2溶液中NO3﹣物质的量浓度为1mol/L×2=2mol/L,故A错误;
B、0.8 mol?L﹣1 Al(NO3)3溶液中NO3﹣物质的量浓度为0.8mol/L×3=2.4mol/L,故B错误;
C、2 mol?L﹣1AgNO3溶液中NO3﹣物质的量浓度为2mol/L,故C错误;
D、0.5 mol?L﹣1 Cu(NO3)2溶液中NO3﹣物质的量浓度为0.5mol/L×2=1mol/L,故D正确;故选D.
【点评】本题考查物质的量浓度的计算,难度较小,明确物质的构成是解答本题的关键,并注意离子的浓度与溶液的浓度的关系来解答即可.
10.下列反应既属于氧化还原反应,又属于置换反应的是()
A.2Fe+3Cl22FeCl3 B.Fe2O3+3CO2Fe+3CO2
C.CaO+CO2═CaCO3D.2H2O+2Na═2NaOH+H2↑
【考点】氧化还原反应.
【分析】置换反应为一种单质和一种化合物反应生成另一种单质和另一种化合物,氧化还原反应的特征是元素化合价的升降,以此解答.
【解答】解:A.Fe、Cl元素的化合价变化,为氧化还原反应,但不是置换反应,故A错误;B.Fe、C元素的化合价变化,为氧化还原反应,但不是置换反应,故B错误;
C.元素化合价没有发生变化,不是氧化还原反应,故C错误;
D.Na置换出水中的H生成氢气,为置换反应和氧化还原反应,故D正确.
故选D.
【点评】本题考查氧化还原反应,侧重于学生的分析能力的考查,注意把握化学反应类型,从元素化合价的角度认识氧化还原反应.
11.下列关于物质的检验说法正确的是()
A.加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定有硫酸根离子
B.用四氯化碳萃取某溶液时,分层且下层显紫红色,可能存在碘单质
C.加入AgNO3溶液,有白色沉淀生成,证明含有Cl﹣
D.加入盐酸,放出能使澄清的石灰水变浑浊的无色无味的气体,证明一定含有CO32﹣
【考点】物质的检验和鉴别的基本方法选择及应用.
【分析】A.白色沉淀可能为AgCl;
B.下层显紫红色,可知碘单质溶解在四氯化碳中;
C.白色沉淀可能为碳酸银或硫酸银等;
D.无色无味的气体为二氧化碳.
【解答】解:A.白色沉淀可能为AgCl,应先加盐酸排除干扰离子、再加氯化钡检验硫酸根离子,故A错误;
B.下层显紫红色,可知碘单质溶解在四氯化碳中,则原溶液存在碘单质,故B正确;C.白色沉淀可能为碳酸银或硫酸银等,检验氯离子,应先加硝酸、再加硝酸银,故C错误;D.无色无味的气体为二氧化碳,则原溶液含有CO32﹣或含有HCO3﹣,或都存在,故D错误;故选B.
【点评】本题考查物质的鉴别和检验,为高频考点,把握物质的性质、常见离子的检验方法是解答本题的关键,侧重分析与应用能力的考查,题目难度不大.
12.下列电离方程式正确的是()
A.NaHCO3═Na++H++CO32﹣B.Al2(SO4)3═2Al3++3SO42﹣
C.H2SO4═H2++SO42﹣D.Ba(OH)2═Ba2++OH﹣
【考点】电离方程式的书写.
【分析】强电解质在溶液中能完全电离,弱电解质则部分电离,离子团在电离方程式中不能拆开.
【解答】解:A、碳酸氢钠是强电解质,能完全电离出钠离子和碳酸氢根离子,碳酸氢根离子团不能拆开,即NaHCO3=Na++HCO3﹣,故A错误;
B、硫酸铝是强电解质,能完全电离,电离方程式为:Al2(SO4)3═2Al3++3SO42﹣,故B正确;
C、硫酸是强酸,能完全电离出氢离子和硫酸根离子,H2SO4═2H++SO42﹣,故C错误;
D、氢氧化钡属于强电解质,能完全电离出钡离子和氢氧根离子Ba(OH)2═Ba2++2OH﹣,故D 错误.
故选B.
【点评】本题考查学生电离方程式的书写知识,可以根据所学知识进行回答,较简单.
13.V L浓度为1mol?L﹣1的盐酸,欲使其浓度增大1倍,采取的措施合理的是()A.通入标准状况下的HCl气体22.4VL
B.将溶液加热浓缩到0.5VL
C.加入10mol?L﹣1的盐酸0.2V L,再稀释至1.5VL
D.加入VL3mol?L﹣1的盐酸混合均匀
【考点】物质的量浓度;物质的量浓度的相关计算.
【分析】A、根据C=计算判断;
B、根据加热时,盐酸会挥发;
C、根据C=计算判断;
D、根据浓稀盐酸混合后体积是否变化判断.
【解答】解:A、标准状况下的HCl气体22.4VL,物质的量是Vmol,VL浓度为1mol?L﹣1的盐酸中HCl的物质的量为Vmol,但无法计算通入氯化氢后溶液的体积,故A错误;
B、加热浓缩盐酸时,导致盐酸挥发,溶质的物质的量偏小,故B错误;
C、VL浓度为0.5mol?L﹣1的盐酸的物质的量是0.5Vmol,10mol?L﹣1的盐酸0.1VL的物质的量是Vmol,再稀释至1.5VL,所以C==2mol/L,故C正确;
D、浓稀盐酸混合后,溶液的体积不是直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,故D错误.
故选C.
【点评】本题考查了物质的量浓度的计算,难度不大,易错选项是D,注意密度不同的溶液混合后,溶液的体积不能直接加和.
14.下列实验操作中错误的是()
A.蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
【考点】物质的分离、提纯的基本方法选择与应用.
【分析】A.蒸发时应防止温度过高而导致固体分解或迸溅;
B.蒸馏时,温度计用于测量馏分的温度;
C.萃取剂的选择与密度大小无关;
D.分液时,应避免液体重新混合而污染.
【解答】解:A.蒸发溶液应到大量固体析出时,靠余热蒸干,不能蒸干,避免固体分解和或迸溅,故A正确;
B.蒸馏时,温度计用于测量馏分的温度,可使温度计水银球靠近蒸馏烧瓶的支管口处,故B正确;
C.萃取剂的选择与密度大小无关,如可用苯、四氯化碳等,故C错误;
D.分液时,下层液体从下端流出,上层液体应从分液漏斗的上口倒出,以避免液体重新混合而污染,故D正确.
故选C.
【点评】本题考查混合物的分离、提纯,侧重混合物分离原理及基本操作的考查,把握实验基本操作为解答本题的关键,题目难度不大.
15.下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)()
选项待提纯的物质选用的试剂操作方法
A NaCl(Na2CO3)稀硫酸蒸发结晶
B CO2(CO) O2点燃
C Zn (Ag)稀盐酸过滤
D 自来水(Cl﹣)﹣﹣﹣蒸馏
A.A B.B C.C D.D
【考点】物质的分离、提纯的基本方法选择与应用;物质的分离、提纯和除杂.
【分析】A.碳酸钠与硫酸反应生成硫酸钠;
B.在二氧化碳中CO不易点燃;
C.Zn与盐酸反应;
D.自来水中水的沸点较低.
【解答】解:A.碳酸钠与硫酸反应生成硫酸钠,引入新杂质,试剂不合理,应选盐酸,故A错误;
B.在二氧化碳中CO不易点燃,不能除杂,应利用灼热的CuO,故B错误;
C.Zn与盐酸反应,将原物质反应掉,故C错误;
D.自来水中水的沸点较低,则选择蒸馏法可除杂,故D正确;
故选D.
【点评】本题考查混合物的分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.
16.用N A表示阿伏加德罗常数的值.下列说法正确的是()
A.标准状况下,1 mol CO2、CO的混合气中含有的氧原子数为1.5N A
B.常温常压下,11.2 L 氯化氢气体中含有的分子数为0.5N A
C.N A个甲烷分子和1mol甲烷的质量相等
D.1 mol?L﹣1 CuCl2溶液中含有的氯离子数为2N A
【考点】阿伏加德罗常数.
【分析】A、CO2、CO中含有的氧原子数分别为2个和1个;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、1mol甲烷中即含N A个甲烷分子;
D、溶液体积不明确.
【解答】解:A、CO2、CO中含有的氧原子数分别为2个和1个,故1mol混合气体中含有的氧原子的个数介于2N A到N A个之间,但不一定为1.5N A个,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故11.2LHCl气体的物质的量小于0.5mol,分子个数小于0.5N A个,故B错误;
C、1mol甲烷中即含N A个甲烷分子,故N A个甲烷分子的质量与1mol甲烷的质量相等,故C 正确;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选C.
【点评】本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.
17.为了除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液.不正确的操作顺序是()
A.⑤②④①③B.⑤④②①③C.②⑤④①③D.①④②⑤③
【考点】化学实验操作的先后顺序.
【分析】除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子.
【解答】解:要先除硫酸根离子,然后再除钙离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加氢氧化钠除去镁离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,只要将三种离子除完了,过滤就行了,最后加盐酸除去过量的氢氧根离子碳酸根离子,顺序为:②⑤④①③或⑤②④①③或⑤④②①③.
故选D.
【点评】本题考查物质的分离、提纯和除杂等问题,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离.
18.与0.2mol H2O含有相同氢原子数的是()
A.0.2molHNO3B.标况下2.24L CH4
C.1.7g NH3D.1.505×1022个HCl分子
【考点】物质的量的相关计算.
【专题】计算题.
【分析】根据n=计算分子数,结合分子构成计算原子数.
【解答】解:0.2mol H2O含有的分子数为0.2N A,1个H2O分子含有2个氢原子,因此0.2mol H2O含有的H原子数为0.4N A.
A、0.2molHNO3含有的分子数为0.2N A,1个HNO3分子含有1个氢原子,因此0.2molHNO3含有的H原子数为0.2N A,故A错误;
B、n(CH4)==0.1mol,N(CH4)=0.1N A,1个CH4分子含有4个氢原子,因此含有的氢原子数为0.4N A,故B正确;
C、n(NH3)==0.1mol,N(NH3)=0.1N A,1个NH3分子含有3个氢原子,因此含有的氢原子数为0.3N A,故C错误;
D、1个HCl分子含有1个氢原子,1.505×1022个HCl分子含有1.505×1022个氢原子,即为
0.025N A,故D错误;
故选:B.
【点评】本题考查了以物质的量为中心的计算,题目综合性较强,熟练掌握n=综合应用以及分子组成是解题的关键.
19.宜兴竹海风景区被称为天然氧吧,其原因是空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”.O2﹣就是一种空气负离子,其摩尔质量为()A.32 g B.33 g C.33 g?molˉ1D.32 g?molˉ1
【考点】摩尔质量.
【分析】根据摩尔质量在以g/mol为单位时,在数值上等于其相对分子质量.
【解答】解:O2﹣比O2多一个电子,电子的质量可以忽略不计,故O2﹣的相对分子质量为32,所以O2﹣的摩尔质量为32g/mol,
故选D.
【点评】本题主要考查的是摩尔质量及其单位,根据与相对分子质量的关系即可判断,难度不大.
20.“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质()
①是溶液
②是胶体
③能产生丁达尔效应
④能透过滤纸
⑤不能透过滤纸
⑥静置后,会析出黑色沉淀.
A.①④⑥B.②③⑤C.②③④D.①③④⑥
【考点】纳米材料.
【专题】溶液和胶体专题.
【分析】纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中形成分散系是胶体,依据胶体的特征和性质分析判断问题;
【解答】解:纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种.属于胶体分散质微粒直径的大小,若将纳米碳均匀地分散到蒸馏水中形成分散系是胶体,具有丁达尔现象,能透过滤纸,具有介稳性,不生成沉淀,故②③④正确;
故选C.
【点评】本题考查了胶体分散系的本质特征,胶体性质的应用,分散系的本质区别是分散质微粒直径大小.
二、解答题(共6小题)(选答题,不自动判卷)
21.取100mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出.计算:
(1)原混合液中Na2SO4的物质的量浓度是多少?
产生的气体在标准状况下的体积为多少L?
(3)过滤出沉淀后,所得滤液的物质的量浓度为多少?(写出计算过程).
【考点】有关混合物反应的计算.
【分析】过滤、干燥后得到14.51g白色沉淀为硫酸钡、碳酸钡的质量,用足量的稀硝酸处理沉淀后,沉淀最后减少到4.66g,故硫酸钡为4.66g,碳酸钡质量为14.51g﹣4.66g=9.85g,(1)根据n=计算硫酸钡的物质的量,根据硫酸根守恒有n(Na2SO4)=n(BaSO4),再根据c=计算原混合液中Na2SO4的物质的量浓度;
根据n=计算碳酸钡的物质的量,生成的气体为二氧化碳,根据碳元素守恒有n(CO2)=n (BaCO3),再根据V=nVm计算二氧化碳的体积;
(3)过滤出14.51g沉淀后,溶液中溶质为NaOH,根据钠离子守恒n(NaOH)=2n(Na2SO4)+2n(Na2CO3),再根据c=计算原混合液中NaOH的物质的量浓度.
大悟县三里城镇初中学校2014-2015年学年度第一学期 第一次化学月考试题 姓名:_______________班级:_______________考号:_______________ 题号一、选择 题 二、填空 题 三、实验, 探究题 总分 得分 一、选择题(每空3 分,共18 分) 1、下列所示的变化中,属于化学变化的是( ) A.铁丝弯曲 B.香水挥发 C.燃放烟花 D.干冰升华 2、下列实验操作错误的是() A.向量筒里倾倒液体 B.从滴瓶里取出液体 C.向试管里加入粉末 D.给试管里液体加热 3、能够使带火星的木条复燃的是( )。 A.氧气 B.二氧化碳 C.水蒸气 D.石蜡 4、人类需要洁净的空气。目前我国城市空气质量日报中的污染物不包括() A、可吸入颗粒 B、二氧化硫 C、二氧化氮 D、二氧化碳 5、人呼出的气体中相对空气增多的成分是( )。 A.水蒸气 B.二氧化碳 C.二氧化碳、水蒸气 D.氧气
6、下列操作中,可以鉴别空气、氧气和二氧化碳三瓶气体的是( )。 A.观察气体颜色 B.闻气体的气味 C.插入燃着的木条 D.倒入澄清的石灰水 二、填空题(每空1 分,共26 分) 7、将下列各仪器名称前的字母序号与其用途相对应的选项填写在相应位置上。 (1)用来夹持试管的工具是____________________________________________。 (2)贮存固体药品的仪器是____________________________________________。 (3)常作为反应用的玻璃容器是________________________________________。 (4)用于洗涤仪器内壁的工具是________________________________________。 (5)用于夹持燃烧铁的工具是________________________________________。 (6)检验物质可燃性,进行固体燃烧实验的仪器是________________________。 (7)用于加热浓缩溶液、析出晶体的瓷器是______________________________。 (8)加热时常垫在玻璃容器与热源之间的用品是__________________________。 8、将一种无色无味的液体A装入试管,用带火星的木条伸入试管,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C且瓶底有少量液体D的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F。 (1)写出它们的名称:A. B. C. D. E. F. 。
上海市高一上学期化学10月月考试卷 姓名:________ 班级:________ 成绩:________ 一、单选题 (共12题;共24分) 1. (2分)经分析,某种物质只含有一种元素,则此物质() A . 一定是一种单质 B . 一定是纯净物 C . 一定是混合物 D . 可能是纯净物,也可能是混合物 2. (2分)某学生用托盘天平称取 3.3g食盐,称量时指针若左偏,此时应该() A . 增加药品 B . 减少药品 C . 增加砝码 D . 减少砝码 3. (2分) (2016高一上·海南期末) 下列叙述中,不正确的是() A . 用酒精萃取碘水中的碘 B . 少量金属钠保存在煤油中 C . 不慎洒出的少量酒精在桌上着火时,立即用湿布盖灭 D . 配制1.00mol/L NaCl溶液时,将称好的NaCl固体放入烧杯中溶解 4. (2分) (2017高一上·佛山期中) 2009年9月25日,我国成功发射“神舟七号”载人飞船.飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为:2NH4ClO4═N2↑+Cl2↑+2O2↑+4H2O.下列有关叙述正确的是() A . 铝粉的作用是点燃时可以置换出氧气
B . 在反应中NH4ClO4仅起到氧化剂作用 C . 该反应属于分解反应,也属于氧化还原反应 D . 上述反应瞬间能产生高温,高温是推动飞船飞行的主要因素 5. (2分) (2019高一上·温州期中) 下列分散系中,能产生“丁达尔效应”的是() A . 食盐水 B . 豆浆 C . 石灰乳 D . 硫酸铜溶液 6. (2分) (2017高二下·南阳期末) 下列有关实验操作、现象和结论都正确的是() A . A B . B C . C
绵阳中学高级第一学期第一学月考试数学试题 一、选择题(每小题4分,共40分) 1.下列各组函数中,表示同一个函数的是( ) A .(),()f x x g x == B .2()()f x g x = = C .21 (),()11 x f x g x x x -= =+- D .()1 1,()f x x g x = -=2.设集合{} 32M m m m Z =-<<∈且,{} 13N n n n Z =-≤≤∈且, 则M N = ( ) A .{}0,1 B .{}1,0,1- C .{}0,1,2 D .{}1,0,1.2- 3.设函数221(1) ()2(1)x x f x x x x ?-≤=?+->? ,则1( )(2)f f =( ) A . 15 16 B .2716 - C . 89 D .16 4.函数0()(2)f x x =+-的定义域是( ) A .{} 1x x ≥- B .{} 12x x x ≥-≠且 C .{} 12x x x >-≠且 D .{} 1x x >- 6.设全集{}{} ,0,1U R A x x B x x ==>=<-,则()()U U A B B A =????????( ) A .? B .{} 0x x ≤ C .{} 1x x >- D .{} 01x x x ><-或 7.设{}12345,,,,M a a a a a ?且{}{}12312,,,M a a a a a =,则集合M 的个数是( )
A .1 B .2 C .3 D .4 8.设全集U R =,{} {}2 21,M x y x N y y x ==+==-,则M 和N 的关系是( ) A .M N ?≠ B .N M ?≠ C .M N = D .{}(1,1)M N =- 9.设函数()f x 在(1,1)-上是奇函数,且在(-1,1)上是减函数,若(1)()0f m f m -+-<,则m 的取值范围是( ) A .1(0,)2 B .(1,1)- C .1(1,)2 - D .1(1,0) (1,)2 - 10.设()f x 是(,)-∞+∞上的奇函数,(2)()f x f x +=-,当01x ≤≤时,()f x x =,则 (3.5)f =( ) A .0.5 B .-1.5 C .-0.5 D .-1.5 二、填空题(每小题4分,共20分) 11.设全集 {}{}23,4,5,3,1a a A a =-+-=-且 {}1U A =, 则实数a = 。 12.设()f x 是偶函数,当0x <时,()(1)f x x x =+,则当0x >时, ()f x = 。 13.设函数2 ()2f x x ax =-+与()a g x x =在区间[]1,2上都是减函数,则实数a 的取值范围是 。 14.函数y =的增区间是 。 15.若函数 y = 的定义域是R ,则实数a 的取值范围是 。
2019届高一上学期(月考一)生物试卷 班级:_______ 姓名:_________ 得分: _________ 注意:①本试卷共6页,答题卡1页,卷面满分100分,考试时间90分钟。 ②请将所有答案填写在答题卡上,用黑色碳素笔或签字笔书写,否则不得分。 第Ⅰ卷选择题(共60分) 一、单选题(30题,每题2分,共60分) 1、植物体生命系统的结构层次为() A.细胞→组织→器官 B.细胞→组织→器官→系统 C.细胞→器官→系统 D.细胞→器官→组织→系统 2.下列生物中,不具有细胞结构的是() A.酵母菌 B.非洲猪瘟病毒 C.蓝藻 D.大肠杆菌 3.下列4种生物中,哪一种生物的细胞结构与他其三种生物的结构有明显的区别? A.乳酸菌 B.酵母菌 C.洋葱鳞片表皮 D.蘑菇 4.下列关于显微镜使用的叙述中,正确的是() A.因为藓类的叶片大,在高倍镜下容易找到,所以可以直接使用高倍物镜 B.在低倍镜下找到叶片细胞,即可换高倍物镜 C.换高倍物镜后,必须先用粗准焦螺旋调焦,再用细准焦螺旋调至物像最清晰 D.为了使高倍镜下的视野亮一些,可使用较大的光圈或凹面反光镜 5、下列哪一项说法不符合细胞学说的主要内容() A.细胞学说揭示了细胞和生物体结构的统一性 B.细胞的作用既有独立性又有整体性 C.细胞通过分裂产生新细胞 D.生物体都是由细胞构成的 6、下列叙述错误的是() A.病毒虽不具有细胞结构,但其体内也存在遗传物质 B.酵母菌体内有核膜包被的细胞核 C.核酸、蛋白质、叶绿体、液泡、细胞核和细胞壁这些物质或结构在衣藻体内都存在 D.蓝藻有叶绿体,能进行光合作用 7、细菌与酵母菌在结构上的区别是,细菌无() A.细胞结构 B.细胞膜 C.染色体 D.细胞质 8、松树和松鼠的体细胞中都含有的结构是() ①细胞壁②细胞膜③线粒体④叶绿体 ⑤中心体⑥核糖体⑦内质网⑧染色质 A.①②⑥⑦⑧ B.②③⑥⑦⑧ C.②④⑥⑦⑧ D.②③④⑥⑧ 9、某氨基酸分子中含有2个氨基(—NH2),其中一个氨基和羧基连在同一个碳原子上,则另一个氨基的部位应是() A.连在氨基和羧基之间 B.一定连在羧基上 C.在R基上 D.与氨基一端相连 10、下列有关组成生物体化学元素的论述,正确的是() A.组成生物体和组成无机自然界的化学元素中,碳元素的含量最多 B.人、动物与植物所含的化学元素的种类差异很大 C.组成生物体的化学元素在无机自然界都可以找到 D.不同生物体内各种化学元素的含量比例基本相似 11、病毒储存遗传信息的物质是() A.DNA B.DNA或RNA C.RNA D.DNA和RNA 12、原核细胞与真核细胞的根本区别是有无() A.细胞核 B.液泡膜 C.细胞膜 D.细胞壁 13、生活在沙漠地带的仙人掌叶肉细胞中,占干重和鲜重最多的化合物分别是() A.水、蛋白质 B.水、糖类 C.蛋白质、水 D.核酸、水 14、毒菇的一种毒素鹅膏草碱是一种环状八肽。若20种氨基酸的平均分子量为128,则鹅膏草碱的肽键数是() A.7 B.8 C.9 D.10 15、蓝藻是最早进行光合作用的原核生物,它含有的细胞器是() A.叶绿体 B.核糖体 C.中心体 D.高尔基体 16、生命活动离不开细胞,不包括下列内容中的( ) A.缩手反射的完成是以细胞为结构基础的 B.生物与环境的物质和能量交换以细胞代谢为基础 C.遗传和变异以细胞内基因的传递和变化为基础 D.蚯蚓的单个细胞也能完成各种生命活动 17、下列哪项不属于生命系统的结构层次( ) A.池塘中的一只青蛙 B.青蛙的表皮细胞 C.表皮细胞中的水和蛋白质分子 D.池塘中的水、阳光等环境因素以及生活在池塘中的青蛙等各种生物 18、下列各项组合中,能体现生命系统由简单到复杂的正确层次是( ) ①一个大西瓜②血液③白细胞④变形虫⑤血红蛋白⑥SARS病毒⑦同一片草原上的所有绵羊⑧一片森林中的所有鸟⑨一片桃园⑩一个池塘中的所有生物 A.⑤⑥③②①④⑦⑩⑨ B.③②①④⑦⑩⑨ C.③②①④⑦⑧⑩⑨ D.⑤②①④⑦⑩⑨ 19、一段朽木上面长满了苔藓、地衣,朽木凹处聚积的雨水中还生活着水蚤等多种生物,树洞中还有老鼠、蜘蛛等。下列各项,与这段朽木所属的“生命系统的结构层次”水平相当的是( ) A.一块稻田里的全部害虫 B.一个池塘中的全部鲤鱼 C.一片松林里的全部生物 D.一间充满生机的温室大棚 20、下列四组生物中,细胞结构相似的是 ( ) A.草履虫、乳酸菌、香菇 B.梧桐、草履虫、大肠杆菌 C.水稻、黄瓜、大豆 D.蘑菇、灵芝、豌豆 21、SARS病毒、蓝细菌、酵母菌的结构及功能有很大区别,但是它们( ) A.都含有蛋白质和核酸 B.都没有核膜和染色体 C.都有细胞壁,只是细胞壁的成分各不相同 D.都是营腐生或寄生的异养生物 22、大部分动植物体是不透明的,不能直接在显微镜下观察,一般要经过特殊处理,如将标本做成很薄的切片。但酵母菌、水绵、洋葱表皮等材料却可以直接做成装片放在显微镜下观察,这主要是因为它们( ) A.是单个或单层细胞 B.都带有特殊的颜色 C.是无色透明的 D.是活的细胞 23、发菜细胞群体呈黑蓝色,状如发丝;生菜是一种绿色植物,两者分别因与“发财”和“生财”谐音而备受百姓青睐。下列属于发菜和生菜的相同点的是( ) A.是真核生物 B.含有叶绿体 C.是自养生物 D.有核膜 24、下列选项中全部属于组成细胞的大量元素的是( ) A.P、N、Mn、K B.N、S、Ca、P C.Fe、S、P、N D.Fe、Mn、B、Mo 25、下列哪项实例能够证明微量元素是生命活动所必需的( ) A.Mg2+是叶绿素的组成成分 B.油菜缺少B时只开花不结果 C.哺乳动物血液中Ca2+含量太低,会抽搐 D.缺P会影响ATP的合成 26、关于生物组织中还原糖的检测,下列叙述正确的是( ) A.常见的还原糖包括葡萄糖、果糖、麦芽糖 B.对还原糖的检测用双缩脲试剂 C.在组织样液中加入斐林试剂后试管内液体呈现无色,加热后变成砖红色 D.实验结束时将剩余的斐林试剂装入棕色瓶,以便长期保存备用 27、下列有关组成生物体化学元素的论述,正确的是( ) A.组成生物体和组成无机自然界的化学元素中,碳元素的含量最多 B.人、动物与植物所含的化学元素的种类差异很大 C.组成生物体的化学元素在无机自然界都可以找到 D.不同生物体内各种化学元素的含量比例基本相似 28、谷氨酸的R基为—CH2CH2COOH,则谷氨酸的分子式是( ) A.C5H9O4N B.C4H9O4N C.C5H8O4N D.C4H9O5N 29、鸡蛋煮熟后,蛋白质变性失活,这是由于高温破坏了蛋白质的( ) A.肽键 B.肽链 C.空间结构D.氨基酸 30下图所列的5种化合物中,属于氨基酸的是() A. ②③④⑤ B. ①③④⑤ C. ①②④⑤ D. ①②③④
人教版九年级第一次月考化学试卷 姓名:________ 班级:________ 成绩:________ 一、单选题 1 . 下列大小关系正确的() A.微粒的大小:分子>原子 B.地壳中元素的含量:Al
C.该反应是分解反应 D.该反应是化合反应 5 . 下列实验操作正确的是() B.量筒读数 A.过滤 D.点燃酒精灯 C.稀释浓硫酸 6 . 世界环境日为每年的6月5日, 2018年的世界环境8日主题为“塑战塑决”(BeatPlastic Polution),中国环境日的主题为“美丽中国,我是行动者”,2019年世界环境日也将在中国杭州举办。以下关于环境保护说法不正确的是() A.将煤炭进行脱硫处理,减少二氧化硫的排放 B.使用一些新型的、可降解的塑料,减少“白色污染” C.化学是环境污染的主因,没有化学,就不会产生环境问题 D.提倡使用无磷洗衣粉,以减少水体污染 7 . 四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示.则有关说法中不正确的() A.丁一定是化合物
江苏省2020-2021年高一上学期化学第一次月考试卷 姓名:________ 班级:________ 成绩:________ 一、选择题(本题共20小题,每小题2分,共40分。) (共20题;共40分) 1. (2分) (2016高二下·丰城期中) 化学与生活、社会密切相关.下列说法正确的是() A . 石油的分馏、煤的气化、海水提溴过程都包含化学变化 B . 地沟油经处理后可作为汽车燃油,故地沟油成分是液态烃 C . 淀粉、油脂、蛋白质都能水解,但水解产物不同 D . 乙烯和苯都能使溴水褪色,且褪色的原因相同 2. (2分) (2016高二上·灌云期中) 下列物质中,属于盐类的是() A . Na2O B . CaCO3 C . Ca(OH)2 D . C2H12O6 3. (2分) (2016高二下·惠州开学考) 下列由实验现象得出的结论正确的是() A . A B . B C . C
D . D 4. (2分)容量瓶上需要标有:①温度,②浓度,③容量,④压强,⑤刻度线,⑥碱式或酸式六项中的() A . ①③⑤ B . ②④⑥ C . ③⑤⑥ D . ①②③ 5. (2分) (2017高二上·济南期末) 电解质溶液有许多奇妙之处,你只有深入思考,才能体会到它的乐趣.下列关于电解质溶液的叙述中正确的是() A . Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 B . 常温下,1 mol?L﹣1的CH3COOH溶液与1 mol?L﹣1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣) C . 物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者 D . 常温下,某溶液中由水电离出的c(H+)=10﹣5 mol?L﹣1 ,则此溶液可能是盐酸 6. (2分) (2015高二上·岳阳期末) 下列应用与盐类的水解无关的是() A . 热的纯碱溶液去除油污能力更强 B . NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火器 C . 保存FeSO4溶液时加入少量铁粉 D . 把AlCl3溶液加热蒸干灼烧至质量不再变化得到Al2O3 7. (2分)与OH-具有相同质子数和电子数的粒子是() A . F- B . Cl- C . NH3 D . Na+
黑龙江省青冈县2016-2017学年高一化学上学期月考试卷(A卷) 一、单项选择题(每题三分,共54分) 1、下列仪器不能用酒精灯直接加热的是 ①烧杯②坩埚③蒸发皿④试管⑤蒸馏烧瓶⑥锥形瓶⑦燃烧匙 A.③⑥⑦ B.①⑤⑥ C.⑤⑥⑦ D.①⑤ 2、现有①MgSO4,②Ba(NO3)2,③NaOH,④CuCl2,⑤KCl五种溶液,不加任何其他试剂,可鉴别且鉴别的先后顺序也正确的是 A.④③②①⑤ B.④⑤③②① C.④③①②⑤ D.④②③①⑤ 3、下列变化中,必须加入氧化剂才能发生的是 A.SO2→S B.SO32—→SO2 C.I—→I2 D.HCO3—→CO32— 4.下列各组物质,前者属于电解质,后者属于非电解质的是 A.NaCl、BaSO4 B.铜、二氧化硫 C.KOH、蔗糖 D.KNO3、硫酸溶液 5、已知:2FeCl3+2KI===2FeCl2+2KCl+I2,2FeCl2+Cl2===2FeCl3,2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O。若某溶液中有Fe2+、I-和Cl-,要氧化除去I-而不影响Fe2+和 Cl-,可加入的试剂是 A.Cl2 B.KMnO4 C.FeCl3 D.HCl 6、下列各组离子在溶液中能大量共存,加入OH-有沉淀生成,加入H+有气体生成的一组离子是 A.K+、Mg2+、Cl-、HCO-3 B.K+、Cu2+、SO2-4、Na+ C.NH+4、CO2-3、NO-3、Na+D.NH+4、Cl-、HCO-3、K+ 7.使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是 ①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了 ②有些固体溶解会放热,若未经冷却即转移至容量瓶 ③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤 ④转移溶液前容量瓶内有少量蒸馏水 ⑤定容时,仰视容量瓶的刻度线 ⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线 A.①③⑤⑥B.①②⑤⑥
2018--2019学年度(下)天宝中学 九年级第一次月考化学试题 (满分:50分;时间:60分钟命题:孟兰英审题:张清) 可能用到的相对原子质量:H-1O-16Fe-56Zn-65 一、选择题(本大题包括10个小题,每题2分,共20分)每小题只有一个选项符合题意,将符合题意的选项填在答题卡表格内 1.下列变化不属于化学变化的是:() A.纸张燃烧B.蔗糖溶解C.食物腐烂D.铁钉生锈 2.浓盐酸.浓硫酸敞口放置在空气中一段时间后,溶液质量变化为() A.增加减小 B.减小减小 C.减小增加 D.增加增加 3.要使右图装置中的小气球鼓起来,则使用的固体和液体可以是() A.硝酸铵和水B.铜和稀硫酸 C.固体氢氧化钠和水D.氯化钠和水 4.下图是甲.乙.丙.丁四种常见金属与盐酸反应的比较示意图。以下说法错误的是()A.如乙金属为Fe,则乙与盐酸反应的化学方程式为: 2Fe+6HCl=2Fe C l+3H↑ 3 2 B.金属甲.乙.丙与盐酸反应属于置换反应 C.若乙是金属Al,则丙可能是Zn和Fe D.四种金属的活动性强弱顺序为:甲.乙.丙.丁 5.下列各组气体中既能用浓硫酸干燥,又能用苛性钠干燥的是() A.H、O 2 2B.C O、N 2 2 C.SO、CO D.SO、 CO 2 22 6.下列书写正确,且属于置换反应的是() A Cu+2HCl= CuCl+H↑B.3Cu+2AlCl= 2Al +3Cu Cl 2 2 3 2 C.NaOH+HCl=NaCl +H O D.2Al+6HCl=2AlCl +3H↑2 3 2 7.推理是化学学习中常用的思维方法.下列推理正确的是 A.酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸 B.某无色气体混入空气后点燃爆炸,可证明该气体一定是H 2 C.在同一化合物中,金属元素显正价,所以非金属元素一定显负价 D.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小8.根据如图所示的溶解度曲线判断,下列说法正确的是() A.甲物质的溶解度大于乙物质的溶解度 B.甲物质的不饱和溶液温度升高后变成饱和溶液 C.将t℃甲、乙两物质的饱和溶液温度降低到t℃时都会析出晶体 2 1
江苏省高一上学期月考化学试卷(1月份) 姓名:________ 班级:________ 成绩:________ 一、选择题 (共20题;共40分) 1. (2分)合金具有优良的机械性能,用途广泛.下列物质不属于合金的是() A . 黄铜 B . 不锈钢 C . 紫铜 D . 生铁 2. (2分)由碳原子构成的纳米碳管可以作为储存氢气的优良容器,其单层部分结构示意图如图,下列说法正确的是() A . 0 12g纳米碳管中含有6.02x1021个碳原子 B . 纳米碳管是一种无机化合物 C . 纳米碳管与石墨互为同位素 D . 纳米碳管不会与氧气反应 3. (2分) (2017高一上·六安期末) 下列表述不正确的是() A . 人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3 B . 硅是制造太阳能电池的常用材料 C . 四氧化三铁俗称铁红,可用于作油漆、红色涂料 D . 分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液 4. (2分) (2016高一上·吉安期末) 下列关于教材中的各项知识的说法或做法不正确的是() A . 漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂
B . 氮肥包括铵态氮肥、硝态氮肥和尿素 C . 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 D . 硅胶可用作食品干燥剂 5. (2分)下列各组气体,在实验室中可用硫酸制取,又能用H2SO4干燥的一组是() A . HCl HI H2 B . H2S CO2 H2 C . H2 SO2 HCl D . NH3 N2 H2 6. (2分)下列关于实验的叙述正确的是() A . 石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 B . 滴定管盛装滴定液前需先用蒸馏水洗净,再用滴定液润洗 C . 配制一定物质的量浓度的溶液时,可直接在容量瓶中稀释或溶解 D . 金属锂保存在煤油中,防止暴露在空气中被氧化 7. (2分) (2017高一上·简阳期中) 为除去括号内的杂质,下列各选项中所选用的试剂或方法不正确的是() A . Na2CO3溶液(NaHCO3):选用适量的NaOH溶液 B . NaHCO3溶液(Na2CO3):通入过量的CO2气体 C . Na2O2粉末(Na2O):将混合物在O2中加热 D . Na2CO3溶液(Na2SO4):加入适量的Ba(OH)2溶液,过滤 8. (2分)(2018·重庆模拟) 普通锌锰电池筒内无机物主要成分为MnO2、NH4Cl、ZnCl2等。某研究小组探究废于电池内的黑色固体并回收利用时,进行如图所示实验。下列有关实验的叙述正确的是()
高一上学期第一次月考试卷 一、完形填空 1. 完形填空 Once a boy really had everything he wanted, so he was1interested in the rarest objects. One day he2a mysterious mirror and took it home. When he looked into the mirror, he found that his 3looked very sad. He tried 4, but it remained the same. Surprised, the boy went off to buy some sweets. He went home and looked into the mirror as happily as possible, 5he still looked sad. He bought all kinds of toys, but he looked forever 6in that mirror. So the boy put the mirror away in a 7. “What a8mirror! I’ve never seen a mirror that didn’t 9properly!” That same afternoon he went out to play, but on his 10to the park he saw a little girl crying loudly. So he went over to see what was happening. The little girl told him that she had 11her parents. Together, they 12in search of them. As the little girl continued crying, the boy 13his money in buying sweets lo cheer her up.14after walking for a long time, they found her parents, who looked very worried. The boy said goodbye, and walked off towards the park. However,15the time, he decided to turn around and head 16home, as he had no time to 17. At home, he went to his room and noticed a shining 18in the comer where he had
高一上学期次月考总结1000字 这是我考得最差的一次考试,是高一上学期的次月考。再次,我深深的反思一下,希望以此警示自己。 语文——基础知识不好,回家没有认真复习背诵,古诗词默写部分错了几个字。《朝花夕拾》的相关资料课后没有看,没做好充分的准备。作文记叙文写得有点跑题,没有抓住其核心内容,没有真情实感和有些语句不通顺势被扣分的主要原因。对此我对以后学习提出改正,上课要仔细听老师讲课,多复习、背诵等,提高写作水平和能力,多练笔,多读书,多参加有益的活动,扩大知识面,做到“读书破万卷,下笔如有神”的境界。 数学——这次考试我最后悔的一件事是倒数第二题,我在抄写时把符号写反了,本来会做的题,为此扣了7分。还有就是X2-kxy+9y2的那道题,由于我考虑问题不够全面,所以只答了一个6,答案是±6。在以后的考试中,我要细心看题,用全面的眼光看待和思考一个问题,不能只知其一,不知其二。并且也要认真仔细的完成老师不值得午练作业。 英语——在这次考试中,完形填空、改句子和翻译句子方面扣分很多。在试卷中有些单词不认识,有些语法不知道。对此,我要上课认真听讲,多读英语的小短文,扩大知识面,牢记老师讲过和学过的知识,争取下次取得一个好成绩。
历史——这次总体来说还是有进步,就是最后的一个大题扣分严重。写出从1919年以来近代先进中国人向西方学习经历了哪些变化?一看问变化,我的脑子就空了,完全找不到答案。回顾中国的近代变化过程,从中感悟是什么?我也完全忘了这道题的标准答案,所以就写出了我自己感悟。无耐,两道题扣掉了5分。另外丢失的几分,就是我基础知识没有背好,选择题扣掉了。以后我要加倍学习,记住每一道题的标准答案,学得更好! 生物——这是我有史以来考的分,以前都在82、81分上徘徊。这次考试的主要原因在于平时做的题目太少,有些题换个方式问就不会了,有些题还是基础知识没有记牢。为了再次提高成绩,我买了一本习题开始做练习,认真背诵课本上的内容,我相信有了这次的提高,就一定会有下一次的。 政治——这次考试考的不好。最后一道15分的大题,只得了2分。在考试前,我把所有的题都看了一遍,除了这一题外的其他题我都背过了。可是,它真考了,而且分数还很高,为什么我背过什么它不考什么,我背不过的它偏要考呢?以后我要改正这种饶幸心理,认真准备好,背过所有的问题。物理——这是物理的次考试,但我认为这么简单的题我考这点分数是完全没道理的。有三道题理解错误。以后我要勤于思考,善于发现问题,去解决问题。
福州市高一上学期月考化学试卷(9月份)B卷 姓名:________ 班级:________ 成绩:________ 一、单项选择题 (共15题;共30分) 1. (2分)下列实验操作中有错误的是() A . 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 B . 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 C . 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 D . 蒸发操作时,应使混合物中的水分蒸干后,才能停止加热 2. (2分) (2020高二上·新宁期末) 下列分离方法不正确的是() A . 用过滤的方法除去食盐水中的泥沙 B . 用蒸馏的方法将自来水制成蒸馏水 C . 用四氯化碳萃取碘水中的碘 D . 用分液漏斗分离汽油和植物油 3. (2分)以下是一些常用的危险品标志图标,在装运乙醇的包装箱上应贴的图标是() A . B .
C . D . 4. (2分) (2018高一上·白城月考) 现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如表所示,据此将乙二醇和丙三醇互相分离的最佳方法是() 物质分子式熔点(℃)沸点(℃)密度(g·cm-3)溶解性 乙二醇C2H6O2-11.5198 1.11易溶于水和酒精 丙三醇C3H8O317.9290 1.26能跟水、酒精以任意比互溶 A . 萃取法 B . 结晶法 C . 分液法 D . 蒸馏法 5. (2分)碘是一种易溶于酒精,苯,汽油,四氯化碳的物质,现有碘的水溶液,要从碘水中萃取出碘,下列试剂不能用作萃取剂的是() A . 四氯化碳 B . 汽油 C . 酒精 D . 苯 6. (2分)下列关于有机物的说法中,正确的是() A . 油脂和蛋白质都是天然高分子化合物,都能水解
高一上学期数学第一次月考试卷 一、单选题 1. 已知集合M={x∈N|x2-1=0},则有() A . B . C . D . 0, 2. 下列函数中,在其定义域内既为奇函数且又为增函数的是() A . B . C . D . 3. 下列各组函数中,表示同一函数的是() A . 与 B . 与 C . 与 D . 与 4. 满足条件集合的子集个数是() A . 15 B . 8 C . 7 D . 16 5. 设函数,则的值为() A . -2 B . -1 C . 1 D . 2 6. 某工厂6年来生产某种产品的情况是:前3年年产量的增长速度越来越快,后3年年产量保持不变,则该厂6年来这种产品的总产量C与时间t(年)的函数关系图象正确的是() A . B . C . D .
7. 集合,则 是() A . B . C . D . 8. 函数的单调递增区间是() A . B . C . D . 9. 已知集合,,若 ,则实数的取值范围是() A . B . C . D . 10. 若关于的不等式的解集为 ,其中,为常数,则不等式 的解集是() A . B . C . D . 11. 若函数的定义域为,值域为 ,则的取值范围是() A . B . C . D . 12. 设函数是定义在上的增函数,则实数取值范围() A . B . C . D . 二、填空题 13. 若,则=________.
14. 已知函数y=f(x)的定义域是[0,4],则函数的定义域是________. 15. 方程组的解组成的集合为________. 16. 已知函数满足关系:,则 的大小关系为________ 三、解答题 17. 已知集合A={x|x<-1,或x>2},B={x|2p-1≤x≤p+3}. (1)若p= ,求A∩B; (2)若A∩B=B,求实数p的取值范围. 18. (1)求函数的值域; (2)已知,求的解析式. 19. 函数是定义在上的奇函数,且 (1)求函数的解析式; (2)用定义证明: 在上是增函数; (3)解不等式: 20. 已知函数,且.
高一上学期第一次月考数学试题 数学试题共4页,满分150分,考试时间120分钟。 注意事项: 1. 答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置上。 2. 答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦擦干净后,再选涂其他答案标号。 3. 答非选择题时,必须使用0.5毫米黑色签字笔,将答案书写在答题卡规定的位置上。 4. 所有题目必须在答题卡上作答,在试题卷上答题无效。 一、选择题(本大题共12小题,每小题5分,共60分) 1.已知全集U {0,1,2,3,4},集合A {1,2,3}, B {2,4},则(命A) U B 为( ⑥{0},其中正确的个数为() 个 D.少于4个 A.6个 B.5 个 C. 4 4.已知A X| X2X60, B X| mx10,且A U B=A,则m的取值范围为 人 1 1 B. 0, 1 11111 A. ------------- C.0,- D.J— 32 3 23,232 乩卫列丛集合盅到篥合B的对应f是映射的是()() A. {1,2,4} B. {2,3,4} C. {0,2,4} 2 .如果A={x | X1},那么D. {0,2,3,4} ( A. 0 A B . {0} A C A D . {0} A 3.下列六个关系式:①a,b b,a ②a,b b, a ③{0} ④0 {0} ⑤{0}
6.下列图象中不能作为函数图象的是(
X 2 1 x 1 7.设函数f (x) 2 ,则 f(f(3))( ) — x 1 x A 1 re 2 13 A.- B. 3 C.- D.— 5 3 9 8. 下列各式中成立的是( ) 1 m 7 7 7 A . (一) n m 7 n B .12J( 3) 4 「3 C. 4 x 3 y 3 (x y)4 D.3 9 3 3 cx 3 9.函数f (x) , (x -)满足f[ f (x)] X,则常数c 等于( ) 2x 3 2 A. 3 B. 3 C. 3或3 D. 5或 3 10.下列函数中,既是奇函数又是增函数的为 ( ) A. y x 1 B y 2 x C. y 1 x D. y x | x | 11 .已知函数f x x 5 ax 3 bx 8, 且 f 2 10,那么 f 2等于() A.-26 B.-18 C.-10 D.10 12.若函数y x 2 2a 1 x 1在 ,2上是减函数,则实数 a 的取值范围是() 二、填空题(本大题共 4小题,每小题5分,共20分) 13?已知集合 A (x, y ) | y 2x 1 , B {(x,y )|y x 3}则 AI B = . 14. 若 f 丄 -^―,则 f x . x x 1 3 2 15. 若f x 是偶函数,其定义域为R 且在0, 上是减函数,则f - 与f a 2 a 1的 4 大小关系是 _____________ ? 16 ?已知定义在实数集R 上的偶函数f (x )在区间0, 上是单调增函数,若 f 1 f 2x 1,则x 的取值范围是 ____________________________ ? 三、解答题(本大题共 6小题,共70分,解答应写出文字说明,证明过程或演算步骤) 17.(本小题12分)全集u=R 若集合A x|3 x 10 , B x|2x7,则 A. [ 丁,)B.( 3 3 3] C. [ 2, )D.(
高一上学期化学第二次月考试卷 姓名:________ 班级:________ 成绩:________ 一、单项选择题 (共17题;共34分) 1. (2分) (2016高二上·拉萨期中) 生活处处有化学.下列说法正确的是() A . 制饭勺、饭盒、高压锅等的不锈钢是合金 B . 做衣服的棉和麻均与淀粉互为同分异构体 C . 煎炸食物的花生油和牛油都是可皂化的饱和酯类 D . 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 2. (2分) (2018高二上·佛山期末) 能产生丁达尔效应的是() A . 酒精 B . CuSO4溶液 C . Fe(OH)3胶体 D . 生理盐水 3. (2分) (2018高二下·杭州期中) 国务院颁布的《“十二五”控制温室气体排放工作方案》提出,2015年我国单位国内生产总值CO2排放要比2010年下降17%。下列说法错误() A . CO2属于酸性氧化物 B . CO2是导致酸雨发生的主要原因 C . 可用Na2CO3溶液捕捉(吸收)CO2 D . 使用氢能源替代化石燃料可减少CO2排放 4. (2分) (2016高二上·重庆期中) 下列关于电解质的说法正确的是() A . 强电解质溶液的导电性一定比弱电解质溶液的导电性强 B . 水溶液中导电能力差的电解质一定是弱电解质
C . 强电解质在稀的水溶液中全部以离子的形态存在 D . 强电解质都是离子化合物,而弱电解质都是共价化合物 5. (2分) (2018高三上·海淀期末) 下列解释事实的方程式中,错误的是() A . 铜和浓HNO3反应可用于制NO2气体:Cu+ 4HNO3((浓) = Cu(NO3)2 + 2NO2↑+ 2H2O B . “84”消毒液中滴少量白醋可增强漂白性:ClO- + H+ = HClO C . 氨水吸收少量SO2防止污染空气:2NH3·H2O + SO2 = 2NH4+ + SO32-+ H2O D . Na2O2在潜艇中可用于吸收二氧化碳并供氧:2Na2O2 +2CO2=2Na2CO3 + O2 6. (2分)加油站应张贴的标志是() A . B . C . D . 7. (2分)下列操作容易造成蔬菜中的维生素损失的是() A . 洗菜:要先洗后切 B . 浸泡:切好的菜要浸泡半天,以除去残留农药 C . 切菜:要随切随炒,切忌切好后久置 D . 烹饪:烹调蔬菜时适当加点醋,可以减少维生素C的损失
高一数学上学期第一次月考测试题 一、选择题: 1.已知集合}1,1{-=A ,}1|{==mx x B ,且A B A =?,则m 的值为 ( ) A .1 B .—1 C .1或—1 D .1或—1或0 2.函数22232 x y x x -=--的定义域为( ) A 、(],2-∞ B 、(],1-∞ C 、11,,222????-∞ ? ????? D 、11,,222????-∞ ? ?? ??? 3. 已知集合{}2{|3},|log 1M x x N x x =<=>,则M ∩N=( ) (A )? (B ){}|03x x << (C ){}|13x x << (D ) 4.若U 为全集,下面三个命题中真命题的个数是( ) (1)若()()U B C A C B A U U == 则,φ (2)若()()φ==B C A C U B A U U 则, (3)若φφ===B A B A ,则 A .0个 B .1个 C .2个 D .3个 5.不等式042<-+ax ax 的解集为R ,则a 的取值范围是( ) A .016<≤-a B .16->a C .016≤<-a D .0