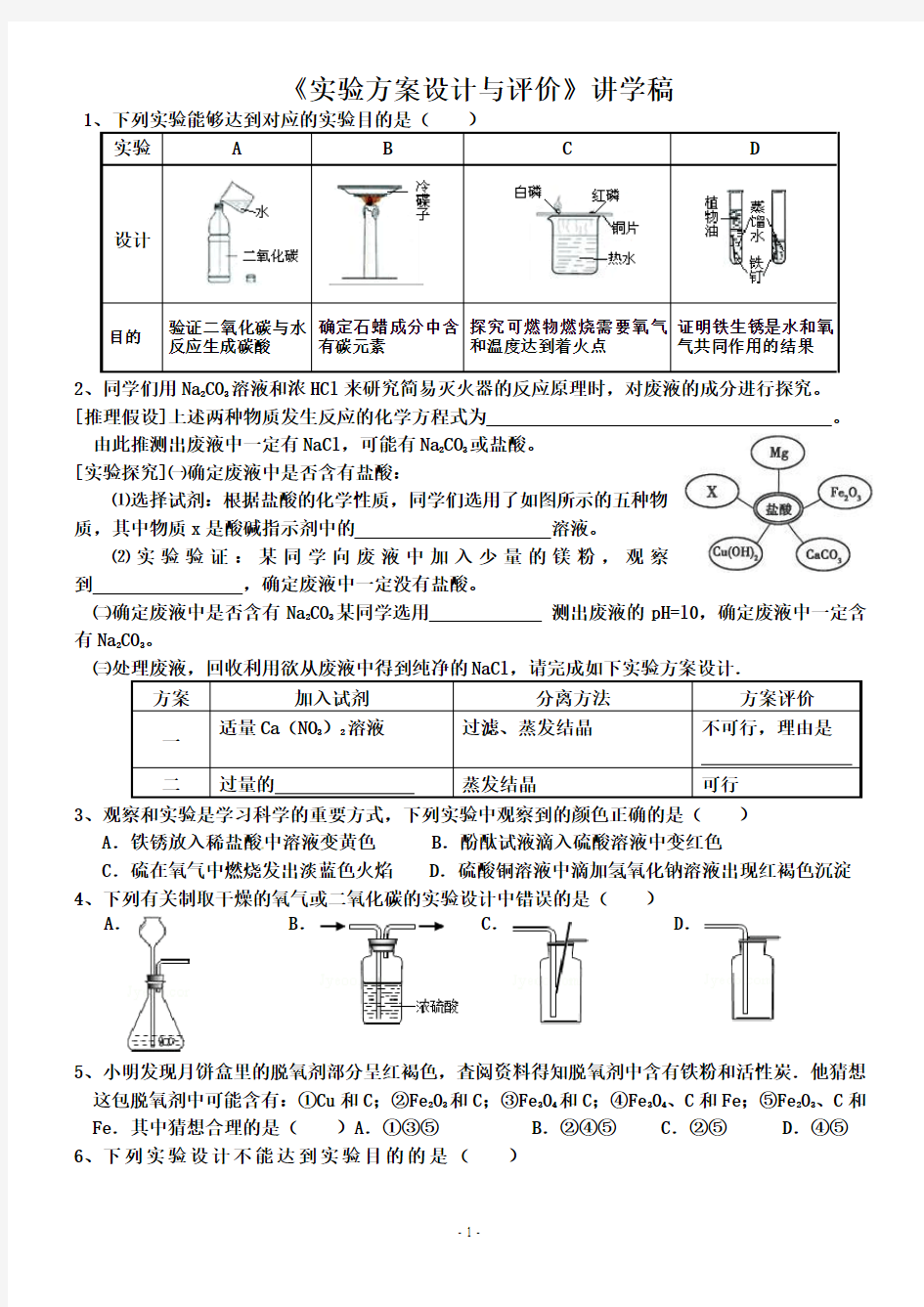
2、同学们用Na 2CO 3溶液和浓HCl 来研究简易灭火器的反应原理时,对废液的成分进行探究。
[推理假设]上述两种物质发生反应的化学方程式为 。 由此推测出废液中一定有NaCl ,可能有Na 2CO 3或盐酸。 [实验探究]㈠确定废液中是否含有盐酸:
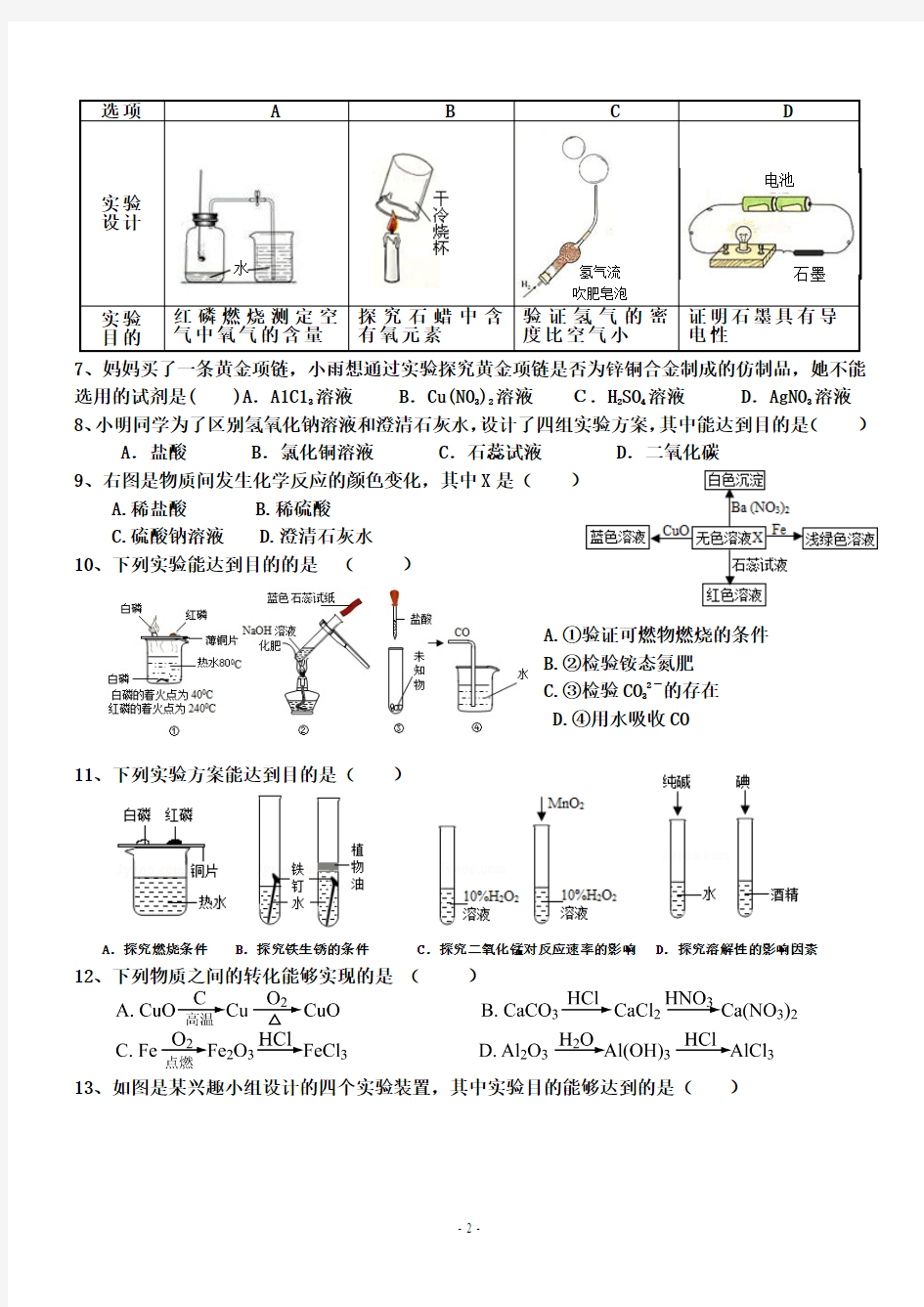
⑴选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物
质,其中物质x 是酸碱指示剂中的 溶液。
⑵实验验证:某同学向废液中加入少量的镁粉,观察到 ,确定废液中一定没有盐酸。
㈡确定废液中是否含有Na
2CO 3某同学选用 测出废液的pH=l0,确定废液中一定含有Na 2CO 3。
A .铁锈放入稀盐酸中溶液变黄色
B .酚酞试液滴入硫酸溶液中变红色
C .硫在氧气中燃烧发出淡蓝色火焰
D .硫酸铜溶液中滴加氢氧化钠溶液出现红褐色沉淀 .
D
5、小明发现月饼盒里的脱氧剂部分呈红褐色,査阅资料得知脱氧剂中含有铁粉和活性炭.他猜想这包脱氧剂中可能含有:①Cu 和C ;②Fe 2O 3和C ;③Fe 3O 4和C ;④Fe 3O 4、C 和Fe ;⑤Fe 2O 3、C 和Fe .其中猜想合理的是( )A .①③⑤ B .②④⑤ C .②⑤ D .④⑤
6、下列实验设计不能达到实验目的的是( )
验证氢气
7、妈妈买了一条黄金项链,小雨想通过实验探究黄金项链是否为锌铜合金制成的仿制品,她不能选用的试剂是( )A.A1C1
3
溶液 B.Cu(NO
3
)
2
溶液C.H
2
SO
4
溶液 D.AgNO
3
溶液8、小明同学为了区别氢氧化钠溶液和澄清石灰水,设计了四组实验方案,其中能达到目的是()
A.盐酸 B.氯化铜溶液 C.石蕊试液 D.二氧化碳
9、右图是物质间发生化学反应的颜色变化,其中X是()
A.稀盐酸
B.稀硫酸
C.硫酸钠溶液
D.澄清石灰水
10、下列实验能达到目的的是()
A.①验证可燃物燃烧的条件
B.②检验铵态氮肥
C.③检验CO
3
2一的存在
D.④用水吸收CO
11、下列实验方案能达到目的是()
A.探究燃烧条件 B.探究铁生锈的条件 C.探究二氧化锰对反应速率的影响 D.探究溶解性的影响因素
12、下列物质之间的转化能够实现的是()
13、如图是某兴趣小组设计的四个实验装置,其中实验目的能够达到的是()
水氢气流
吹肥皂泡
石墨
电池
、某同学设计了下列四个实验方案.其中不合理的是()
、某同学对下列四个实验都设计了两种方案,其中方案1合理、方案2不合理的是(17、下列依据实验目的所设计的实验操作中,正确的是( )
21、在做的实验时,实验室常通过加热草酸晶体(C
2H
2
O
4
)的方法来获取一氧化碳,加热草酸反解
⑵王强同学设计的系列实验的装置顺序是:
混合气体→A→B→C→D→B,其中C装置的作
用是;
装置D中可看到的现象是;第
二次使用装置B作用是;
⑶针对王强同学的设计,小美同学提出,应该在装置C后加一个装置B,目的是;
⑷周密同学提出,该系列装置还有一个缺点就是。
22、下列A~F是初中化学中的六个实验,
请按要求填空:
⑴上述实验中能达到实验目的且正确的
是 (填字母)。
⑵B实验中反应的化学方程
为,
实验说明空气中氧气的体积约
为,实验成功的关键是
①;
②;
③。
⑶D实验中烧杯③的作用是,F实验中玻璃棒的作用是。
⑷E实验的全过程观察到的现象是,发生反应的化学方程式为。
23、结合下列各图装置,回答有关问题。
⑴实验室中,用加热高锰酸钾的方法制取氧气,发生装置可选用 (填序号)。
⑵氢气是最清洁的燃料,密度比空气小,难溶于水,实验室常用锌粒与稀硫酸反应来制得。其制
备氢气发生装置和收集装置可选用。(填序号)。
⑶实验室用石灰石与稀盐酸反应制备二氧化碳,并测定所收集的二氧化碳的体积,应选用的装置是(填序号)。
⑷用下列实验装置完成对应实验(部分仪器已省略),操作正确并能达到实验目的的
是。
24、水蒸气通过灼热的焦炭后得到的混合气体有哪些成分?某化学兴趣小组在老师的指导下,对此进行了实验探究。【提出猜想】①该混合气体只含有一氧化碳、氢气;②该混合气体含有一氧化碳、二氧化碳、氢气和水蒸气;③该混合气体只含有二氧化碳、氢气和水蒸气;④该混合气体只含有一氧化碳、二氧化碳和氢气
【查阅资料】a.无水硫酸铜遇水由白色变为蓝色。b.碱石灰是固体氢氧化钠和氧化钙的混合物。
c.浓硫酸具有强烈的吸水性,常用作某些气体的干燥剂。
【实验过程】同学们在老师的指导下设计了如下图所示装置,并进行了实验(部分夹持仪器已略去)。
⑴装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,由此得出的结论为混合气体
中有。B中变化的化学方程式为。
⑵装置C中的药品为。
⑶E中氧化铜变红、F中无水硫酸铜变蓝、G中澄清石灰水变浑浊,说明混合气体中还
存在的气体是; E中的变化说明氧化铜具有性。
【实验结论】猜想正确。
【实验反思】经过讨论,同学们将上图中装置C~H进行了简化,只用下图
所示装置并自选必要试剂就能完成探究。
其中,干燥管中碱石灰的作用为,烧杯
上能观察到的现象是。最后一步的实验操作
及现象是。
25、小明在探究CO
2
和NaOH是否发生反应时,设计出下列三种装置进行
实验:⑴写出上图中标有字母的仪器
名称:a ,
b 。
⑵以上三个实验中,①③有明显现象,
请你帮小明记录他观察到的实验现
象:实验①。实
③。
⑶实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广.
口瓶
..,以使实验取得成功,你将选用的物品是,改进后能看到的实验现象是。
⑷请你进一步设计实验来检验CO
2和NaOH溶液反应生成了Na
2
CO
3
,并将有关的实验操作、现象、
26、在高效复习课堂中,同学们利用“硫酸、硝酸钡、氢氧化钠、碳酸钾”四种物质的溶液对“复
分解反应发生的条件”进行再探究。
【知识回放】
通过判断上述四种溶液两两之间能否发生反应,我能写出其中符合下列条件的两个化学方程式:⑴一个中和反应;⑵一个有沉淀生成的反应。
【挖掘实质】
⑴图1是HCl 和NaOH 在水中解离出离子的示意图,小丽发现HCl 在水中会解离出H +和Cl -,NaOH
在水中会解离出Na +
和OH -
,以此类推硝酸钡在水中会解离出的离子是 (填离子符号)。 ⑵图2是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该化学反应的实质可以表示为H + + OH - = H 2O 。我也能用同样的方式表示上述四种溶液两两之间发生反应时有气体...生成的反应的实质 。 【实践运用】
⑴通过上述探究发现,在溶液中H +和OH -不能大量共存,我还发现在溶液中 和 (填离子符号,下同)也不能大量共存。
⑵利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液。经测定,该溶液显酸性。则在该溶液中一定含有的离子是 。为了验证该溶液中可能含
【知识升华】
对“复分解反应发生的条件”的再探究,我发现在分析多种溶液混合后所得溶液中离子的成分时,应考虑的因素是 。 27、 “课内比教学”活动中,化学兴趣小组的同学对初中化学常见物质进行了如下探究. 【活动与探究一】
如图是实验室自制汽水的配方.为了检验自制汽水中是否含有二氧化碳, 小燕和小苗设计了如下两个实验方案:
小燕:取汽水样品于试管中,滴入紫色石蕊溶液,观察到溶液
. 小苗:振荡汽水瓶,将产生的气体通入澄清石灰水,观察到澄清石灰水 , 该反应的化学方程式是 . 以上两个方案中,我认为 (填“小燕”或“小苗”)的方案正确. 【活动与探究二】
写出其中任意一个反应的化学方程式 . 【活动与探究三】
实验桌上老师提供了六瓶失去标签的无色溶液,分别是碳酸钠、盐酸、氯化钠、硫酸锌、氢氧化钠和氢氧化钡,
28、化学小组同学对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学
们进行了硝酸性质的实验探究。
【实验设计】⑴将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变 色。 ⑵将Zn 片投入稀硝酸中,预计将产生H 2,其名称为 。
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn 片投入稀HNO 3后,溶液中冒出气泡,产生无色气体A ,在试管口气体A 变成红棕色有刺激性气味的气体B 。 【提出问题】⑴石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料: ⑴硝酸可与Zn 、Cu 等多种金属反应生成相应的硝酸盐,但不生成H 2。 (2)【猜想与分析】
⑴小明认为石蕊变色后又褪色的原因是因试管不干净,含其他杂质造成的,要证明他的观点,
应进行的操作是。
⑵大家一致认同了红棕色气体B是NO
2
,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH
3
,但遭到大家的一致反对,原因是;
②小强同学认为A是N
2
,也遭到大家的一致反对,原因是;
③经讨论,最终大家获得了A是NO的共识。NO遇氧变成NO
2
的化学方程式为。
【实验探究】小红同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO
3
中,发现Cu
溶解,也出现上述Zn与稀HNO
3
反应的类似现象,确证生成了NO,并在老师的帮助下,测出恰好
反应的Cu和HNO
3的质量比为8∶21,由此获得了Cu与稀HNO
3
的反应方程式
为。
【交流与反思】根据探究结果,请你解释稀HCl跟铜不反应而稀HNO
3
却能跟铜反应的原因。
29、某实验小组用图A完成课本实验“碳酸氢钠与盐酸反应的探究”后,他们发现两种反应物的用量不同时反应后溶液中的成分也可能不同,于是他们对碳酸氢钠与盐酸反应后的大试管中溶液的成分进行探究,请回答以下问题:
⑴写出图A中大试管发生反应的化学方程
式:;
写出小试管中发生反应的化学方程
式:;
(2)若实验室制二氧化碳应选装置
(填B或C),药品为:(填名称);
【提出假设】小组成员认为A中大试管的溶液的溶质只能存在三种情况:
假设1.两溶液恰好完全反应,溶质为NaCl;
假设2.两溶液完全反应后,盐酸过量,溶质为NaCl和HCl;
假设3. 。
【设计并进行实验和得出结论】小组同学讨论后发现只要用反应物本身两种试剂(碳酸氢钠溶液
30、化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.老师告诉他们,这瓶溶液中的溶质可能是氢氧化钠、氯
化钠或碳酸钠.同学们很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 (填字母代号).
A .酸
B .碱
C .盐 【查阅资料】碱性的Na 2CO 3溶液与中性的CaCl 2溶液能发生复分解反应.
⑴可能是 溶液; (2)可能是Na 2CO 3溶液; ⑶可能是NaCl 溶液.
老师指出该结论不严密.理由是:氢氧化钠溶液在空气中敞开放置,发生变质,能产生与实验Ⅰ和Ⅱ相同现象.请写出氢氧化钠溶液在空气中变质的化学反应方程式 .老师提示,不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl 2溶液,若观察到 现象,即可说明该溶液中有氢氧化钠. 31、同学们,你们爱吃巧克力吗?你们可知道,在巧克力中含有一种常见的化学物质——草酸(化
学式为C 2H 2O 4)。草酸通常以晶体(C 2H 2O 4·2H 2O )的形式存在,在常温下为固体。以下是某化学兴趣小组提取了草酸晶体之后对其进行研究的过程。 【提出问题】草酸晶体受热分解产生了什么?
【猜想与假设】根据质量守恒定律,草酸晶体分解的产物中可能含水、CO 或CO 2。 【实验论证】研究小组设计了以下实验装置(图1)对上述猜想进行了探究。
信息提示:装置B 为干燥管,其中的无水硫酸铜与水反应会变成蓝色
⑴装置A 中饱和澄清石灰水的作用是 ⑵如分解产物中存在一氧化碳,则C 中实验现象为___________________,该反应的化学方程式为
_____________________。
⑶该反应装置中的酒精灯是否应在实验前先点燃,以便对氧化铁进行预热?____(填“是”或“否”),
为什么?__________。
⑷装置E 的作用是__________________________________________________________。
【反思与评价】⑴该实验装置在设计上存在一个明显的错误,请你将其指出:__________,可以
改进的方法是______________________。