
胎盘植入是妊娠的严重并发症之一,自然分娩时胎盘植入可导致
大出血甚至死亡,已往在围产期紧急子宫切除术中占较大比例[1]
。随着诊疗方法的进步,目前大多可采用保守治疗而免于切除子宫。胎盘植入的主要检查手段是超声。MRI可以多方位、多序列成像,作为补充手段诊断胎盘植入具有较大优势。本研究回顾性分析10例自然分娩后胎盘植入的患者资料,分析其MRI表现。 1 资料与方法
1.1 一般资料 收集本院2012年1月至2013年12月自然分娩后临床拟诊胎盘植入并经MRI检查的患者资料,剔除3例(经综合诊断排除胎盘植入2例,产后时间2月余且资料不完整1例),经临床综合诊断证实,共10例纳入本组,年龄28~40岁(平均34.4岁),9例足月产(孕37+3周至40+2周),1例早产(孕29周),均为自然分娩。产后胎盘胎膜娩出不完整2例,其中予清宫术1例;产后30分钟胎盘不能娩出8例,其中手取胎盘失败4例、手取胎盘不完整后清宫术3例、钳刮术1例。首次分娩5例,第2次分娩4例,第3次分娩1例。流产2~5次各1例,流产1次4例,无流产史1例。MRI检查时间为产后当天至12天(平均6.0天)。
1.2 仪器与方法 采用P h i l i p s A c h i e v a 3.0T X 磁共振扫描仪,体部相控阵线圈。矢状位T S E 序列T 2W I (T R /TE=2753~3210ms/80ms,层厚4~6mm,间距10%);轴位TSE序列T2WI(TR/TE=2753~3210ms/80ms),轴位TSE序列T2WI脂肪抑制(T2WI-fat saturation,T2WI-FS)(TR/TE=3454ms/80ms),轴位TSE序列T1WI(TR/TE=423ms/10ms),轴位层厚5~10mm,间距10%;矢状位动态增强THRIVE序列(TR/TE=4.4ms/
2.1ms,层厚4mm,间距-2mm),用高压
MRI Manifestations of Placenta Accreta after
注射器经肘静脉以2.5ml/s速率按0.2mmol/kg体重注入Gd-DTPA,再以相同速率注入0.9%氯化钠溶液20ml,注射前先平扫(记为0期),注射后15s~20s开始扫描5期(记为1-5期),前4期间隔15s~34s,第5期间隔95s,5期持续时间共139s~197s。部分病例辅以冠状位或斜冠状位平扫、延迟扫描。 1.3 图像分析 由两名副高及以上的影像科医师进行诊断分析,测量子宫和胎盘大小,观察胎盘的位置、形态、信号强度、强化程度、植入部位及与子宫肌层的关系。胎盘植入以临床随诊和病理综合诊断为标准。胎盘MRI 信号强度以同序列的子宫肌层信号强度为参照。强化程度以正常子宫肌层为中等强化,与之对比分为明显、中度、轻度强化。子宫和胎盘大小测量结合多方位观察,取轴位、矢状位最大层面,记录为轴位长径×轴位短径×矢状位上下最大径。测量植入部对侧子宫肌层厚度与植入部侧厚度,比值≥4认为植入部子宫肌层
明显变薄,≥2认为轻度变薄,<2认为无明显变薄。 2 结 果
2.1 临床及病理结果 子宫动脉栓塞治疗6例,其中1例加用甲氨碟呤灌注,有2例配合甲氨碟呤静脉化疗。1例入院后7天行清宫术,术后病理为变性成熟胎盘组织。输血纠正贫血5例,其它治疗包括抗炎、促宫缩等。住院日为6~14天(平均8.8天)。出院
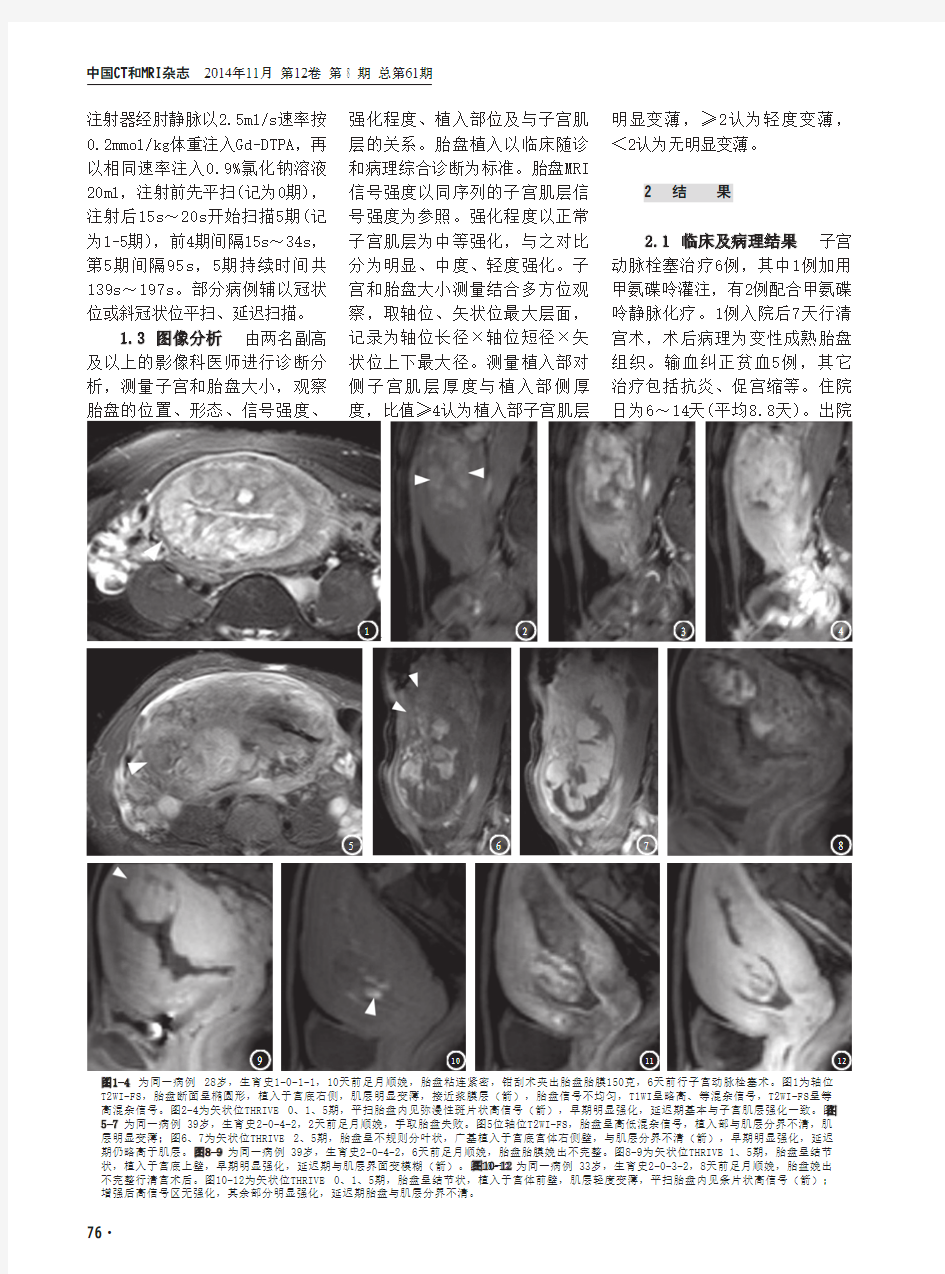
图1-4 为同一病例 28岁,生育史1-0-1-1,10天前足月顺娩,胎盘粘连紧密,钳刮术夹出胎盘胎膜150克,6天前行子宫动脉栓塞术。图1为轴位T2WI-FS,胎盘断面呈椭圆形,植入于宫底右侧,肌层明显变薄,接近浆膜层(箭),胎盘信号不均匀,T1WI呈略高、等混杂信号,T2WI-FS呈等高混杂信号。图2-4为矢状位THRIVE 0、1、5期,平扫胎盘内见弥漫性斑片状高信号(箭),早期明显强化,延迟期基本与子宫肌层强化一致。图5-7 为同一病例 39岁,生育史2-0-4-2,2天前足月顺娩,手取胎盘失败。图5位轴位T2WI-FS,胎盘呈高低混杂信号,植入部与肌层分界不清,肌层明显变薄;图6、7为矢状位THRIVE 2、5期,胎盘呈不规则分叶状,广基植入于宫底宫体右侧壁,与肌层分界不清(箭),早期明显强化,延迟期仍略高于肌层。图8-9 为同一病例 39岁,生育史2-0-4-2,6天前足月顺娩,胎盘胎膜娩出不完整。图8-9为矢状位THRIVE 1、5期,胎盘呈结节状,植入于宫底上壁,早期明显强化,延迟期与肌层界面变模糊(箭)。图10-12 为同一病例 33岁,生育史2-0-3-2,8天前足月顺娩,胎盘娩出不完整行清宫术后。图10-12为矢状位THRIVE 0、1、5期,胎盘呈结节状,植入于宫体前壁,肌层轻度变薄,平扫胎盘内见条片状高信号(箭);增强后高信号区无强化,其余部分明显强化,延迟期胎盘与肌层分界不清。
1234
5678
9
101112
后门诊诊疗随访直至超声检查子宫正常,随访时间为产后40天至4月。1例出院后2月余门诊行清宫术,病理为变性坏死的胎盘组织。
2.2 MRI表现 除早期检查的第1例为子宫动脉栓塞后6天检查外,后9例均为栓塞前检查。子宫不同程度增大,早产1例约103mm×86mm×130mm,足月产9例最大约165mm×105mm×248mm,最小约142mm×78mm×131mm。胎盘最大约122mm×85mm×110mm,最小约40mm×32mm×26mm。以三径乘积乘以π/6的数值将胎盘区分大小(以150000分界),较大胎盘呈分叶状5例,椭圆形1例,较小胎盘4例均呈结节状。按该数值从小到大排序,胎盘/子宫测量比值为0.026~0.352(平均0.145),除第4、5顺序(分别为0.081和0.077)外依次递增。
平扫胎盘T2WI及T2WI-FS信号不均匀,呈高低混杂信号5例、等高混杂信号1例、等低混杂信号1例、高信号为主3例(图1、5)。T1WI呈略高、等混杂信号4例、略高、低混杂信号5例、等信号为主1例。在增强前T1WI-FS(THRIVE 序列),上述等信号1例未见高信号,其余9例高信号显示更明显,7例高信号呈斑片状、条状、环状,其中范围较大的2例呈弥漫性或大片状(图2、10),2例呈少量散在斑点状高信号。
动态增强后胎盘均见强化,1例早期呈中度强化、后期子宫肌层强化亦较弱,可能与对比剂注射有关,其余9例早期均呈明显不均匀强化,随后强化范围增大,渐趋均匀强化,晚期与子宫肌层强化一致或略高,10例均只有小部分区域不强化或轻度强化(图3、4、6-9、11、12)。
胎盘植入部与子宫肌层界面模糊,10例均显示,界面宽度与
植入范围有关,部分界面可借由
T1WI-FS显示胎盘高信号而得以辨
认,动态增强早期因胎盘早于肌
层强化亦可辨认,延迟期肌层强
化后与胎盘分界面不能辨认。植
入部7例位于宫底,其中偏右侧4
例,偏右前2例,偏上壁1例;2例
位于宫体前壁;1例位于宫底宫体
右侧壁。植入部肌层厚度,较大
胎盘6例均明显变薄(图1、5),较
小胎盘明显变薄1例,轻度变薄3
例(图10-12)。有2例接近或达到
浆膜层(图1)。
3 讨 论
胎盘植入是因子宫蜕膜发育
不良或缺如等原因导致胎盘绒毛
植入或穿透子宫肌层所致的一
种异常的胎盘种植。按植入程
度可分为3类,胎盘附着在子宫
肌层(placenta accreta,粘连
性胎盘)、侵入肌层(placenta
increta,植入性胎盘)或侵入
以至穿透子宫浆膜(p l a c e n t a
percreta,穿透性胎盘)[2]。通
常,广义上的胎盘植入(placenta
accreta)可以包含各种类型的胎
盘异常种植。
通常认为胎盘植入的诊断金
标准为病理学检查。但在实际工
作中,随着介入治疗等保守治疗
的应用,大部分患者不需要切除
子宫,而在清宫过程中,若胎盘
组织碎裂或产后出血能及时控
制,残留的胎盘就有可能留在子
宫中,这些情况下均难以进行病
理检查。剖宫产、阴道产后以及
手取胎盘时进行临床诊断更具有
现实意义。本组采用以下诊断标
准综合诊断胎盘植入:①产后30
分钟或促宫缩处理后胎盘不能娩
出,手取胎盘困难或手取(钳夹)
胎盘不完整,胎盘剥离面粗糙、
出血;②超声或MRI检查证实子
宫腔内有残留胎盘组织,有侵入
性影像改变,与子宫肌层分界不
清;③保守治疗后排出的胎盘组
织病理检查证实为变性坏死或陈
旧胎盘组织。
超声是胎盘植入的主要检查
手段,MRI相对超声有更好的软组
织对比度和更大的视野。超声和
MRI对产前诊断胎盘植入均有较好
的敏感性[3]。在超声不能确定的
可疑病例,MRI可以提高诊断准确
性[4]。由于产后子宫复旧导致子
宫壁不均匀,胎盘出现皱缩,形
态不规整,产后诊断胎盘植入较
产前困难。目前产后胎盘植入的
MRI报道较少[5]。
本组为产后病例,与产前MRI
检查不同,因无需考虑胎儿运动
的影响而未采用屏气的快速扫描
序列[6],由此在子宫底位置较高
的病例,上腹部层面出现较多呼
吸运动伪影而降低了图像质量。
有作者认为矢状位T2WI-FS显示病
灶位置及范围较好[5]。本组矢状
位因主要考虑软组织分辨率而不
常规采用脂肪抑制,T2WI-FS改在
轴位应用,显示植入胎盘的位置
及范围较T2WI、T1WI好。
产后孕妇体内激素水平发生
明显变化可导致子宫平滑肌收缩
挤压植入胎盘病灶,使植入胎盘
组织出血坏死。本组除1例常规
T1WI高信号范围较明确外,8例
胎盘内仅见略高信号,因未加作
脂肪抑制难以确定出血范围,以
THRIVE动态增强前的扫描作为替
代,9例高信号显示更明显,范围
明确。
由于植入胎盘部分或全部胎
盘绒毛植入于子宫肌层内并紧密
粘连,子宫动脉血供丰富。MRI动
态增强扫描可显示并区分明显强
化的胎盘组织和相对弱强化的肌
层,有利于胎盘植入的诊断[7]。
动脉期与子宫肌层相连的胎盘外表面即可明显强化,界限清晰,而子宫肌层到后期才强化,可较好地明确植入深度[3]。
正常胎盘有早期快速强化和延迟明显强化两种强化方式,前者为绒毛膜的强化方式,后者为底蜕膜的强化方式,产后正常胎盘残留具有这两种强化方式,而胎盘植入导致底蜕膜的缺失则只有早期快速强化一种方式[8,9]。本组9例显示胎盘早期快速强化,该征象可作为胎盘植入诊断的重要依据。
有作者认为植入部位子宫轮廓可呈不规整的局限性外凸的形态[5],本组未见此征象,可能与病例数较少有关。
结合文献及本组资料,以下MRI征象提示产后胎盘植入:胎盘附着部子宫肌层变薄甚至完全消失;胎盘附着部子宫局限性外凸;胎盘与子宫肌层界面模糊;平扫T1WI(最好是T1WI-FS)胎盘内出现高信号;增强早期胎盘快速强化。
总之,MRI对自然分娩后胎盘植入有较高的诊断价值,结合动
态增强能更好地确认有无植入并
判断植入程度,为临床制定治疗
方案提供诊断依据,是重要的辅
助诊断工具。
参考文献
1. Rahman J, Al-Ali M, Qutub HO,
et al. Emergency obstetric
hysterectomy in a university
hospital: a 25-year review[J].J
Obstet Gynaecol, 2008,28(1):69-
72.
2.F i n b e r g H J,W i l l i a m s J W.
Placenta accreta: prospective
s o n o g r a p h i c d i a g n o s i s i n
p a t i e n t s w i t h p l a c e n t a
previa and prior cesarean
section[J]. J Ultrasound Med,
1992,11(7):333-343.
3.W a r s h a k C R,E s k a n d e r R,
H u l l A D, e t a l.A c c u r a c y
o f u l t r a s o n o g r a p h y a n d
magnetic resonance imaging
in the diagnosis of placenta
accreta[J]. Obstet Gynecol,
2006,108(3 Pt 1):573-581.
4. Dwyer BK, Belogolovkin V, Tran L,
et al. Prenatal diagnosis of
placenta accreta: sonography
o r m a g n e t i c r e s o n a n c e
imaging[J]. J Ultrasound Med,
2008,27(9):1275-1281.
5.卢晓丹,陈燕萍,周和秀,等.产
后胎盘植入的M R I表现及诊
断价值[J].临床放射学杂
志,2012,31(10):1440-1444.
6. Teo TH, Law YM, Tay KH, et
al. Use of magnetic resonance
i m a g i n g i n e v a l u a t i o n o f
p l a c e n t a l i n v a s i o n.C l i n
Radiol[J]. 2009,64(5):511-516.
7. Leyendecker JR, Gorengaut
V,B r o w n J J.M R i m a g i n g
o f m a t e r n a l d i s e a s e s o f
t h e a b d o m e n a n d p e l v i s
d u r i n g p r
e g n a n c y a n d t h e
i m m e d i a t e p o s t p a r t u m
period[J]. Radiographics,
2004,24(5):1301-1316.
8. Tanaka YO, Sohda S, Shigemitsu S,
et al. High temporal resolution
dynamic contrast MRI in a
high risk group for placenta
accreta[J]. Magn Reson Imaging,
2001,19(5): 635-642.
9.T a n a k a Y O,S h i g e m i t s u S,
Ichikawa Y, et al. Postpartum
M R d i a g n o s i s o f r e t a i n e d
p l a c e n t a a c c r e t a[J].E u r
Radiol, 2004,14(6):945-952.
(本文编辑: 汪兵)
【收稿日期】2014-09-22
6. Koo JH,Kim CK,Choi D,et al.
Diffusion-Weighted Magnetic
Resonance Imaging for the
Evaluation of Prostate Cancer:
Optimal b Value at 3T[J].
Korean J Radiol, 2013,14(1):61-
69.
7. 李飞宇,王霄英,许玉峰,等.不同
年龄段正常成人前列腺外周带ADC
值的初步研究[J].实用放射学杂
志,2006,22(12):1496-1499.
8. Tan CH,Wei W,Johnson V,Kundra
V.Diffusion-weighted MRI in
the detec tion of prostate
cancer:meta-analysis[J]. AJR,
2012,199(4):822-829.
9.马周鹏,章顺壮,滕华英.磁共振
D W I对前列腺癌诊断价值的初步
研究[J].中国临床医学影像杂
志,2011,22(8):581-584.
10.何海清,樊树峰,陈邦文,等.M R
扩散加权成像在前列腺病变中
的诊断价值[J].医学影像学杂
志,2009,19(2):187-191.
11.肖利华,郑晓林,蔡庆文,等.M R
扩散加权成像对前列腺癌的
诊断价值[J].临床放射学杂
志,2010,29(7):923-925.
12.T a m a d a T,S o n e T,J o Y,e t
al.Diffusion-weighted MRI and
its role in prostate cancer[J].
NMR Biomed, 2014,27(1):25-38.
13.赵武华,樊琪玮,黄丹江.磁共振
扩散加权成像技术在前列腺癌
的应用研究[J].医学影像学杂
志,2011,21(7):1107-1108.
(本文编辑: 汪兵)
【收稿日期】2014-09-22
(上接第 68 页)